桔皮中橙皮苷的新型雙水相萃取
朱紅菊 , 丁 玉 , 賈亞偉
(1.中國礦業(yè)大學 國家煤加工與潔凈化工程技術研究中心,江蘇 徐州221116;2.中國礦業(yè)大學 化工學院,江蘇 徐州 221116;3.江蘇洋河酒廠股份有限公司技術中心,江蘇 宿遷 223800)
橙皮苷具有抗氧化、降血脂、消炎、維持滲透壓、增強毛細血管韌性及降低膽固醇等作用[1-3],被廣泛用于醫(yī)藥及日用化工等領域[4-6]。同時,作為天然抗氧化劑、食品添加劑、果蔬保鮮劑及保健品等,也被食品行業(yè)廣泛應用。
傳統(tǒng)的雙水相體系是由兩種水溶性高分子或一種水溶性高分子與無機鹽組成的混合體系。與其他常規(guī)分離方法相比,其顯著特點及獨有的技術優(yōu)勢在于:由于兩相均為水相,故兩相界面張力極低,大大低于有機溶劑與水相之間的相間張力,故相分離條件溫和,相間傳質和平衡過程迅速,產(chǎn)物回收率高。另外,低的界面張力有助于保持被分離物質的生物活性,特別適合于分離有生物活性的物質,在生物大分子等生物類產(chǎn)品的分離過程中得到廣泛應用[7]。基于此,為了增加雙水相體系的選擇性,近年來有諸如雙水相與其它分離技術的集成化、親和雙水相等萃取技術的不斷發(fā)展[8-10]。但這類雙水相體系的主要不足是用于分離的高分子聚合物價格昂貴、難以回收、黏度大、聚合物難處理及環(huán)境污染等[11],限制了它們的工業(yè)化應用。
近年來,先后出現(xiàn)了無機鹽-低分子有機溶劑雙水相體系[12]、離子液體雙水相體系[13-15],以及表面活性劑的雙水相體系[16]等。這類雙水相體系具有傳統(tǒng)體系所沒有的一些特點,如分相快、成本低、易于處理等。其中以無機鹽/低分子有機溶劑形成的雙水相體系最為價廉、易得,近年來得到廣泛應用[17-20],且多以微波、超聲等手段輔助,以增強萃取效果。用于黃酮類化合物提取的這類雙水相體系主要是由一些低分子醇類與硫酸銨構成[17-18,20],多用于不同天然產(chǎn)物中黃酮類物質的分離。但這類體系對橙皮苷的選擇性如何,則研究較少,而對于除低分子醇類之外的有機溶劑更少有人涉及。由于分離是利用目的產(chǎn)物與雜質的性質不同而進行,故萃取介質的不同必然會影響目的產(chǎn)物的分離程度。因此,有必要對低分子醇類以外的有機溶劑及硫酸銨以外的鹽類的雙水相構成及性質進行研究,以尋求最佳的雙水相萃取體系,豐富雙水相的構成。
作者采用新型親水性低分子有機溶劑/無機鹽雙水相體系純化橙皮苷,輔以纖維素酶助提取,考察不同的低分子有機物質及無機鹽類對橙皮苷純化的影響。采用制備型高效液相色譜(HPLC)對其進一步純化。用HPLC檢測所得橙皮苷的純度及橙皮苷回收率,以考察新型雙水相體系對橙皮苷的分離特異性及其純化效率。
1 材料與方法
1.1 粗提物制備
市購蜜桔取皮、清洗、冷凍干燥至恒重。粉碎、過40目篩,所得桔皮粉冷藏備用。
取適量桔皮粉于錐形瓶中,加入乙醇并輔以纖維素酶,水浴振蕩浸提30 min后滅酶、冷卻,抽濾得粗提液待用。
1.2 雙水相成相
關于乙醇、丙醇等低分子醇類與硫酸銨形成的雙水相體系研究者眾多,故本研究取異丙醇、丙酮及3種無機鹽類構建雙水相體系,進一步考察這類物質的成相性質及對目的產(chǎn)物的選擇性。
分別取異丙醇/(NH4)2SO4、異丙醇/Na2CO3、異丙醇/K2HPO4、丙 酮/(NH4)2SO4、 丙酮/Na2CO3、丙 酮/K2HPO46對物質進行研究,用濁點法繪制各自雙節(jié)線圖(相圖),考察最優(yōu)成相、萃取體系。
1.3 雙水相體系萃取
將一定量構成雙水相體系的有機溶劑、無機鹽置于離心管中,取橙皮苷粗提液與之混合,調節(jié)pH,旋渦混合,一定溫度下恒溫萃取一定時間后,記錄兩相體積,用紫外分光光度法測定橙皮苷濃度。計算相比R,分配系數(shù)K和回收率Y。
1.4 橙皮苷粗品制備
將雙水相上相溶液加質量分數(shù)1%鹽酸溶液調pH為4.0,加熱至65℃,冷卻過夜結晶,過濾洗滌數(shù)次,真空冷凍干燥得橙皮苷粗品。
1.5 制備型HPLC精制
將所得粗品用流動相稀釋至相應濃度,與標準品溶液及流動相進行超聲處理,過0.45 μm的濾膜后上樣。梯度洗脫,收集主要峰值流出液。
制備條件:色譜柱DAC-HB50-C18(Φ50 mm×250 mm,10 μm);紫外檢測器,檢測波長 286 nm;柱溫為室溫;進樣量15 mL;流動相體積流量55 mL/min。
1.6 相關計算
1.6.1 雙水相萃取收率

式(1)中:R為雙水相體系上下相體積之比;K為雙水相體系分配系數(shù)。
1.6.2 相比

式(2)中:Vt,Vb為雙水相體系上、下相體積,mL。
1.6.3 分配系數(shù)

式(3)中:Ct,Cb為上、下相中橙皮苷的質量濃度,mg/mL。

1.6.5 總回收率Y計算

2 結果與討論
2.1 雙水相體系萃取橙皮苷
2.1.1 雙水相體系成相研究 一般認為,普通有機物形成雙水相是鹽溶液與有機溶劑爭奪水分子形成締合水合物的結果。通過繪制雙水相雙節(jié)線圖,選擇合適的雙水相體系。3種鹽分別與丙酮、異丙醇構成雙水相體系,見圖1。


圖1 不同雙水相體系的成相相圖Fig.1 Phase diagram for different aqueous two-phase Systems
由圖1可以看出,碳酸鈉形成穩(wěn)定的雙水相體系所需鹽及醇量均較少,意即其分相能力最強。磷酸氫二鉀具有較寬的分相范圍。
2.1.2 雙水相體系構成對橙皮苷選擇性的影響取碳酸鈉與磷酸氫二鉀進一步研究,分別與異丙醇、丙酮構成4組雙水相體系,即異丙醇/Na2CO3、異丙醇/K2HPO4、丙酮/Na2CO3、丙酮/K2HPO4體系,探討橙皮苷粗品在兩相間的分配情況,考察體系對橙皮苷的選擇性。各體系的成相相比、分配系數(shù)及橙皮苷收率見表1。

表1 橙皮苷在不同雙水相體系中分配效果比較Table 1 Comparison ofhesperidin partitioning in different aqueous two-phase systems
由表1可知,橙皮苷在丙酮/K2HPO4體系中雖然相比不太理想,但分配系數(shù)較大,表明該體系的選擇性較高,其回收率Y1可達到93.77%。因而確定丙酮/K2HPO4體系作為萃取橙皮苷的適宜雙水相體系。
2.1.3 丙酮和K2HPO4質量濃度對橙皮苷選擇性的影響 取系統(tǒng)總質量20 g,加入相當0.20 g橙皮苷的粗提液,在pH 9.0、室溫情況下,考察K2HPO4、丙酮質量濃度對橙皮苷粗品在兩相間的選擇性及回收率的影響,結果如圖2所示。
由圖2可知,K2HPO4、丙酮質量分數(shù)對橙皮苷粗品的萃取效果影響較為顯著;當K2HPO4質量分數(shù)一定時,隨著丙酮量的增加,分配系數(shù)K和萃取率Y1總是先明顯上升,而后趨于平穩(wěn)或略有下降。這是由于體系分相能力隨丙酮量增加而增大,更有利于橙皮苷分配于上相,提高萃取率;但丙酮質量分數(shù)過高,就會有更多的水進入上相,而使分配系數(shù)降低,同時K2HPO4的水化作用不足以奪取這些水分子而出現(xiàn)鹽析現(xiàn)象。而K2HPO4的量也不宜太高,否則導致相比進一步降低,加之鹽析的同時作用,會造成橙皮苷萃取率下降,導致原料浪費。欲提高萃取收率Y1,必須同時考慮分配系數(shù)K和相比R兩個參數(shù)的作用。因此,取質量分數(shù)28%丙酮-質量分數(shù)20%K2HPO4構成的雙水相體系作為后續(xù)萃取體系。

圖2 K2HPO4、丙酮質量濃度對橙皮苷粗品選擇性影響Fig.2 Effect of dipotassium hydrogen phosphate and acetone concentration on the selectivety of crude hesperidin
2.1.4 粗提物用量對橙皮苷選擇性的影響 仍取系統(tǒng)總質量為20 g、pH 9.0,室溫操作,固定K2HPO4質量分數(shù)為20%、丙酮質量分數(shù)28%,考察粗提物加入量對橙皮苷萃取過程的影響,結果示于表2。
繼續(xù)加大人才培養(yǎng)與引進力度,一方面支持在崗職工通過外出進修學習、出國深造、提升學歷等途徑,不斷提升現(xiàn)有醫(yī)務人員的工作能力和學歷層次。另一方面,則通過廣納各方賢才,吸引更多優(yōu)秀的高層次人才來院工作,進一步優(yōu)化學科結構,形成合理的內(nèi)部競爭機制,實現(xiàn)醫(yī)院的可持續(xù)發(fā)展。
由表2可以看出,分配系數(shù)K、萃取率Y1隨著粗提物量的加大而不斷波動,但在用量達到0.4 g后,相比下降,Y呈現(xiàn)下降趨勢。綜合考慮,取粗提物用量為0.4 g。
2.1.5 溫度對橙皮苷分配系數(shù)的影響 固定上述條件,即系統(tǒng)總質量20 g,K2HPO4質量分數(shù)20%、丙酮質量分數(shù)28%,pH 9.0,粗提物加入量0.4 g。不同溫度下橙皮苷粗品的萃取收率與分配系數(shù)等參數(shù)變化如表3所示。

表2 粗提物用量對橙皮苷分配的影響Table 2 Effect of the amount of crude hesperidin on its partitioning
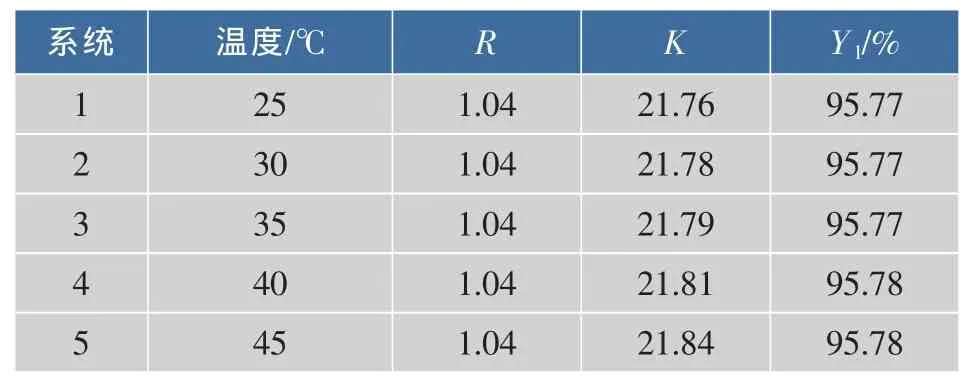
表3 溫度對橙皮苷分配系數(shù)的影響Table 3 Effect of temperature on the partition coefficient of crude hesperidin
由表3可知,隨著溫度上升,分配系數(shù)略有增加,相比未見變化,橙皮苷的萃取收率幾乎無變化。出于操作方便和節(jié)能降耗的考慮,萃取溫度取為室溫。
2.1.6 pH值的影響 萃取條件固定為:系統(tǒng)總質量為20 g,K2HPO4質量分數(shù)為20%、丙酮質量分數(shù)為28%,室溫,粗提物加入量0.4 g。一般而言,丙酮/K2HPO4雙水相體系成相時,溶液pH范圍在7~12之間。因此,考察此區(qū)間內(nèi)pH值對橙皮苷粗品萃取過程的影響,結果見表4。

表4 pH值對橙皮苷分配系數(shù)的影響Table 4 Effect of pH value on the partition coefficient of crude hesperidin
由表4可知,pH值在7~10之間時,隨著pH值的增加,相比R與分配系數(shù)K不斷增大,橙皮苷萃取收率上升趨勢顯著,pH=10時萃取收率達到最大值。pH大于10后,相比與選擇性均降低,萃取收率亦緩慢下降。這可能是因為在pH<10時,隨著pH的增加,溶液中水解產(chǎn)生的H2PO4-減少而HPO42-相應有所增加。負電荷的增多致使其對橙皮苷酚羥基氧負離子的排斥作用增強,從而促使更多的橙皮苷分配于上相,提高了橙皮苷的分配系數(shù)。pH>10后,K2HPO4會進一步電離,上、下相的差別縮小,從而使得橙皮苷的選擇性減少。最后導致其萃取收率下降。
2.2 HPLC制備橙皮苷
2.2.1 流動相及洗脫方式對橙皮苷分離的影響以甲醇溶劑為對照液,用紫外可見分光光度計對質量濃度1.5 mg/mL的橙皮苷標準品于波長200~600 nm之間進行全波長連續(xù)掃描,發(fā)現(xiàn)在286 nm處有特征吸收峰。因此,以286 nm為檢測波長,對雙水相純化后的橙皮苷樣品進行HPLC精制純化。
配制質量濃度為1.0 mg/mL的樣品溶液,按一定的色譜條件進行HPLC實驗。考察不同流動相及洗脫方式對樣品分離效果的影響。按以下3種洗脫方式進行考察:
1)純甲醇洗脫方式。
2)固定 v(甲醇)∶v(水)=45∶55 的洗脫方式。
3)梯度洗脫方式。以甲醇與水的初始體積比例為40∶60開始,不斷增加甲醇比例至二者體積比例達到1∶1。而后,逐漸恢復初始比例,直至洗脫結束。所得結果分別示于圖3—5。

圖3 純甲醇洗脫時樣品的流出情況Fig.3 Elution profile while methanol as the elution solvent

圖4 v(甲醇)∶v(水)=45∶55 比例洗脫時樣品流出情況Fig.4 Elution profile of sample when the ratio of methanol to water is 45∶55

圖5 梯度洗脫時樣品流出情況Fig.5 Elution profile of sample as gradient elution strategy
由圖3—5可見,流動相為純甲醇時,出峰時間較早,但是分離效果較差,并且有拖尾現(xiàn)象和溶劑峰干擾;流動相為甲醇-水(體積比 45∶55)時,出峰時間較適宜,峰形較佳,但部分組分不能完全分開;流動相為梯度洗脫時,出峰時間適中,每個組分基本可逐一分離,但個別峰有前滯現(xiàn)象。綜合考慮,采取梯度洗脫法精制橙皮苷。
2.2.2 HPLC精制橙皮苷 按以上色譜條件對樣品進行精制。以質量濃度1.5 mg/mL的標準品作為基準,對相當質量濃度3.0 mg/mL的樣品進行梯度分離。收集峰流出液,真空旋轉蒸發(fā)濃縮,回收甲醇溶劑。所得產(chǎn)品用去離子水洗滌數(shù)次,真空干燥得橙皮苷精制品。
2.3 產(chǎn)品純度分析 分別將橙皮苷標準品、雙水相純化樣品及HPLC精制樣品配制成質量濃度為20 μg/mL的溶液,用HPLC分析色譜對各樣品進行分析,通過面積歸一化方法計算各出峰組分的百分比,近似看作各組分的質量分數(shù)。3種樣品的色譜如圖6—8所示。
根據(jù)圖6橙皮苷標準品的分析色譜圖,可知圖7中出峰時間7.380 min即第4個峰為橙皮苷,面積歸一化得面積分數(shù)71.36%,即雙水相純化后的橙皮苷干樣品純度約為71.36%。

圖6 橙皮苷標準品分析圖譜Fig.6 HPLC chromatogram of the standard hesperidin

圖7 雙水相純化樣品分析圖譜Fig.7 HPLC chromatogram of purified hesperidin
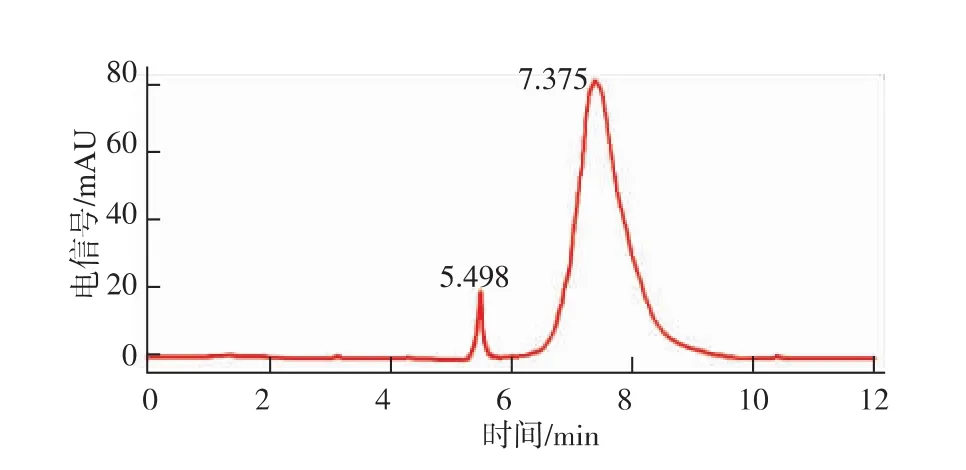
圖8 HPLC精制品分析圖譜Fig.8 HPLC chromatogram of the refined hesperidin
圖8中保留時間7.375 min處的峰與橙皮苷標準品(7.373 min)保留時間一致,歸一化面積分數(shù)為96.09%,即制備型HPLC系統(tǒng)制備得到的橙皮苷干品純度約為96.09%。
制備型HPLC精制橙皮苷回收率

則橙皮苷總回收率

由雙水相純化樣品的分析圖譜可以看出,丙酮/K2HPO4體系對橙皮苷有一定的富集、純化作用。對照標準品可知,除主要成分橙皮苷外,還有其他的一些雜質存在。由于缺少對應物質的標準品,尚不能確定它們是哪種物質。這有待于以后的進一步研究。而經(jīng)制備色譜精制后的樣品已經(jīng)與標準峰值基本無異,說明制備色譜對于橙皮苷類物質的純化十分有效。
3 結語
1)采用不同類型有機溶劑/無機鹽雙水相體系分離純化橙皮苷粗提物,效果不同。實驗條件下,以丙酮/K2HPO4體系效果較好。其最佳萃取條件為:K2HPO4質量分數(shù)為20%、丙酮質量分數(shù)為28%;室溫,pH 10,粗提物用量0.4 g。其時,相比R為1.25,分配系數(shù)K為23.36,萃取回收率96.69%。
2)丙酮/K2HPO4雙水相萃取體系對橙皮苷有一定的選擇性,可達到70%以上的純度,純化倍數(shù)達20倍以上。但其選擇專一性還有待進一步研究。
3)制備型HPLC的流動相洗脫方式對橙皮苷的分離效果有一定影響。實驗條件下,以甲醇-水梯度洗脫方式純化效果較好。
4)丙酮/K2HPO4雙水相體系純化后的橙皮苷樣品的純度約71.36%,制備型HPLC精制所得橙皮苷干品純度可達到96.09%,且回收率較高。
5)本實驗橙皮苷總回收率約為83.54%。
6)由丙酮/K2HPO4構成的雙水相體系選擇性較高,K2HPO4是生物活性物質的常用緩沖溶液用藥品,由此構成的雙水相體系更適合于具有生物活性的天然物質的萃取分離,值得對此作進一步研究。
[1]錢俊臻,王伯初.橙皮苷的藥理作用研究進展[J].天然產(chǎn)物研究與開發(fā),2010,22:176-180.QIAN Jun-zhen,WANG Bo-chu.New research progress in harmacological activities of hesperidin[J].Nat Prod Res Dev,2010,22:176-180.(in Chinese)
[2]Pradeep K,Park S H,Ko K C.Hesperidin a flavanoglycone protects against γ-irradiation induced hepatocellular damage and oxidative stress in Sprague-Dawley rats[J].European Journal of Pharmacology,2008,587(1-3):273-280.
[3]Balakrishnan A,Menon V P.Effect of hesperidin on matrix metalloproteinases and antioxidant status during nicotine induced toxicity[J].Toxicology,2007,238(2-3):90-98.
[4]Yeh M H,Kao S T,Hung C M,et al.Heperidin inhibited acetaldehyde-induced matrix metalloproteinase-9 gene expression in human hepatocellular carcinoma cells[J].Toxicology Letters,2009,184:204-210.
[5]Marder M,Viola H,Wasowski C,et al.6-Methylapigenin and hesperidin:new valeriana flavonoids with activity on the CNS[J].Pharmacology,Biochemistry and Behavior,2003,75:537-545.
[6]Fernández S P,Wasowski C,Loscalzo L M,et al.Central nervous system depressant action of flavonoid glycosides[J].European Journal of Pharmacology,2006,539(3):168-176.
[7]江詠,李曉璽,李琳,等.雙水相萃取技術的研究進展及應用[J].食品工業(yè)科技,2007,28(10):235-238.JIANG Yong,LI Xiao-xi,LI Lin,et al.Study and application of aqueous two-phase systems extraction[J].Science and Technology of Food Industry,2007,28(10):235-238.(in Chinese)
[8]林東強,朱自強,姚善涇,等.生化分離過程的新探索—雙水相分配與相關技術的集成化[J].化工學報,2000,51(1):1-6.LIN Dong-qiang,ZHU Zi-qiang,YAO Shan-jing,et al.Novel technology in bioseparation process-integration of aqueous twophase partitioning with related techniques[J].Journal of Chemical Industry and Engineering,2000,51(1):1-6.(in Chinese)
[9]陸瑾,趙珺,林東強,等.金屬螯合雙水相親和分配技術分離納豆激酶的研究[J].高等化學工程學報,2004,18(4):465-470.LU Jin,ZHAO Jun,LIN Dong-qiang,et al.Separation of nattokinase by immobilized metal ions affinity partitioning in aqueous two-phase systems[J].Journal of Chemical Engineering of Chinese Universities,2004,18(4):465-470.(in Chinese)
[10]汪苗苗,丁玉.天花粉蛋白的鹽析工藝和親和雙水相分離工藝[J].中國食品添加劑,2012(1):128-133.WANG Miao-miao,DING Yu.Salting-out process and affinity aqueous two-phase extraction process of trichosanthin[J].China Food Additives,2012(1):128-133.(in Chinese)
[11]陳叢瑾,屈麗娟,陳東.雙水相萃取法分離純化黃酮類化合物的研究進展[J].應用化工,2010,39(10):1587-1589,1596.CHEN Cong-jin,QU Li-juan,CHEN Dong.Research progress on separation and purification of flavonoids by aqueous two-phase systems extraction[J].Applied Chemical Industry,2010,39(10):1587-1589,1596.(in Chinese)
[12]趙云燦,薛學東,趙波,等.頭孢菌素C的新型雙水相萃取[J].中國醫(yī)藥工業(yè)雜志,2012,43(5):337-339,371.ZHAO Yun-can,XUE Xue-dong,ZHAO Bo,et al.Extraction of Cephalosporin C with a new type aqueous two-phase system[J].Chinese Journal of Pharmaceuticals,2012,43(5):337-339,371.(in Chinese)
[13]姜大雨,朱紅,王良,等.離子液體雙水相萃取的應用研究進展[J].化學試劑,2010,32(9):805-810.JIANG Da-yu,ZHU Hong,WANG Liang,et al.Ionic liquids aqueous two-phase extraction and progress in study on its application[J].Chemical Reagent,2010,32(9):805-810.(in Chinese)
[14]戈延茹,潘如,傅海珍,等.離子液體雙水相溶劑浮選法分離/富集桑黃酮類成分[J].分析化學,2012,40(2):317-320.GE Yan-ru,PAN Ru,F(xiàn)U Hai-zhen,et al.Separation/Richment total flavonoids in Phellinus Igniarius by ionic liquid/salt aqueous two-phase Flotation[J].Chinese Journal of Analytical Chemistry,2012,40(2):317-320.(in Chinese)
[15]Muller A,Górak A.Extraction of 1,3-propanediol from aqueous solutions using different ionic liquid-based aqueous two-phase systems[J].Separation and Purification Technology,2012,97:130-136.
[16]王艷.表面活性劑雙水相萃取分離茶氨酸研究[D].無錫:江南大學,2012.
[17]陳利梅.超聲波輔助雙水相提取條斑紫菜黃酮類物質及其抗氧化活性研究[J].食品科學,2012,33(4):41-46.CHEN Li-mei.Ultrasonic-assisted aqueous two-phase extraction and antioxidant activity of total flavonoids from porphyrayezoensis[J].Food Science,2012,33(4):41-46.(in Chinese)
[18]左光德,趙志云,高云濤.超聲與雙水相體系耦合提取竹葉總黃酮研究[J].安徽農(nóng)業(yè)科學,2010,38(23):12448-12449.ZUO Guang-de,ZHAO Zhi-yun,GAO Yun-tao.Extraction of total flavonoids from bamboo leaf based on propyl alcohol ammonium sulfate aqueous two-phase system coupling with ultrasonic[J].Journal of Anhui Agri Sci,2010,38(23):12448-12449.(in Chinese)
[19]劉琳,董悅生,修志龍.微波輔助雙水相提取盾葉薯蕷中的皂苷成分[J].過程工程學報,2009,9(6):1147-1152.LIU Lin,DONG Yue-sheng,XIU Zhi-long.Microwave-assisted aqueous two-phase extraction of steroidal saponins in Dioscored zingiberensis[J].The Chinese Journal of Process Engineering,2009,9(6):1147-1152.(in Chinese)
[20]閆蕊.微波輔助/雙水相法提取分離蘆薈中黃酮類化合物及蘆薈多糖的研究[D].長春:東北師范大學,2008.

