采用HBL101萃取石煤高酸浸出液中的釩
李青剛,許 亮,齊兆樹,莫興德,廖宇龍
(中南大學 冶金科學與工程學院,長沙 410083)
我國石煤提釩工藝起步于20世紀70年代末期,經過 30年的發展,目前在釩行業中已占據重要的地位。據統計,目前石煤提釩的產量已達到我國釩總產量的45%左右。近年來,由于釩的市場價格急劇下降,環境要求日益嚴格,生產成本較高,大部分石煤提釩廠處于停產狀態,仍在生產的少數幾家也處于虧本或持平狀態,因此技術改革、降低生產成本迫在眉睫。目前石煤提釩的生產工藝主要有:鈉化焙燒、鈣化焙燒、酸浸萃取、堿法工藝等。鈉化焙燒工藝對環境造成巨大破壞,在我國很多地方已禁止使用。鈣化焙燒由于技術的原因,目前在國內還沒有產業化的先例。堿法工藝對礦石適應性差,目前國內只有兩家工廠采用。酸浸萃取工藝具有釩的回收率高、可自動化操作的特點,應用廣泛,成為目前石煤提釩的主流工藝。
當前國內萃取釩的工業中常用的萃取劑有堿性萃取劑、中性萃取劑、酸性萃取劑等,其中應用較為成熟的是酸性磷類萃取劑 P204[1]。在P204萃取石煤酸浸液的釩之前一般需要用堿中和石煤酸浸出液中的酸,再用硫代硫酸鈉還原溶液中高價態的釩,由于料液的中的酸經中和后減少,很難循環使用,因此試劑消耗量大[2-8]。伯胺N1923萃取釩(Ⅴ),在pH值為2時,釩(V)萃取率能達到95%以上,而pH大于6時萃取率不到35%[9-10]。劉波等[11]采用N263從釩(Ⅴ)溶液中回收釩(Ⅴ),研究發現萃取料液的pH值控制在5~7時,萃取率達90%以上。張云等[12]在石煤酸浸液中采用三正辛胺萃取釩(Ⅴ),并以TBP為協萃劑,結果發現在pH值為2~3時萃取速度快,萃取率大于98%。伯胺N1923、N263和三正辛胺用于萃取釩(V)時,對溶液的pH要求比較苛刻,工業上一般不采用。姚寶書[13]采用TBP對偏釩酸銨進行萃取研究,發現在濃度為0.5 mol/L NH4VO3的HCl溶液中,O/A=1/1、室溫下,萃取率可達98%以上,關于其工業應用未見報道。沈明偉等[14]研究了P507分離釩(Ⅳ)、鉬(Ⅵ),發現在用P507+磺化煤油組成的有機相萃取石煤酸性浸出液中的釩(Ⅳ)的同時,溶液中的鉬也被萃取,且常溫下,O/A=1/2時,經5級逆流萃取,鉬(Ⅵ)、釩(Ⅳ)的萃取率均達到98%以上。P507對釩(Ⅳ)、鉬(Ⅵ)的選擇性較差,因此難以應用于工業生產中。劉玉國等[15]研究了P538環己烷溶液萃取硫氰酸釩(Ⅴ)的機理,研究發現在溫度為20℃的條件下,萃取機理為 VO+2離子與萃取劑電離出的H+交換,萃合物的組成中n( VO+2):n(HA-)=1:1,但其萃取效果并未見詳細報道。KIM等[16]報道了采用乙酰丙酮從廢催化劑蘇打浸出液中萃取鉬(Ⅵ)、釩(Ⅴ)的研究,釩(Ⅴ)的萃取率接近100%。但沒有關于該研究成果更進一步的詳細報道。
綜上所述,目前釩萃取的研究及工業生產上存在工藝流程長、循環利用效果差、生產成本高、萃取劑選擇性差、溶液的酸堿度要求嚴格等不足。此外,未見從高酸浸出液中直接萃取釩的報道。為了克服上述不足,同時解決高酸條件下萃取釩的問題,本文作者首次提出了在不對石煤高酸浸液進行中和處理的情況下,用氧化劑將高酸溶液中低價態釩氧化為釩(Ⅴ),然后用肟類萃取劑HBL101直接從高濃度的硫酸浸出溶液中選擇性萃取釩;其中萃余液的酸度不降低,可返回用于浸出;減少了 P204萃取工藝中浸出液的中和、還原和反萃液氧化等工序,降低了試劑的消耗,節約了生產成本,提高了生產效率。肟類萃取劑常用于從水溶液中萃取銅、鈷、鎳等,其用于萃取釩曾有學者研究。ZENG等[17]進行了用肟類萃取劑LIX63從酸性溶液中萃取回收鉬(Ⅵ)、釩(Ⅴ)的研究,結果顯示,在pH值為1~2時該萃取劑可以從含Fe的溶液中選擇性萃取鉬(Ⅵ)、釩(Ⅴ),其研究也停留在酸度較低的條件下,未見高酸條件下萃取釩研究的報道。
1 實驗
1.1 實驗試劑與設備
1.1.1 實驗試劑
萃取劑主要有 HBL101,這是一種肟類螯合萃取劑,國內某廠提供;稀釋劑為磺化煤油。
料液為國內某公司提供的高濃度的石煤硫酸浸出液,料液酸度為1.458 mol/L,在本實驗中提到的酸度均為H+濃度,其單位均為mol/L,其成分見表1。
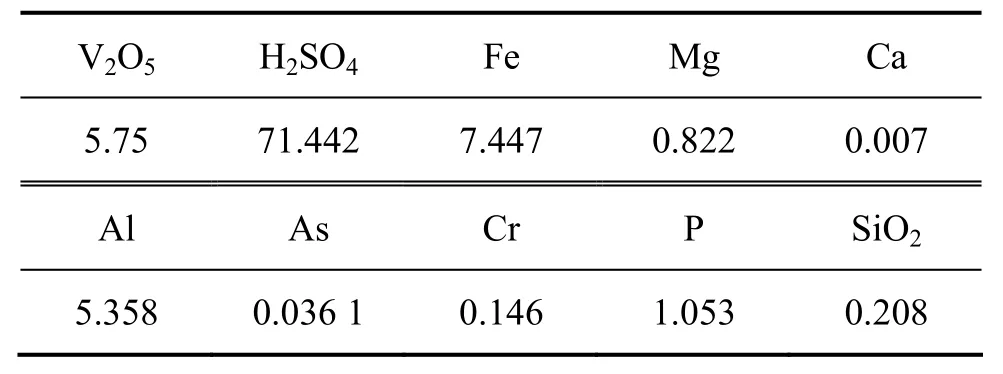
表1 料液各組分的濃度Table1 Chemical components of feed solution (g/L)
1.1.2 實驗設備
125 mL/250 mL梨型分液漏斗,康氏振蕩器,pH/ORP-4571酸度計/氧化還原電位計,電感耦合等離子體發射光譜儀。
1.2 實驗原理
由于萃取劑是肟類螯合萃取劑,被萃取的金屬陽離子與HL作用生成螯合物MLn,進入有機相生成萃合物,其反應方程如下:
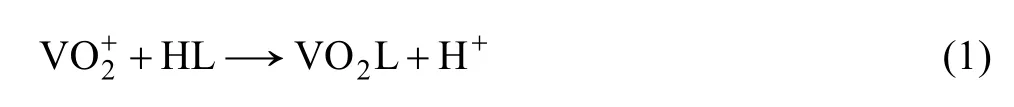
負載有機相反萃采用NaOH溶液,其中Na+與萃合物中的 VO+2交換,Na+進入有機相發生反萃反應,其反應方程式如下:
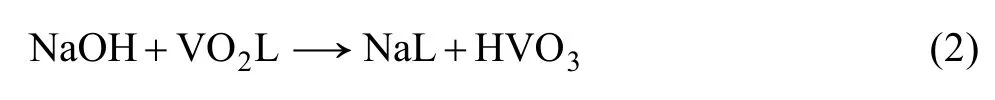
1.3 實驗方法
(1) 料液預處理:實驗前將沉淀過濾后,向料液中加入氯酸鈉進行氧化,氧化時攪拌30 min,攪拌結束后靜置8~24 h。(2) 有機相的配制:按萃取劑與稀釋劑體積比為1:9,量取有機相于燒杯內,充分攪拌,使其混合均勻即得所需的有機相。(3) 萃取實驗:先量取一定體積有機相裝入125 mL分液漏斗,再量取需要量的料液,加入裝有有機相的分液漏斗,根據要求的萃取條件,將分液漏斗放入水浴恒溫振蕩器中勻速振蕩,根據實驗要求的時間等條件來控制振蕩過程,振蕩結束后,取出分液漏斗,置于萃取架分層。分析萃余液中各元素的濃度,計算萃取率(E)。

式中:[Me]a為萃余液中離子濃度,g/L;[Me]o為料液中離子濃度,g/L;Va為萃余液的體積,L;Vo為料液的體積,L。
2 結果與討論
2.1 料液酸度對各元素萃取率的影響
實驗料液:用NaClO3將料液氧化到電位950 mV,靜置24 h以上開始實驗,料液中V2O5濃度5.75 g/L。
萃取條件如下:O/A為1/2,萃取時間為10 min,分相時間3 min,溫度為28℃,水相體積為60 mL,實驗結果如圖1所示。
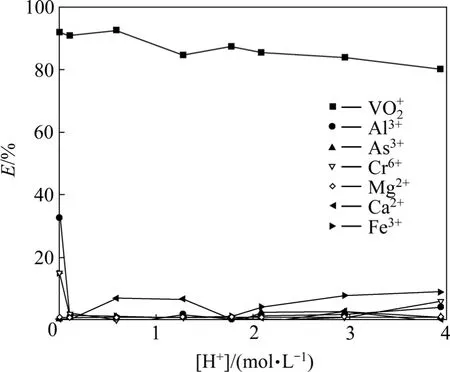
圖1 酸度對各元素萃取率的影響Fig.1 Effect of [H+]on extraction of elements
從圖1可看出,溶液酸度對釩的萃取率影響不顯著。隨著酸度的增加,釩的萃取率呈略微下降的趨勢,在O/A=1/2、酸度為4 mol/L時釩的單級萃取率仍然達到80%以上。從萃取原理 Mn+(aq)+nHL(org)=MLn(org)+nH+(aq)看出,在高酸條件下釩與萃取劑的結合能力大于H+及其他金屬雜質離子的結合能力。隨著酸度的降低,從圖1可以出,少量Fe、Al離子被萃取,分析認為,酸度的降低使萃取平衡反應向右移動,有利于萃取金屬離子,Fe3+、Al3+與萃取劑結合能力隨著酸度的降低而增強,故有少部分 Fe3+、Al3+在低酸條件下被萃取。其中,Ca2+在酸度為0.5~1.5 mol/L時,也有少部分被萃取,但Ca2+的總濃度為0.007 g/L,可能是由于存在分析誤差,使其萃取率接近 8%。而在各酸度條件下釩的萃取率均在80%以上,而其他雜質的萃取率較低,說明該萃取劑在0~4 mol/L酸度條件下對釩(Ⅴ)具有較好的選擇性,可以直接從高酸溶液中萃取釩(Ⅴ),同時達到與Fe3+、Al3+等雜質分離的效果。
2.2 料液電位對釩、鐵、鈣、鎂萃取率的影響
實驗料液:用NaClO3將料液氧化到電位分別為445、578、605、782、884、956、1 072、1 135 mV,靜置24 h后再萃取,料液酸度為1.458 mol/L。
萃取條件如下:O/A為1/1,萃取時間為10 min,分相時間3 min,溫度為28℃,水相體積為50 mL,考察溶液電位對萃取的影響,實驗結果如圖2所示。
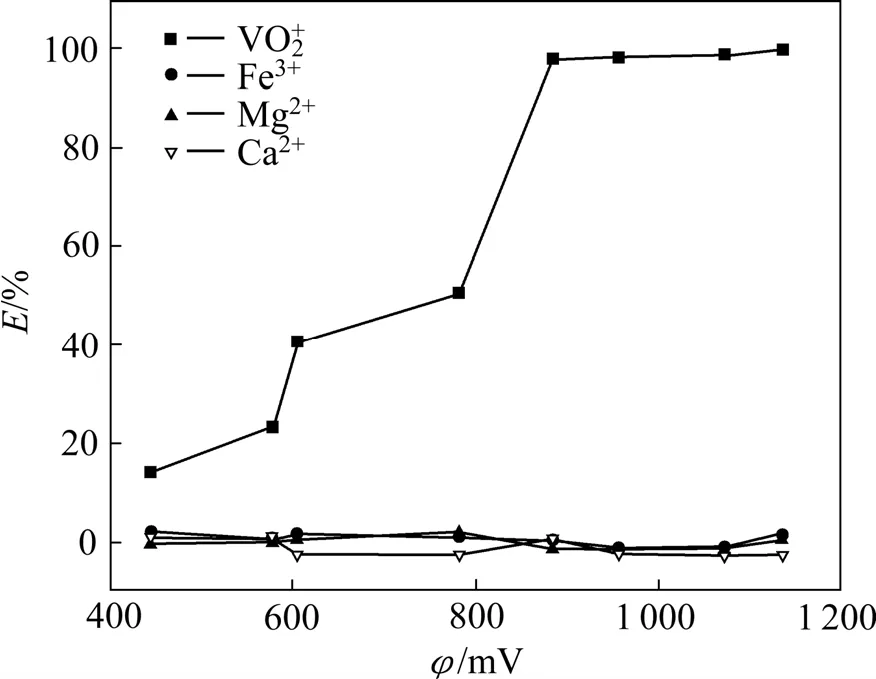
圖2 料液電位與萃取率的關系Fig.2 Effect of potential of feed solution on extraction of metals
由圖2可看出,釩的萃取率隨電位的增大呈上升趨勢。且當電位在850~900 mV 時,釩的萃取接近100%,而高于該電位范圍時,釩的萃取率基本不發生改變。根據釩水溶液φ—pH圖[18]可知,在溶液酸度為1 mol/L、電位在900 mV以上釩是以VO+2形式存在。結合圖2可知,在電位低于850 mV時,釩大部分是以VO+2和VO2+陽離子形式存在,隨著電位的升高,溶液中 VO+2占的比例升高,而萃取率也隨著電位的增大而升高,說明該萃取劑對VO+2具有較好的萃取效果。隨著電位的變化,溶液中Fe的價態也在變化,在低電位時,Fe以Fe2+形式存在,隨著電位的升高,由Fe2+變成Fe3+,而Fe的萃取率不管電位如何變化幾乎為零。溶液中的Ca2+、Mg2+的價態不隨電位的變化而發生改變,其萃取率幾乎都為零,實驗結果表明該萃取劑對VO+2具有較高的選擇性,避免了Fe2+、Fe3+、Mg2+、Ca2+等離子給濕法冶金分離帶來的困擾。
2.3 萃取時間對釩和鐵萃取率的影響
實驗料液:用NaClO3將料液氧化到電位880 mV,靜置24 h開始實驗,料液[H+]為1.458 mol/L,料液中V2O5濃度為5.75 g/L。在本文作者的后續實驗的料液均與本實驗的相同。
萃取條件如下:O/A為1/1,分相時間為3 min,溫度為28℃,水相體積為50 mL,實驗結果如圖3所示。
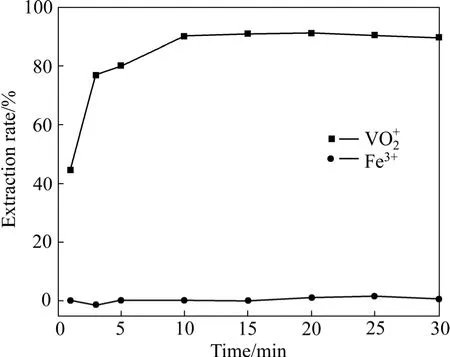
圖3 萃取時間與釩萃取率的關系Fig.3 Effect of time on extraction of metals
從圖3可看出,在10 min內,VO+2萃取率隨著時間的延長而提高,當萃取時間超過10 min時萃取率基本不變,即該萃取劑萃取釩在10 min左右達到了萃取平衡,故選擇最佳萃取時間為10 min。而不管時間如何變化鐵萃取率幾乎為零,由于料液經過預處理,料液中的鐵為Fe3+,說明該萃取劑能有效地分離 VO+2和Fe3+。
2.4 萃取相比對釩萃取率的影響
萃取條件如下:萃取時間為10 min,溫度為28℃,分相時間為3 min,有機相體積為30 mL,實驗結果如圖4所示。
從圖4可以看出,隨著O/A的減小釩萃取率降低,對于含10%的肟類萃取劑,O/A=1/1時其單級萃取率在95%以上,相比越小,水溶液中的釩(Ⅴ)含量越高。為了保證浸出液的萃取率,應采取相比1/1。在實際生產中,采用相比1/1,通過改變水相和有機相流量來保證有機相的飽和萃取。
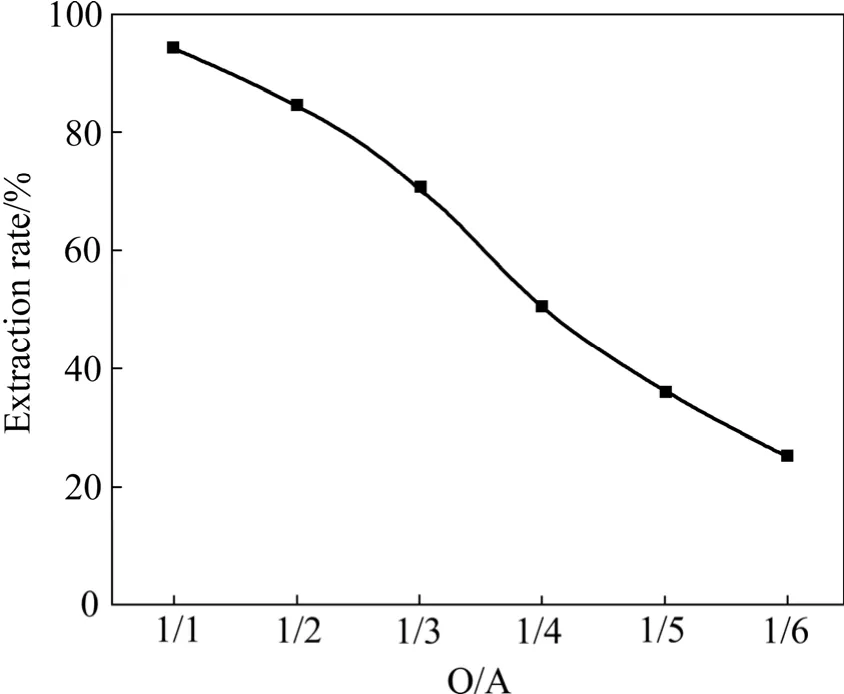
圖4 相比對釩萃取率的影響Fig.4 Effect of O/A on extraction of vanadium
2.5 萃取溫度對釩和鐵萃取率的影響
萃取條件如下:O/A=1/1,萃取時間為10 min,分相時間為3 min,水相體積為50 mL,實驗結果如圖5所示。
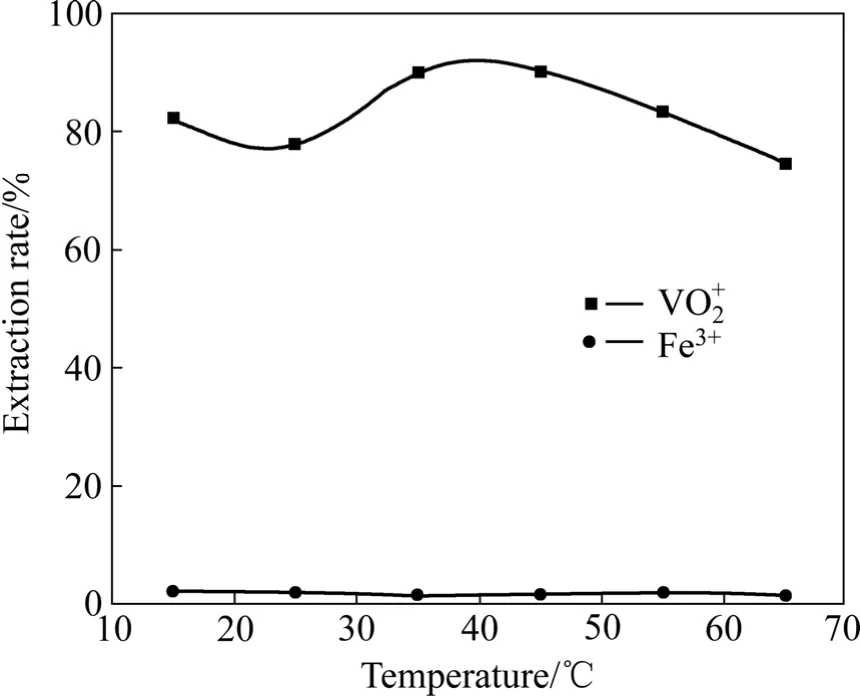
圖5 溫度對萃取的影響Fig.5 Extraction of temperature on extraction of vanadium
從圖5可看出,肟類萃取劑在低溫下其萃取釩(Ⅴ)的效果并沒有達到最佳,這可能與溫度低萃取反應的活性低有關。35~45℃時,萃取率達到最高,隨著溫度升高萃取率反而降低。因為溫度過高,肟類萃取劑會發生突變[19],有機相的揮發增大,造成有機相的損失增大。同時溫度越高對能源的需求也越多。故萃取釩的最佳溫度應該為35~45℃。不管溫度如何變化,Fe的萃取率幾乎為0,說明溫度改變不會使該萃取劑萃取鐵。
2.6 釩萃取等溫曲線
在相比O/A=1/1、溫度為28℃、萃取時間為10 min時,采用相比法測定萃取飽和量,繪制萃取等溫曲線如圖6所示。
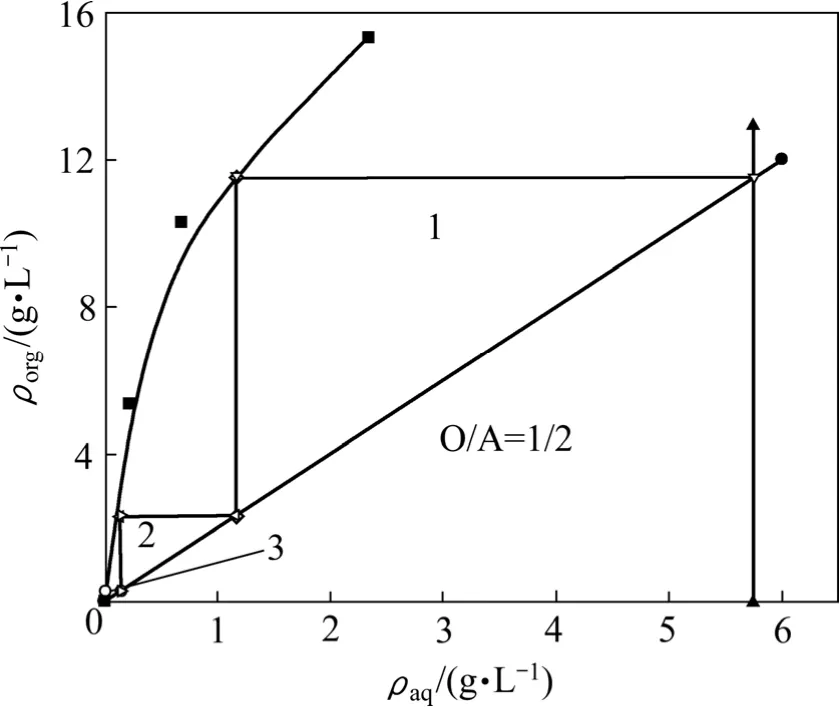
圖6 釩(Ⅴ)的萃取等溫曲線Fig.6 Isotherm extraction curves of vanadium(V)
從圖6可以看出,在有機組成為10%HBL101+90%磺化煤油的飽和萃釩量(V2O5)為15.28 g/L左右。由圖6可知,釩(Ⅴ)的萃取等溫線的斜率較大,說明釩(Ⅴ)在該萃取體系中萃取性能較好。依照逆流萃取原理,繪制馬克凱勒—齊利圖,設萃余液中釩(Ⅴ)濃度為0.03 g/L時,按照相比 O/A=1/2操作線,繪制釩(Ⅴ)的操作曲線,從圖6可以看出,通過三級逆流萃取,水相中的釩(Ⅴ)濃度可以降低至0.03 g/L。因此,該萃取體系需經過三級逆流萃取提取釩(Ⅴ)。
2.7 三級逆流實驗
在本實驗中,進行了6組三級逆流萃取實驗,操作流程圖如圖7,圖中A代表水相,O代表有機相,方框代表梨形分液漏斗。萃取條件如下:t=30℃,O/A=1/2.4,接觸時間10 min,分相時間3 min,V0=30 mL。圖7中,A1、A2、A3、A4、A5、A6分別表示三級迸流萃取后的萃余液,O1、O2、O3、O4、O5、O6分別表示三級迸流萃取的負載有機相。實驗結束后,用硫酸亞鐵銨滴定法分析 A1、A2、A3、A4、A5、A6中的釩濃度,用ICP分析A6中各雜質金屬離子的濃度。實驗結果分別見表2和表3。由表2可知,采用三級逆流萃取,萃余液中釩濃度低于0.02 g/L,釩的萃取率達到99.7%以上。從表3可以看出,料液中的雜質金屬離子萃取率幾乎為零,說明萃取劑對釩具有較高的選擇性。
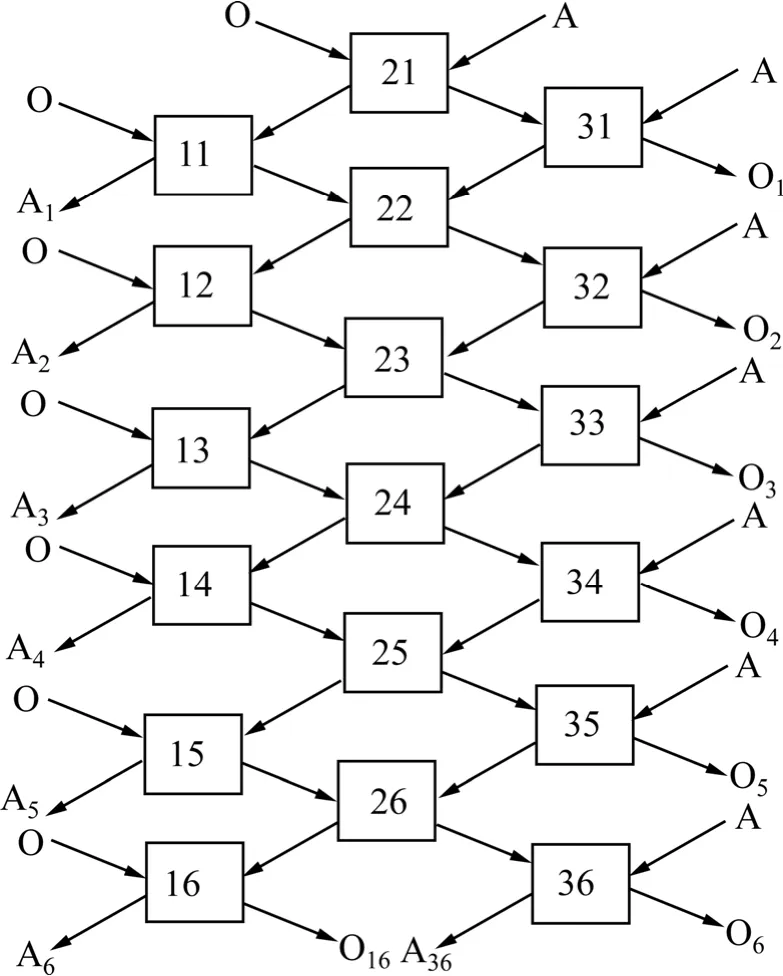
圖7 三級逆流萃取模擬實驗流程Fig.7 Flowchart of simulated three-stages counter current extraction
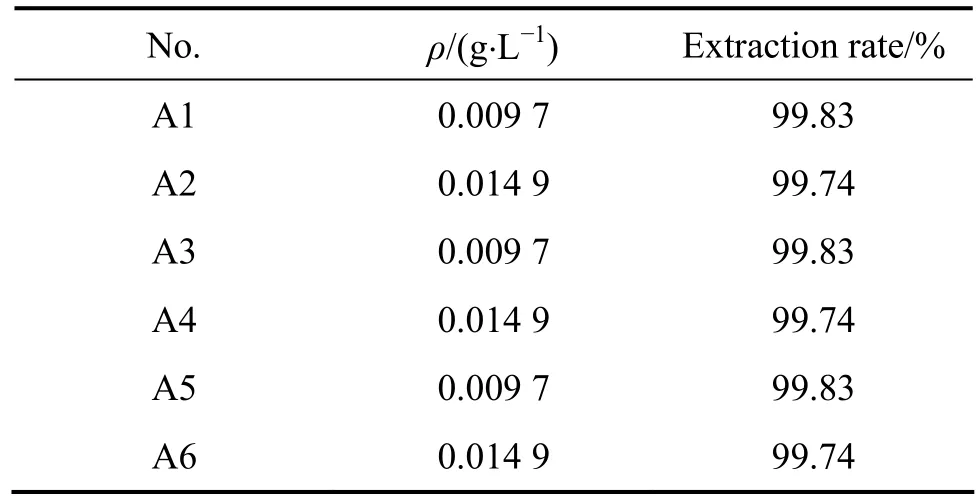
表2 釩的三級逆流模擬試驗結果Table2 Vanadium of simulated three-stage counter current extraction
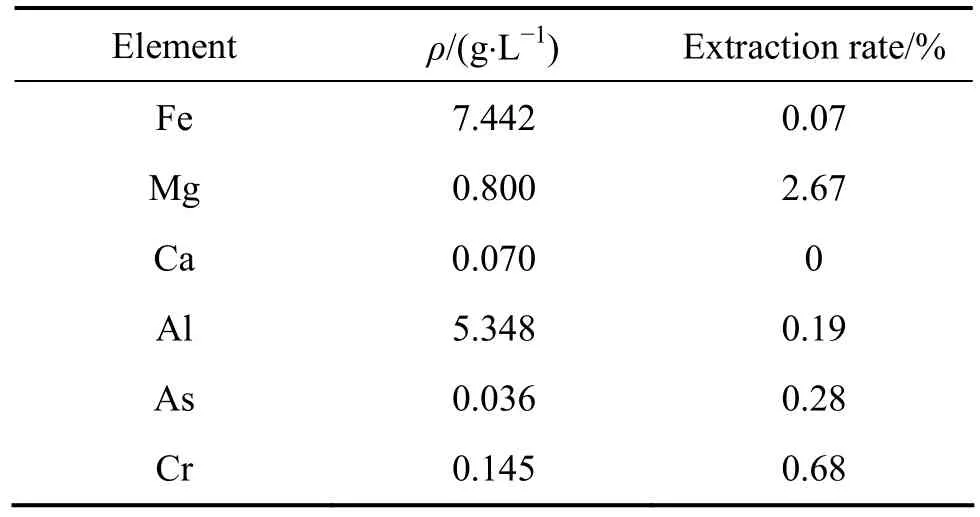
表3 A6中各種雜質金屬離子的實驗結果Table3 Metals of simulated counter current extraction in A6
將按照圖7所示操作流程圖實驗得到的負載有機相O1、O2、O3、O4、O5、O6混合后,用1 mol/L 的NaOH按O/A=1/1,在室溫下反萃30 min得到的反萃液調節pH為8.8后采用銨鹽直接沉釩,得到的偏釩酸銨烘干后煅燒得到V2O5,采用ICP分析V2O5中各雜質含量,結果見表4。
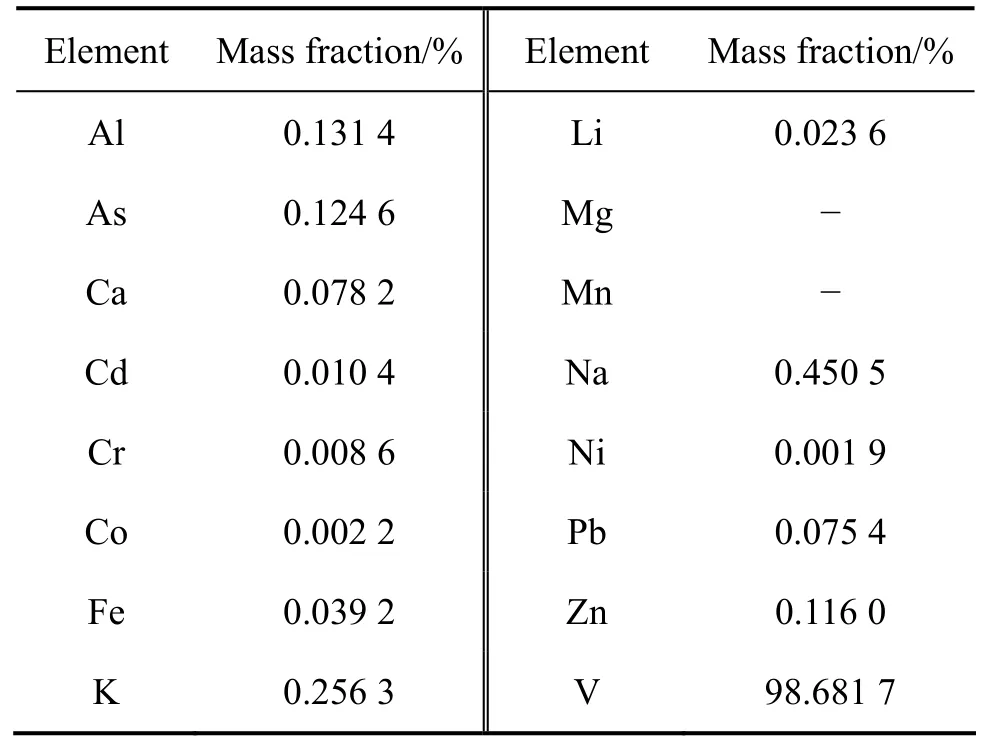
表4 五氧化二釩中主要雜質元素的質量分數Table4 Major impurity contents in V2O5
從表4可以看出,負載有機相直接反萃后得到反萃液,反萃液直接沉釩得到的產品純度達到98.68%。該萃取劑不萃取料液中的Fe等元素,所得萃余液的釩(Ⅴ)含量均較低,且分相速度快,得到的反萃液可直接沉釩,最終得到的產品純度達到98.68%以上。
3 結論
1) HBL101能在酸度為0~4 mol/L的范圍內萃取VO+2,且不萃取Fe3+、Al3+、Ca2+、Mg2+等雜質金屬,具有較優良的選擇性。
2) HBL101萃取石煤高酸溶液中V2O5的最佳萃取條件如下:溫度 35~45℃,萃取時間 10 min,O/A=1/1,在該條件下釩(Ⅴ)的單級萃取率達到95%以上。
3) 通過 HBL101萃取等溫曲線求得逆流萃取的理論級數為3級,經3級逆流萃取,釩的萃取率達到99.68%以上。
4) HBL101不需要調節酸度,可直接萃取料液,節約了生產成本,降低了環境污染。其萃取飽和量相比P204大,達到15.28 g/L,該萃取劑應用于工業生產能有效地避免 P204萃取工藝中的中和調酸、還原等步驟,且該萃取劑 VO+2具有較高的選擇性,避免了濕法冶金中Fe3+的干擾。負載有機相反萃后,反萃液經調節pH值后,可直接用氯化銨沉釩,同樣也避免了P204萃取工藝中反萃液氧化后沉釩。
[1]李尚勇, 謝 剛, 俞小花.從含釩的浸出液中萃取釩的研究現狀[J].有色金屬, 2011, 63(1): 100-104.LI Shang-yong, XIE Gang, YU Xiao-hua.Vanadium extraction with acidic medium[J].Nonferrous Metals, 2011, 63(1):100-104.
[2]魯兆伶.用酸法從石煤中提取五氧化二釩的試驗研究與工業實踐[J].濕法冶金, 2002, 21(4): 175-183.LU Zhao-ling.Investigation and industrial practice on extraction of V2O5from stone coal containing vanadium by acid process[J].Hydrometallurgy of China, 2002, 21(4): 175-183.
[3]王曉丹, 朱 云.制酸廢催化劑回收釩[J].有色金屬, 2010,62(4): 62-64.WANG Xiao-dan, ZHU Yun.Vanadium recovery from spent acid-making catalyst[J].Nonferrous Metals, 2010, 62(4): 62-64.
[4]胡建鋒, 朱 云.P204萃取硫酸體系中釩的性能研究[J].稀有金屬, 2007, 31(7): 367-370.HU Jian-feng, ZHU Yun.Extraction of vanadium by P204 from sulfuric acid solution[J].Chinese Journal of Rare Metals, 2007,31(7): 367-370.
[5]LI Xing-bin, WEI Chang, DENG Zhi-gan, LI Min-ting, LI Cun-xiong, FAN Gang.Selective solvent extraction of vanadium over iron from a stone coal/black shale acid leach solution by D2EHPA/TBP[J].Hydrometallurgy, 2010, 105: 359-363.
[6]李興彬, 魏 昶, 樊 剛, 鄧志敢, 李旻廷, 李存兄.溶劑萃取-銨鹽沉釩法從石煤酸浸液中提取五氧化二釩的研究[J].礦冶, 2010, 19(3): 49-53.LI Xing-bin, WEI Chang, FAN Gang, DENG Zhi-gan, LI Min-ting, LI Cun-xiong.Research of vanadium pentoxide from an acid leaching solution of stone coal using solvent extraction and ammonium precipitation[J].Mining & Metallurgy, 2010,19(3): 49-53.
[7]李曉健.酸浸-萃取工藝在石煤提釩工業中的設計與運用[J].湖南有色金屬, 2000, 16(3): 21-23.LI Xiao-jin.Design and application of acid leaching—Extraction processing in bone coal extracting vanadium industry[J].Hunan Nonferrous Metals, 2000, 16(3): 21-23.
[8]曹耀華, 高照國, 劉紅召, 李 琦.萃取法從含釩酸浸液中提取釩的研究[J].河南化工, 2007, 24(6): 20-23.CAO Yao-hua, GAO Zhao-guo, LIU Hong-zhao, LI Qi.Study on vanadium extraction from vanadium acid leaching solution[J].Henan Chemical Industry, 2007, 24(6): 20-23.
[9]WANG Yu-xing, LUO Qin-ge, LIU Shu-me.A study on extraction mechanism of vanadium(Ⅴ) by primary amine N1923[J].Natural Science Journal of Xiangtan University, 1990,19(3): 139-146.
[10]劉彥華, 楊 超.用溶劑萃取法從含釩浸出液中直接沉淀釩[J].濕法冶金, 2010, 29(4): 263-267.LIU Yan-hua, YANG Chao.Research on direct precipitate of vanadium in vanadiferous leaching solution[J].Hydrometallurgy of China, 2010, 29(4): 263-266.
[11]劉 波, 馮光熙, 黃祥玉, 張 敏.用N263從釩溶液中回收釩[J].化學研究與應用, 2003, 15(1): 54-57.LIU Bo, FENG Guang-xi, HUANG Xiang-yu, ZHANG Min.Recovery of vanadium pentoxide from contained vanadium solution with methyltri (C9-11 alkyl) ammonium chloride[J].Chemical Research and Application, 2003, 15(1): 54-57.
[12]張 云, 范必威, 彭達平, 陳細發.從石煤酸浸液中萃取釩的工藝研究[J].成都理工學院學報, 2001, 28(1): 107-109.ZHANG Yun, FAN Bi-wei, PENG Da-ping, CHEN Xi-fa.Technology of extracting V2O5from the stone coal acid-leaching solution with TOA[J].Journal of Chengdu University of Technology, 2001, 28(1): 107-109.
[13]姚寶書.TBP萃取偏釩酸銨的條件[J].化學世界, 1990, 31(1):12-14.YAO Bao-shu.The conditions of ammonium metavanadate extraction using TBP[J].Chemical World, 1990, 31(1): 12-14.
[14]沈明偉, 朱昌洛, 李華倫.P507-煤油體系在釩鉬萃取分離中的試驗研究[J].礦產綜合利用, 2007(4): 14-18.SHENG Ming-wei, ZHU Chang-luo, LI Hua-lun.P507-Kerosene system in extraction separation of vanadium and molybdenum[J].Multipurpose Utilization of Mineral Resources,2007(4): 14-18.
[15]劉玉國, 安 悅, 付曉東, 楊 東.P538萃取釩(Ⅳ)的研究[J].光譜實驗室, 1998, 15(5): 32-34.LIU Yu-guo, AN Yue, FU Xiao-dong, YANG Dong.Study on vanadium(Ⅳ) extracted by P538[J].Chinese Journal of Spectroscopy Laboratory, 1998, 15(5): 32-34.
[16]KIM K, CHO J W.Selective recovery of metals from spent desulphurization catalyst[J].Korean Journal of Chemical Engineering, 1997, 14(3): 162-167.
[17]ZENG L, CHENG C Y.Recovery of molybdenum and vanadium from synthetic sulphuric acid leach solutions of spent hydrodesulphurisation catalysts using solvent extraction[J].Hydrometallurgy, 2010, 101: 141-147.
[18]POST K, RIBINS R G.Thermodynamic diagram for the vanadium-water system at 298.15 K[J].Electrochimica Acta,1976, 21: 401-405.
[19]BARNARD K R, TURNER N L.The effect of temperature on hydroxyoxime stability in the LIX63-versatic 10-tributyl phosphate synergistic solvent extraction system under synthetic nickel laterite conditions[J].Hydrometallurgy, 2011, 109:245-251.

