不同維生素D制劑對育齡女性血清甲狀旁腺激素及總抗氧化能力的影響
鄭 振,李世云,李 勤
維生素D(VitD)是人體必需的營養素,需要通過日光照射或食物攝入獲得。VitD缺乏已經成為一個全球性問題引起廣泛關注,我國VitD的缺乏尤其突出[1],而女性VitD缺乏更為顯著。近年來研究顯示VitD除具有經典的調節鈣磷平衡和維持骨骼健康的作用外,還具有其他更為廣泛的骨外生物學效應,如調節免疫、抗腫瘤、防治代謝綜合征和保護中樞神經系統的功能等[2]。VitD缺乏與糖尿病[3]、多發性硬化、心血管疾病[4]、卒中、代謝綜合征[5]以及其他慢性疾病的發生有重要關系。研究證實VitD缺乏誘導的氧化應激是引起這些慢性病的重要原因,而血清甲狀旁腺激素(PTH)處于VitD與氧化應激相互關系的中心環節[6]。血清總抗氧化能力(T-AOC)系統主要起著防護氧化作用,通過消除自由基、活性氧及分解過氧化物、阻斷過氧化鏈,防止組織細胞脂質過氧化,在評價對機體是否造成氧化損傷時比其他單項抗氧化指標敏感[7]。本研究對育齡女性補充VitD,觀察其血清PTH、T-AOC的變化,探討不同VitD制劑對機體抗氧化能力的影響。
1 資料與方法
1.1 納入和排除標準 納入標準:(1)年齡在18~49歲的未絕經女性,近2個月無外出居住者;(2)常規體檢無異常發現,體檢結論為健康者。排除標準:(1)有煙酒嗜好;(2)近3個月使用含鈣、VitD及維生素C(VitC)、維生素E(VitE)等其他抗氧化劑者;(3)妊娠女性;(4)合并有糖尿病、高血壓及其他慢性疾病。
1.2 臨床資料 選擇2012年9―10月成都大學附屬醫院體檢科體檢健康未絕經女性78例為研究對象,年齡18~49歲。取得知情同意后將受試者采用計算機隨機數字表法分為兩組:VitD2組38例,平均年齡(30.9±5.0)歲,體質指數(21.1±2.4)kg/m2;口服藥組40例,平均年齡(31.6±4.8)歲,體質指數(20.6±2.8)kg/m2;兩組年齡和體質指數比較,差異均無統計學意義(t值分別為0.613和0.873,P值分別為0.541和0.385),具有可比性。
1.3 方法 VitD2組予以VitD2注射液肌肉注射,每兩周注射40萬U;口服藥組予以碳酸鈣D3片+多維元素片各1片/d,口服。干預時間均為8周。干預期間,要求受試者保持不變的飲食和生活方式。VitD2注射液來自江西贛南海欣藥業公司,碳酸鈣D3片(每片含元素鈣600 mg+VitD3125 U)、多維元素片(每片含VitD3400 U)來自美國惠氏公司。干預前后分別測定血清PTH、T-AOC水平。血清PTH測定采用放射免疫法,T-AOC測定采用分光光度法。
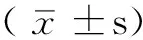
2 結果
干預前,VitD2組與口服藥組血清PTH和T-AOC比較,差異均無統計學意義(P>0.05);干預后,VitD2組較口服藥組血清PTH降低,T-AOC升高,差異均有統計學意義(P<0.05,見表1)。

Table1 Comparison of serum PTH and T-AOC between the two groups before and after intervention

組別例數PTH(ng/L)干預前 干預后T-AOC(U/ml)干預前 干預后VitD2組3828.22±11.9822.97±8.9422.69±5.2634.03±10.58口服藥組4028.05±13.2029.30±10.8423.56±5.2423.60±6.07t值0.0592.9080.7335.371P值0.9530.0060.4660.000
注:PTH=甲狀旁腺激素,T-AOC=總抗氧化能力
3 討論
VitD作為人體必需的一種維生素,是機體鈣磷代謝的重要調節因子。VitD缺乏與多種心、腦、腎疾病和代謝性疾病相關。這是由于維生素D受體(VDR)普遍存在于心臟、腎臟、免疫系統、腦和肌肉的細胞和組織中[8]。研究表明VitD作為抗氧化劑可以保護內皮細胞防御氧化應激的影響[9]。
本研究結果顯示,VitD2組干預后PTH水平下降。研究發現大劑量的VitD2注射液可以顯著提高血25-羥維生素D〔25(OH)VD〕的水平[10],且PTH和血清25(OH)VD呈負相關[11]。PTH分泌受鈣離子濃度的調節,當血鈣過低時可刺激PTH分泌,血鈣濃度過高時則可抑制PTH分泌。25(OH)VD可以通過調節血鈣的濃度間接影響PTH的水平。VDR廣泛存在于機體中的各個組織及器官,包括甲狀旁腺,VitD的最終活性產物1,25-二羥維生素D〔1,25(OH)2VD〕通過甲狀旁腺上的VDR直接調節PTH的分泌。
本研究結果顯示,給予VitD2干預后,血清T-AOC水平升高,說明機體氧化應激狀態得到了改善。Salum等[12]認為VitD通過影響氧化應激介導的通路,減少心血管疾病的風險,通過對糖尿病大鼠的研究證實VitD可以改善糖尿病存在的氧化應激狀態。本研究受試者為非糖尿病人群,即使沒有合并類似慢性病,大劑量VitD同樣可以改善機體的氧化應激狀態。本研究口服藥組含VitD總量525 U,劑量較小,PTH水平無明顯改變。目前研究未發現有關碳酸鈣D3片和多維元素片有產生氧化應激作用,不考慮口服藥物中525 U的VitD所產生的抗氧化作用被藥物中其他成分產生氧化作用所拮抗,表明525 U的VitD沒有產生抗氧化作用。
本研究VitD2組干預后血清PTH水平較口服藥組下降,補充大劑量VitD2對VitD缺乏所致繼發性PTH水平升高有一定的改善作用。甲狀旁腺功能亢進作為動脈硬化的獨立危險因素,可能激活內皮細胞的氧化應激損傷,而VitD缺乏易引起繼發性PTH升高,從而導致氧化應激損傷的發生[13]。VitD吸收減少,使得25(OH)VD降低首先引起低1,25(OH)2VD,血清離子鈣(Ca2+)減少,因此PTH釋放增加,PTH可以直接激活腎素-血管緊張素系統(RAS)。同時PTH激活腎臟1α-羥化酶,1,25(OH)2VD通過激活細胞膜VDR,使細胞內鈣不斷增加。鈣的流入激活煙堿腺嘌呤二核苷酸磷酸(NADPH)氧化酶、穩定NADPH氧化酶的蛋白激酶C(PKC)及髓過氧化物酶,產生活性氧(ROS)。此外,1,25(OH)2VD結合核VDR抑制解偶聯蛋白2(UCP2)活動,從而降低ROS清除[6]。補充VitD可以從起始階段抑制PTH的產生,直接抑制RAS,減少ROS的產生,增加ROS的清除。
最近的包括51個隨機試驗的薈萃分析顯示,補充小劑量的VitD(1 000 U /d)在改善內皮細胞氧化應激狀態上無明顯獲益[14]。香港大學的Yiu等[15]對100例2型糖尿病患者進行隨機雙盲的臨床試驗,分別予以補充VitD(5 000 U/d,n=50)和安慰劑(n=50),時間為12周。相對于安慰劑組,治療組的血清PTH水平降低。然而,反映內皮細胞氧化應激狀態的指標——超敏C反應蛋白(hs-CRP)、超氧化物歧化酶和8-異前列腺素卻沒有變化。本研究結果顯示,對于非糖尿病人群,大劑量VitD可改善機體的氧化應激狀態。對于是否可以降低因氧化應激引起的內皮細胞損傷,從而可以在降低糖尿病心血管并發癥及其他心血管疾病的病死率上獲益有待進一步臨床試驗研究。
綜上所述,大劑量VitD可以抑制育齡女性PTH的分泌,增加T-AOC水平,減輕機體氧化應激反應。將VitD進一步應用于臨床,預防與氧化應激緊密相關的慢性疾病的發生,還需要更大樣本、多種劑量和長期系統的研究。
1 Lips P.Worldwide status of vitamin D nutrition[J].J Steroid Biochem Mol Biol,2010,121(1/2):297-300.
2 畢曉娜,衣明紀.維生素D 缺乏與臨床疾病[J].青島大學醫學院學報,2011,47(3):280-282.
3 郭麗芳,李彩萍.血維生素D與2型糖尿病及其大血管病變關系的研究進展[J].疑難病雜志,2011,10(11):879.
4 Forman JP,Giovannucci E,Holmes MD,et al.Plasma 25-hydroxyvitamin D levels and risk of incident hypertension[J].Hypertension,2007,49(5):1063-1069.
5 Lu L,Yu Z,Pan A,et al.Plasma 25-hydroxyvitamin D concentration and metabolic syndrome among middle-aged and elderly Chinese individuals[J].Diabetes Care,2009,32(7):1278-1283.
7 鄧洋,許秀舉,于海平.啤酒對大鼠血清的LDH 和T-AOC的影響[J].食品科技,2009,34(5):120-122.
8 余華,朱再勝,高志立,等.維生素D缺乏與老年高血壓的相關性研究[J].中國全科醫學,2012,15(10):3345.
9 Polidoro L,Properzi G,Marampon F,et al.Vitamin D protects human endothelial cells from H2O2oxidant injury through the Mek/Erk-Sirt1 axis activation[J].Cardiovasc Transl Res,2013,6(2):221-231.
10 李世云,李勤,李強,等.不同維生素D制劑對長期從事室內工作的女性血25-羥維生素D水平的影響[J].中國全科醫學,2013,16(4):1411-1413.
11 Kestenbaum B,Katz R,de Boer I,et al.Vitamin D,parathyroid hormone,and cardiovascular events among older adults[J].J Am Coll Cardiol,2011,58(14):1433-1441.
12 Salum E,Kals J,Kampus P,et al.Vitamin D reduces deposition of advanced glycation end-products in the aortic wall and systemic oxidative stress in diabetic rats[J].Diabetes Res Clin Pract,2013,100(2):243-249.
13 Lavie CJ,Lee JH,Milani RV.Vitamin D and cardiovascular disease will it live up to its hype[J].J Am Coll Cardiol,2011,58(15):1547-1556.
14 Elamin MB,Abu Elnour NO,Elamin KB,et al.Vitamin D and cardiovascular outcomes:a systematic review and meta-analysis[J].J Clin Endocrinol Metab,2011,96(7):1931-1942.
15 Yiu YF,Yiu KH,Siu CW,et al.Randomized controlled trial of vitamin D supplement on endothelial function in patients with type 2 diabetes[J].Atherosclerosis,2013,227(1):140-146.

