通過左心室心外膜導線行心臟再同步治療六例分析
戴研,陳柯萍,華偉,陳若菡,張競濤,張澍
通過左心室心外膜導線行心臟再同步治療六例分析
戴研,陳柯萍,華偉,陳若菡,張競濤,張澍
目的:回顧性分析對于經冠狀靜脈竇放置左心室導線失敗的心力衰竭(心衰)患者,通過左心室心外膜導線行心臟再同步治療(CRT)的安全性和療效。
心力衰竭;再同步化治療;心外膜;外科手術
臨床研究提示,心力衰竭(心衰)患者中約30%合并心臟傳導異常,表現為QRS波增寬,或是左束支傳導阻滯[1],而引起心室收縮不同步,導致心衰的惡化及死亡率增加[2]。近年來,越來越多的證據顯示,對于左心室射血分數≤35%且QRS寬度≥120 ms,特別是左束支傳導阻滯患者,心臟再同步治療(CRT)能夠改善預后,降低死亡率[3]。
通過冠狀靜脈竇放置左心室導線是CRT植入中最困難的部分,隨著器械的進步,其成功率能夠達到90%以上,但仍有不到10%的患者因心臟擴大、冠狀靜脈竇變形,而導致經靜脈放置導線失敗[4];另外,因膈神經刺激造成左心室導線無法到達最佳部位,或者左心室導線術中及術后脫位,也是臨床上行CRT時經常遇到的問題[4]。在這些情況下,考慮經胸部小切口或者胸腔鏡放置左心室心外膜導線,是成功行CRT的另一種選擇[5,6]。本研究回顧分析了我院近年心內科與心外科聯合,雜交放置左心室心外膜導線與右心心內膜導線,行CRT患者6例,為臨床醫生提供參考。
1 資料與方法
病例選擇:選取2010-11至2013-01因慢性心衰住院行CRT,經心內科手術不成功而通過內、外科雜交行CRT的患者6例,男性4例,女性2例,年齡26~68(45±15)歲;其中5例為竇性心律,1例為持續性心房顫動(房顫)。入選患者均符合:①經藥物最優化治療至少3個月,紐約心功能分級(NYHA)為II~IV級;②左心室射血分數≤35%;③QRS波增寬:完全性左束支傳導阻滯伴QRS時限>120 ms;或非左束支傳導阻滯,QRS時限>150 ms。
手術經過: 6例患者經靜脈行CRT未成功后,經與心外科會診后,擇期再次行內、外科雜交行CRT。手術過程如下:全麻下,取右側30°~40°臥位;經第5肋間左前外側切口切開皮膚4~5 cm,逐層分離至胸腔內,切開心包,在左心室選擇適當部位縫合左心室導線,測試閾值滿意后關閉心包,放置引流管;經皮下隧道將左心室導線引致左鎖骨下。左鎖骨下切開皮膚,逐層分離至筋膜層,穿刺左鎖骨下靜脈,經左鎖骨下靜脈置入右心房、右心室導線,測試閾值滿意后,制作皮下囊袋,將右心房、右心室及左心室導線與脈沖發生器相接,將脈沖發生器埋于囊袋中。逐層縫合皮下組織及皮膚,返回病房。
研究方法:對所有病例進行臨床情況分析,包括病因、術前心功能狀況、心電圖和超聲心動圖結果、手術記錄及術后情況;出院后定期隨訪,第1次隨訪為3個月,以后每半年隨訪1次,觀察患者心功能、心電圖以及超聲心動圖變化,以觀察雜交行CRT的安全性及有效性。
2 結果
患者基線資料:本組6例患者均為擴張性心肌病,經優化藥物治療后,心功能II~III級,左心室射血分數18%~29%,平均(22±4)%;術前QRS波≥120 ms;除病例5為持續性房顫,其余均為竇性心律。所有患者均符合CRT標準,入院后擬行CRT。表1
手術結果:6例患者經靜脈行CRT失敗,一周內擇期行經胸左心室心外膜導線+經靜脈心內膜右心導線,雜交行CRT和(或)CRT聯合植入式心臟復律除顫器(CRT-D)。6例患者手術成功,左心室導線閾值(1.0±0.3)V/0.4 ms,植入位置見表2。手術后平均住院10.5天,無死亡。
經靜脈行CRT不成功原因:放置左心室導管時,4例因導管未找到冠狀竇開口,致冠狀竇插管失敗;1例因冠狀竇開口異常,1例因靜脈入路異常(永存左上腔靜脈),而導致經靜脈行CRT失敗(失敗原因詳見表1)。
術后并發癥:2例患者7天拆線后出院,其余4例患者分別因術后發熱、血象高,或肝腎功能受損,而延長住院時間至10~14天,其中病例5在出院前,通過CRT-D體內除顫,房顫轉復為竇性心律。6例患者均好轉后出院。表2
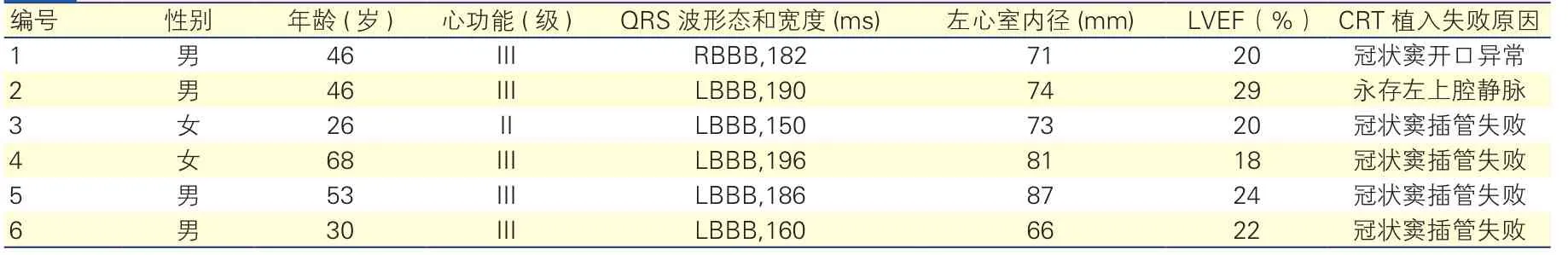
表1 6例患者基線臨床特征及靜脈植入心臟再同步治療失敗原因
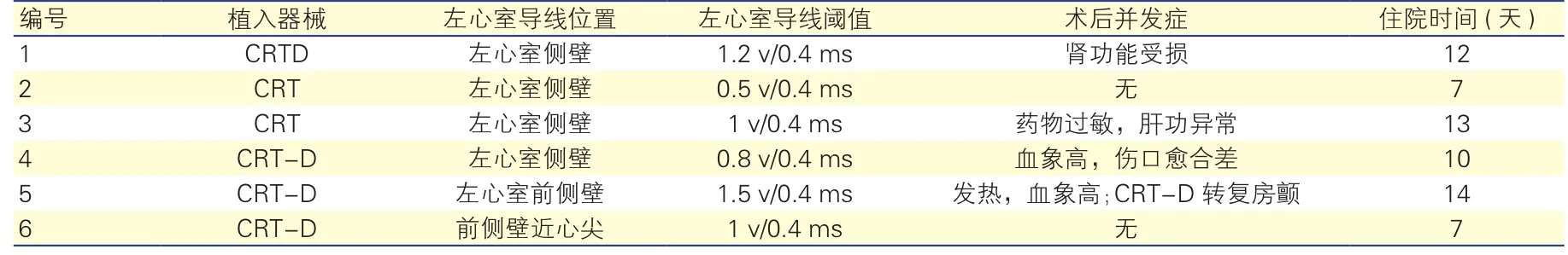
表2 6例患者手術情況、并發癥與住院時間
隨訪:①6例患者中,除例6術后QRS波較術前略增寬外,其他5例患者術后QRS波均有不同程度縮短(表3)。經隨訪3~18個月(平均10.5個月),6例患者均存活,例6因心衰惡化在CRT植入后6個月行心臟移植手術。②在出院后第1次隨訪時,6例患者雙心室起搏百分比均超過95%。從NYHA來看,4例患者(例1、2、4、5)心功能改善了1級(即由III級為II級),2例患者(例3及例6)心功能無改善;復查超聲心動圖顯示,3例(例1、2和5)患者左心室射血分數提高(10%以上),其中1例患者(例4)左心室射血分數增加(超過5%),2例患者(例3、6)左心室射血分數值無變化;2例患者(例2、5)左心室舒張末內徑有所減小,3例患者(例1、4、6)左心室大小無明顯變化,1例(例3)左心室舒張末內徑有所增加(表3)。③6例患者中,有3例患者隨訪超過1年(例1、2和5),其中例1、例2患者心功能恢復為I級,例5心功能為II級;左心室射血分數值分別較術前提高24%(例1),18%(例2)和11%(例5)。
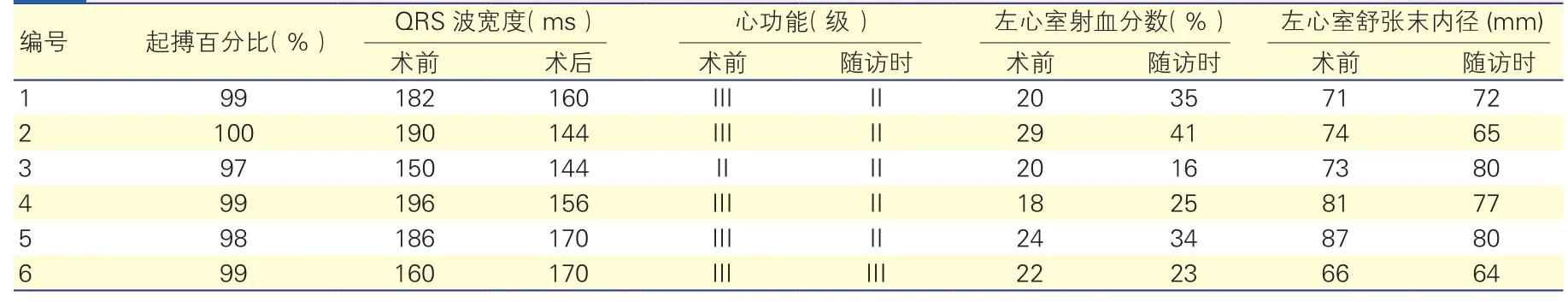
表3 6例患者術后QRS波變化以及第1次隨訪時心功能和超聲心動圖改變
3 討論
隨著循證醫學的進展,CRT治療慢性心衰的適應證越來越為廣泛;而QRS波的寬度和形態在選擇患者時具有非常重要的意義,很大程度決定了CRT的療效。本研究中,6例患者病因均為擴張性心肌病,且QRS波均≥120 ms,其中5例為左束支傳導阻滯,符合CRT植入的I類和IIa類適應證[3]。CRT植入中,左心室導線的放置是保證CRT療效的關鍵,目前首選經冠狀靜脈竇將導線放置在左心室靜脈分支而達到再同步的目的。早期經靜脈放置左心室導線失敗率較高,有報道超過20%;近些年隨著CRT適應證的拓寬、技術的成熟,失敗率降至8%~10%[4,7]。放置導線失敗的常見原因包括解剖因素異常(例如上腔靜脈閉塞、冠狀靜脈竇開口異常、右心房高度擴大、靜脈狹窄和永存左上腔靜脈等)和左心室導線相關問題(例如導線脫位,閾值過高和膈神經刺激)[4],本組6例患者經靜脈植入左心室導線失敗的原因全部為解剖因素異常,且4例均因冠狀靜脈竇插管失敗所導致。
直視下心外科放置左心室導線是靜脈植入失敗時行CRT的選擇之一,除此之外左心室心內膜起搏也是可供考慮的方案[4]。心外科放置左心室導線通常可采用經胸小切口的方法[6,8],此外還有通過胸腔鏡或其他機器輔助的方法[5,9],手術成功率及圍術期的預后相似[8]。目前關于外科手術放置左心室導線的研究很少,總體而言與經靜脈方法相比,因患者需要全麻以及創傷較大,因此圍術期并發癥發生率較高[8],主要為感染和腎功能損傷;同時住院天數延長[10]。本研究中,6例患者在經冠狀靜脈竇植入左心室導線失敗后,擇期通過外科方法,先經胸小切口切開心包,放置左心室導線,術中閾值滿意(均≤1.5 V/0.4 ms),且無膈神經刺激;隨后再經靜脈放置右心心內膜導線,通過皮下隧道,將導線與脈沖發生器相接,手術均成功,無術中并發癥。術后并發癥主要為肝功能異常和腎功能受損,無其他嚴重并發癥及死亡,術后平均10.5天出院。由此可見,在靜脈植入失敗時,內外科雜交行CRT為安全有效的替代方法。還有學者建議,CRT植入手術應直接在雜交室進行,在經靜脈放置左心室導線失敗時立即可通過外科方法植入左心室導線,以減少住院時間,降低感染并發癥,從而減少費用,獲得最大的經濟--效益比[11];但因缺乏大樣本研究,目前尚無定論。
大規模臨床研究已經證實CRT能夠改善心衰患者的癥狀,提高生活質量,逆轉左心室重構,增加左心室射血分數值,同時降低死亡率[3,12,13],但結果均來自經靜脈行CRT的研究;近年有研究發現,外科方法放置左心室導線與經冠狀靜脈竇植入相比盡管圍術期并發癥略高,長期隨訪兩組患者受益相似[6,8]。本組6例慢性心衰患者雜交行CRT后,經3~18個月隨訪,4例患者(占67%)心功能改善I級以上,這4例患者超聲心動圖左心室射血分數升高超過5%,其中2例患者伴有左心室舒張末內徑縮小;且隨著手術時間的延長,對心功能改善和增加左心室射血分數的作用持續存在,至1年隨訪時,左心室射血分數值較術前增加10%以上。由此可見,左心室心外膜起搏進行再同步治療同樣能夠改善心衰患者的預后,與文獻報道相符。
盡管CRT越來越多的應用于心衰患者,并大大改善了心衰患者的預后,然而仍有超過30%符合適應證的患者在CRT植入后沒有得到獲益(即CRT無反應)。本組6例患者中,從臨床和超聲兩方面評價,2例患者(占33%)發生了“CRT無反應”:1例在術后3個月及6個月隨訪時,心功能無改善,超聲心動圖顯示左心室射血分數及舒張末內徑等參數均無好轉;還有1例在行CRT6個月后因心衰惡化而行心臟移植。目前缺乏對于外科放置左心室導線行CRT的大樣本研究,因此CRT治療的無反應率以及預測因素尚不明確。有學者認為,因通過外科放置左心室導線不受血管條件影響,可將導線放置在“最佳”部位(多數為左心室側壁/后側壁),由此可能有益于提高CRT的“反應性”[8],但仍需要臨床研究證實。分析本組發生無反應的2例患者時發現,其中1例患者左心室導線放置靠近心尖部,且術后QRS波寬度無縮短,術后6個月因心衰惡化而行心臟移植。大規模臨床研究證實,經靜脈行CRT時,左心室導線位置與患者的預后有關,左心室導線放置在靠近心尖部較非心尖部相比,心衰惡化和死亡的風險明顯增加[14],因此本例患者術后發生“無反應”可能與導線位置有一定關系,應該在今后的臨床工作中予以重視。
研究結果提示,雖然經靜脈放置左心室導線是目前最為常用的行CRT的途徑,但在因解剖異常而導致手術失敗時,經胸小切口放置左心室心外膜導線是一種安全有效的替代方法;且通過雜交行CRT可以改善心衰患者的預后。本研究的不足之處在于樣本量過小,為觀察性研究,且未設立對照組與經靜脈行CRT進行比較,因此對于通過雜交行CRT的長期療效及其與常規經靜脈方法對患者預后的影響,還需要大樣本的對照研究證實。
[1] Farwell D, Patel NR, Hall A, et al. How many people with heart failure are appropriate for biventricular resynchronization? Eur Heart J, 2000, 21: 1246-1250.
[2] Bleeker GB, Schalij MJ, Molhoek SG, et al. Relationship between QRS duration and left ventricular dyssynchrony in patients with end-stage heart failure. J Cardiovasc Electrophysiol, 2004, 15: 544-549.
[3] Epstein AE, DiMarco JP, Ellenbogen KA, et al. 2012 ACCF/AHA/HRS Focused Update of the 2008 Guidelines for Device-Based Therapy of Cardiac Rhythm Abnormalities: A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines and the Heart Rhythm Society. J Am Coll Cardiol, 2013 , 61: e6-75.
[4] Daubert JC, Saxon L, Adamson PB, et al. 2012 EHRA/HRS expert consensus statement on cardiac resynchronization therapy in heart failure: implant and follow-up recommendations and management. Europace , 2012, 14: 1236-1286.
[5] Zhang HB, Meng X, Han J, et al. Minimally invasive video-assisted epicardial lead cardiac resynchronization therapy for the dilated cardiomyopathy heart failure cases. Innovations, 2010, 5: 345-348.
[6] Miller AM, Kramer DB, Lewis EF, et al. Event-Free Survival Following CRT with Surgically Implanted LV Leads Versus Standard Transvenous Approach. Pacing and Clin Electrophysiol, 2011, 34: 490-500.
[7] Abraham WT, Fisher WG, Smith AL, et al. Cardiac resynchronization in chronic heart failure. N Engl J Med, 2002, 346: 1845-1853.
[8] Ailawadi G, LaPar DJ, Swenson BR, et al. Surgically placed left ventricular leads provide similar outcomes to percutaneous leads in patients with failed coronary sinus lead placement. Heart Rhythm , 2010, 7: 619-625.
[9] DeRose JJ, Ashton RC, Belsley S, et al. Robotically assisted left ventricular epicardial lead implantation for biventricular pacing. J Am Coll Cardiol, 2003, 41: 1414-1419.
[10] Atoui R, Essebag V, Wu V, et al. Biventricular pacing for endstage heart failure : early experience in surgical vs. transvenous left ventricular lead placement. Interact Cardiovasc Thorac Surg , 2008, 7: 839-844.
[11] Quigley RL. A hybrid approach to cardiac resynchronization theray. Ann Thorac Cardiovasc Surg , 2011, 17: 273-276.
[12] Carvert M, Freemantle N, Cleland JG. Cardiac resynchronization therapy in heart failure. Ann Intern Med, 2005, 142: 305-307.
[13] Cleland JG, Daubert JC, Erdmann E, et al. The effect of cardiac resynchronization on morbidity and mortality in heart failure. N Engl J Med, 2005, 352: 1539-1549.
[14] Singh JP, Klein HU, Huang DT, et al. Left ventricular lead position and clinical outcome in the multicenter automatic defibrillator implantation trial-cardiac resynchronization therapy (MADIT-CRT) trial. Circulation , 2011, 123: 1156-1159.
Analysis of Cardiac Resynchronization Therapy via Left Ventricular Epicardial Lead Insertion in 6 Patients
DAI Yan, CHEN Ke-ping, HUA Wei, CHEN Ruo-han, ZHANG Jing-tao, ZHANG Shu.
Department of Cardiology, Cardiovascular Institute and Fu Wai Hospital, CAMS and PUMC, Beijing (100037), China Corresponding Author: CHEN Ke-ping, Email: chenkeping@263.net
Objective: To analyze the safety and eff i cacy of cardiac resynchronization therapy (CRT) via left ventricular (LV) epicardial lead implantation in chronic heart failure (CHF) patients who failed to coronary sinus lead insertion method.Method: We retrospectively studied 6 CHF patients who failed to coronary sinus lead insertion and received CRT implantation by hydride approach of epicardial LV minithoracotomy in our hospital from 2010-11 to 2013-01. We analyzed the pathogenesis, cardiac condition before, during and after the operation, examined ECG and echocardiography. The patients were fi rst followed-up at 3-6 months, and then every 6 months to observe the relevant changes.Results: All 6 patients received elective minithoracotomy for LV lead implantation within 1 week of the failed procedure, the pacing threshold was (1.0±0.3) V/0.4ms, the average in-hospital time was 10.5 days, there were no complication and death. During 3-18 (10.5) months follow-up period, 4 patients’ cardiac function improved for at least I degree, echocardiography showed that LVEF increased for at least 5% and 2 of them had decreased left ventricular end diastolic diameter. All patients survived, 1 received heart transplantation at 6 months after CRT implantation due to CHF worsening.Conclusion: CRT implantation by hydride approach of epicardial LV minithoracotomy is a safe and feasible alternation in patients who failed to coronary sinus lead insertion method, it may improve the cardiac function in CHF patients.
Heart failure; Cardiac resynchronization therapy; Epicardial lead; Surgery (Chinese Circulation Journal, 2014,29:44.)
2013-07-30)
(編輯:梅平)
100037 北京市,中國醫學科學院 北京協和醫學院 心血管病研究所 阜外心血管病醫院 心律失常診治中心
戴研 副主任醫師 博士 主要從事起搏電生理專業的臨床及科研工作 Email:daiy7516@sina.com 通訊作者:陳柯萍 Email:chenkeping@263.net
R541
A
1000-3614(2014)01-0044-04
10.3969/j.issn.1000-3614.2014.01.012
方法:選取2010-11至2013-01因慢性心衰住院行CRT,經心內科手術不成功而通過內、外科雜交行CRT的患者6例。對所有病例進行臨床情況分析,包括病因、術前心功能狀況、心電圖和超聲心電圖結果、手術記錄及術后情況;出院后定期隨訪,第1次隨訪為3~6個月,以后每半年隨訪1次,觀察患者心功能、心電圖以及超聲心動圖變化。
結果:6例患者經靜脈行CRT失敗后,1周內擇期雜交行CRT/CRT聯合植入式心臟復律除顫器(CRT-D),手術成功,左心室導線閾值( 1.0 ± 0.3)V/0.4 ms,無術中并發癥;手術后平均住院10.5天,無嚴重并發癥及死亡。隨訪3~18個月(平均10.5個月),其中4例患者心功能分級改善至少I級,且超聲心動圖顯示左心室射血分數(LVEF)值增加至少5%,其中2例伴左心室舒張末內徑縮小。6例患者均存活,1例因心衰惡化在CRT植入后6個月行心臟移植術。
結論:因解剖因素異常而導致經靜脈行CRT失敗時,經胸小切口放置左心室心外膜導線是一種安全有效的替代方法;且通過雜交行CRT可以改善心衰患者的預后。

