南極假絲酵母脂肪酶B在制備手性藥物中的應用
矯春麗,劉學杰
(煙臺市食品藥品檢驗所,山東煙臺264000)
南極假絲酵母脂肪酶B在制備手性藥物中的應用
矯春麗,劉學杰
(煙臺市食品藥品檢驗所,山東煙臺264000)
結合近期國內外的文獻,本文詳細介紹了南極假絲酵母脂肪酶B(CALB)在手性醇、胺、酸選擇性的拆分以及轉酯等的應用。利用脂肪酶合成手性藥物是藥物合成研究的一個重要領域,CALB在一些藥物的拆分和合成中表現出了良好的選擇性,本文主要綜述了其在手性醇、胺、酸選擇性拆分以及轉酯中的應用,希望能夠為手性藥物的合成提供方向。
南極假絲酵母脂肪酶;南極假絲酵母脂肪酶B;手性藥物;合成
生物催化劑能夠在溫和的條件下催化化學反應并同時展現出極高的選擇性,由于這種獨特的性質,生物催化逐漸成為精細化工、醫藥、農藥化學品及其中間體合成的核心技術[1],特別是在小分子手性藥物的制備過程中,生物催化不僅能夠達到各種法規所規定的合成手性藥物所需的光學純度,還能夠減少對環境的影響、替代復雜的化學合成路線等,是發展綠色、環境友好、高效節能的制藥工業的有力工具[2]。近年來,不斷有利用生物催化制備小分子手性藥物中間體特別是“重磅藥物”的例子出現,如阿托伐他汀[3]、西格列汀[4]等。
脂肪酶(甘油三酯水解酶,EC 3.1.1.3)是廣泛存在于有機體內能夠催化甘油三酯水解的一類酶。目前,脂肪酶是在有機合成中研究和應用最多的生物催化劑,因為脂肪酶具有底物范圍廣、催化效率、選擇性高,耐受有機溶劑[5]、可適度耐高溫、無毒、對環境友好并且低成本等優點。來源于南極假絲酵母(Candida antarctica)的脂肪酶A(Candida antarctica lipase A,CALA)和脂肪酶B(Candida antarctica lipase B,CALB)便是研究和應用較多的兩種脂肪酶[6],本文將著重討論CALB在制備手性藥物中的應用。
1 南極假絲酵母脂肪酶
1.1 CALA、CALB簡介 CALA和CALB都具有獨特的催化性質,CALA是熱穩定性的酶,其最適溫度可達90℃,盡管CALB的熱穩定性不及CALA,但固定化的CALB和CALA均可在適度高溫的環境中維持活性的長時間穩定。雖然來源于同一菌種,但CALA和CALB的一些催化性質卻有所差別[6]:相對于CALA,CALB具有Sn-3選擇性;類似于大多數脂肪酶,CALA具有界面接觸效應,CALB則是少數沒有這種效應的脂肪酶之一,因而CALB能夠在單相溶媒介質中具有高的催化活性;CALB是拆分醇和胺的最優催化劑之一,CALB在制備光學純的羥基和氨基化合物中得到了廣泛的應用,高的對映選擇性和簡單的操作流程是CALB廣泛應用于拆分仲醇和伯胺的基礎;盡管CALA在有機合成中應用遠少于CALB,但卻被證明在酰化叔醇和仲胺時比CALB具有更高的活性,這使得CALA在拆分具立體位阻的化合物中具有極大的應用前景[7]。
1.2 動力學拆分 CALA和CALB可催化水解、酯化、轉酯、氨解等反應,這些反應可用來拆分外消旋的醇、氨和酸等從而制備光學純的化合物。以仲醇為例,外消旋的仲醇分為R型和S型,脂肪酶在選擇性的將R型的仲醇酰化的同時卻不催化S型的反應,從而將消旋的仲醇拆分,該過程稱為動力學拆分(kinetic resolution,縮寫為KR)[8]。
CALB和CALA對消旋的仲醇、伯胺的高選擇性是由脂肪酶立體結構及底物的結構共同決定的。這種選擇性可用Kazlauskas經驗法則[9]來解釋,以CALB為例,其模型化合物手性仲醇中手性碳兩側取代基分別為中等大小的基團(ML,不大于丙基)和較大的基團(LL,大于丙基),其中R構型的化合物能與CALB的活性中心充分結合而很快反應,S型化合物則由于無法進入CALB活性中心而反應很慢或基本不能反應如圖1。

圖1 CALB對消旋仲醇的選擇性示意圖
由于反應速率上的巨大差異,CALB對符合上述模型的對映體表現出極高的選擇性(>99%),這種高選擇性使CALB在動力學拆分外消旋醇、氨、羧酸等化合物中廣泛應用[6],特別在制備小分子手性藥物及其關鍵中間體中。此外,CALB還可通過轉酯、氨解等反應應用于藥物合成中。下文將據反應類型,綜述CALB在制備手性藥物中的應用。
2 南極假絲酵母脂肪酶B在制備手性藥物中的應用
2.1 (動態)動力學拆分醇
2.1.1 伯醇 帕羅西汀(Paroxetine)為強效、高選擇性5-羥色胺再攝取抑制劑,主要用于治療各種抑郁癥,其關鍵中間體(-)-paroxol可通過重結晶、不對稱合成、生物催化拆分的方法進行制備,利用脂肪酶介導的動力學拆分便是其中之一。CALB可對映選擇性酰化(±)-trans-1從而拆分得到用于合成帕羅西汀的中間體(3S,4R)-1[10],通過優化反應條件,當采用苯甲酸乙烯酯作為酰基供體、甲苯作為溶劑時,反應具有較高的轉化率(51%)和對映選擇性(E>100)見圖2。與化合合成相比,該反應簡單且易于放大,適宜于進行規模化應用。

圖2 CALB通過動力學拆分反應制備帕羅西汀中間體
依地普侖(Escitalopram)也是一種抗抑郁藥,是S構型西酞普蘭的,盡管西酞普蘭以外消旋混合物形式用于抑郁癥的治療,但研究表明R-構型西酞普蘭與S構型(依地普侖)相比基本無活性,因此制備單一對映體(依地普侖)就極其重要。rac-3為合成依地普侖的重要中間體,可利用CALB進行拆分[11]。由于化合物3其手性叔醇位置空間位阻較大,CALB不能將其酰化,但CALB可將遠離手性中心的伯醇酰化,從而將rac-3拆分,未參與反應的化合物(s)-3可用于合成依地普侖。盡管反應未發生在手型中心位置,但該反應仍具有較高的產率(53%)和選擇性,化合物ee值可達99%(見圖3)。

圖3 CALB通過動力學拆分反應制備依地普侖中間體
2.1.2 仲醇 利斯的明(Rivastigmine)是膽堿酯酶抑制劑,商品名為艾斯能,可用于治療老年癡呆。Miotine也是膽堿酯酶抑制劑主要用作縮瞳藥。化合物(R)-6可用于合成這兩種手性藥物,利用CALB結合金屬Ru催化劑,可將消旋的化合物rac-5進性動態動力學拆分,該典型的DKR反應具有較高的產率和選擇性,得到酯產率可達95%,ee值大于99%[12],該化合物可較容易的通過CALB催化的水解反應將乙酰基脫掉,從而用于進一步合成。類似的,通過動態動力學拆分化合物rac-7也可得到合成利斯的明的中間體[13](見圖4)。
度洛西汀(Duloxetine)是一種5-羥色胺和去甲腎上腺素再攝取雙重抑制劑,用于治療各種抑郁癥。逆合成分析表明,化合物(3)-9可用于合成度洛西汀。該化合物可利用CALB動力學拆分得到[14],盡管化合物rac-9并不完全符合Kazlauskas模型,且含有吸電子的鹵族元素,但CALB依舊對該化合物具有較高的選擇性(見圖5)。

圖4 CALB通過動態動力學拆分反應制備利斯的明中間體
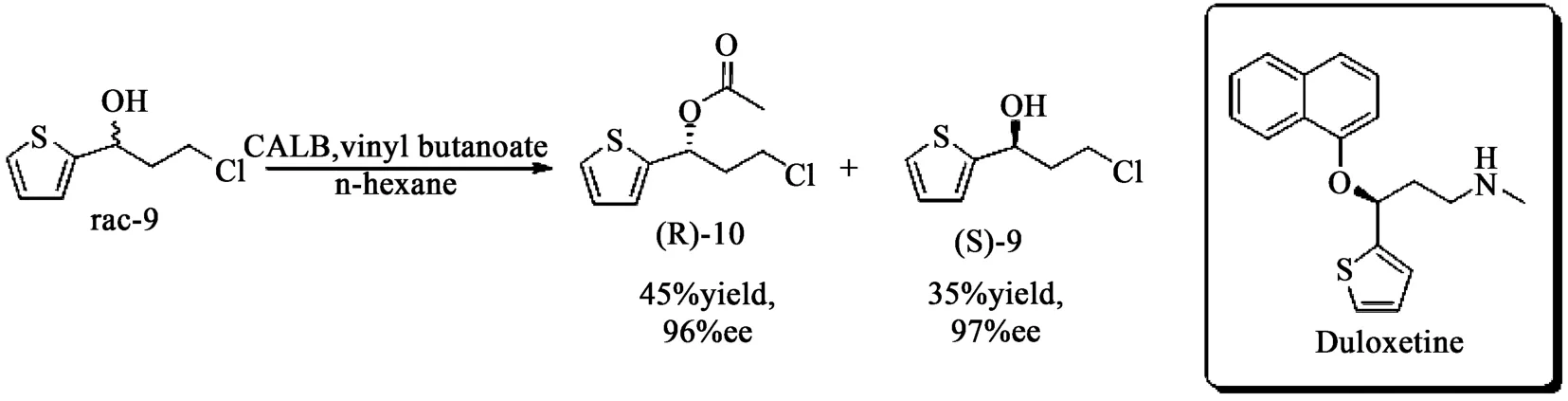
圖5 CALB通過動力學拆分反應制備洛西汀中間體
2.2 (動態)動力學拆分胺 CALB在動力學拆分上述仲醇中展現出了良好的活性及選擇性,與仲醇類似,符合Kazlauskas經驗法則的伯胺同樣可作為CALB的底物。如圖所示,化合物rac-11可用CALB進行動力學拆分,得到的R構型酰胺和未反應的S構型伯胺都有較高的ee值[12]。在動力學拆分反應中,剩余的S構型可用于合成利斯的明和Miotine(見圖6)。
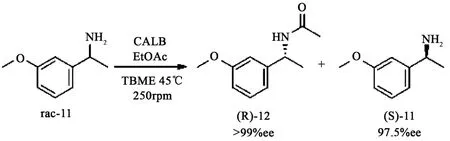
圖6 CALB通過動力學拆分反應制備利斯的明中間體
具有藥理學活性的苯丙胺及其一系列衍生物同樣可以利用CALB進行動力學拆分,得到光學純化合物可用于合成一系列的手性藥物,例如對位、鄰位、間位甲氧基取代的苯丙胺可用于合成安非他命類藥物(Amphetamine)[15]和阿福特羅(Arformoterol,(R,R)-福莫特羅)[16],間位三氟甲基取代的苯丙胺可用于合成芬氟拉明(Fenfluramine)[17]等(見圖7)。與拆分醇不同,動力學拆分胺時,作為溶劑的乙酸乙酯可同時作為酰基供體。
2.3 其他(酸、轉酯、氨解等) 類似于仲醇及伯胺,消旋的羧酸及衍生物也可通過CALB進行動力學拆分。布洛芬(Ibuprofen)主要用于解熱鎮痛及抗炎,盡管目前大部分布洛芬制劑以外消旋混合物使用,但實驗表明其S構型活性是R構型活性的160倍。利用CALB催化的轉酯反應,可將布洛芬乙烯酯進行動力學拆分[18],得到的S布洛芬酯ee值可達99%(見圖8)。
阿夫唑嗪(Alfuzosin)為新型的α1受體阻滯劑,可用于治療高血壓,也可用于治療前列腺增生。報道的以化合物17為起始原料的化學合成路線包含一些有毒的試劑且需采用苛刻的反應條件,而利用脂肪酶CALB通過酯化、氨解可一步合成化合物19[19],不僅無毒條件溫和,且具有較高的產率。得到的化合物19可用于合成阿夫唑嗪(見圖9)。
嗎替麥考酚酯(Mycophenolate mofetil)一種新型的免疫抑制劑,主要用于預防和治療器官移植后的排斥反應。目前主要采用將麥考酚酸與N-羥乙基嗎啉在高溫下酯化來合成嗎替麥考酚酯,該反應的缺點是容易生成麥考酚酸的縮聚物。最近報道了一種利用脂肪酶催化合成嗎替麥考酚酯的新方法[20],首先利用CALB催化麥考酚酸與低分子量脂肪族醇(如乙醇)酯化得到化合物21,再利用CALB介導21與N-羥乙基嗎啉轉酯從而合成嗎替麥考酚酯。與化學合成相 比,該反應副產物少且產率高(見圖10)。

圖7 CALB通過動力學拆分反應制備安非他命類藥物中間體
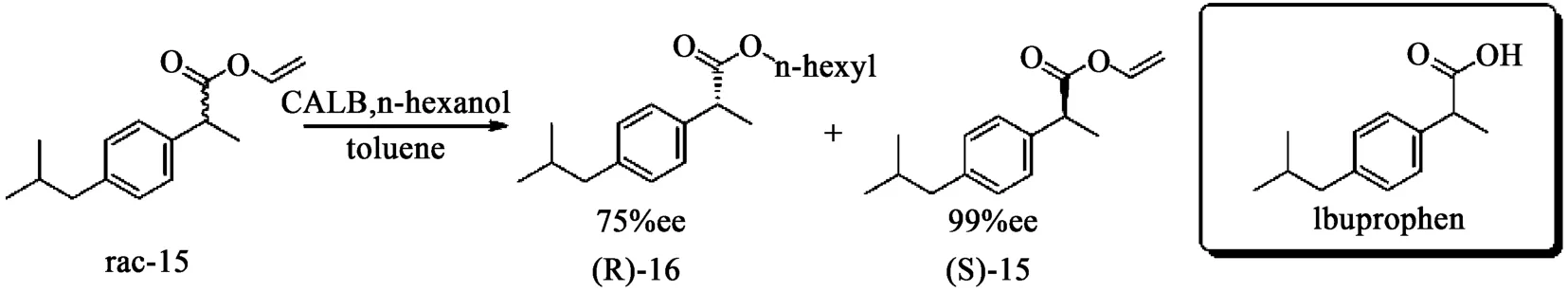
圖8 CALB通過轉酯反應制備布洛芬中間體

圖9 CALB通過酯化、氨解反應制備阿夫唑嗪中間體

圖10 CALB通過酯化、轉酯反應制備嗎替麥考酚酯中間體
3 結論與展望
天然來源的抗生素等藥物多為具有純光學活性的手性藥,但是經由化學合成得到的藥物往往是對映異構,因此,手性藥物的分離,甚至在化學合成中定向的進行制備,消除對應異構體的影響成了合成制備手性藥物的關鍵。CALB能夠在較溫和的條件下具有較高的選擇性,由于生物催化劑的這種特性,使得生物催化劑正在或者已經在手性藥物的合成中得到應用,因此,CALB的研究對于手性藥物的制備具有重要的意義。
[1]Pollard DJ,Woodley JM.Biocatalysis for pharmaceutical intermediates:the future is now[J].Trends Biotechnol,2007,25(2):66-73.
[2]Tao J,Xu JH.Biocatalysis in development of green pharmaceutical processes[J].Curr Opin Chem Biol,2009,13(1):43-50.
[3]Steven K.Ma,John Gruber,Chris Davis,et al.A greenby-design biocatalytic process for atorvastatin intermediate[J].Green Chem,2010,12:81-86.
[4]Savile CK,Janey JM,Mundorff EC,et al.Biocatalytic asymmetric synthesis of chiral amines from ketones applied to sitagliptin manufacture[J].Science,2010,329(5989):305-309.
[5]Klibanov AM.Improving enzymes by using them in organic solvents[J].Nature,2001,409(6817):241-246.
[6]Ole Kirk,Morten Würtz Christensen.Lipases from Candida antarctica:Unique biocatalysts from a unique origin[J],Organic process research&development,2002,6(4):446-451.
[7]Vicente Gotor-Fernández,Eduardo Busto,Vicente Gotor.Candida antarctica Lipase B:An Ideal Biocatalyst for the Preparation of Nitrogenated Organic Compounds[J].Advanced Synthesis&Catalysis,2006,348(7-8):797-812.
[8]Ghanem A,Aboul-Enein,HY.Lipase-mediated chiral resolution of racemates in organic solvents[J].Tetrahedron:Asymmetry,2004,15(21):3331-3351.
[9]Kazlauskas RJ,Weissfloch ANE,Rappaport AT,et al.A rule to predict which enantiomer of a secondary alcohol reacts faster in reactions catalyzed by cholesterol esterase,lipase from Pseudomonas cepacia,and lipase from Candida rugosa[J].J Org Chem,1991,56(8):2656-2665.
[10]de Gonzalo G,Brieva R,Sanchez VM,etal.Enzymatic esolution of trans-4-(4′-luorophenyl)-3-hydroxymethylpiperidines,key intermediates in the synthesis of(-)-Paroxetine[J].J Org Chem,2001,66(26):8947-8953.
[11]Solares LF,Brieva R,Quirós M,et al.Enzymatic resolution of a quaternary stereogenic centre as the key step in the synthesis of(S)-citalopram[J].Tetrahedron:Asymmetry,2004,15(2):341-345.
[12]Mangas-Sanchez J,Rodriguez-Mata M,Busto E,et al.Chemoenzymatic synthesis of rivastigmine based on lipase-catalyzed processes[J].JOrg Chem,2009,74(15):5304-5310.
[13]Han K,Kim C,Park J,et al.Chemoenzymatic synthesis of rivastigmine via dynamic kinetic resolution as a key step[J].JOrg Chem,2010,75(9):3105-3108.
[14]Kamal A,Khanna,Ramu R,et al.Chemoenzymatic synthesis of duloxetine and its enantiomer:lipase-catalyzed resolution of 3-hydroxy-3-(2-thienyl)propanenitrile[J].Tetrahedron Letters,2003,44(25):4783-4787.
[15]Gonzalez-Sabin J,Gotor V,Rebolledo F.CAL-B-catalyzed resolution of some pharmacologically interestingβ -substituted isopropylamines[J].Tetrahedron:Asymmetry,2002,13(12):1315-1320.
[16]Campos F,Guerrero A,Bosch MP.An efficientenantio selective synthesis of(R,R)-formoterol,a potent bronchodilator,using lipases[J].Tetrahedron:Asymmetry,2000,11(13):2705-2717.
[17]Garcia-Urdiales E,Rebolledo F,Gotor V.Enzymatic one-pot resolution of two nucleophiles:alcohol and amine[J].Tetrahedron:Asymmetry,2000,11(7):1459-1463.
[18]Henke E,Schuster S,Yang H,et al,Lipase-Catalyzed Resolution of Ibuprofen[J].Monatshefte für Chemie,2000,131(6):633-638.
[19]Alicia Baldessari,Constanza P,Mangone.One-pot biocatalyzed preparation of substituted amides as intermediates of pharmaceuticals[J].JMol Catal B Enzym,2001,11(4-6):335-341.
[20]Paride G,Paolo P.Method for the preparation ofmycophenolate mofetil by enzyme tranesterification:US,7727751[P].2005-07-25.
The application for cardida antarctica lipase B in chiral drugs preparation
JIAO Chun-li,LIU Xue-jie
(Yantai Institute for Food and Drug Contorl,Yantai264000,China)
Brief introduction for CALB in chiral drugs preparation.According to recent domestic and foreign literature,details of the application for CALB in chiral alcohols,amines,acid selective separation transesterification and so on were introduced.The application for lipase in chiral drugs preparation is an important area for drug synthesis,the authormainly reviewed the application for CALB in chiral alcohols,amines,acid selective separation,transesterification,expecting to provide reference for chiral drugs preparation.
Cardida antarctica lipase;CALB;Chiral drug;Synthesis
R918
:A
2095-5375(2014)07-0406-005
矯春麗,女,研究方向:藥物分析,E-mail:baoran03_17@sina.cn

