重組人B型利鈉肽治療慢性心力衰竭急性發作失代償期的臨床療效觀察
戴培勝,韓亞巖,崔娟敏,王 巖,李學奇
(1.雙鴨山煤炭總醫院心內科,黑龍江 雙鴨山 155100; 2.哈醫大四院心內科,哈爾濱 150001)
慢性心力衰竭急性發作失代償期(decompensated acute attack of chronic heart failure,DAACHF)是因急性心肌損害或突然加重的負荷使處于慢性心力衰竭代償期的心臟在短時間內發生衰竭[1]。DAACHF在我國的年病死率高達34%[2]。伴隨心力衰竭發生機制的深入研究,神經內分泌因素在心力衰竭發生中所起的作用已明確,其中B型利鈉肽(B-type natriuretic peptide,BNP)是研究較多的神經體液因子,該因子具有利尿、利鈉、擴張血管、抑制交感神經系統等作用。重組人B型利鈉肽(recombinant human B-type natriuretic peptide,rhBNP)與內源性BNP具有相同的32個氨基酸序列和空間立體結構,有相同的生物活性和作用機制。本研究對DAACHF患者在常規治療基礎上聯合使用rhBNP,效果較為明顯,現報道如下。
1 資料與方法
1.1臨床資料 選擇雙鴨山煤炭總醫院心內科2011年3月至2013年2月收治的DAACHF患者68例,其中男、女各34例,年齡55~71歲,平均(62.5±5.4)歲。患者入院表現為充血和水鈉潴留體征、端坐呼吸伴勞力性呼吸困難。紐約心臟病協會心功能Ⅲ~Ⅳ級,其中Ⅲ級39例、Ⅳ29例。原發性疾病為高血壓性心臟病21例、冠心病22例、擴張型心肌病25例。納入標準:既往有心力衰竭診斷史,心功能Ⅲ級以上。排除標準:心源性休克、嚴重心瓣膜病、縮窄性心包炎、重度肺動脈高壓、甲狀腺功能亢進、惡性腫瘤患者及肝功能不全(谷丙轉氨酶、谷草轉氨酶均高于60 U/L)、腎功能不全(血肌酐高于120 μmol/L)患者。所有患者按照隨機數字表法分為兩組:常規治療組(33例)和聯合治療組(35例),兩組患者在年齡、性別、心功能、原發病構成方面比較差異無統計學意義(P>0.05),具有均衡性(表1)。
1.2治療方案 兩組患者入院后均給予常規抗心力衰竭治療,如吸氧、靜臥、低鈉飲食,并給予利尿劑、血管緊張素酶抑制劑、正性肌力藥物、營養心肌類藥物、他汀類藥物、硝酸酯類藥物等。聯合治療組在此基礎上加用rhBNP(商品名:新活素,0.5 mg/支,成都諾迪康生物制藥有限公司,國藥準字S20050033),首先以1.5~2 μg/kg負荷劑量3~5 min內靜脈推注,隨后以0.0075 μg/(kg·min)連續靜脈滴注72 h,用藥總量0.5~1.0 mg。

表1 兩組DAACHF患者臨床特征對比情況
a:為t值,余為χ2值
1.3觀察指標
1.3.1心功能指標 采用美國通用公司Vivid7多普勒超聲診斷儀測定兩組患者治療前與治療7 d后左心室舒張末期直徑(left ventricular end-diastolic diameter,LVEDD)、左心室收縮末期直徑(left ventricular systolic diameter,LVESD)、左心室射血分數(left ventricular ejection fraction,LVEF)、左心室短軸縮短率(left ventricular systolic fraction,LVSF)。同時測定治療7 d后患者6 min步行運動耐量。
1.3.2臨床療效判定標準 顯效:紐約心臟病協會心功能評分改善2級以上者;有效:心功能改善1級,癥狀及體征減輕,但仍有心力衰竭癥狀;無效:心功能改善不足1級,或癥狀、體征無改善,甚至惡化、死亡者[3]。
1.3.3不良反應指標 肝腎功能損害及其他不良心血管事件。
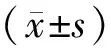
2 結 果
2.1兩組患者治療前后心功能指標對比 聯合治療組和常規治療組患者入院后雖經積極搶救,但分別有1例、2例死于終末心力衰竭。治療后,兩組患者的LVEDD、LVESD水平均低于治療前,且聯合治療組下降幅度優于常規治療組,差異均有統計學意義(P<0.05);治療后,兩組患者的LVEF、LVSF水平均高于治療前,且聯合治療組上升幅度優于常規治療組,差異均有統計學意義(P<0.05)。同時,聯合治療組治療后6 min步行運動耐量顯著高于常規治療組[(294.3±41.7) m vs (258.5±35.4) m],差異有統計學意義(t=3.741P<0.05)(表2)。

表2 兩組DAACHF患者治療前后心功能指標對比情況
LVEDD:左心室舒張末期直徑;LVESD:左心室收縮末期直徑;LVEF:左心室射血分數;LVSF:左心室短軸縮短率
2.2兩組患者臨床療效和住院天數的對比 聯合治療組(1例)和常規治療組(2例)死于終末心力衰竭的患者視為無效。聯合治療組總有效率高于常規治療組,差異有統計學意義(z=2.401,P=0.016)(表3)。聯合治療組平均住院天數顯著少于常規治療組[(14.2±3.2) d vs (17.4±4.4) d](t=3.413,P=0.001)。

表3 兩組患者臨床療效的對比 [例(%)]
2.3兩組患者藥物不良反應情況比較 兩組患者治療過程中均無明顯肝腎功能損害。聯合治療組和常規治療組分別發生體位性低血壓3例、9例,頭痛2例、5例,聯合治療組和常規治療組藥物不良反應發生率分別為14.7%(5/34)和45.2%(14/31),差異有統計學意義(χ2=7.271,P=0.007)。不良反應未經特殊處理,均耐受或自行緩解。
3 討 論
心力衰竭是由功能性或結構性心臟病導致心室充盈和射血功能受損而引起的一組臨床綜合征,主要表現為肢體水腫、呼吸困難、運動耐量受限等癥狀。心力衰竭發生、發展主要有血心肌能量代謝與利用障礙、血流動力學異常引發去甲腎上腺素過度分泌導致的心血管功能障礙、神經體液激活及細胞因子活化導致心肌損害、繼續行心室重構等病理生理原因[4]。DAACHF階段,體循環和肺循環的容量負荷、壓力負荷明顯升高,進行性惡化會增加患者死亡危險性,需要緊急處理[5]。內分泌系統長期過度激活是DAACHF發作的重要原因[6],心力衰竭出現后機體會啟動一系列代償性機制來維持泵血功能,主要表現為交感神經系統及腎素-血管緊張素-醛固酮系統激活,血管活性物質釋放增加,代償性維持心臟泵血功能。DAACHF患者多伴有腎素-血管緊張素-醛固酮系統的過度激活,臨床治療心力衰竭的常用藥物有利尿劑、正性肌力藥物、兒茶酚胺、磷酸二酯酶抑制劑、硝酸酯類擴血管藥等,這些藥物可明顯降低心臟灌注壓和增加心輸出量,有效糾正血流動力學紊亂,改善患者癥狀,但無抑制該系統過度激活的作用,甚至還可能進一步激活神經內分泌系統,對改善心肌重構沒有意義[7]。
伴隨神經內分泌系統在DAACHF發生中的作用明確,對神經體液因子的研究逐步深入。BNP就是其中較為受關注的研究對象之一。BNP是由心室壁肌細胞等合成分泌的廣泛存在于心房、心室肌細胞內的含32個氨基酸組成的多肽類激素。在心力衰竭的神經內分泌變化中,BNP合成及分泌的增加,拮抗腎素-血管緊張素-醛固酮系統的縮血管和體液潴留作用。BNP具有利尿、利鈉、誘導血管擴張、抑制內皮素和血管緊張素Ⅱ的分泌等多種生化效應,參與調節血壓、血容量及鹽的平衡等。事實上,DAACHF時雖然BNP分泌增多,但代償不足[8]。rhBNP與內源性BNP具有相同的氨基酸排序、空間結構和生物活性,rhBNP通過增加激活鳥苷酸環化酶而使環磷酸鳥苷濃度增加,環磷酸鳥苷作為第二信使具有強有力的血管舒張作用;rhBNP抑制腎素-血管緊張素-醛固酮系統,抵消腎素、血管緊張素的效應,擴張腎小球入球小動脈,收縮出球小動脈,抑制近曲小管對鈉的重吸收,增加腎小球濾過率,增強水鈉排泄,與利尿劑合用具有協同利尿、利鈉作用,減少體液潴留,減輕心臟前負荷;同時擴管降壓,尤其是對冠狀動脈有明顯擴張作用,改善缺血狀態下心肌的微循環,降低心肌耗氧,減輕心臟后負荷;此外也能拮抗內皮素過度分泌引起的心肌細胞纖維化,還可抑制炎性因子基因的表達和心肌肥厚增殖,預防心室病理性重構[9]。rhBNP的主要不良反應為血壓降低、頭痛、腹痛、室性心動過及可能的腎功能損害[10]。
Burger等[11]比較rhBNP和多巴胺、多巴酚丁胺治療急性心力衰竭的療效和促心律失常的作用,發現rhBNP較之正性肌力藥物無增加心肌耗氧量與促心律失常作用;2005年歐洲心臟病學會將rhBNP列入心力衰竭的治療指南[12];龍雙祁等[13]利用rhBNP治療急性心肌梗死伴急性左心衰患者的總有效率高達93.8%;李文明等[14]利用該藥治療風濕性心臟病引發的心力衰竭,用藥2 h后總有效率(93.0%)顯著高于常規療法(60.0%)(P<0.05)。以上研究說明,rhBNP對多種類型的心力衰竭表現出廣泛的積極療效。本組資料中,兩組心功能指標均較之治療前顯著改善,聯合治療組LVEDD、LVEF、LVSF、6 min步行運動耐量指標均顯著優于常規治療組,且聯合治療組總有效率、平均住院天數均高于常規治療組,此外聯合治療組出現低血壓、頭痛等不良反應的比例低于常規治療組,也充分說明補充外源性BNP對常規藥物不良反應的減緩作用。
綜上所述,在常規抗心力衰竭治療的基礎上聯合使用rhBNP治療DAACHF,能顯著改善心肌收縮力,增加心輸出量,提高常規藥物療效,同時能減緩常規抗心力衰竭藥物的不良反應,具備較高的臨床安全性。
[1] 羅苑苑,孫少喜,李蘅,等.重組人腦利鈉肽和硝普鈉對急性失代償性心力衰竭的療效比較[J].醫學臨床研究,2010,27(2):196-197.
[2] 顧東風,黃廣勇,吳錫桂,等.中國心力衰竭流行病學調查及其患病率[J].中華心血管病雜志,2003,30(1):3-6.
[3] 陸再英,鐘南山.內科學[M].7版.北京:人民衛生出版社,2008:180.
[4] 盧敏,張夢璽,曹軍香.心力衰竭患者腦鈉肽、C反應蛋白與心功能的關系[J].實用醫學雜志,2007,23(5):658-660.
[5] 王日軍,李慧芳,張月安,等.重組人腦利鈉肽治療老年慢性心衰患者急性加重期的臨床療效觀察[J].中國老年醫學雜志,2010,5(20):1176-1177.
[6] 李愛華,唐良秋,張社兵.凍干重組人腦利鈉肽與米力農治療心衰的療效比較[J].中國現代醫生,2012,50(21):56-57.
[7] 付堯,楊光,白小涓,等.重組人腦利鈉肽治療充血性心力衰竭的療效評價[J].中國醫科大學學報,2006,35(2):191-192.
[8] Dickstein K,Cohen Solal A,Filippatos G,etal.ESC guidelines for the diagnosis and treatment of acute and chronic heart failure 2008:the Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2008 of the European Society of Cardiology[J].Eur J Heart Fail,2008,10(10):933-989.
[9] Witteles RM,Kao D,Christopherson D,etal.Impact of nesiritide on renal function in patients with acute decompensated heart failure and pre-existing renal dysfunction a randomized,double-blind,placebo-controlled clinical trial[J],J Am Coll Cardiol,2007,50(19):1835-1840.
[10] Masson S,Latini R,Anand IS,etal.Direct comparison of B-type natriuretic peptide(BNP)and amino-terminal proBNP in a large populmion of patients wiht chronic and symptomatic heart failure:the Valsartan Heart Failure(Val-HeFT)data[J].Clin Chem,2006,52(8):1528-1538.
[11] Burger AJ,Aronson D,Horton DP,etal.Comparison of the effects of dobutamine and nesiritide (B-type natriuretic peptide)on ventricular ectopy in acutely decompensated ischemic versus nonischemic cardiomyopathy[J].Am J Cardiol,2003,91(11):1370-1372.
[12] 吳清華,鄔濤.利鈉肽在急性心臟救治中的應用——來自2011 歐洲心臟病協會年會(ESC)的建議[J].江西醫藥,2012,47(5):383-385.
[13] 龍雙祁,劉彬,鄒桂和,等.重組人腦利鈉肽對急性心肌梗死伴心衰患者的療效觀察[J].中國醫藥導報,2011,8(8):81-82.
[14] 李文明,陳冬冬,謝文韜,等.重組人腦利鈉肽治療急性左心衰療效觀察[J].臨床和實驗醫學,2010,9(15):1123-1124.

