由蛇紋石制備高純氧化鐵的研究
肖景波,夏嬌彬,陳居玲
(南陽東方應用化工研究所,河南南陽 473000)
由蛇紋石制備高純氧化鐵的研究
肖景波,夏嬌彬,陳居玲
(南陽東方應用化工研究所,河南南陽 473000)
以蛇紋石酸浸出液凈化過程所獲鐵鋁沉淀物為原料,采用氧化沉淀及煅燒法工藝制備了高純氧化鐵。通過對鐵鋁沉淀物精制、鐵沉淀物的酸解、酸解液中三價鐵的還原、鐵溶液的凈化、氧化鐵前驅物α-FeOOH的制備與煅燒過程的研究,確定了優化工藝條件。實驗結果表明,在優化工藝條件下,鐵收率為99.9%,氧化鐵純度達99.8%,符合軟磁鐵氧體用氧化鐵的質量要求。
蛇紋石;氧化鐵;軟磁鐵氧體
中國蛇紋石資源儲量十分豐富,已探明的總儲量超過50億t,居世界第三位[1]。蛇紋石礦含有硅、鎂、鐵、鋁、鎳、鈷等有價元素,具有可觀的綜合利用價值。
高純氧化鐵是現代電子工業生產彩色電視機玻殼的重要原料之一,亦是生產軟磁鐵氧體所需的一種重要原材料。其制備方法可分為干法和濕法[2]:干法主要包括焙燒法、熱分解法、魯式法等;濕法主要包括溶膠凝膠法、空氣氧化法、水解法、沉淀法等,其中濕法工藝的改進方法有水熱法、催化法和包核法,還有超臨界流體干燥法和微波輻射法等。
為了綜合利用蛇紋石中的鐵資源,尋找一種制備高純氧化鐵新途徑,筆者提出了由濕法冶金工藝綜合利用蛇紋石過程所獲得的鐵鋁沉淀物制備高純氧化鐵的方法,并進行了實驗研究。
1 實驗部分
1.1 實驗原料、試劑與儀器
原料與試劑:實驗所用鐵鋁沉淀物由南陽蛇紋石綜合利用產業化實驗基地提供,其w(Fe2O3)=71.62%,w[Al(OH)3]=15.10%;氫氧化鈉;復合溶液,實驗室配制;硫酸、還原鐵粉、氟化鈉、硫化鈉、雙氧水、氨水,均為分析純;純水,電阻率為16.5MΩ·cm。
儀器:BS423S型電子天平、025-2F型電動攪拌機、HH-4型數顯恒溫水浴鍋、SHB-ⅢA型循環水式多用真空泵、HG101型電熱恒溫鼓風干燥箱、XKMF-2000A型馬弗爐。
1.2 實驗方法
1.2.1 鐵鋁沉淀物精制
蛇紋石中含有鐵、鋁等元素。由于Fe3+和Al3+沉淀的pH相近,且有一個交叉區,在以氧化沉淀法沉淀蛇紋石酸解液中的Fe3+時,Al3+也共同沉淀。因此所獲沉淀物為鐵與鋁,即α-FeOOH和Al(OH)3的混合物。
實驗稱取一定量的鐵鋁沉淀物置于燒杯中,加水并打制成漿,再加氫氧化鈉,調整氫氧化鈉用量、反應時間、反應溫度,將鐵鋁沉淀物中的鋁離子轉化為可溶性鋁鹽進入液相,再經分離、洗滌得到除鋁后的鐵沉淀物。
1.2.2 α-FeOOH制備
將一定量的除鋁后鐵沉淀物置于燒杯中,加水并打制成漿,加硫酸使鐵沉淀物分解并生成硫酸鐵。反應完全后加入還原鐵粉使酸解液中的Fe3+還原為Fe2+,并以高錳酸鉀溶液做定性實驗,至溶液中無Fe3+為止。加適量氟化鈉去除溶液中的鈣離子、鎂離子,反應完全后再加硫化鈉去除其中的重金屬離子[3-4]。反應完成后過濾得到相對純凈的硫酸亞鐵溶液。以氨水為pH調節劑調整溶液的pH,使溶液中的Al3+及殘留的Fe3+轉化為氫氧化物沉淀,經過濾得到純凈的Fe2+溶液。向Fe2+溶液中加雙氧水,將Fe2+氧化為Fe3+,再以純水為底液,以氨水為pH調節劑,采用并流的方式將Fe3+溶液和pH調節劑加入到底液中。過程中控制反應溫度、反應時間和反應終點的pH,使Fe3+轉化為α-FeOOH沉淀。將沉淀分離,洗滌,脫水制得中間產品α-FeOOH。
1.2.3 α-Fe2O3制備
將所制得的α-FeOOH在馬弗爐中煅燒,調整煅燒溫度和時間,制得α-Fe2O3產品。
1.3 分析方法
鐵的測定采用重鉻酸鉀滴定法;鈣、鎂的測定采用EDTA滴定法;鋁的測定采用乙酸鋅反滴定法。
2 結果與討論
2.1 鐵鋁沉淀物精制
從蛇紋石酸解液沉鐵過程中所獲得的沉淀物是由α-FeOOH和Al(OH)3組成的混合物。要實現對蛇紋石中鐵元素的綜合利用,制備出高純度的氧化鐵產品,首先要實現沉淀物中鐵與鋁的分離,以獲得化學組成較為單一的鐵源。實驗以氫氧化鈉為凈化劑,考察了配料固液比、氫氧化鈉加入量、反應溫度和反應時間對鐵鋁沉淀物中鋁離子去除率的影響。
2.1.1 配料固液比
較高的配料濃度有利于提高反應速率,促使反應向右進行,但配料濃度過高又會對反應物的分散性產生影響,使反應速率和反應的完全程度受到限制,同時對后期固液分離不利。實驗在反應溫度為80℃、反應時間為60min、氫氧化鈉加入量為理論量3倍的條件下,考察了配料固液比(鐵鋁沉淀物的質量與水的體積比,g/mL,下同)對鋁離子去除率的影響,結果見表1。
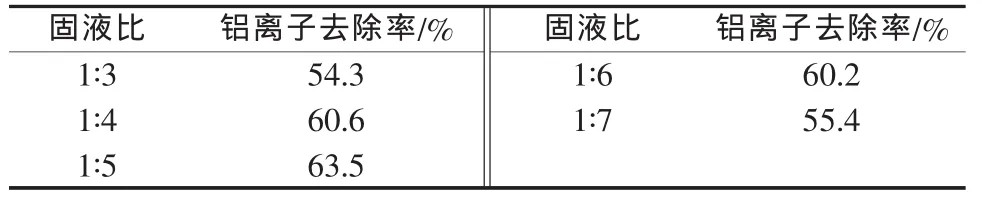
表1 配料固液比與鋁離子去除率關系
由表1可以看出,鋁離子去除率隨固液比增大先升高后降低,在固液比為1∶5時,鋁離子去除率最高。因此,實驗確定適宜的固液比為1∶5。
2.1.2 氫氧化鈉加入量
氫氧化鈉為實驗室復配的鋁離子去除劑,其加入量的變化會對鋁離子的去除率造成影響。實驗在配料固液比為1∶5、反應溫度為80℃、反應時間為60min的條件下,考察了氫氧化鈉加入量對鐵鋁沉淀物中鋁離子去除率的影響,結果見圖1。由圖1可以看出,鋁離子去除率隨氫氧化鈉加入量增加而升高,當氫氧化鈉加入量為理論量5倍時,再繼續增加氫氧化鈉用量鋁離子去除率幾乎不變。因此,實驗確定氫氧化鈉的最佳加入量為理論量的5倍,此時鋁離子的去除率為79.56%。
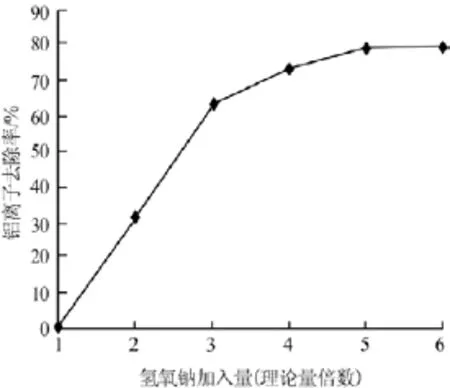
圖1 氫氧化鈉加入量與鋁離子去除率的關系
2.1.3 反應溫度
反應溫度對鋁離子去除率有明顯影響,實驗在配料固液比為1∶5、氫氧化鈉加入量為理論量的5倍、反應時間為60min的條件下,考察了反應溫度對鐵鋁沉淀物中鋁離子去除率的影響,結果見圖2。
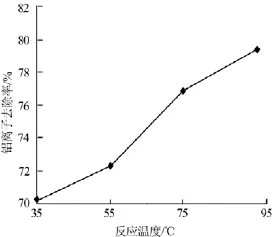
圖2 反應溫度與鋁離子去除率的關系
由圖2可以看出,鋁離子去除率隨反應溫度升高而升高,在反應溫度為95℃時,鋁離子去除率達到最大(79.58%)。因此,實驗確定的適宜的反應溫度為95℃。
2.1.4 反應時間
在配料固液比為1∶5、氫氧化鈉加入量為理論量的5倍、反應溫度為95℃的條件下,考察了反應時間對鐵鋁沉淀物中鋁離子去除率的影響,結果見圖3。由圖3可以看出,鋁離子去除率隨反應時間增加而升高,當反應時間增加至40min時,再繼續延長反應時間鋁離子去除率幾乎不變。因此,實驗確定最佳反應時間為40min,此時鋁離子去除率為79.69%。
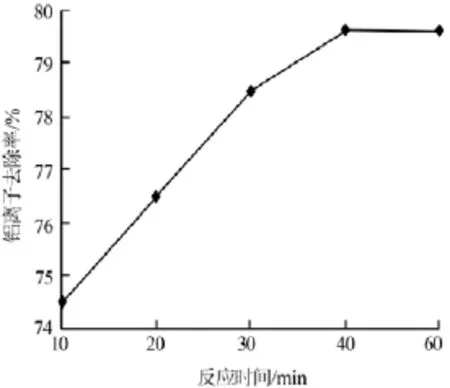
圖3 反應時間與鋁離子去除率的關系
2.2 鐵沉淀物的酸解
將精制過的鐵沉淀物酸解制得含鐵溶液是制備高純氧化鐵的基礎工序之一。實驗考察了硫酸用量、反應溫度和反應時間對鐵沉淀物分解率的影響并確定了優化工藝條件。
2.2.1 硫酸用量
在反應溫度為80℃、反應時間為60min的條件下,考察了硫酸加入量對鐵沉淀物分解率的影響,結果見圖4。
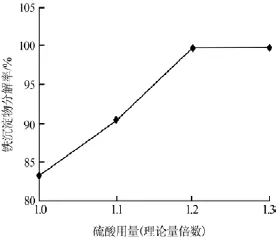
圖4 硫酸用量與鐵沉淀物分解率的關系
由圖4可以看出,加酸量為理論量1.2倍時鐵沉淀物基本分解完全,繼續增加硫酸用量鐵沉淀物分解率幾乎沒有變化。因此,實驗確定了鐵沉淀物酸解過程硫酸的適宜用量為理論量的1.2倍,此時鐵沉淀物分解率為99.8%。
2.2.2 反應溫度
在硫酸加入量為理論量1.2倍、反應時間為60min的條件下,考察了反應溫度對鐵沉淀物分解率的影響,結果見圖5。
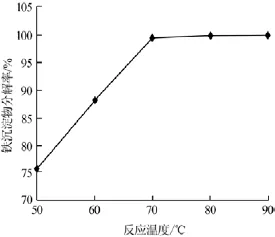
圖5 反應溫度與鐵沉淀物分解率的關系
由圖5可以看出,鐵沉淀物分解率隨反應溫度的升高而升高,在反應溫度為70℃時分解率達到99.9%,繼續升高反應溫度已無實際意義。因此,實驗確定適宜的反應溫度為70℃。
2.2.3 反應時間
反應時間不足鐵沉淀物分解率較低,反應時間過長不僅會增加能耗,而且還會對工業化過程的生產能力造成影響。在硫酸加入量為理論量1.2倍、反應溫度為70℃的條件下考察了反應時間對鐵沉淀物分解率的影響,結果見圖6。
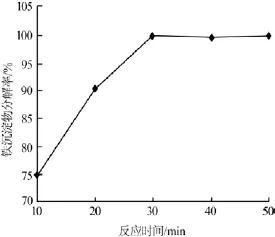
圖6 反應時間與鐵沉淀物分解率的關系
由圖6可以看出,鐵沉淀物分解率隨反應時間的延長而升高,當反應時間為30min時,鐵沉淀物已基本分解完全。因此,實驗確定最佳的反應時間為30min,此時鐵沉淀物分解率為99.9%。
2.4 鐵沉淀物酸解液的還原與凈化
鐵沉淀物酸解后生成的溶液主要成分為Fe3+和少量Al3+,同時還含有微量的Mg2+、Ca2+、Ni2+、Mn2+、Pb2+等雜質。要制得高純氧化鐵就必須將上述雜質去除以獲得純凈的鐵溶液。實驗首先去除溶液中的Al3+,再去除Mg2+、Ca2+,最后去除Ni2+、Mn2+、Pb2+等重金屬。
2.4.1 Fe3+的還原
查閱文獻可知,Fe3+開始沉淀的pH為1.5,沉淀完全后pH為4.1;而Al3+開始沉淀的pH為3.3,沉淀完全后pH為5.2。Fe3+與Al3+沉淀的pH接近并且存在一個交叉區。此外,Fe2+開始沉淀的pH為7.1,沉淀完全后pH為9.1。由此可以判斷,通過調整pH,會使Al3+沉淀時體系內的Fe3+共沉淀,造成鐵資源的損失。因此,要達到既要去除溶液中的Al3+,又不造成鐵損失的目的,首先要改變鐵離子的價態,將溶液中的Fe3+還原為Fe2+。
實驗以鐵粉為還原劑將Fe3+還原為Fe2+。通過多次實驗確定的優化工藝條件:還原鐵粉用量為理論量1.3倍、反應溫度為60℃、反應時間為30min。在此條件下Fe3+的還原率為99.8%。
2.4.2 Mg2+、Ca2+的去除
實驗采用氟化法去除溶液中的Mg2+、Ca2+。通過實驗確定的優化工藝條件為氟化鈉用量為理論量的15倍、反應溫度為80℃、反應時間為30min。在此條件下Mg2+、Ca2+的去除率均為100%。
2.4.3 重金屬離子的去除
實驗采用硫化法去除溶液中的重金屬離子。通過實驗確定的優化工藝條件:硫化鈉用量為理論量的10倍、反應溫度為80℃、反應時間為30min。在此條件重金屬離子的去除率為99.6%。
2.4.4 溶液中Al3+的去除
去除鈣鎂和重金屬離子后的溶液中含有少量的Al3+,采用氧化水解法將其去除。實驗向溶液中滴加稀氨水將pH調整至5.2~5.5,使其中的Al3+轉化為氫氧化鋁沉淀,經過濾獲得純凈的硫酸亞鐵溶液。實驗確定的最佳工藝條件:氨水質量分數為6%、反應溫度為50℃、反應時間為20min。在此條件下溶液中Al3+的去除率為98.08%。
綜上所述,在優化工藝條件下對鐵沉淀物進行酸解、還原與凈化制得了高純度的硫酸亞鐵溶液,從而為α-FeOOH的制備提供了優質鐵源。
2.5 α-FeOOH的制備
2.5.1 鐵離子價態調整
實驗采用廉價且不引入雜質的雙氧水為氧化劑將體系中的Fe2+氧化為Fe3+,以制備高純氧化鐵的前驅物α-FeOOH,并確定了最佳工藝條件:雙氧水加入量為理論量的1.3倍、反應溫度為40℃、反應時間為30min。在此條件下反應,以高錳酸鉀溶液做定性實驗,溶液中無Fe2+。
2.5.2 α-FeOOH的制備
實驗采用了氧化沉淀法工藝,即以實驗室配制的復合溶液為底液,以氨水為pH調節劑,在一定溫度條件下將氧化充分的Fe3+溶液和pH調節劑加入底液中,使溶液中的Fe3+轉化為α-FeOOH沉淀,再經過濾、漂洗、脫水制得α-FeOOH。實驗考察了沉淀過程反應終點pH、反應溫度和反應時間對Fe3+沉淀率的影響并確定了最佳工藝條件。
1)反應終點pH。Fe3+開始沉淀的pH為1.5,沉淀完全后pH為4.1,反應終點pH直接影響著Fe3+的沉淀率。在反應溫度為90℃、反應時間為60min的條件下,考察了反應終點pH對Fe3+沉淀率的影響,結果見圖7。從圖7可以看出,隨著反應終點pH的升高,Fe3+的沉淀率逐漸上升;在pH=3.5時Fe3+基本沉淀完全,再繼續升高pH則Fe3+沉淀率基本無變化。因此,確定適宜的反應終點pH為3.5,此時的Fe3+沉淀率為99.4%。
2)反應溫度。在反應終點pH為3.5、反應時間為60min的條件下,考察了反應溫度對Fe3+沉淀率的影響,結果見圖8。從圖8可以看出,隨著反應溫度的升高,Fe3+沉淀率逐漸上升;在85℃時Fe3+基本沉淀完全,再繼續升高溫度則Fe3+沉淀率變化不大。因此,實驗確定適宜的反應溫度為85℃,此時的Fe3+沉淀率為99.6%。
3)反應時間。在反應終點pH=3.5、反應溫度為85℃的條件下,考察了反應時間對Fe3+沉淀率的影響,結果見圖9。從圖9可以看出,在反應時間為30min時,Fe3+基本沉淀完全;繼續延長反應時間,Fe3+沉淀率變化不大。因此,實驗確定適宜的反應時間為30min,此時的Fe3+沉淀率為99.7%。
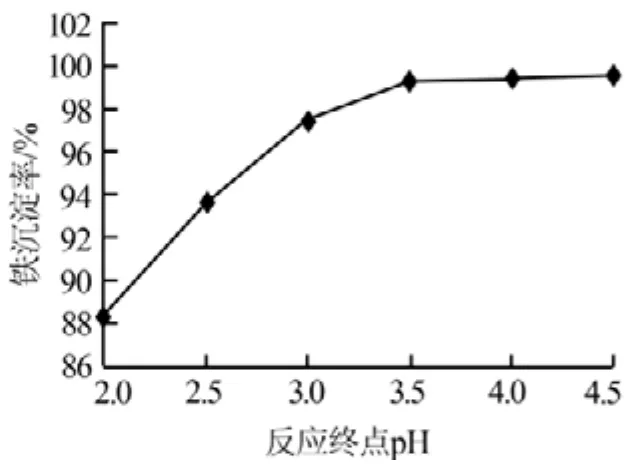
圖7 反應終點pH與Fe3+沉淀率的關系
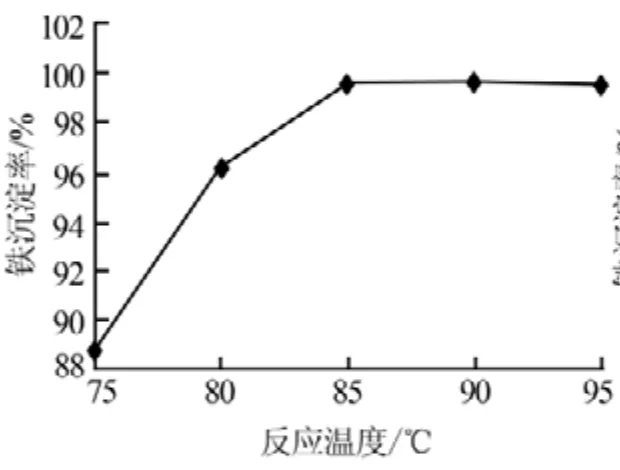
圖8 反應溫度與Fe3+沉淀率的關系
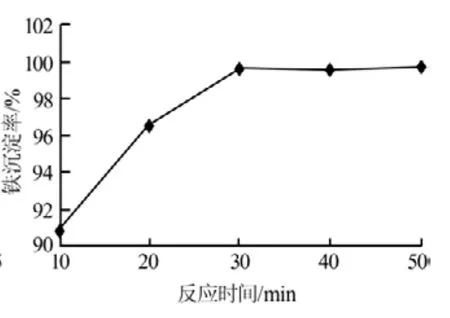
圖9 反應時間與Fe3+沉淀率的關系
2.6 α-Fe2O3的制備
α-FeOOH經過高溫煅燒制得α-Fe2O3,煅燒溫度的高低及煅燒時間的長短對產物純度及能源消耗有著直接影響。實驗考察了煅燒溫度和煅燒時間對產物純度的影響,結果見圖10和圖11。由圖10可以看出,在控制煅燒時間為240min的情況下,α-Fe2O3含量隨著煅燒溫度的升高而升高;當煅燒溫度為700℃時,α-Fe2O3的質量分數為99.68%,繼續升高煅燒溫度則α-Fe2O3含量基本無變化。因此,實驗確定適宜的煅燒溫度為700℃。由圖11可以看出,在煅燒溫度為700℃條件下,α-Fe2O3含量隨著煅燒時間的延長而升高;當煅燒時間達到180min時,α-Fe2O3的質量分數達到99.8%,繼續延長煅燒時間則α-Fe2O3含量基本無變化。因此,實驗確定適宜的煅燒時間為180min。
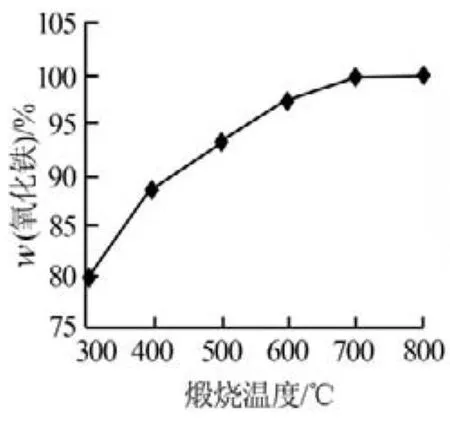
圖10 氧化鐵含量與煅燒溫度的關系
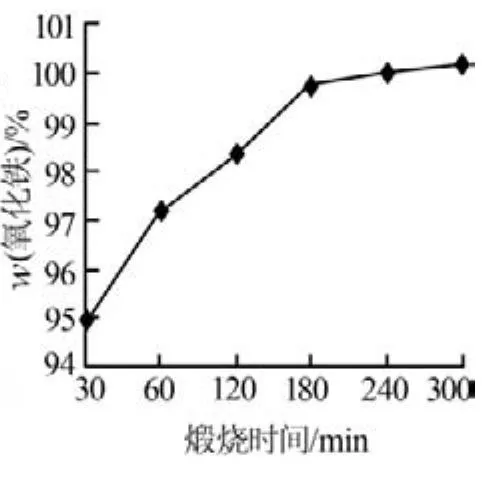
圖11 氧化鐵含量與 煅燒時間的關系
綜上所述,由α-FeOOH制備α-Fe2O3的優化工藝條件:煅燒溫度700℃、煅燒時間180min。在此條件下制得的α-Fe2O3質量分數為99.8%。經分析,其他雜質含量(質量分數):SiO2,0.005%、CaO,0.01%、Al2O3,0.01%、MnO,0.25、MgO,0.01%。該組成符合SJ/T 10383—1993《軟磁鐵氧體用氧化鐵》[5]中的相關要求。
3 結論
實驗以蛇紋石為鐵源制備出了符合軟磁鐵氧體用氧化鐵質量要求的高純氧化鐵,并確定了優化工藝條件。在優化工藝條件下將蛇紋石加工過程所得鐵鋁沉淀物進行精致、洗滌、酸解、還原、凈化、氧化、沉淀、煅燒制得高純氧化鐵產品,主含量達到99.8%(質量分數),其他雜質指標符合軟磁鐵氧體用氧化鐵標準要求。該工藝具有操作簡單、鐵轉化率高、產物純度高等特征,從而為蛇紋石的綜合利用及高純氧化鐵的制備開辟了一條新途徑。
[1]楊杰茹,于少明,左鵬.由蛇紋石制取鎂、硅系列產品的研究進展[J].化工礦物與加工,2007,36(10):25-29.
[2]何蘇萍,高倩,余曉婷,等.氧化鐵紅的制備方法及其在涂料中的應用[J].化工生產與技術,2011,18(1):29-32.
[3]馬紅欽,李玉培,婁紅斌,等.鹽礦鹵水中鈣鎂離子的深度凈化研究[J].中國井礦鹽,2005,36(6):8-11.
[4]李秀芬.硫化鈉從稀土礦淋出液中除重金屬離子[J].礦產綜合利用,2000(3):46-47.
[5]SJ/T 10383—1993.軟磁鐵氧體用氧化鐵[S].
聯系方式:nypengmei@126.com
一種廢石膏制備納米碳酸鈣漿料的方法
本發明公布了一種以廢棄石膏為碳源制備納米碳酸鈣漿料的方法。具體步驟:1)將石膏漿料與氨水混合并攪拌;2)連續攪拌條件下注入二氧化碳,直到石膏中的硫酸鈣完全轉化為納米碳酸鈣;3)過濾后,將濾餅在水中分散,形成納米碳酸鈣漿料。該工藝操作簡單、成本低廉、分散溫度較低,便于推廣和使用。
US,8846562
Preparation of high purity ferric oxide from serpentine
Xiao Jingbo,Xia Jiaobin,Chen Juling
(Nanyang Oriental A pplication Chemical Research Institute,Nanyang 473000,China)
Iron oxide with high purity was prepared by oxidation precipitation and calcination method.The Fe-Al precipitate formed in the purification process of acid leaching solution of serpentine was adopted as raw material.By some detailed investigation,such as the refined preparing of Fe-Al precipitate,the acid hydrolysis of iron-based precipitate,the reducing of Fe3+in the acid hydrolysis solution,the purifying of iron solution,the preparation of iron oxide precursor(α-FeOOH)and the study of the calcination process,the optimum conditions were confirmed.Moreover,the corresponded experimental results indicated that the yield of iron and the purity of iron oxide could be up to 99.9%and 99.8%,respectively,which met with the quality requirements of ferrite iron applied in soft ferrite.
serpentine;iron oxide;soft ferrite
TQ138.11
A
1006-4990(2014)11-0030-05
2014-05-21
肖景波(1962— ),男,高級工程師,主要研究方向為濕法冶金、工業廢棄物及非金屬礦綜合利用,已公開發表論文10篇。

