ATR-FTIR檢測畢赤酵母發酵中甘油和甲醇濃度*
吳勝,杭海峰,郭美錦,儲炬,莊英萍,張嗣良
(華東理工大學生物反應器工程國家重點實驗室,上海,200237)
甲醇營養型畢赤酵母已經成為生產外源蛋白最常用的生產菌種之一,培養基的改進及發酵條件的優化顯著提高了工業化生產通量[1-3]。畢赤酵母發酵主要采用無機鹽培養基,在甘油批培養階段,以甘油為碳源菌體快速生長,獲得合適的菌體密度之后,需要監測甘油是否全部耗盡[4],發酵液中殘余的甘油將會影響外源蛋白的啟動表達效率[5]。進入誘導階段后碳源轉換為甲醇,此時甲醇既充當唯一的碳源又是誘導劑[6],培養過程中甲醇不會被完全利用而累積,為了防止甲醇在發酵液中的過量累積抑制細胞生長,動態監測發酵液中的甲醇濃度成為必要[7-9]。
紅外光譜(4 000~400 cm-1)能夠提供幾乎所有物質的結構信息,特別是在1 800~800 cm-1,這一波段稱為指紋圖譜區,對應分子和官能團的指紋振動,既能對已知物定量分析,也能鑒定可能存在的未知物[10]。通過使用衰減全反射(Attenuated Total Reflection,ATR)技術,有效地解決了在發酵液中強烈的水吸收和MIR穿透能力較弱的問題[11-14]。生物過程中所包含的物質是十分復雜的,采集的紅外光譜通常包含了諸多信息,選取合適的化學計量學方法能夠在復雜的光譜圖中提取有效信息,建立預測模型[15-16]。傅里葉紅外光譜法(Fourier Transform Infrared Spectroscopy,FIIR)的快速、通用、穩定、無破壞性和化學計量學方法的發展,使得紅外光譜法結合衰減全反射技術已經在生物過程監測中有了諸多應用[17-21]。
本研究中,應用ATR-FTIR結合偏最小二乘法(Partial Least Squares,PLS)建立了甘油、甲醇濃度的預測模型,該方法快速、無破壞性、樣品無需處理。模型成功在5 L發酵罐中監測甘油和甲醇的濃度變化,并通過分析比生長速率和比生產速率,比較了兩種甲醇濃度調控的方法。
1 材料和方法
1.1 材料
1.1.1 菌株
表達重組人溶菌酶的 Mut+型的畢赤酵母SMD1168,由本實驗室提供。
1.1.2 培養基
種子培養基(L):蛋白胨20 g,酵母粉10 g,葡萄糖 10 g。
5 L罐培養基(L):甘油40 g,85%磷酸6.7 mL,CaSO40.93 g,K2SO418.2 g,MgSO4·7H2O 14.9 g,KOH 4.13 g,PTM1 4.5 mL。
甘油補料培養基:50%(W/V)甘油(含12 mL/L PTM1)。
甲醇補料培養基:含有12 mL/L PTM1的甲醇。
1.2 實驗方法
1.2.1 種子培養
平板上挑取單菌落到種子培養基中,30℃,220 r/min,培養20 ~25 h。
1.2.2 5 L 罐發酵
本實驗采用5 L攪拌式反應器(上海國強生化工程裝備有限公司)進行批培養發酵,工作體積為3 L,起始攪拌、通氣量和溫度分別為300 r/min、1 vvm和30℃,發酵過程中用28%氨水控制發酵液pH至5.5,接種量為10%,培養過程中調節攪拌轉速和通氣量控制溶氧。
1.2.3 分析方法
菌體濃度及細胞干重:菌液稀釋后于波長600 nm處以去離子水為對照進行比色測定,OD600=OD讀數×稀釋倍數。10 mL發酵液,10 000 r/min離心10 min,去上清液,水洗2次,80℃烘干至恒重,光密度值與細胞干重呈線性。
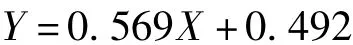
式中:X,OD600值;Y,細胞干重(DCW)。
甘油含量:通過甘油試劑盒(北京普利萊基因技術有限公司)測定。
甲醇含量:通過GC-1120氣相色譜儀(上海舜宇恒平儀器有限公司)測定。檢測條件:N2流量為15 mL/min,H2和空氣的流量分別為30 mL/min和300 mL/min,毛細管色譜柱溫度為180℃,氣化室氫火焰溫度為100℃,氫火焰溫度為180℃,進樣量為1 μL。
溶菌酶活性測定:制備溶壁微球菌懸浮液,450 nm波長下吸光值在0.7~0.8。取100 μL發酵液的上清液迅速加入微球菌懸浮液中反應1 min,觀察讀數值的下降并計算斜率:

FTIR:紅外光譜圖由帶有ATR附件的NicoLet-6700型傅里葉紅外光譜儀(美國賽默飛世爾科技有限公司)采集,維持恒定的環境溫度和濕度,分辨率2 cm-1,掃描次數64次,波數范圍4 000~400 cm-1,每1個樣品掃描3次。采集的光譜由自帶光譜處理軟件OMNIC5.1進行處理,PLS模型建立由Unscrambler 10.2軟件完成。
2 結果和分析
2.1 畢赤酵母發酵表達溶菌酶概述
圖1為本研究中一批畢赤酵母發酵甘油、甲醇濃度變化圖。分為3個階段:第1階段為甘油批培養階段,經過一段時間的遲滯期后進入對數期,甘油開始快速消耗,菌體量快速增加,第24 h左右初始甘油耗盡。第2階段為甘油補料批培養階段,維持DO>30%,限制性補加甘油,獲得合適的菌體濃度后,停止甘油流加。經過1~2 h的饑餓,甘油全部耗盡之后,進入甲醇誘導外源蛋白表達階段,這一階段維持DO大于20%。誘導前48 h溶菌酶酶活穩定增長,誘導進入到48 h之后酶活有一個躍升,72 h之后比生產速率下降,到培養結束時酶活為47 200 u/mL。
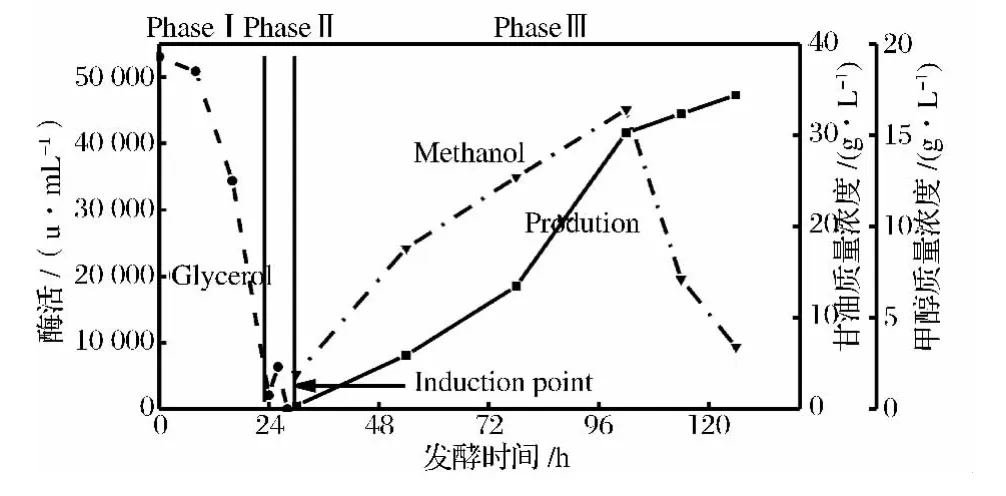
圖1 畢赤酵母批培養中甘油、甲醇和產物變化Fig.1 Product,glycerol and methanol concentrations versus time during the course of a fed batch process
2.2 PLS定量模型的建立
培養采用無機鹽培養基,成分明確,生長階段甘油作為碳源,誘導階段以甲醇為碳源。為了對發酵液紅外光譜有定性認識以及確定菌體、培養基中無機鹽成分是否對紅外光譜圖有影響,分別采集不含碳源的培養基溶液(Med)和甘油批培養階段、甲醇誘導階段發酵液的紅外光譜圖。

圖2 培養開始和過程中的發酵液光譜圖Fig.2 Spectra of(A)fermentation medium at the beginning and in the process with glycerol(B)fermentation medium at the beginning and in the process with methanol
圖2中的光譜圖基本重合,在1 150~1 000 cm-1波數內出現變化,鑒于兩者的差別只有碳源的不同,說明此處代表碳源對光譜的影響。培養基中無機離子增減變化可以用滲透壓強度來表示,測定培養過程中發酵液的滲透壓,圖3中在培養初期滲透壓有一個小幅的下降,從開始時的1 355 mOsm/L下降到1 210 mOsm/L后基本維持恒定,說明培養過程中無機離子強度沒有發生較大的變化,從另一個角度說明無機鹽對紅外譜圖的影響可以忽略不計。所以后續光譜采集中均采用無甘油和甲醇的培養基(Med)作為背景。
1 800~800 cm-1波數內的紅外光譜吸收對于組分定量有十分重要的意義。以Med為背景,采集20、10、5、1 g/L的甘油紅外吸收譜圖,如圖4A所示,在1 115.8~994 cm-1區間處有甘油的C—O鍵對稱與反對稱的伸縮振動吸收峰,分別在1 098,1 046,992 cm-1處有3個明顯的峰,且隨濃度升高峰面積增加,而在1 480~1 130 cm-1區間雖然光譜有不同,但是并沒有與濃度成一定關系。以Med為背景,采20、10、5、1 g/L的甲醇紅外吸收譜,圖 4B中甲醇在1 018 cm-1處有一單峰,且峰形較好,吸光度與甲醇濃度呈現出一定線性關系。
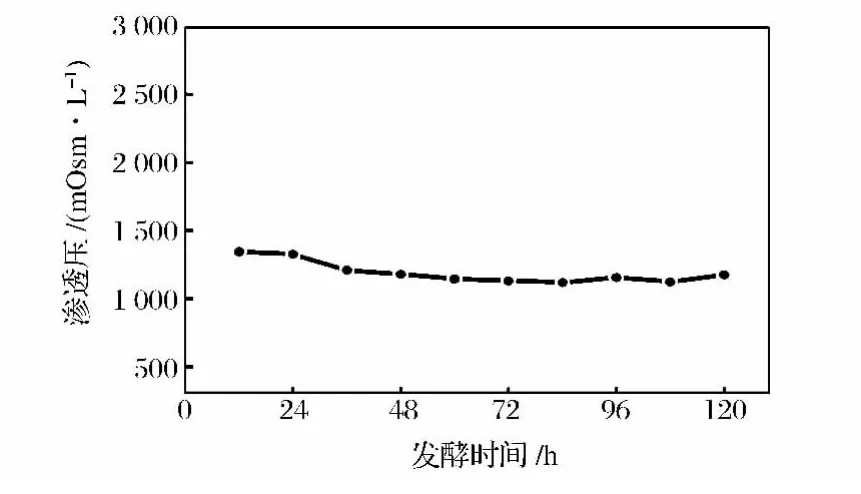
圖3 培養過程中的滲透壓Fig.3 Alteration of osmotic pressure during the process

圖4 甘油和甲醇的紅外特征吸收峰Fig.4 Absorption peak of IR spectrum of glycerol and methanol
甘油初始濃度較大,采用培養開始時無甘油的培養基作為背景,選取甘油紅外譜圖中1 140~950 cm-1的波數范圍,在0.5~50 g/L配置了28個不同濃度水平的甘油-培養基溶液,其中17個作為建模集,11個作為驗證集;由于甲醇初始濃度較小,誘導時間較長,為了校正背景變化對對譜圖的干擾,采集誘導開始時和結束后繼續培養直至DO回升至滿度時的2個背景,視此時甲醇濃度為零,分別為B1和B2,以B=(B1+B2)/2作為背景,選取1 075-930 cm-1的波數范圍,在0.1~30 g/L配置26個不同濃度水平的甲醇-培養基溶液,其中14個作為建模集,12個作為驗證集。以2 cm-1為輸入值點,構成輸入變量,輸入到UnscrambLer10.2中。光譜的預處理,通常有平滑、均值化、基線校正,多元散射校正,導數等。本研究中分別以原始光譜、基線校正及一階導數進行光譜預處理,分別建立PLS模型,結果如表1所示。模型的質量通常校正標準誤差(SEC)和驗證標準誤差(SEV)來評價,模型的預測能力由預測標準誤差(SEP)來評價。

表1 甘油和甲醇FTIR模型Table 1 FTIR models of glycerol and methanol
從表1可以看出,采用未經處理的原始光譜得到的甘油定量模型的 SEC為0.171 g/L,SEV為0.532 g/L,均小于另外2種光譜預處理方法。采用未經處理的原始光譜得到的甲醇定量模型的SEC為0.129 g/L,SEV為0.248 g/L,同樣均小于另外2種光譜預處理方法。原因可能是由于模型需要預測的甘油和甲醇成分單一,特征吸收峰明顯,基線校正及一階導數對光譜進行處理反而去掉了光譜定量的關鍵信息,所以本研究中甘油和甲醇的定量模型均采用原始光譜圖。
圖5為模型計算值與對照方法測得值的相關圖,可以看出低濃度和高濃度甘油和甲醇的模型值和對照測量值均緊密貼近性能線,表明模型質量較好。
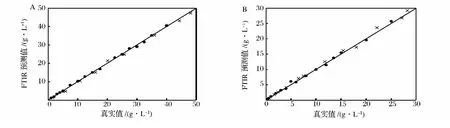
圖5 甘油和甲醇相關線性圖Fig.5 Correlation plot of calibration and validation sets for(A)glycerol and(B)methanol
2.3 5 L發酵罐FTIR調控
5 L攪拌式生物反應器中進行批發酵,每隔1 h采集1次發酵液的紅外光譜圖。設定的甘油初始濃度分別為65、55和45 g/L,圖6A中采用FTIR測得的甘油濃度和試劑盒測得的濃度有很好的相關性,預測標準誤差(SEP)為1.09 g/L。雖然起始的甘油濃度不相同,但均在12 h左右進入對數期生長,甘油濃度迅速下降,甘油耗盡后,限制性補加甘油,發酵液中的甘油濃度有小幅的上升,在補料結束后,甘油再次耗盡,最終菌體干重分別達到 204.5,168.4 和 146.7 g/L。甲醇誘導階段,需要將甲醇濃度控制在0.5% ~2%,誘導92 h,圖6B中,采用FTIR預測的甲醇濃度和氣相色譜測得的濃度有良好的相關性,預測標準誤差(SEP)為0.86 g/L。誘導開始后,發酵液中的甲醇開始累積,至40 h左右,發酵液中甲醇濃度接近20 g/L,采用FTIR調控下,降低甲醇的補加速率,甲醇濃度開始下降,在56 h下降到11.09 g/L,增加甲醇的補加速率,濃度上升,在69 h再次降低補加速率,直到培養結束。由于Mut+菌株有相對較大的甲醇耐受性,即使在沒有氧限制的情況下,甲醇也能累積。維持DO>20%控制甲醇流加(DO-stat),誘導開始后,發酵液中的甲醇濃度不斷累積,至培養結束時甲醇濃度達到34.55 g/L,可知采用FTIR調控的甲醇濃度要優于DO-stat調控。兩個模型的SEP均大于SEC和SEV,可能是由于發酵過程中產生的副產物分泌到發酵液當中,干擾了預測的精度。
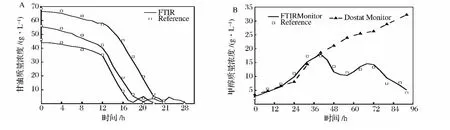
圖6 5L發酵罐中FTIR監測甘油和甲醇濃度Fig.6 Monitor the concentration of glycerol and methanol by FTIR
誘導結束后,繼續培養24h,目的是通過短時間內不斷改變甲醇的補加速度,驗證模型能夠迅速響應濃度變化。由圖7可知,模型預測的甲醇濃度隨著甲醇補加速度的改變有相應的變化趨勢,說明模型能對補加速度的改變快速做出反應。Cervera[22]總結了在生物過程中采用紅外光譜法的預測精度為0.2~3 g/L,Crowley[7]的研究中,甘油和甲醇定量模型的預測精度分別為2.04和0.24 g/L,本文的研究結果與之類似,模型能夠在畢赤酵母發酵過程中得到有效的應用。
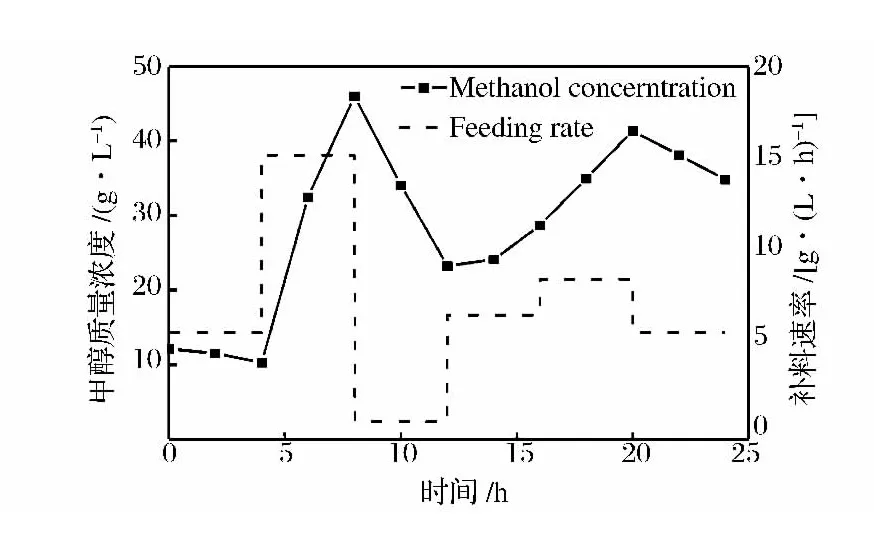
圖7 甲醇模型對甲醇補加速率的響應Fig.7 Response to different methanol feeding rate of methanol model
2.4 生長和生產能力的影響
比較FTIR調控和DO-Stat調控甲醇濃度下的比生長速率(μ)和比生產速率(Qp),結果如圖8所示。隨著誘導時間延長,菌體的比生長速率均呈下降趨勢,這既是甲醇的抑制作用,也是轉而表達溶菌酶產物的需要。
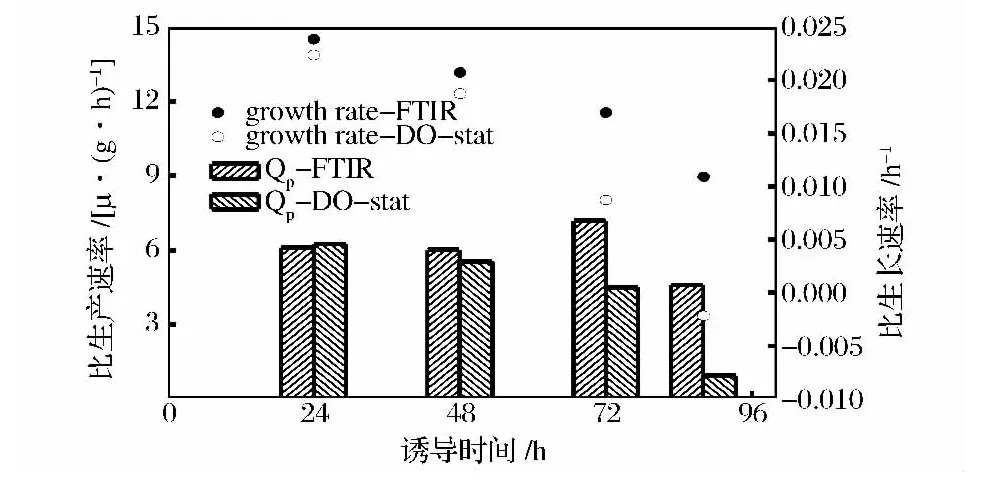
圖8 FTIR和DO調控下的比生長速率和比生產速率Fig.8 Specific growth rate and production rate monitored by FTIR and DO respectively
圖8中,FTIR調控下比生長速率從誘導開始的0.024 h-1下降到結束時的 0.011 h-1,下降 54.1%,而在DO-Stat調控下,不斷升高的甲醇濃度對菌體生長抑制作用更加明顯,比生長速率從誘導開始的0.022 h-1下降到結束時的 -0.002 18 h-1。有報道比生產速率和發酵液中甲醇的濃度存在一定的關系[6],本研究中,DO-Stat調控下誘導48 h時發酵液中甲醇濃度為2.1%,FTIR調控約為1.3%,而2種方法下比生產速率區別不大,說明在2%以內的甲醇濃度對外源蛋白的生產影響不大,而當甲醇濃度超過2%以后,比生產速率出現明顯的分化,72 h時DO-stat調控的比生產速率比FTIR調控下降37.8%,92 h時下降79.2%。圖9中,雖然在48h時,DO-Stat調控甲醇濃度大于2%,但是還不至于抑制菌體代謝,2種調控下的菌體攝氧率(OUR)相似,而在50 h以后,OUR出現分化,FTIR調控下,OUR不斷升高,而DO調控下,甲醇濃度不斷升高,菌體呼吸被抑制,OUR呈下降趨勢。
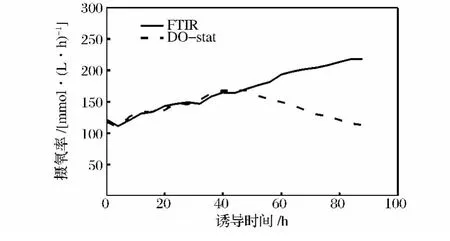
圖9 FTIR和DO調控下的OURFig.9 OUR monitored by FTIR and DO respectively
3 總結
本文通過ATR-FTIR監測畢赤酵母發酵過程中底物濃度的變化情況。甘油和甲醇的紅外光譜有明顯的特征吸收峰。以培養開始時的無甘油培養基(Med)為背景,配置一系列甘油標準溶液,通過PLS建模獲得甘油預測模型,SEC和SEV分別為0.171和0.532 g/L。以誘導開始和結束后溶氧反彈至滿度時的發酵液背景[B=(B1+B2)/2]為背景,配置一系列甲醇標準溶液,通過PLS建模獲得甲醇預測模型,SEC和SEV分別為0.129和0.248 g/L。5 L發酵罐中利用建立的模型預測發酵液中的甘油和甲醇的濃度,SEP分別為1.09和0.86 g/L。比較了誘導階段分別采用FTIR調控和DO-stat調控發酵液甲醇的濃度,FTIR調控將甲醇濃度控制小于2%,比生長速率和比生產速率均高于DO-stat調控,對于其他畢赤酵母發酵表達外源蛋白具有借鑒意義。當甲醇濃度大于2%以后,菌體生長和外源蛋白生產均受到明顯的抑制。
本研究采用ATR-FTIR能夠快速準確對發酵過程中甘油和甲醇濃度做出預測,成功應用于畢赤酵母的發酵調控,有效指導人溶菌酶的生產。但是該方法也存在一定不足,如定量模型的建立需要較多的樣品數,取樣頻繁造成發酵液體積的減少等。隨著在位ATR探頭的出現,在生產應用中能夠做到實時在線測量,這將符合實際過程中的情況,FTIR技術將會在生物過程監測領域中得到廣泛的應用。
[1] Curvers S,Linnemann J,Klauser T,et al.Recombinant protein production with Pichia pastoris in continuous fermentation-kinetic analysis of growth and product formation[J].Engineering in Life Sciences,2002,2(8):229-235.
[2] Macauley-Patrick S,Fazenda M L,McNeil B,et al.Heterologous protein production using the Pichia pastoris Expression System[J].Yeast,2005,22(4):249-270.
[3] Cregg J M,Cereghino J L,Shi J,et al.Recombinant protein expression in Pichia pastoris[J].Molecular Biotechnology,2000,16(1):23-52.
[4] Gao M J,Zheng Z Y,Wu J R,et al.Improvement of specific growth rate of Pichia pastoris for effective porcine interferon-α production with an on-Line model-based glycerol feeding strategy[J].Applied Microbiology and Biotechnology,2012,93(4):1 437-1 445.
[5] Daly R,Hearn M T W.Expression of heterologous proteins in Pichia pastoris:a useful experimental tool in protein engineering and production[J].Journal of Molecular Recognition,2005,18(2):119-138.
[6] Zhang W,Bevins M A,PLantz B A,et al.Modeling Pichia pastoris growth on methanol and optimizing the production of a recombinant protein,the heavy-chain fragment C of botulinum neurotoxin,serotype A[J].Papers in Biotechnology,2000:18.
[7] Crowley J,McCarthy B,Nunn N S,et al.Monitoring a recombinant Pichia pastoris fed batch process using Fourier transform mid-infrared spectroscopy(FT-MIRS)[J].Biotechnology Letters,2000,22(24):1 907-1 912.
[8] Roychoudhury P,Harvey L M,McNeil B.The potential of mid infrared spectroscopy(MIRS)for real time bioprocess monitoring[J].Analytica Chimica Acta,2006,571(2):159-166.
[9] Landgrebe D,Haake C,H?pfner T,et al.On-Line infrared spectroscopy for bioprocess monitoring[J].Applied Microbiology and Biotechnology,2010,88(1):11-22.
[10] 李潤卿.有機結構波譜學[M].天津:天津大學出版社,2002:145-151.
[11] Schenk J,Marison I W,von Stockar U.A simple method to monitor and control methanol feeding of Pichia pastoris fermentations using mid-IR spectroscopy[J].Journal of Biotechnology,2007,128(2):344-353.
[12] Dahlbacka J,Weegar J,von Weymarn N,et al.On-Line measurement of the substrate concentrations in Pichia pastoris fermentations using FT-IR/ATR[J].Biotechnology Letters,2012,34(6):1 009-1 017.
[13] Dahlbacka J,Kiviharju K,Eerik?inen T,et al.Monitoring of Streptomyces peucetius cultivations using FTIR/ATR spectroscopy and quantitative models based on Library type data[J].Biotechnology Letters,2013:35(3):337-343.
[14] Cozzolino D,Curtin C.The use of attenuated total reflectance as tool to monitor the time course of fermentation in wild ferments[J].Food Control,2012,26(2):241-246.
[15] Rathore A S,Bhushan N,Hadpe S.Chemometrics applications in biotech processes:a review[J].Biotechnology Progress,2011,27(2):307-315.
[16] Wold S,Sj?str?m M,Eriksson L.PLS-regression:a basic tool of chemometrics[J].Chemometrics and Intelligent Laboratory Systems,2001,58(2):109-130.
[17] Pistorius A,Degrip W J,Egorova-Zachernyuk T A.Monitoring ofbiomasscomposition from microbiological sources by means of FT ‐ IR spectroscopy[J].Biotechnology and Bioengineering,2009,103(1):123-129.
[18] Muller J,Neumann M,Scholl P,et al.Online monitoring of biotransformations in high viscous multiphase systems by means of FT-IR and chemometrics[J].Analytical Chemistry,2010,82(14):6 008-6 014.
[19] Roychoudhury P,Harvey L M,McNeil B.At-Line monitoring of ammonium,glucose,methyl oleate and biomass in a complex antibiotic fermentation process using attenuated total reflectance-mid-infrared(ATR-MIR)spectroscopy[J].Analytica Chimica Acta,2006,561(1):218-224.
[20] Kornmann H,Valentinotti S,Duboc P,et al.Monitoring and control of Gluconacetobacter xylinus fed-batch cultures using in situ mid-IR spectroscopy[J].Journal of Biotechnology,2004,113(1):231-245.
[21] Kansiz M,Billman-Jacobe H,McNaughton D.Quantitative determination of the biodegradable polymer poly(βhydroxybutyrate)in a recombinant Escherichia coli strain by use of mid-infrared spectroscopy and multivariative statistics[J].Applied and Environmental Microbiology,2000,66(8):3 415-3 420.
[22] Cervera A E,Petersen N,Lantz A E,et al.Application of near-infrared spectroscopy for monitoring and control of cell culture and fermentation[J].Biotechnology Progress,2009,25(6):1 561-1 581.

