殼聚糖希夫堿及殼聚糖改性微球的吸附性能研究
楊小玲,黃怡
(咸陽師范學院化學與化工學院,陜西咸陽 712000)
殼聚糖是迄今為止發現的唯一天然堿性多糖,分子內含有大量的官能團,如氨基和羥基等,對酚類、蛋白質、氨基酸等有機物有較強的吸附作用,并且具有良好的生物降解性、生物相容性和無毒性等特點,可以在污水處理中用作吸附劑、絮凝劑和重金屬離子的螯合劑等。由于殼聚糖存在一些缺點,如耐酸性差,吸附率低,往往需要進行改性[1-4]。通過改性將殼聚糖交聯成球,可以得到表面積大孔隙多的網狀結構的殼聚糖微球,并提高殼聚糖在溶液中的穩定性,更有利于殼聚糖的吸附性能的發揮[5-8]。
本課題以殼聚糖為原料,制備殼聚糖希夫堿,并采用反相懸浮聚合法制備殼聚糖希夫堿微球。用靜態吸附法,以殼聚糖為吸附劑,分別以磁流體及模型藥物亞甲基藍為吸附質,比較殼聚糖希夫堿及殼聚糖改性微球的吸附性能。
1 實驗部分
1.1 試劑與儀器
殼聚糖,脫酰度為90%;對二甲氨基苯甲醛、冰乙酸、甲苯、亞甲基藍均為分析純;甲苯2,4-二異氰酸酯(TDI),化學純。
IRPrestige-21型傅里葉變換紅外光譜儀;SPECORD-50紫外可見分光光度計。
1.2 實驗方法
1.2.1 殼聚糖希夫堿的制備 稱取3.2 g殼聚糖,溶于200 mL 2%的醋酸溶液中,80℃下加熱攪拌,滴加溶有3.0 g對二甲氨基苯甲醛的乙醇溶液,反應5 h,冷卻,抽濾,洗滌,干燥,得殼聚糖希夫堿。
1.2.2 四氧化三鐵的制備 在150 mL蒸餾水中溶解3.47 g FeCl3,將其倒入250 mL的三口燒瓶中,在恒溫水浴30℃下反應20 min,緩慢加入60 mL 8.43 g/L的 Na2SO3,經過 20 min 后,再快速加入60 mL 233.33 g/L的NaOH,將水浴升溫至55℃,繼續反應15 min,再升溫至80℃,反應30 min后,得灰棕色液體,冷卻,離心,除去上層清液,得四氧化三鐵磁流體。
1.2.3 殼聚糖希夫堿微球的制備[9-10]稱取1.0 g殼聚糖希夫堿,加入到25 mL 0.5%的NaOH溶液中浸泡數小時,作為水相。將20 mL環己烷、20 mL甲苯以及定量Span-60和Tween-20加入到250 mL三口瓶中,加熱攪拌,使乳化劑完全溶解,作為油相。70℃時將水相滴加到油相中,再加TDI 8滴,同時攪拌,回流反應2 h,得到黃色乳液,離心,除去上層油相,用蒸餾水多次洗滌,50℃真空干燥,得到殼聚糖希夫堿微球。
1.3 殼聚糖希夫堿及希夫堿微球的吸附性
1.3.1 對四氧化三鐵磁粉吸附 稱取0.15 g殼聚糖希夫堿及希夫堿微球分別溶脹于2個100 mL蒸餾水中,加入1.0 g四氧化三鐵,靜置吸附,磁分離,得產物,即磁性/殼聚糖希夫堿及磁性希夫堿微球。稱取磁性/殼聚糖希夫堿及磁性微球各0.1 g,用鄰二氮菲分光光度法分別測定其磁含量。
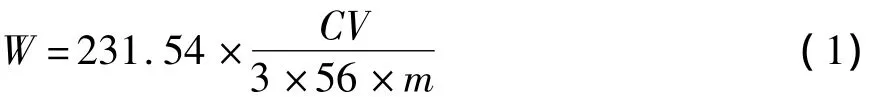
式中 W——磁含量,mg/g;
C——Fe2+濃度,mg/L;
V——Fe2+溶液體積,L;
m——磁性殼聚糖希夫堿或磁性微球質量,g。
1.3.2 對亞甲基藍的吸附 配制亞甲基藍標準溶液,在其最大吸收波長668 nm處測定溶液的吸光度,繪制標準曲線,得出標準曲線方程y=0.154 9x+0.046 5(R2=0.996 2)。
稱取0.2 g殼聚糖希夫堿和殼聚糖希夫堿微球各2份,分別加入100 mL濃度為40 mg/L的亞甲基藍溶液中,吸附3 h時取上清液10 mL,同時補充原液,在668 nm波長處測上清液的吸光度,用以下公式計算吸附量Q及吸附率η。

式中 Q——吸附量,mg/g;
C0、C——分別為吸附前、后溶液中亞甲基藍的質量濃度,mg/L;
m——吸附劑質量,g;
V——亞甲基藍溶液體積,L。
1.4 希夫堿及微球中磁含量測定
用鄰二氮菲分光光度法,分別配制濃度為1.0,2.0,3.0,4.0,5.0 mg/L 的 Fe2+溶液,測定吸光度,得到濃度-吸光度標準曲線方程 y=0.004 7x-0.002 5(R2=0.997 2)。
2 結果與討論
2.1 紅外測定結果
殼聚糖、希夫堿及微球的紅外測試結果見圖1。
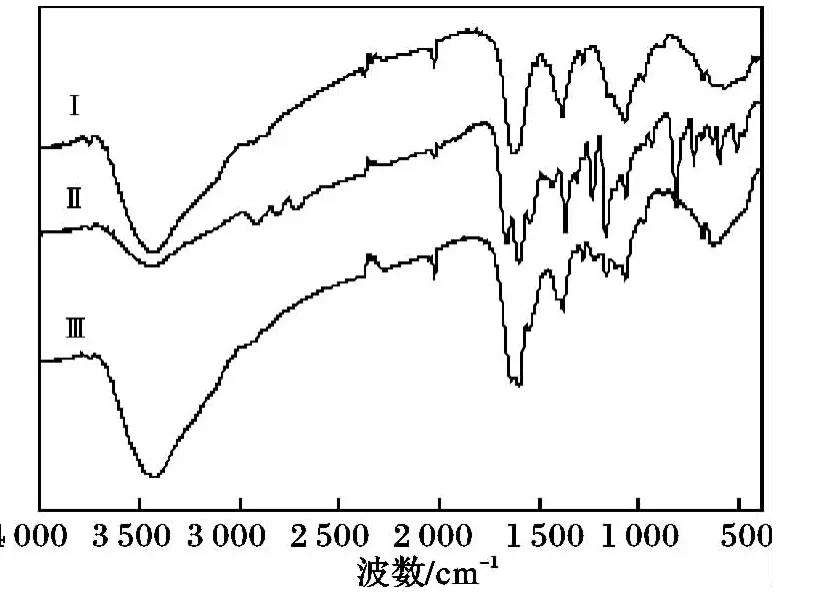
圖1 殼聚糖與殼聚糖希夫堿及微球的紅外譜圖Fig.1 IR spectrum of CS and its Schiff base

2.2 磁含量測定結果
根據標準曲線方程計算,當以殼聚糖希夫堿為吸附劑時,溶液中Fe2+離子含量為2.850 mg/g,用公式(1)換算為四氧化三鐵的吸附容量為39.279 mg/g;而希夫堿微球中,Fe2+離子含量為8.212 mg/g,換算為四氧化三鐵的吸附容量為113.179 mg/g。結果表明,形成微球后的殼聚糖希夫堿對金屬離子的吸附性要明顯優于單純的殼聚糖希夫堿,這是由于殼聚糖交聯成的微球中有豐富孔隙結構,有利于提高吸附量,同時形成的空間網絡結構通過鍵合作用提高吸附四氧化三鐵的穩定性。
2.3 對亞甲基藍吸附結果
2.3.1 中性水溶液動力學吸附 常溫下,在不同時間,當亞甲基藍濃度為40 mg/L時,殼聚糖希夫堿及希夫堿微球對亞甲基藍的吸附結果見圖2。
由圖2可知,殼聚糖希夫堿與希夫堿微球對亞甲基藍的吸附隨著時間推移吸附率上升,從開始到30 min,吸附速率較快,30 min后吸附速率逐漸緩慢,到120 min后趨于平衡,150 min時均達到吸附平衡。當亞甲基藍的初始濃度為40 mg/L,吸附劑濃度為2 g/L時,達到飽和吸附,殼聚糖希夫堿及希夫堿微球對亞甲基藍的吸附率分別為60.7%和68.63%。在同一時間,殼聚糖希夫堿微球的吸附率總是大于殼聚糖希夫堿。
2.3.2 熱力學吸附 圖3、圖4給出了殼聚糖希夫堿以及殼聚糖希夫堿微球對亞甲基藍的吸附容量及吸附率隨溶液中亞甲基藍濃度的變化情況。
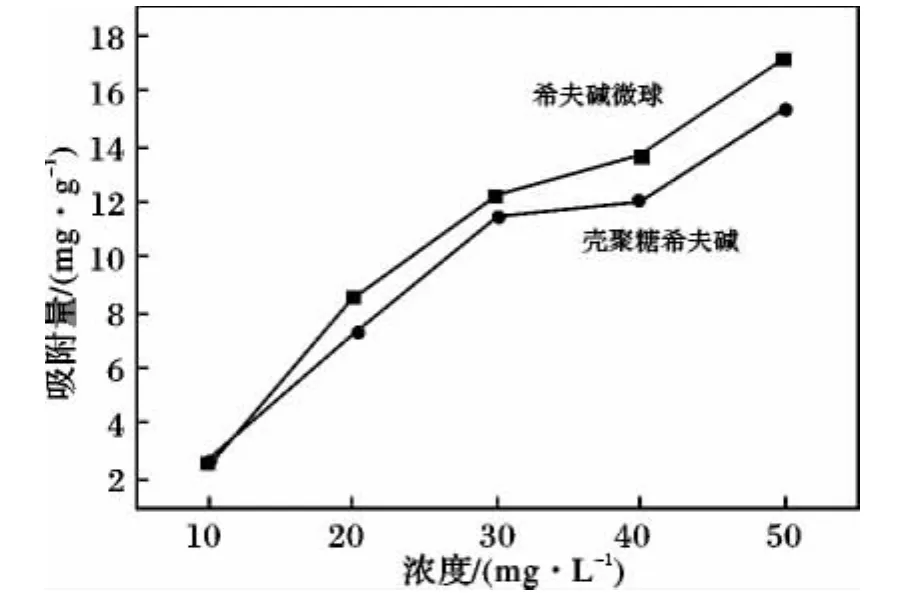
圖3 亞甲基藍溶液初始濃度對吸附容量影響Fig.3 Effect of the initial methylene blue concentration on adsorption capacity of methylene blue
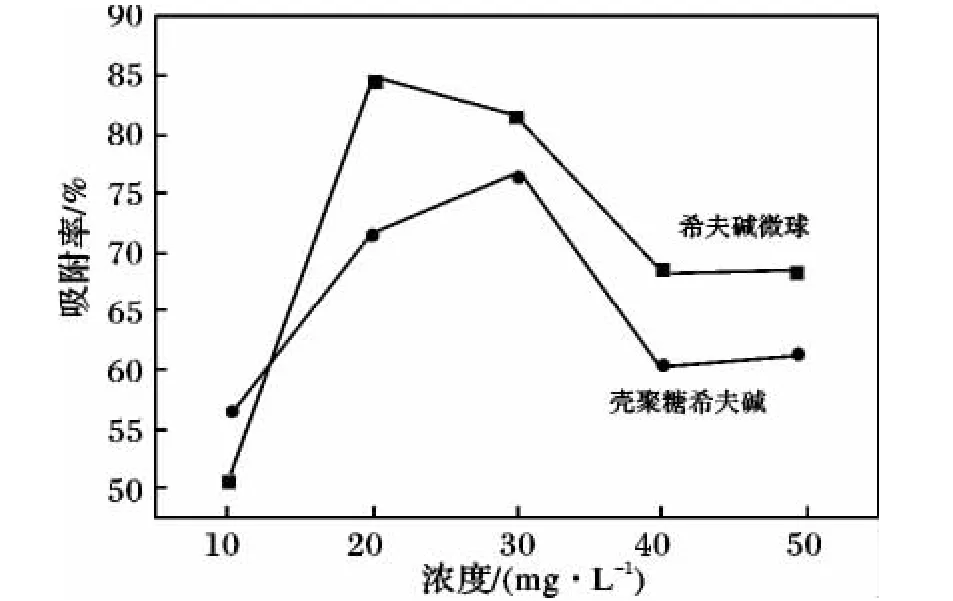
圖4 亞甲基藍溶液濃度對吸附率的影響Fig.4 Effect of the initial methylene blue concentration on adsorption rate of methylene blue
由圖3、圖4可知,隨著亞甲基藍濃度的增大,殼聚糖希夫堿及希夫堿微球的吸附容量均不斷增大,而吸附率出現一個極大值。除了初始濃度10 mg/L時,殼聚糖希夫堿的吸附率高之外,其他亞甲基藍溶液濃度相同的情況下,殼聚糖希夫堿微球的吸附容量及吸附率均大于殼聚糖希夫堿。當亞甲基藍濃度為50 mg/L時,殼聚糖希夫堿及希夫堿微球對亞甲基藍的吸附容量分別為 15.33,17.15 mg/g;二者的吸附率最大值分別是:當亞甲基藍濃度為30 mg/L時,殼聚糖希夫堿的吸附率為76.73%;亞甲基藍濃度為20 mg/L時,微球的吸附率為84.9%。因此整體上,微球吸附性能高于殼聚糖希夫堿。
3 結論
以殼聚糖和對二甲氨基苯甲醛為原料,制得殼聚糖希夫堿,然后以殼聚糖希夫堿為底物,制備殼聚糖希夫堿微球。并選取2種吸附對象:四氧化三鐵和亞甲基藍,比較希夫堿及其微球的吸附性能。結果表明,希夫堿及其微球對四氧化三鐵的吸附為物理吸附,吸附容量分別為 39.279,113.179 mg/g,殼聚糖希夫堿及其微球對亞甲基藍的吸附平衡時間均為150 min,飽和吸附容量隨著亞甲基藍初始質量濃度的增大而增大,且微球的吸附容量大于殼聚糖希夫堿,吸附率不隨濃度增大單調遞增,而是有一極大值。整體上,微球吸附性能優于殼聚糖希夫堿。
[1]張艷雅,馬啟敏.殼聚糖改性吸附劑的制備及其吸附性能研究[J].中國海洋大學學報,2006,36(增刊):153-156.
[2]安勝姬,張蘭英,鄭松志,等.二異氰酸酯與殼聚糖交聯產物對金屬離子的吸附性能[J].長春科技大學學報,1999,29(2):197-199.
[3]趙春祿,劉輝,劉振儒.殼聚糖的化學改性及其吸附性能的研究[J].環境化學,2005,24(2):209-212.
[4]曹佐英,賴聲禮.微波輻射下甲醛交聯殼聚糖的制備及其吸附性能的研究[J].現代化工,1999,19(6):24-26.
[5]蘇苗,王麗麗,林強.殼聚糖/β-環糊精交聯聚合物的制備及其對葛根素的吸附性能[J].過程工程學報,2011,11(6):978-983.
[6]賀小進,譚天偉,戚以政,等.球形殼聚糖樹脂制備方法及吸附性能研究[J].離子交換與吸附,2000,16(l):47-53.
[7]葛華才,黃仕英,梁愷.殼聚糖改性微球的微波輻射制備及吸附性能[J].華南理工大學學報:自然科學版,2009,37(6):27-30,36.
[8]張所信,江龍法,王為國,等.球形殼聚糖希夫堿的制備及性質[J].南京化工大學學報,1999,21(6):89-91.
[9]李桂銀,楊棟梁,黃可龍,等.Fe3O4/羧基改性殼聚糖復合納米粒子的制備、表征及生物學應用[J].功能材料,2009,40(7):1184-1187.
[10]季業,邵慧萍,郭志猛,等.超聲乳化法制備納米Fe3O4磁性顆粒及殼聚糖表面改性[J].北京科技大學學報,2011,33(6):751-755.

