重組人血管內皮抑素聯合同步放化療治療晚期非小細胞肺癌療效和安全性Meta分析
徐慧琳,戈偉,曹德東,明平坡,鄭永法,宋婧,羅衛
(武漢大學人民醫院腫瘤二病區,武漢 430060)
重組人血管內皮抑素聯合同步放化療治療晚期非小細胞肺癌療效和安全性Meta分析
徐慧琳,戈偉,曹德東,明平坡,鄭永法,宋婧,羅衛
(武漢大學人民醫院腫瘤二病區,武漢 430060)
目的 系統評價重組人血管內皮抑素聯合同步放化療與同步放化療比較治療晚期非小細胞肺癌(NSCLC)的有效性和安全性。方法計算機系統檢索Cochrane圖書館、PubMed、中國生物醫學文獻數據庫、中國學術期刊全文數據庫、EMbase、維普數據庫、萬方數據庫所收錄的相關研究,檢索時間截止至2013年8月。研究對象為NSCLC患者,治療組采用重組人血管內皮抑素聯合同步放化療,對照組僅用同步放化療,比較兩組療效及安全性。使用Cochrane手冊5.1.0版的質量評價標準對納入研究進行質量評價,使用RevMan 5.1.0版軟件進行數據分析。結果最終納入5項研究,共217例患者。Meta分析結果表明:與對照組比較,治療組有效率提高[OR=2.62,95%CI(1.41,4.86),P=0.002]。在臨床獲益率[OR=2.08,95%CI(0.92,4.73),P=0.08]、1年生存率[OR=1.18,95%CI(0.53,2.66),P=0.68]、生活質量改善[OR=1.57,95%CI(0.40,6.07),P=0.52]、白細胞減少[OR=1.25,95%CI(0.72,2.17),P=0.43]、放射性食管炎[OR=1.16,95%CI(0.42,3.21),P=0.77]、放射性肺炎[OR=2.47,95%CI(0.34,17.68),P=0.37]等方面,兩組均差異無統計學意義。結論與僅用同步放化療比較,重組人血管內皮抑素聯合同步放化療治療晚期NSCLC可提高療效,兩組生活質量改善情況及毒副反應發生率相當。受納入研究質量限制和可能存在的發表偏倚影響,上述結論尚需更多高質量的隨機對照試驗加以驗證。
重組人血管內皮抑素;肺腫瘤;同步放化療;Meta分析
重組人血管內皮抑素注射液(rh-endostatin, Endostar,商品名:恩度)是由我國學者自主研究開發的抗血管生成藥物,主要用于治療初治和復治的晚期非小細胞肺癌(non small cell lung cancer,NSCLC)。王金萬等[1]進行的Ⅲ期臨床試驗研究顯示,重組人血管內皮抑素與長春瑞濱加順鉑方案聯合應用治療晚期NSCLC能夠顯著提高客觀療效,改善生活質量,延長生存時間。周琦超等[2]進行的多中心Ⅰ+Ⅱ期臨床試驗提示,重組人血管內皮抑素聯合同步放化療(concurrent chemoradiotherapy,CRCT)對不可手術切除Ⅲ期NSCLC近期療效和耐受性良好,晚期NSCLC的有效性和安全性的臨床觀察可見報道[3-9],卻無相關循證醫學證據。因此筆者利用循證醫學方法對重組人血管內皮抑素聯合CRCT能否提高晚期NSCLC患者的臨床療效進行系統評價,以期為臨床應用提供依據。
1 資料與方法
1.1 納入與排除標準 ①研究對象:經細胞學或病理學確診為晚期NSCLC,治療前卡氏評分(Karnofsky, KPS)>70分,肝腎功能、血常規、心電圖正常。排除標準:小細胞肺癌患者,孕婦,用藥過敏者,存在心功能不全、糖尿病、并發肺栓塞、嚴重肝腎疾病等基礎疾病的患者。②研究類型:臨床隨機對照試驗(randomized controlled trial,RCT)。③干預措施:在CRCT的基礎上聯用重組人血管內皮抑素。④結局指標:有效率(response rate,RR),腫瘤進展時間(time to progress, TTP),臨床獲益率(clinical benefit rate,CBR),毒副反應,生活質量(quality of life,QoL),1年生存率,1年無進展生存率。
1.2 檢索策略 計算機檢索Cochrane圖書館(2013年第1期),PubMed(1966年至2013年8月),EMbase (1974年1月至2013年8月),重慶維普數據庫(VIP, 1989年1月至2013年8月),中國學術期刊全文數據庫(CNKI,1994年至2013年8月),中國生物醫學文獻數據庫(CBM,1978年至2013年8月),萬方數據庫(WanFang Data,1997年至2013年8月)。同時運用Coogle Scholar等搜索引擎在互聯網上查找相關文獻。中文檢索詞:肺癌、肺腫瘤、非小細胞肺癌、晚期非小細胞肺癌、放化療、化療、放療、同步放化療、重組人血管內皮抑素、重組人血管內皮抑素、內皮抑素、英文檢索詞:endostatin,rh-endostatin,endostar,YH-16,advanced non small cell lung cancer,non small cell lung cancer, NSCLC,concurrent chemoradio-therapy,chemoradiotherapy。
1.3 資料提取與質量評估 兩位研究者根據Cochrane評價手冊設計相關資料的提取表格,并對所納入研究進行資料提取。提取的資料信息包括:①試驗的基本情況、兩組患者的基線情況;②干預措施、結局指標、失訪及其處理。如遇到文獻資料不全,可通過與作者聯系獲取。兩名評價員按Cochrane手冊5.1.0版的質量評價標準對納入的RCT進行質量評價。評價內容包括:具體隨機分配方法、分配方案是否隱藏、是否采用盲法、結果數據的完整性、是否選擇性報道研究結果、其他偏倚來源。
1.4 統計與分析 使用Cochrane協作網的RevMan5.1.0版軟件進行Meta分析。采用ZLung cancer檢驗分析納入研究的異質性,若P>0.1采用固定效應模型,若P<0.1,則首先分析異質性原因,若無臨床異質性,則采用隨機效應模型進行Meta分析。計數資料采用比值比(odds ratio,OR)及其95%可信區間(confidence interval,CI)表示效應;連續性變量采用權重均數差(weighted mean difference,WMD)表示療效效應量,各效應量均配以95%CI表示療效效應。若各研究采用不同的測量方法且測量單位不同時,則使用標準均數差(standardized mean differenee,SMD)。
2 結果
2.1 檢索結果 初檢文獻116篇。閱讀題目及摘要后,排除明顯不符合納入標準的文獻后得到10篇文獻,進一步仔細查閱全文排除干預措施、研究對象不合格的文獻,最終納入5個RCT[5-9],包括217例患者,進入分析的文獻兩組基線資料具有可比性。見表1。
2.2 納入文獻的質量評價 筆者所納入的5個研究,包含217例患者。這些研究均不是大樣本多中心RCT,且對隨機方法的具體內容沒有闡述,同時缺乏對盲法及隨訪應用的說明,為低質量文獻。
2.3 統計分析
2.3.1 治療有效率 納入的5個RCT[5-9]均報道了有效率,各研究間具有同質性(P=0.85,I2=0%),故采用固定效應模型進行Meta分析。結果顯示,治療組的治療有效率較對照組高,其差異有統計學意義。P= 0.002,[OR=2.62,95%CI(1.41,4.86)](圖1)。

表1 納入研究的一般情況Tab.1 General characteristics of the included studies
2.3.2 臨床獲益率 3個RCT[5,7,9]報道了臨床獲益率,各研究間具有同質性(P=0.37,I2=0%),故采用固定效應模型進行Meta分析。結果顯示兩組差異無統計學意義(P=0.08)[OR=2.08,95%CI(0.92,4.73)](圖2)。
2.3.3 1年生存率 3個RCT[6,8-9]報道了1年生存率,各研究間具有同質性(P=0.75,I2=0%),故采用固定效應模型進行Meta分析。結果顯示兩組差異無統計學意義(P=0.68)[OR=1.18,95%CI(0.53,2.66)] (圖3)。
2.3.4 生活質量改善率 2個RCT[6-7]報道了QoL的改善穩定率,各研究間具有同質性(P=0.82,I2= 0%),故采用固定效應模型進行Meta分析:結果顯示兩組差異無統計學意義(P=0.52)[OR=1.57,95%CI (0.40,6.07)](圖4)。
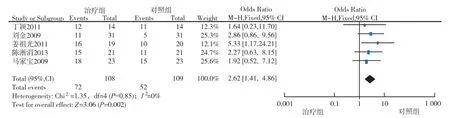
圖1 重組人血管內皮抑素聯合CRCT與CRCT治療NSCLC有效率比較的Meta-分析Fig.1 Meta-analysis on response rate of CRCT with or without endostar for advanced NSCLC

圖2 重組人血管內皮抑素聯合CRCT與CRCT治療NSCLC臨床獲益率比較的Meta-分析Fig.2 Meta-analysis on clinical benefit rate of CRCT with or without endostar for advanced NSCLC

圖3 重組人血管內皮抑素聯合CRCT與CRCT治療NSCLC 1年生存率比較的Meta-分析Fig.3 Meta-analysis on one year survival rate of CRCT with or without endostar for advanced NSCLC

圖4 重組人血管內皮抑素聯合CRCT與CRCT治療NSCLC生活質量改善率比較的Meta-分析Fig.4 Meta-analysis on improvement of life quality of CRCT with or without endostar for advanced NSCLC
2.3.5 白細胞減少發生率 納入的5個RCT[5-9]均報道了白細胞減少發生率,各研究間具有同質性(P= 0.71,I2=0%),故采用固定效應模型進行Meta分析。結果顯示兩組差異無統計學意義(P=0.43)[OR= 1.25,95%CI(0.72,2.17)](圖5)。
2.3.6 放射性食管炎發生率 納入的4個RCT[5-8]報道了Ⅲ、Ⅳ級放射性食管炎發生率,各研究間具有同質性(P=0.71,I2=0%),故采用固定效應模型進行Meta分析。結果顯示兩組差異無統計學意義(P=0.77) [OR=1.16,95%CI(0.42,3.21)](圖6)。

圖5 重組人血管內皮抑素聯合CRCT與CRCT治療NSCLC白細胞減少發生率比較的Meta-分析Fig.5 Meta-analysis on leukopenia of CRCT with or without endostar for advanced NSCLC
2.3.7 放射性肺炎發生率 納入的3個RCT[6-8]報道了Ⅲ、Ⅳ級放射性肺炎發生率,各研究間具有同質性(P=0.85,I2=0%),故采用固定效應模型進行Meta分析。結果顯示兩組差異無統計學意義(P=0.37) [OR=2.47,95%CI(0.34,17.68)](圖7)。
3 討論
肺癌是我國發病率和死亡率占首位的惡性腫瘤,其中80%的患者為非小細胞肺癌,其治療效果尚不令人滿意,尤其以晚期NSCLC為甚。CRCT是目前不能手術切除NSCLC的標準治療模式,但5年生存率仍然僅約20%[10]。如何提高放化療的療效已經成為目前研究的熱點。
實體瘤的持續生長、血行轉移和蔓延都依賴于血管生成。抑制血管生成是控制腫瘤生長的一種重要靶向治療方法[11]。抗血管生成藥重組人血管內皮抑素通過特異性地作用于新生血管的內皮細胞并抑制內皮細胞遷移,同時誘導其凋亡,從而發揮抗血管生成作用[12]。HUANG等[13]發現重組人血管內皮抑素下調血管內皮生長因子(vascular endothelial growth factor, VEGF)的表達,使Lewis肺癌血管正常化,從而提高紫杉醇的化療敏感性。重組人血管內皮抑素與放療聯合可以通過抑制缺氧誘導因子-1α(hypoxia-inducible factor-1α,HIF-1α)、VEGF的表達來抑制肺腺癌A549細胞的生長[14-15]。PENG等[16]通過動物實驗發現重組人血管內皮抑素使腫瘤血管正常化,改善低氧,從而增加鼻咽癌對放療的敏感性。以上研究為重組人血管內皮抑素聯合放化療的臨床研究提供理論依據。關于重組人血管內皮抑素聯合CRCT對晚期NSCLC的療效和安全性評價目前已有較多報道,筆者采用循證醫學的方法,通過數據合并及相關統計學計算,為評價者提供更可信的結論。
本文Meta分析結果顯示,重組人血管內皮抑素聯合CRCT治療晚期NSCLC可提高治療有效率(OR= 2.62),主要機制是重組人血管內皮抑素可以使腫瘤雜亂無章的血管出現短暫的“正常化”[17],這個短暫時期腫瘤重新獲得正常的氧供,增加化療藥物到達腫瘤的濃度;同時改善腫瘤低氧,提高腫瘤組織放療敏感性。但是重組人血管內皮抑素聯合CRCT在臨床受益率、1年生存率、生活質量、毒副反應方面的改善效果與CRCT相當,差異無統計學意義。本研究中所觀察到的毒副反應與其他單用CRCT治療局部晚期NSCLC的報道相似,重組人血管內皮抑素的使用并未增加CRCT的不良反應[18]。
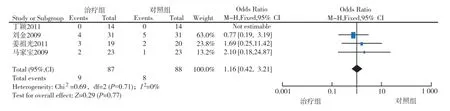
圖6 重組人血管內皮抑素聯合CRCT與CRCT治療NSCLC放射性食管炎發生率比較的Meta-分析Fig.6 Meta-analysis on radioactive esophagitis of CRCT with or without endostar for advanced NSCLC
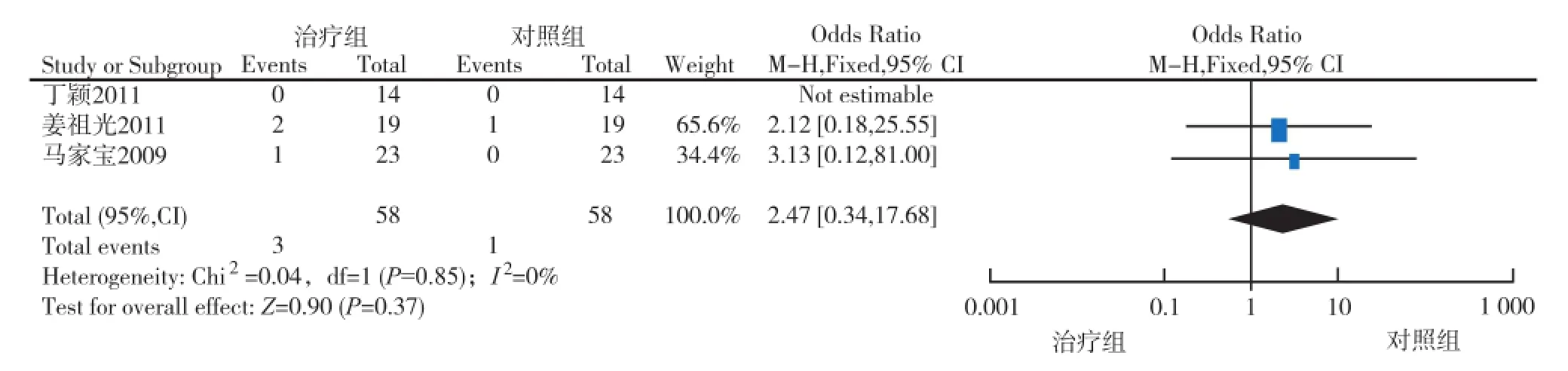
圖7 重組人血管內皮抑素聯合CRCT與CRCT治療NSCLC放射性肺炎發生率比較的Meta-分析Fig.7 Meta-analysis on radiation pneumonitis of CRCT with or without endostar for advanced NSCLC
綜上所述,本研究結果顯示,重組人血管內皮抑素與CRCT聯合治療晚期NSCLC的有效性較CRCT高,其安全性相當。鑒于Meta分析為二次研究,納入研究較少,樣本量小,質量不高,并且評價時間不同,可能存在偏倚等局限性,在今后的臨床應用中尚需進行更高質量、更大樣本的臨床研究進一步驗證重組人血管內皮抑素聯合CRCT治療晚期NSCLC的有效性和安全性。
[1] 王金萬,孫燕,劉永煜,等.重組人血管內皮抑素聯合NP方案治療晚期NSCLC隨機、雙盲、對照、多中心Ⅲ期臨床研究[J].中國肺癌雜志,2005,8(4):283-290.
[2] 周琦超,包勇,余忠華,等.不可手術切除Ⅲ期非小細胞肺癌重組人血管內皮抑素聯合同期放化療多中心Ⅰ+Ⅱ期臨床試驗[J].中華放射腫瘤學雜志,2012,21(6): 500-503.
[3] 王斌,張麗萍,張軍,等.重組人血管內皮抑制素聯合放化療治療肺癌臨床研究[J].現代腫瘤醫學,2012,20 (6):1192-1194.
[4] 隋黎麗,王欣,管樂靜,等.重組人血管內皮抑素聯合放化療同步治療非小細胞肺癌的臨床觀察[J].中國肺癌雜志,2009,12(6):560-561.
[5] 劉金,黃京子,全吉鐘,等.放化療同步聯合YH-16治療局部晚期NSCLC的臨床研究[J].中國醫藥導報,2009, 6(16):253-254.
[6] 馬家寶,楊家林,李志琳,等.重組人血管內皮抑素聯合同步放化療治療局部晚期非小細胞肺癌的隨機對照臨床研究[J].實用臨床醫藥雜志,2009,13(21):20-24.
[7] 姜祖光,李慎柯,岳文彬,等.重組人血管內皮抑素聯合同步放化療治療老年晚期非小細胞肺癌的臨床觀察[J].中國實用醫刊,2011,38(18):55-58.
[8] 丁穎,王希成,楊帆,等.重組人血管內皮抑素聯合同步放化治療局部晚期非小細胞肺癌[J].廣東藥學院學報, 2011,27(2):202-206.
[9] 陳淅涓,王建華,劉英強,等.重組人血管內皮抑素聯合同步放化療治療局部晚期非小細胞肺癌[J].河南醫學研究,2013,22(3):337-339.
[10] CURRAN W J,PAULUS R,LANGER C J,et al.Sequential vs.concurrent chemoradiation for stage III non-small cell lung cancer:randomized phase III trial RTOG 9410[J].J Natl Cancer Inst,2011,103(19):1452-1460.
[11] FOLKMAN J.Angiogenesis:an organizing principle for drug discovery?[J].Nat Rev Drug Discov,2007,6(4):273-286.
[12] FOLKMAN J.Antiangiogenesis in cancer therapy——endostatin and its mechanisms of action[J].Exp Cell Res, 2006,312(5):594-607.
[13] HUANG G,CHEN L.Recombinant human endostatin improves anti-tumor efficacy of paclitaxel by normalizing tumor vasculature in Lewis lung carcinoma[J].J Cancer Res Clin Oncol,2010,136(8):1201-1211.
[14] ZHANG L,GE W,HU K,et al.Endostar down-regulates HIF-1andVEGFexpressionandenhancesthe radioresponse to human lung adenocarcinoma cancer cells [J].Mol Biol Rep,2012,39(1):89-95.
[15] 胡科,戈偉,張彥彥,等.Endostar聯合放療對A549細胞凋亡及HIF-1、VEGF表達的影響[J].武漢大學學報:醫學版,2010,31(2):182-185,后插1.
[16] PENG F,XU Z,WANG J,et al.Recombinant human endostatin normalizes tumor vasculature and enhances radiation response in xenografted human nasopharyngeal carcinoma models[EB/OL].[2012-04-09].http://www.plosone.org/articl.
[17] JAIN R K.Normalization of tumor vasculature:an emerging concept in antiangiogenic therapy[J].Science,2005,307 (5706):58-62.
[18] NAKAMURA M,KOIZUMI T,HAYASAKA M.et al.Cisplatinandweeklydocetaxelwithconcurrentthoracic radiotherapy for locally advanced stage III non-small-cell lung cancer[J].Cancer Chemother Pharmacol,2009,63 (6):1091-1096.
DOI 10.3870/yydb.2014.09.036
Effectiveness and Safety of Recombinant Human Endostatin Combined with Concurrent Chemoradiotherapy for Advanced Non-small Cell Lung Cancer:a Meta-Analysis
XU Hui-lin,GE Wei,CAO De-dong,MING Ping-po,ZHENG Yong-fa,SONG Jing,LUO Wei
(Department of Oncology,Renmin Hospital of Wuhan University,Wuhan 430060,China)
Objective To evaluate the effectiveness and safety of recombinant human endostatin combined with concurrent chemoradiotherapy versus concurrent chemoradiotherapy for advanced non small cell lung cancer(NSCLC).MethodsElectronic databases including the Cochrane library,PubMed,the Chinese biomedical literature database,China national knowledge internet(,EMbase,VIP andWanfangdatabase system were searched,until August,2013.The inclusion criteria was efficacy and safety studies of randomized controlled clinical studies in which recombinant human endostatin combined with concurrent chemoradiotherapy was compared with concurrent chemoradiotherapy alone for patients with advanced NSCLC.Cochrane handbook 5.1.0 was applied in evaluating the quality of included trials and RevMan 5.1.0 software was used for data analysis.ResultsFive studies including 217 cases of advanced NSCLC were included.The results of the meta-analysis exhibited that compared with concurrent chemoradiotherapy alone,recombinant human endostatin combined with concurrent chemoradiotherapy could increase effective rate[OR=2.62,95%CI(1.41,4.86),P=0.002].But there were no significant differences in clinical benefit rate[OR=2.08,95%CI(0.92,4.73),P=0.08],one year survival rate[OR=1.18,95%CI(0.53,2.66),P=0.68], improvement in quality of life[OR=1.57,95%CI(0.40,6.07),P=0.52],rate of leucopenia[OR=1.25,95%CI(0.72,2.17),P=0.43],radioactive esophagitis[OR=1.16,95%CI(0.42,3.21),P=0.77]and radiation pneumonitis[OR=2.47,95%CI (0.34,17.68),P=0.37].ConclusionCompared with concurrent chemoradiotherapy alone,recombinant human endostatin combined with concurrent chemoradiotherapy may be more effective for advanced NSCLC,whereas improvement of life quality and toxicities are similar.For the quality restriction and possible publication bias of the included studies,more high quality randomizedcontrolled trials are required to further verify this conclusion.
Recombinant human endostatin;Lung neoplasms;Concurrent chemoradiotherapy;Meta-analysis
R979.1;R969.3
B
1004-0781(2014)09-1237-06
2013-10-03
2014-01-05
徐慧琳(1986-),女,湖北襄陽人,住院醫師,碩士,主要從事腫瘤分子靶向治療的研究。電話:(0) 15071048798,E-mail:370290075@qq.com。
戈偉(1960-),男,湖北武漢人,主任醫師,博士,碩士生導師,研究方向:腫瘤的分子靶向治療。電話:(0) 15327113399,E-mail:gewei514@126.com。

