α,β-不飽和酰胺TRPV1抑制劑的Topomer CoMFA模型
戴 康,方 華,溫 超,徐 暉
(中南民族大學 藥學院,武漢 430074)
瞬時感受器電位香草酸1(TRPV1)是一個新的鎮痛藥物分子靶點,主要存在于背根神經節和三叉神經節的較小直徑細胞的細胞膜或胞內細胞器膜上,是一種非選擇性陽離子通道.克隆的TRPV1可被多種傷害性刺激激活,故TRPV1被認為是一種多信號探測和感受多種疼痛刺激的整合器[1].主要包括3個方面:芳香草醛化合物、傷害性熱刺激和氫離子[2, 3].
治療疼痛多應用TRPV1激動劑,激活TRPV1通道后,引起Ca2+內流,導致初級感覺神經元興奮[4],長期使用能導致神經元脫敏,阻斷痛覺的傳遞[5-7].但這種鎮痛機制有很多副作用,如辣椒素與TRPV1結合后,神經細胞內的Ca2+大量內流,導致細胞膜破壞,使線粒體膜通透性發生改變,使神經細胞凋亡[8],故TRPV1阻斷劑近年來受到重視.經典的TRPV1阻斷劑包括:Capsazepine、RTX和釕紅.小分子TRPV1阻斷劑有硫脲類、尿素類、肉桂酰胺類、氨基化合物、甘氨酰胺類、鹵化辣椒堿和吡啶基哌嗪類[9].但這些TRPV1阻斷劑均存在著一個共同的問題,很多候選藥物都會引發高熱反應,甚至影響記憶等大腦機能.故尋找一種無毒高效的新的TRPV1抑制劑顯得尤為重要.
本文利用Topomer CoMFA設計的α,β-不飽和酰胺TRPV1抑制劑有效解決了這個問題.利用第二代CoMFA 方法Topomer CoMFA來研究α,β-不飽和酰胺TRPV1抑制劑的3D-QSAR模型.與傳統的CoMFA方法相比,Topomer CoMFA不需要手動分子疊合,每個模型中分子疊合都是客觀的,增強了模型之間的可比性,提高了CoMFA的重現性,并大大提高了計算效率[10].
1 數據描述
本文研究了42個α,β-不飽和酰胺類TRPV1抑制劑,其中34個選為訓練集,8個選為測試集(帶*的化合物).其中用訓練集建立3D-QSAR模型,測試集測試模型的外部穩定性.α,β-不飽和酰胺類TRPV1抑制劑的活性數據和化合物的結構見表1.
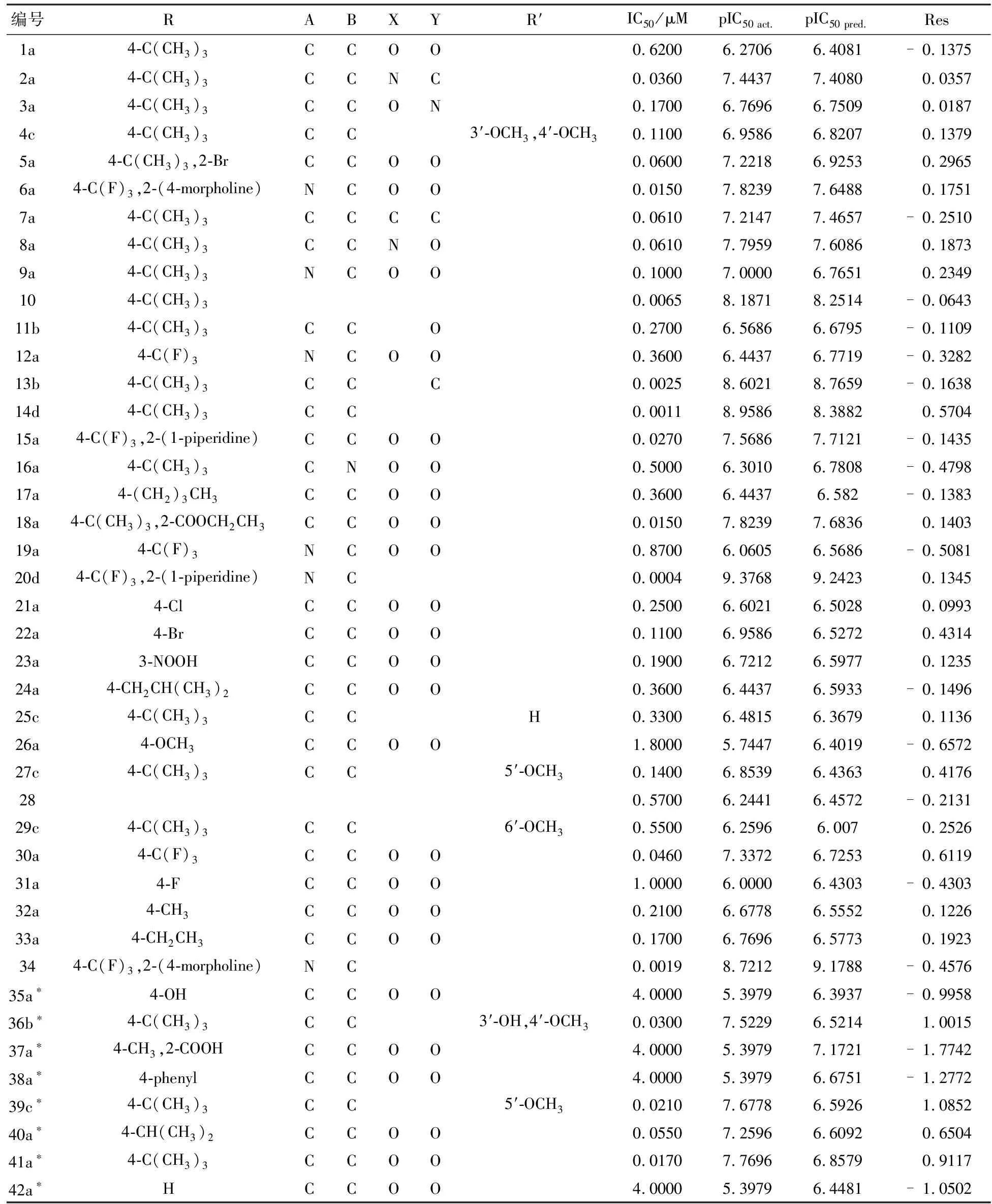
表1 化合物的結構和生物活性數據
*測試組
2 模型建立
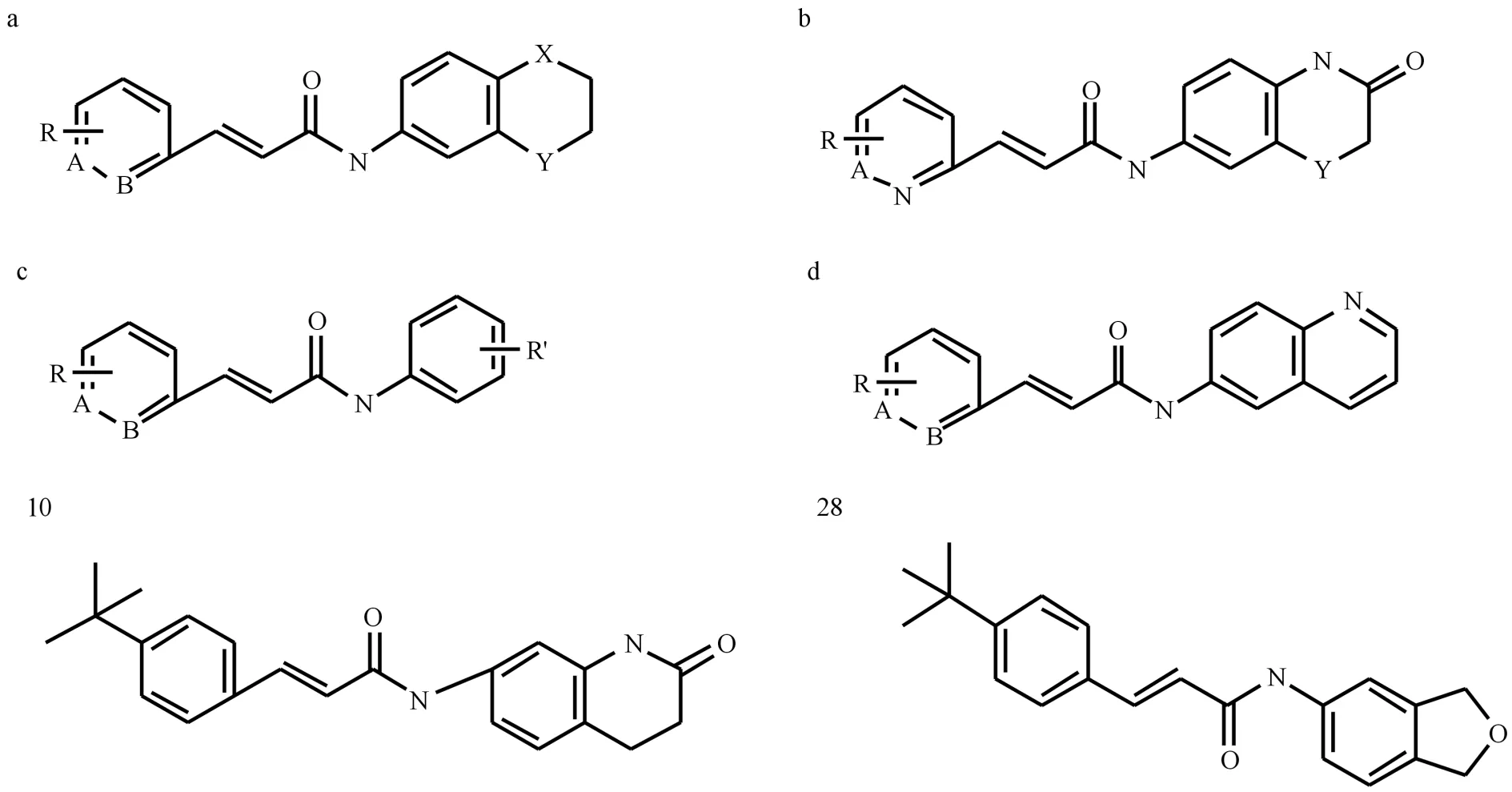
本文利用SYBYL-X軟件對對34個訓練集化合物進行切割,隨機選擇1個化合物結構作為模板,切割酰胺鍵,生成R1基團和R2基團(見圖1).Sybyl軟件會自動識別并切割剩下的化合物并計算R1基團和R2基團周圍的分子場,以立體場和靜電場性質為自變量,化合物活性為因變量,采用最小偏二乘法建立化合物立體場特征和活性的關系生成3D-QSAR模型.其中交叉驗證相關系數q2為0.702,非交叉驗證相關系數r2為0.881,表明該模型有較好的擬合與內部預測能力.
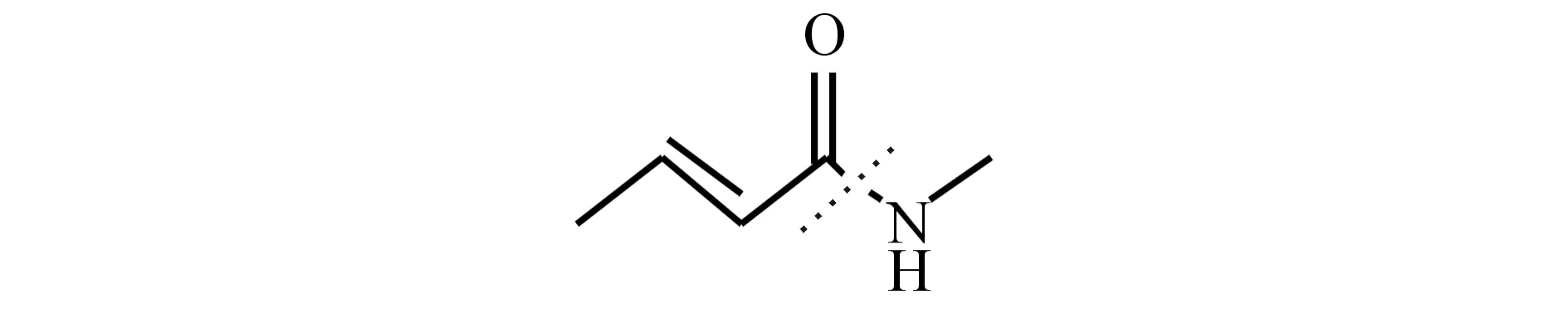
圖1 分子的切割方式Fig.1 The cuting way of the molecular
3 結果與討論
為測試該模型的穩定性和外部預測能力,對8個測試集化合物進行了活性預測.其結構活性數據見表1,線性相關回歸圖見圖2,由圖2和表1可見測試集圓點分布在回歸線兩側,說明該模型有較好的外部預測能力.
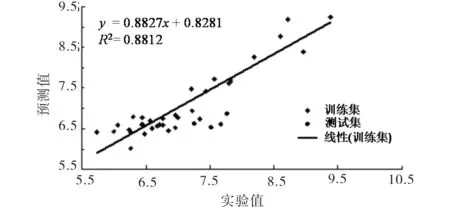
圖2 42個化后物的實驗值和預測值的散點圖Fig.2 The scatter plots of the experimental value and predicted value of 42 chemical compounds
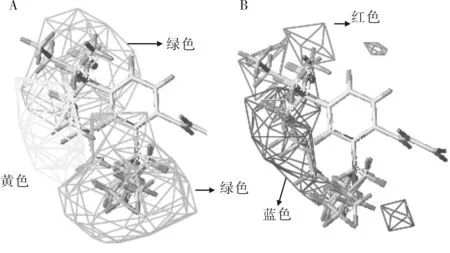
圖3 R1的立體場和靜電場對化合物活性的影響Fig.3 The effect of steric and electrostatic field of R1 on the activity of the compound

圖4 R2的立體場和靜電場對活性的影響Fig.4 The effect of steric and electrostatic field of R2 on the activity of the compound
圖3和圖4分別是R1和R2的立體場和靜電場對活性的影響,左邊綠色部分表示增大取代基的體積有利于增加活性,黃色部分表示減小取代基體積有利于增加活性;右邊藍色區域有正電性基團活性會增加,紅色區域有負電性基團活性會增加.
圖3A中R1基團的苯環的2、4位處于綠色區域,3號位處于黃色區域,那么在2、4號位引入大體積的取代基有利于增加活性,而在3號位減小取代基體積有利于提高活性.表1中活性5a>1a,22a>21a,1a>42a均能驗證這一點,5a中因為比1a在2位多了一個溴取代而活性增強;22a的溴取代比21a的氯取代基體積稍大,因而活性也略強;1a中叔丁基4位有取代而42a中沒取代因而活性增強.在圖3B中,2′號到4′號位之間的區域處于藍色區域,應該引入正電性取代基,而在2′號、4′號區域部分處于紅色區域,應該引入負電性取代基.表1中活性15a>16a,36b>35a,15a>12a均可以驗證這一點.
圖4C中R2基團的苯環2、4號位上并的環上的取代基處于綠色區域,增加取代基的體積有利于增加活性,而在垂直于該環的平面的取代基在黃色區域,縮小取代基的體積有利于增加活性,表1中活性4c>1a,36b>1a均能很好地證明這一點;圖4D中該環靠近酰胺鍵端兩處處于紅色區域,引入負電性取代基有利于增加活性,遠離酰胺鍵端處于藍色區域,引入正電性取代基有利于增加活性,表1中活性8a>2a,因8a結構中苯并六元環上靠近酰胺端是氧取代,引入了電負性基團,而活性10遠遠大于11b,都與這點相符.預測結果表明整體而言R2基團的貢獻大于R1基團.
綜上所述,在R1基團的苯環4號位引入三氟化碳基團與圖中連接苯環處為藍色區域,而該處的3個取代基處于紅色區域相符,能夠增強藥物的活性,在R2基團的苯并六元環上靠近酰胺鍵端引入酰胺鍵有利于增強藥物的活性.
參 考 文 獻
[1] Caterina M J, Schumacher M A, Tominaga M, et al. The capsaicin receptor: a heat-activated ion channel in the pain pathway[J]. Nature, 1997, 389(6653): 816-824.
[2] Liu D L, Wang W T, Xing J L, et al. Research progress in transient receptor potential vanilloid 1 of sensory nervous system[J]. Neurosci Bull, 2009, 25(4): 221-227.
[3] 陳 敏, 張陸勇, 嚴 明. 辣椒素受體研究進展[J].中國臨床藥理學與治療學,2006,11(2): 126-130.
[4] 劉悅雁, 解 敏, 黃 擎, 等.辣椒素通過鈣信號抑制感覺神經元的電壓門控性鈣離子通道[J].安徽醫科大學學報, 2009, 44(1): 1-5.
[5] Wachtel R E. Capsaicin[J]. Reg Anesth Pain Med, 1999, 24(4): 361-363.
[6] 郭 峰, 姜曉鐘. 辣椒素的作用機制及其鎮痛應用[J]. 第二軍醫大學學報, 2002, 23(1): 96-98.
[7] 朱潔平, 劉悅雁. 辣椒素與疼痛研究綜述[J].衛生職業教育,2010, 28(16): 155-159.
[8] Olah Z, Szabo T,Karai L,et al. Ligand-induced dynamic membrane changes and cell deletion conferred by vanilloid receptor 1[J]. J Biol Chem,2001,276(14): 11021-11030.
[9] 王 樂,曹 宇. TRPV1 阻斷劑的研究進展[J]. 國際病理科學與臨床雜志200828(3): 220-224.
[10] Cramer R D. Topomer CoMFA: a design methodology for rapid lead optimization[J]. J Med Chem,2003,46(3): 374-388.

