低分子肝素聯合依那普利對單側輸尿管梗阻大鼠腎組織結締組織生長因子表達的影響
王琳娜 李強翔 楊山華
(河南省中醫院腎內科,河南 鄭州 450000)
腎小管間質損害是影響腎臟疾病進展和預后的重要因素,結締組織生長因子(CTGF)作為轉化生長因子β(TGF-β)的下游介質,有促進細胞增生和細胞外基質(ECM)合成的作用,細胞外基質的主要成分包括Ⅰ,Ⅲ,Ⅳ型膠原和纖維黏連蛋白(FN)。單側輸尿管梗阻(UUO)模型是以進行性小管間質纖維化為特征的實驗性腎病模型。血管緊張素轉換酶抑制劑(ACEI)可延緩腎間質纖維化的發生發展,對此國內外有不同的報道〔1,2〕。低分子量肝素有抗凝、抗血栓和改善微循環的作用,并能減輕蛋白尿和延緩腎小球硬化。本實驗通過低分子肝素和依那普利的聯合治療觀察兩者聯合使用對腎間質纖維化大鼠腎組織CTGF表達和Ⅰ型膠原mRNA表達的影響,探討兩者聯用抗腎間質纖維化機制。
1 材料和方法
1.1實驗動物及分組 清潔級雄性SD大鼠40只,體質量180~220 g,由鄭州大學實驗動物學部提供。分成UUO模型組、依那普利組、低分子肝素組、低分子肝素+依那普利聯合組各8只和假手術組(8只)。UUO模型的制備:10%水合氯醛(3 ml/kg)腹腔注射麻醉后,無菌手術操作打開腹腔,分離左輸尿管,用4-0號線雙重結扎并離斷輸尿管,分層縫合關閉腹腔;假手術組只分離輸尿管后即關閉腹腔。每組大鼠于UUO后第14天處死,留取梗阻側腎組織備用。依那普利組自術前24 h開始給予依那普利10 mg·kg-1·d-1灌胃,直至造模后第14天;低分子肝素組自術前24 h開始給以低分子肝素鈣410 U/kg皮下注射,每天2次直至造模后第14天;聯合組給予上述兩種治療聯用;UUO模型組和假手術組只給同量生理鹽水灌胃和生理鹽水皮下注射。
1.2主要材料 馬來酸依那普利購自江蘇揚子江制藥股份有限公司,低分子肝素鈣購自葛蘭素史克有限公司組織,總RNA提取試劑盒(RNeasyMini Kit試劑盒)購自美國Qiangen公司,逆轉錄試劑盒購自美國Promega公司,real-time PCR試劑盒(q-PCR Mixture)購自日本TaKaRa公司,熒光探針實時定量PCR儀(ABI 7900HT)購自美國Applied Biosystems公司,real-time PCR所用引物由上海生物工程有限公司合成,羊抗CTGF多克隆抗體購自美國Abcam公司,鼠抗β-actin單克隆抗體購自美國Sigma公司,二抗均購自美國Sigma公司,增強化學發光(ECL)顯色液購自美國Pierce公司。
1.3觀察指標及檢測方法
1.3.1腎臟組織HE染色 腎組織以4%多聚甲醛固定,常規包埋、切片,做HE染色觀察腎組織病理變化,每張標本低倍鏡下單盲依序觀察左上、右上、左下、右下、中間5個腎小管間質視野,依據腎小管上皮細胞空泡變性、腎小管擴張、腎小管萎縮、紅細胞管型、蛋白管型、間質水腫、間質纖維化、間質炎性細胞浸潤等8項指標來觀察腎間質病理改變并進行腎小管間質損傷指數評分〔3〕。
1.3.2腎臟組織Masson染色 腎組織以4%多聚甲醛固定,常規包埋、切片,做Masson染色觀察腎組織病理變化膠原的沉積,每例切片低倍鏡下觀察10個互不重疊腎小管間質視野,計算每例切片腎間質Masson染色陽性面積占整個視野百分比,以對腎間質膠原含量進行半定量分析〔4〕。計分如下:0分:無著色;1分:輕度<10%;2分:中度:11%~25%;3分:重度:26%~50%;4分:極重度:>50%。
1.3.3CTGF和Ⅰ型膠原的Real-time PCR檢測
1.3.3.1組織總RNA的提取 依照Werbrock等〔5〕報道的方法,用RNeasyMini Kit試劑盒提取組織總RNA,抽提的總RNA用紫外分光光度計測OD值,比值在1.9~2.0之間,取3 μl RNA用1%瓊脂糖凝膠電泳,可見5 S,18 S,28 S 3條清晰的RNA帶,提示RNA無污染和降解。
1.3.3.2cDNA的合成 按O’Neill等〔6〕報道的方法,用逆轉錄試劑盒合成cDNA,再以此cDNA為模板進行Real-time PCR反應操作。Real-time PCR的引物序列如下:β-actin 上游5′-GGCCAACCGTGAAAAGATGA-3′,下游5′-GACCAGAGGCATACAGGGACAA-3′;CTGF上游5′-CCTGTGAAGCTGACCTAGAGGAAA-3′,下游5′-ACA-GAACTTAGCCCGGTAGGTCTT-3′;Ⅰ型膠原上游5′-TCAGGGGCGAAGGCAACAGT-3′,下游5′- TTGGGATGGAGGGAGTTTACACGA-3′。
1.3.3.3Real-time PCR檢測 在ABI 7900型熒光定量PCR儀上進行擴增,96孔板加樣,設計復孔和標準曲線,用Se-quence Detection System軟件分析各檢測樣本的Ct值(達到一定熒光閾值的循環數),計算2-ΔΔCt評價CTGF在腎組織中的表達水平。
1.3.4腎組織CTGF蛋白的Western印法檢測
1.3.4.1腎皮質總蛋白質的提取 取組織塊100 mg加入組織總蛋白提取液1 ml勻漿,冰上裂解30 min,4 ℃ 12 000 r/min離心15 min,取上清,按Bio-rad蛋白定量試劑盒方法進行蛋白定量,取80 μl上清加5×變性緩沖液20 μl混勻,100 ℃下變性10 min。
1.3.4.2免疫印跡檢測 灌制10%的分離膠和4%的堆積膠,取總蛋白100 μg行上樣電泳,電泳結束后260 mA電轉印90 min至PVDF膜。封閉液(5%牛奶)搖床上封閉2 h,加入羊抗CTGF多克隆抗體(1∶200),4℃搖床過夜。洗膜后再加相應的二抗,室溫孵育1 h,加ECL液后顯影、定影,以β-actin為內參照。將膠片掃描后,采用Quantity One軟件分析各條帶灰度值,將各目的條帶灰度值除以同一標本內參照β-actin條帶灰度值得到一比值,將該比值除以同一膠片上假手術組的比值作為該目的蛋白表達量的半定量結果。
1.4統計學處理 采用SPSS12.0軟件進行單因素方差分析。
2 結 果
2.1HE染色 假手術組腎臟未見明顯病變,模型組UUO術后第14天,大體觀腎皮質變薄,鏡下見腎小管上皮細胞空泡變性及炎性細胞浸潤,部分小管萎縮,遠曲小管、集合管呈囊狀擴張,部分近端小管保存尚好,間質可見成纖維細胞增殖和纖維化。低分子肝素治療組術后第14天,炎性細胞浸潤較模型組減輕,但腎小管上皮細胞變性、腎小管擴張及萎縮和間質纖維化程度與模型組相比無明顯差別;依那普利組術后第14天,炎性細胞浸潤明顯減輕,腎小管上皮細胞空泡變性、腎小管擴張及萎縮及間質纖維化程度有所減輕;聯合組術后第14天,炎性細胞浸潤較模型組明顯減輕,腎小管上皮細胞變性、腎小管擴張及萎縮和間質纖維化程度明顯減輕,與模型組相比均有明顯好轉。對HE染色進行腎間質損傷指數評分。見表1。
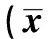
表1 各組大鼠腎間質損傷指數評分±s,n=8)
2.2梗阻側腎組織膠原相對面積 假手術組腎小球基底膜、腎小管基底膜、系膜基質染成綠色,腎間質無明顯膠原纖維;模型組腎間質可見大量染成綠色的膠原纖維;低分子肝素組、依那普利組和聯合組腎間質可見少量染成綠色的膠原纖維。對Masson染色進行腎間質膠原相對面積評分。見表1。
2.3Real-time PCR結果 UUO術后14 d,腎組織CTGF和Ⅰ型膠原mRNA的表達較模型組明顯增多。經低分子肝素和依那普利治療后,腎組織CTGF和Ⅰ型膠原mRNA的表達均較模型組有所減少(P<0.05)。聯合組CTGF和Ⅰ型膠原mRNA的表達與模型組比較有明顯降低(P<0.05);與低分子肝素組和依那普利組比較,聯合組CTGF和Ⅰ型膠原mRNA的表達有明顯降低(P<0.05);低分子肝素組和依那普利單獨治療組比較差異無統計學意義(P>0.05),見表2
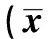
表2 各組大鼠腎組織CTGF和Ⅰ型膠原 mRNA的表達±s,n=8)
2.4Western印跡法結果 與假手術組大鼠相比,模型組UUO術后14 d CTGF蛋白表達增加,低分子肝素和依那普利組后,腎組織CTGF蛋白的表達均較模型組減少(P<0.05);聯合組CTGF的表達與模型組比較有明顯降低(P<0.05);與低分子肝素組和依那普利組比較,聯合組CTGF的表達有明顯降低(P<0.05);低分子肝素組和依那普利單獨治療組比較差異無統計學意義(P>0.05)。見圖1。

1假手術組;2模型組;3低分子肝素組;4依那普利組;5聯合組
3 討 論
CFGF是新近發現的一種細胞因子,廣泛存在于人類多種組織器官中,尤以腎臟中含量最高。CTGF因種類不同,表現不同的生物學效應,在腎臟中,CTGF對腎臟多種固有細胞,包括成纖維細胞、系膜細胞和腎小管上皮細胞有促增殖和促ECM合成的作用〔7〕。CTGF作為TGF-β的下游介質,在TGF-β的誘導下,由成纖維細胞分泌,介導TGF-β發揮促有絲分裂、細胞趨化、誘導黏附、細胞增殖和ECM合成等作用,而對TGF-β的抗炎、抗細胞分化作用無影響〔8〕。低分子肝素有抗凝、抗血栓和改善微循環的作用,并能減輕蛋白尿和延緩腎小球硬化〔9,10〕。
本研究前期試驗發現依那普利對腎間質纖維化有防治作用,依那普利的抗纖維化作用在UUO術后14 d內效果好,這一作用機制與依那普利拮抗UUO早期血流動力學改變和腎素-血管緊張素-醛固酮系統(RAAS)激活有關,進而抑制TGF-β1 / Smad通路的活化及腎小管上皮細胞的轉分化有關。
本實驗發現,LMWH和依那普利聯合應用能明顯減輕腎間質膠原沉積程度,減少損傷腎組織GTGF和Ⅰ型膠原mRNA的表達,聯合用藥的治療作用優于低分子肝素和依那普利的單獨應用,抗纖維化作用可能與抑制腎間質GTGF的表達,從而抑制膠原成分的合成有關。低分子肝素和依那普利組間比較結果顯示,依那普利抗纖維化作用稍優于低分子肝素,這一作用可能與依那普利作為RAAS系統阻斷劑的降壓作用相關。本試驗僅觀察至UUO術后14 d,隨著纖維化進程的延長,RAAS系統激活在腎間質纖維化的致病過程中所起的作用逐漸退居其次,依那普利抗纖維化作用不再突出。低分子肝素和依那普利的聯合用藥能通過多個靶點起到抗纖維化作用,隨著纖維化進程的延長,抗纖維化作用可能逐漸顯著。抗纖維化研究的觀察時間點及低分子肝素安全的劑量范圍有待于進一步的研究證實。
4 參考文獻
1Beharrie A,Franc-Guimond J,Rodriguez MM,etal.A functional immature model of chronic partial ureteral obstruction〔J〕.Kidney Int,Apr;65(4):1155-61.
2陳 東,黃海長,喻 陸.腎間質行維死組織中組織型轉谷氨酰胺酶和結締組織生長因子共表達〔J〕.北京大學學報,2005;37(2):143-6.
3Radford G,Donadio JV,Bergstralh EJ,etal.Predicting renal outcoming in IgA nephropathy〔J〕.J Am Soc Nephrol,1997;8(2):199-207.
4Wu MJ,Wen MC,Chiu YT,etal.Rapamycin attenuates unilateral ureteral obstruction-induced renal fibrosis〔J〕.Kidney Int,2006;69(11) :2029-36.
5Werbrock H,Bottelboom N,Uyttendaele M,etal.Quantification of gene expression of Listeria monocytogenes by real time reverse transcription PCR:optimization,evaluation and pitfalls〔J〕.J Microbiol Methods,2007;9(2):306-14.
6O’Neill HJ,McCaughey C,Coyle PV,etal.Clinical utility of nested multiplex RT-PCR for group F adenovirus,rotavirus and norwalk-like viruses in acute viral gastroenteritis in children and adults〔J〕.J Clin Virol,2002;25(3):335-8.
7Phanish MK,Winn SK,Dockrell ME.Connective tissue growth factor-(CTGF,CCN2)--a marker,mediator and therapeutic target for renal fibrosis〔J〕.Nephro Exp Nephrol,2010;114(3):e83-92.
8Takeuchi H,Kubota S,Murakashi E,etal.Effect of transforming growth factor-beta1 on expression of the connective tissue growth factor(CCN2/CTGF) gene in normal human gingival fibroblasts and periodontal ligament cells〔J〕.J Periodontal Res,2009;44(2):161-9.
9Deepa PR,Varalakshmi P.Influence of a low-molecular-weight heparin derivative on the nitric oxide levels and apoptotic DNA damage in adriamycin-induced cardiac and renal toxicity〔J〕.Toxicology,2006;217(2-3):176-83.
10Benchetrit S,Golan E,Podjarny E,etal.Low molecular weight heparin reduces proteinuria and modulates glomerular TNF-alpha production in the early phase of adriamycin nephropathy〔J〕.Nephron,2001;87(2):155-60.

