氨基酸離子液體促進的醇胺水溶液捕集CO2的研究進展
付 東,張 盼,杜磊霞
(華北電力大學 環境科學與工程學院,河北 保定 071003)
0 引言
工業生產及燃煤鍋爐大量排放的CO2已嚴重影響了環境保護和國民經濟的可持續發展。為了應對CO2的減排壓力,發展技術上可行、經濟上可承受的煙氣中CO2減排方法,已引起廣泛關注。在眾多的CO2捕集方法中,醇胺吸收法[1~6]具有技術成熟、吸收量大、操作成本較低等優點,適宜大規模商業化應用,特別是在天然氣和煉廠氣CO2分離方面,醇胺法處于主導地位。隨著華能北京熱電廠和華能上海石洞口第二電廠CO2捕集示范工程的展開,在火電廠CO2減排領域,醇胺吸收法也將占據舉足輕重的地位。
因醇胺水溶液吸收CO2后易腐蝕設備,CO2捕集過程需嚴格控制水溶液中醇胺的質量分率。如以乙醇胺 (Monoethanolamine,MEA)水溶液為吸收劑時,MEA的質量分率不超過30%,以避免嚴重的腐蝕。但醇胺質量分率較低時,溶液中大量的水分導致吸收容量較小、高溫再生時加熱蒸汽消耗量巨大。為了降低操作成本,常使用復配醇胺水溶液作為吸收劑,即以吸收能力強且腐蝕性較小的 N-甲基二乙醇胺 (N-methyldiethanolamine,MDEA)或2-氨基-2-甲基-1-丙醇 (2-Amino-2-methyl-1-propanol,AMP)與吸收速率較快的MEA、二乙醇胺 (diethanolamine,DEA)或哌嗪(Piperazine,PZ)復配,以MDEA或AMP為吸收劑主體,以MEA,DEA或PZ為促進劑,溶液中各種醇胺的總質量分率不超過50%。Chakrvarty[2],Kohl和 Nielsen 等[3]實驗驗證了 MDEA-MEA及MDEA-DEA復配醇胺水溶液對CO2的吸收效果;Praxair公司采用MDEA-MEA復配醇胺水溶液作為吸收劑,當MEA質量分率介于10%~20%之間時,既有效地提高了吸收速率和吸收容量,又可降低設備腐蝕,減少加熱蒸汽量。但吸收劑溶液中水分仍在50%左右,富液再生和貧液冷卻過程的能耗仍居高不下,開發新型吸收劑以進一步節能降耗,尚有較大的拓展空間。
1 研究現狀
近年來,離子液體 (Ionic liquids,ILs)吸收CO2的研究已引起廣泛的關注[7~11]。與普通 ILs對CO2的物理吸收過程不同,功能型離子液體(Functionalized ionic liquids,FILs)[12]通過化學反應吸收CO2,具有吸收速率快和吸收容量大的特點;同時由于FILs具有性能穩定、蒸汽壓極低、再生溫度低和無腐蝕等特點,與常用的MEA和MDEA等傳統醇胺吸收劑相比有較強的優勢。目前,CO2在FILs及醇胺-FILs復配溶液中的溶解度和吸收動力學研究已有大量報道[13~23]。研究結果均表明,FILs可顯著改善MEA和MDEA等傳統醇胺水溶液對CO2的吸收效果,并降低再生溫度。
在眾多的FILS中,氨基酸離子液體 (amino acid ionic liquid,AAIL)在常壓下即對CO2具有較大的吸收容量和較高的吸收速率,同時具有原料易得、制備過程穩定、生產成本低和產品毒性低等優點,在工程上具有很好的應用前景。吸收動力學實驗表明[22],在MDEA水溶液中加入少量的AAIL,如四甲基銨甘氨酸 (Tetramethylammonium glycinate,[N1111][Gly]),即可顯著提高 CO2吸收速率。但AAIL粘度較大,且在吸收CO2后粘度進一步上升,導致流動阻力大、吸收過程傳質不充分,難以直接應用于碳捕集工程實踐。以適量的 AAIL與 MEA,MDEA,AMP等醇胺復配[13~23],既可保證適當的體系粘度,又可降低設備腐蝕、提高吸收速率并減少加熱蒸汽量,對目前在運行的醇胺法CO2捕集工藝的改進及新型醇胺法吸收工藝的開發均具有重要的指導意義。
2 發展方向
在CO2醇胺吸收工藝中,粘度是控制氣-液傳質過程的重要參數,對吸收塔的設計及CO2吸收效果均具有重要影響。如在吸收塔中,從塔頂貧液到塔底富液,粘度隨CO2載荷的變化而變化,CO2擴散難易程度也相應變化。目前,醇胺-AAIL水溶液粘度研究已有報道,如Gao等[23]發現,323.15K條件下,質量分率為40%的MDEA水溶液中加入10%[N1111][Gly] 時,水溶液的粘度為 1.81 mPa·s,與常用醇胺水溶液相當,適宜塔內吸收;當[N1111][Gly]質量分率為15%時,水溶液粘度快速上升為5.39 mPa·s。吸收CO2后,由于大量離子的存在,吸收液的粘度將顯著高于水溶液,如Fu等[24~28]的研究表明,當醇胺水溶液吸收CO2后,在接近飽和的CO2載荷條件下,體系粘度比未吸收CO2的水溶液高數倍。因此,醇胺-AAIL吸收劑在碳捕集過程的應用,首先應保證醇胺-AAIL體系具有適當的粘度。
迄今為止,醇胺-AAIL水溶液的粘度與操作溫度、醇胺類型和濃度、AAIL類型和濃度之間的定量關系尚不明晰;吸收CO2后的AAIL-醇胺-水溶液的粘度實驗測定及理論計算均鮮見報道,CO2載荷對吸收液粘度的影響規律尚不明晰。水溶液和吸收液粘度實驗數據及計算模型的缺乏,給吸收塔設計和涉及增強傳質的過程設計帶來諸多困難。亟需結合實驗測定和理論計算,闡明溫度、醇胺種類和濃度、AAIL種類和濃度、以及CO2載荷等諸多因素對體系粘度的影響規律。
適宜煙氣中CO2捕集的AAIL-醇胺吸收劑的遴選,可按圖1所示的路徑進行。即首先通過溶解度和吸收動力學實驗,確定AAIL對CO2的吸收容量及其對醇胺水溶液吸收CO2的促進作用,在此基礎上,結合實驗測定和理論計算,綜合考慮CO2載荷,確定吸收劑中AAIL和醇胺的組成,保證AAIL-醇胺水溶液及其CO2吸收液具有適當的粘度,從而保證整塔范圍內,流動阻力適當、吸收過程傳質充分。
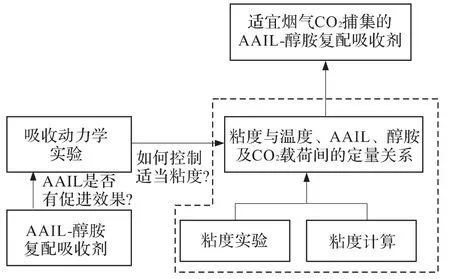
圖1 適宜煙氣中CO2捕集的AAIL-醇胺吸收劑的遴選路徑
3 結論
以AAIL促進傳統醇胺水溶液對CO2的吸收效果,在碳捕集領域具有很好的應用前景,但推廣應用首先需解決體系的高粘問題。本文對AAIL促進醇胺水溶液吸收CO2的動力學及體系粘度的研究進展進行了綜述,并從吸收容量、促進效果和體系粘度等3個方面分析了適宜煙氣中CO2捕集的AAIL-醇胺吸收劑的遴選方法。
[1]Nakicenovic N,John A.CO2Reduction and removal:measures for the next century[J].Energy,1991,16(11):1347-1377.
[2]Chakravarty T,Phukan U K,Weiland R H.Reaction of acid gases with mixtures of amines[J].Chem.Eng.Prog,1985,81(4),32-36.
[3]Kohl A L,Nielsen R.Gas Purification,5th Ed[M].Houston:Gulf Professional Publishing,1997.
[4]Navaza J M,Gomez-Diaz D,Rubia,La Rubia M D.Removal process of CO2using MDEA aqueous solutions in a bubble column reactor[J].Chemical Engineering Journal,2009,146(2):184-188.
[5]Dubois L,Thomas D.Screening of aqueous amine-ased solvents for postcombustion CO2capture by chemical absorption[J].Chemical Engineering & Technology,2012,35,513.
[6]Chowdhury F A,Yamada H,Higashii T,et al.CO2Capture by tertiary amine absorbents:A performance comparison study[J].Industrial& Engineering Chemistry Research,2013,52(24):8323-8331.
[7]Blanchard L A,Hancu D.Beckman E J.,et al.Green processing using ionic liquids and CO2[J].Nature,1999,399(6731):28-29.
[8]Anthony J L,Maginn E J,Brennecke J F.Solubilities and thermodynamieproperties of gases in the ionic liquid 1-n-Butyl-3-methylimi- dazolium hexafluorophosphate[J].Phys.Chem.B,2002,106,7315-7320.
[9]Perez-Salado Kamps A,Tuma D,Xia J,et al.Solubility of CO2in the ionic liquid[bmim][PF6][J].Journal of Chemical & Engineering Data,2003,48(3):746-749.
[10]Shiflett M B,Drew D W,Cantini R A,et al.Carbon dioxide capture using ionic liquid 1-butyl-3-methylimidazolium acetate[J].Energy & Fuels,2010,24(10):5781-5789.
[11]Zhang X,Liu Z,Wang W.Screening of ionic liquids to capture CO2by COSMO-RS and experiments[J].AIChE journal,2008,54(10):2717-2728.
[12]Bates E D,Mayton R D,Ntai I,et al.CO2capture by a task-specific ionic liquid[J].Journal of the American Chemical Society,2002,124(6):926-927.
[13]Gurkan B E,de la Fuente J C,Mindrup E M,et al.E-quimolar CO2absorption by anion-functionalized ionic liquids[J].Journal of the American Chemical Society,2010,132(7):2116-2117.
[14]Baj S,Siewniak A,Chrobok A,et al.Monoethanolamine and ionic liquid aqueous solutions as effective systems for CO2capture[J].Journal of Chemical Technology and Biotechnology,2013,88(7):1220-1227.
[15]Yu H,Wu Y T,Jiang Y Y,et al.Low viscosity amino acid ionic liquids with asymmetric tetraalkylammonium cations for fast absorption of CO2[J].New Journal of Chemistry,2009,33(12):2385-2390.
[16]Zhang J,Zhang S,Dong K,et al.Supported absorption of CO2by tetrabutylphosphonium amino acid ionic liquids[J].Chemistry-a European Journal,2006,12(15):4021-4026.
[17]Galán Sánchez L M,Meindersma G W,De Haan A B.Kinetics of absorption of CO2in amino-functionalized ionic liquids[J].Chemical Engineering Journal,2011,166(3):1104-1115.
[18]Guo H,Zhou Z,Jing G.Kinetics of carbon dioxide absorption into aqueous[Hmim][Gly]solution[J].International Journal of Greenhouse Gas Control,2013,16:197-205.
[19]Zhou Z,Jing G,Zhou L.Characterization and absorption of carbon dioxide into aqueous solution of amino acid ionic liquid[N1111][Gly]and 2-amino-2-methyl-1-propanol[J]. ChemicalEngineering Journal,2012,204:235-243.
[20]方誠剛,張鋒,馬靜文,等.氨基酸離子液體-MDEA混合水溶液對 CO2的降膜吸收[J].化工學報,2011,62(3):723-729.
[21]Feng Z,Yuan G,Xian-Kun W,et al.Regeneration performance of amino acid ionic liquid(AAIL)activated MDEA solutions for CO2capture[J].Chemical Engineering Journal,2013,223:371-378.
[22]Feng Z,Jing-Wen M,Zheng Z,et al.Study on the absorption of carbon dioxide in high concentrated MDEA and ILs solutions[J].Chemical Engineering Journal,2012,181:222-228.
[23]Gao Y,Zhang F,Huang K,et al.Absorption of CO2in amino acid ionic liquid(AAIL)activated MDEA solutions[J].Int.Greenh.GasCon,2013,19 ,379-386.
[24]Fu D,Chen L H,Qin L G.Experiment and model for the viscosity of CO2-MDEA-MEA aqueous solutions[J].Fluid Phase Equilibria,2012,319,42-47.
[25]Fu D,Chen L H,Qin L G.Experiment and model for the viscosity of CO2-MDEA-DEA aqueous solutions[J].Mol.Liq,2013,181,105-109.
[26]Fu D,Qin L G,Hao H M.Experiment and model for the viscosity of CO2-PZ-MDEA aqueous solutions[J].Mol.Liq,2013,186,81-84.
[27]Fu D,Hao H M,Liu F.Experiment and model for the viscosity of CO2-AMP-MEA and CO2-AMP-DEA aqueous solution[J].Mol.Liq,2013,188,37-41.
[28]Fu D,Li Z X,Liu F.Experiments and model for the viscosity of CO2-AMP-PZ aqueous solution[J].Chem.Thermodyn,2014,68,20-24.

