老年2型糖尿病患者并發低鉀血癥的臨床探討
郭玫 ,劉瑛 ,顧勇 ,3
1.復旦大學附屬上海市第五人民醫院,上海 200240;2.寧夏回族自治區人民醫院,寧夏銀川 750001;3.復旦大學附屬華山醫院,上海 200040
伴隨著中國老齡化社會進程的加速,老年2型糖尿病發病率的逐年上升[1]及因糖尿病病程的進展伴發的慢性并發癥對患者本人,家庭及社會醫療帶來了沉重的負擔。低鉀血癥是老年糖尿病患者易于發生及被忽視的并發癥之一。嚴重低鉀可造成心律失常,肌麻痹[2]等嚴重的后果。早期發現和治療對于老年糖尿病患者的預后具有重要的意義,該文就2011年4月—2014年4月住院治療的年齡大于60周歲的糖尿病合并低血鉀的115例患者的臨床資料進行分析總結,并對其產生的機制及處理原則進行探討以提高臨床診治水平,現報道如下。
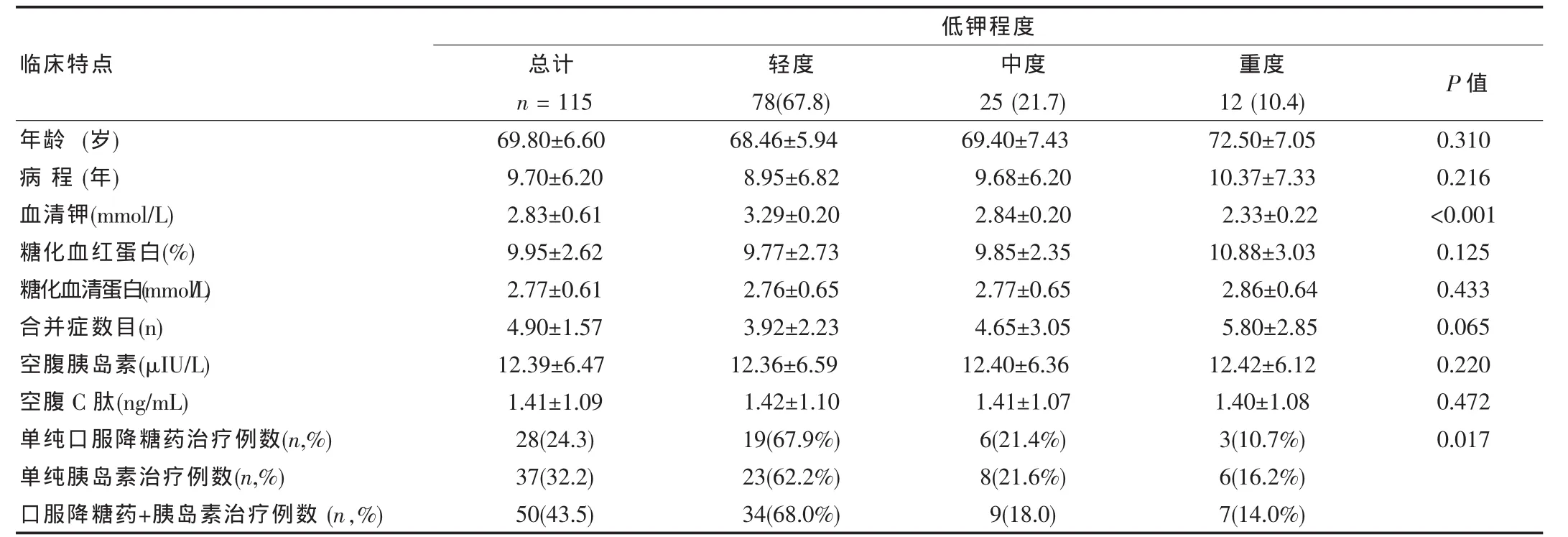
表1 115例糖尿病并發不同組別血鉀患者臨床特點及降糖藥物治療狀況
1 資料與方法
1.1 一般資料
選取2011年3月—2014年3月收住寧夏自治區人民醫院內分泌及綜合內科的年滿60周歲及以上的2型糖尿病患者115例為研究對象。其中男52.2%(60例),女 47.8%(55 例)。 年齡 60~82 歲,平均年齡為(69.8±6.6)歲,糖尿病病史1個月~28年,平均診斷糖尿病病史為(9.7±6.2)年。
1.2 診斷標準
(1)2型糖尿病診斷依據2013年《中國2型糖尿病防治指南》[1],(2)血清生化測定使用日本7600-020 HITACHI生化測定儀,以血清鉀濃度低于3.5 mmol/L為低血鉀癥。 其中3.0~3.5 mmol/L為輕度低鉀血癥,2.5~3.0 mmol/L為中度低鉀血癥,低于2.5 mmol/L為重度低鉀血癥[2]。(3)排除標準:①繼發性糖尿病者。②癡呆,嚴重腎功能不全,心功能不全及肝功能不全。③重癥感染,酮癥酸中毒患者。④已在院外行補鉀治療者。
1.3 臨床癥狀
115例患者中乏力,口干30例;便秘20例;四肢麻木19例;食欲下降,惡心16例;胸悶,心悸10例;無明星癥狀20例。 出現低鉀ECG表現者56例 (48.7%):T波低平,倒置,甚至出現U波最常見,其次是P-R間期延長,QRS波增寬,少數有典型心律失常及ST段壓低。
1.4 方法
回顧性分析符合入選標準患者的空腹血糖,糖化血紅蛋白,糖化血清蛋白,空腹胰島素,空腹C-肽,腎功能、血壓情況,周圍血管,神經,眼底并發癥狀況,治療藥物種類、治療年限,了解當時癥狀及體征、輸液情況,十二導聯心電圖表現等,力爭找出低鉀原因。
1.5 統計方法
以SPSS 17.0軟件進行統計學分析,分析比較不同程度低血鉀組患者的臨床特征,根據變量為計數或計量資料應用方差分析(ANOVA)或檢驗。計算各致病相關因素占全部病例的比率(%)。符合正態分布的計量資料應用均數±標準差(±s)表示,不符合正態分布的計量資料應用中位數表示。各計量因素與血鉀間的相關性檢驗采用Spearman相關分析。P<0.05為差異有統計學意義。
2 結果
2.1 不同血鉀組別在臨床特點上的比較
經實驗室檢查血鉀濃度為2.1~3.4 mmol/L,平均濃度為(2.83±0.61)mmol/L。患者以輕中度低鉀血癥為主(103例占總數的89.5%)。其中單純使用胰島素治療37例,單純口服降糖藥28例,胰島素聯合口服降糖藥50例。長期應用胰島素治療的患者占多數(約75.7%)。見表1。
2.2 合并其他慢性疾患狀況及可能的低血鉀原因
該組糖尿病患者中約108例(94%)合并有2種以上慢性疾病,各種慢性疾患可單獨或合并存在,如超過90%此組患者合并有周圍血管病變,76%合并有高血壓病,56%合并有冠心病,60%此組患者合并有糖尿病周圍神經病變和/或中樞神經病變如腔隙性腦梗塞,合并有腎臟病變者40%,眼病者36%,合并支氣管肺部疾患者25%,反復低血糖發作者13.0%。可能的低血鉀原因及構成比。見表2。
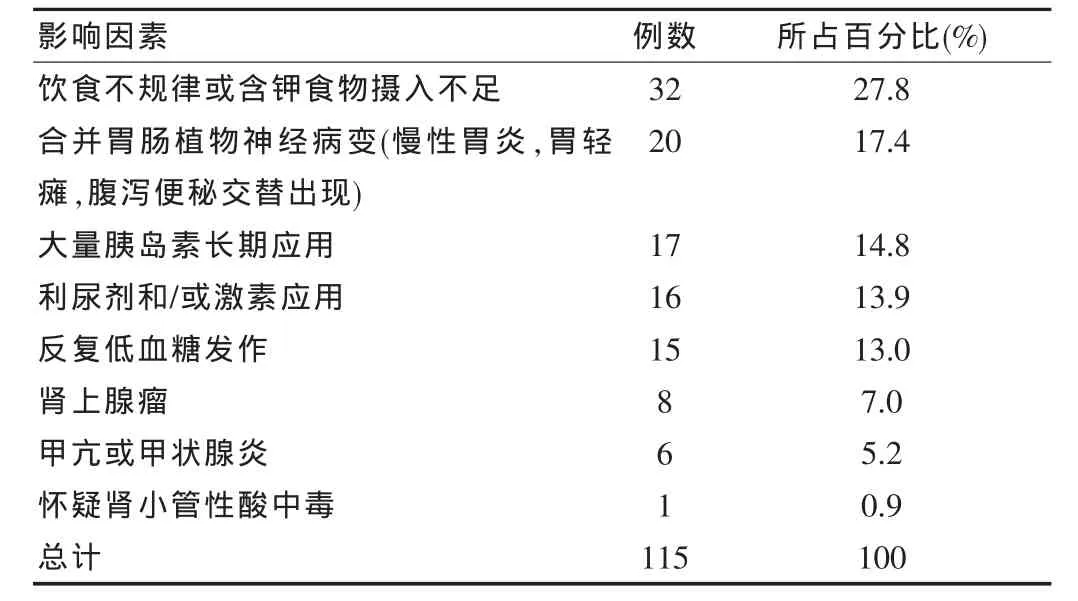
表2 115例老年糖尿病患者低血鉀可能原因
2.3 各計量因素與低血鉀的相關性分析
患者年齡,糖尿病病程,糖化血紅蛋白水平,糖尿病合并其他疾患數目,胰島素及C-肽水平與低血鉀的相關性分析顯示,低血鉀水平與糖化血紅蛋白(r=-0.318,P<0.05),合并癥數目(r=-0.406,P<0.05)顯著負相關且差異有統計學意義,但與胰島素水平呈正相關關系(r=0.236,P=0.172),與 C-肽水平呈負相關關系(r=-0.064,P=0.713)。見表3。
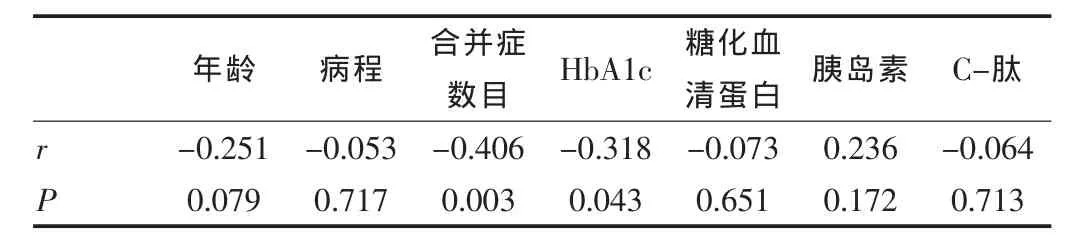
表3 血鉀水平與計量變量的相關關系(Spearman Correlation)
3 討論
3.1 病因分析
鉀離子是體內重要的陽離子,對維持細胞的正常代謝、滲透壓和酸堿平衡、神經肌肉的興奮性、心肌的正常功能等有重要意義。根據該文總結老年糖尿病患者低鉀血癥的發病主要為:鉀攝入不足,藥物源性和/或內分泌,腎臟因素,使鉀排出過多或使細胞外鉀向細胞內轉移三種因素的混合。分析如下:第一,老年糖尿病患者因消化功能減退,食量減少,或因合并有慢性胃腸疾患引起食欲下降,飲食營養結構不合理,鉀攝入減少;并發糖尿病胃腸植物神經功能紊亂,或胃輕癱時常會影響消化系統功能,引起胃排空延遲等癥狀,導致鉀攝入障礙,引發低鉀血癥。此組患者中約45.2%合并有此類疾患,其中有1例患者因嚴重低血鉀發生腸麻痹,另有1例合并有神經性膀胱。第二,藥物源性低鉀:當老年糖尿病患者部分因病史長,血糖長期控制不理想,血糖波動,尤其長期大量應用胰島素者,一方面用胰島素治療糖尿病時,胰島素促進細胞葡萄糖利用及糖原合成的同時,還直接剌激骨骼肌及肝臟細胞膜上的Na+-K+-ATP酶,從而使細胞內Na+排出增多而細胞外K+進入細胞增多,鉀離子向細胞內轉運,促使血鉀降低。其次,胰島素抵抗,或注射胰島素誘發低血糖與促腎上腺皮質激素(ACTH),皮質醇過度分泌和慢性垂體-腎上腺軸功能紊亂有關[3],腎上腺皮質激素超量釋放,使血鉀降低。另一方面,老年糖尿病患者抵抗力弱,易于支氣管肺部感染,或大多已有慢性阻塞性肺疾病等疾患,該例患者中有近25%患者合并此類疾患。其發生低血鉀與應用抗菌素,如大量使用青霉素及其衍生物后,可由于增加腎遠端鈉流量導致K+排泄增多,再加上并發高血壓,心衰者排鉀利尿劑的使用,使機體缺鉀。吸入β2受體激動劑,如異丙腎上腺素或沙丁胺醇等,提高Na+-K+-ATP酶活性,輸注茶堿等可刺激擬交感胺的釋放,還可抑制磷酸二酯酶而增強Na+-K+-ATP酶活性,使細胞外鉀向細胞內轉移,故也易出現低鉀[4]。第三,各種原因引起內分泌調節,腎小管功能障礙使血鉀向細胞內轉移或尿鉀排出增多。如甲亢時甲狀腺激素刺激Na+-K+-ATP酶合成,促進鉀向細胞內轉移,而發生低鉀。各種原因所致繼發性醛固酮增多而使腎遠曲小管和集合管Na+-K+交換增加,因而起排鉀保鈉的作用,促進腎排鉀。由于嘔吐,腹瀉所致的血容量減少可使醛固酮分泌增多,而醛固酮不僅可使尿鉀排出增多,也可使結腸分泌鉀的作用加強[5]。臨床上以腎小管鈉鉀轉運障礙,繼發醛固酮增多,如Bartter或 Gitelman綜合征[6],Liddle綜合征[7](假性醛固酮增多癥,家族性疾病),原發性醛固酮增多癥,腎小管酸中毒等所致低鉀者不易糾正,需進行尿電解質,醛固酮,腎素,皮質醇,血氣分析等檢查明確診斷后對癥治療,對于不明原因且難于糾正的低鉀血癥者需考慮上述疾患。該組患者中發現腎上腺瘤患者共7例,不明原因長期低鉀1例,因未能常規行尿電解質,腎素等檢查未追蹤到最后的診斷結果。
相關分析提示血鉀水平與年齡,糖尿病病程呈負相關,即血鉀隨年齡,病程增長而下降,但無統計學意義。血鉀與合并其他疾患的數目,及糖化血紅蛋白水平呈負相關且有統計學意義,提示平均血糖的增高及慢性病數目的增多伴隨著血鉀水平的降低。機體總鉀量隨生理年齡增長而下降,與老年人鉀離子豐富的非脂肪組織逐年減少而含鉀離子很少的脂肪組織逐年相應增加有關。而且老年人隨著肌肉萎縮,細胞衰老減少,細胞內液較年輕人相對少,故老年人體內保鉀能力減弱。該組糖尿病患者中約108例(94%)合并有2種以上慢性疾病,各種慢性并發癥可單獨或合并存在,尤以心血管及神經系統合并癥多見,考慮與使用引起低鉀的藥物治療有關。
3.2 診治體會
由此可見長期血糖控制不理想及多種疾患并存所致機體對鉀攝入,排出及細胞內外液鉀動態調控的失平衡而使老年糖尿病患者易于發生低血鉀。內科醫師在診治老年患者時需常規注意電解質變化。低鉀血癥可抑制胰島素分泌,使糖耐量下降,血糖進一步增高,造成惡性循環[8]。另有研究表明低鉀血癥與高血壓的發病及腦血管病的發生有關[9],且與AMI患者的梗死時間、部位和面積相關,并嚴重影響患者的預后[10]。可能與低鉀血癥時反饋抑制醛固酮釋放,而醛固酮降低的同時,腎素血管緊張素水平升高有關[11]。另外與低鉀引起一氧化氮水平降低和內皮功能受損,影響血管功能有關[12]。
血清鉀測定僅僅是反映細胞外液的鉀離子濃度,不能正確反映體內鉀的總量,但體內的鉀離子經常不斷地在細胞內與細胞外液之間相互交換,以保持動態平衡。研究表明患有心衰及慢性腎臟疾患的患者血鉀低于4.0與住院率及死亡率的增高有關,血鉀維持在4.0~5.0 mmol/L為臨床相對安全的范圍[13]。該文研究表明糖尿病患者易于并發心腦腎等血管神經疾患,血鉀水平也應維持于此水平以利于增加胰島素的敏感性,利于糖尿病的控制。該文因僅為回顧性研究,尚需進行進一步的前瞻性研究明確不同血鉀水平對糖尿病患者預后的影響。
總之,老年糖尿病并發低鉀血癥是綜合因素造成的,各因素之間是相互作用的,因此應重視低血鉀的早期診斷及預防,鼓勵高鉀低鈉飲食。早期糾正不利因素,適當補鉀,綜合治療,預防及避免低鉀血癥及與其相關的慢性病的發生發展。
[1]中華醫學會糖尿病學分會.中國2型糖尿病防治指南(2013年版)[J].中華糖尿病雜志,2014,6(7):466-488.
[2] Oram RA,McDonald TJ,Vaidya B.Investigating hypokalemia[J].British Medical Journal,2013(347):5137.
[3]林東源,劉志梅,李劍軍,等.2型糖尿病60例下丘腦-垂體-腎上腺軸功能的變化[J].內科,2009(2):235-237.
[4]Sung CC,Lin SH.Drug-induced hypokalaemia:Part 1[J].Adverse Drug Reaction Bulletin,2012(273):1051-1054.
[5]Greenlee M,Wingo CS,McDonough AA,et al.Narrative review:evolving concepts in potassium homeostasis and hypokalemia[J].Annals of Internal Medicine,2009(150):619-625.
[6]趙蔚菁,陳海冰,包玉倩.Gitelman綜合征一例并文獻復習[J].上海醫學,2012,35(1):74-76.
[7]武倩琳,田浩明.Liddle綜合征[J].國際內分泌代謝雜志,2011,31(5):346-348.
[8]Chatterjee R,Yeh HC,Shafi T,et al.Serum and dietary potassium and risk of incident Type 2 Diabetes Mellitus:The Atherosclerosis Risk in Communities (ARIC)Study[J].Arch Intern Med,2010,170(19):1745-1751.
[9]張蘇明,褚倩,梅愛農.腦血管病防治研究的回顧,進展與展望[J].中華神經科雜志,2005,38(3):140-144.
[10]華琦,李東寶.低鉀血癥對急性心肌梗死患者預后的影響[J].中華老年心腦血管病雜志,2006,8(9):582-584.
[11]王朋波,張書信.低鉀血癥與胰島素抵抗[J].醫學信息,2013(3):163-164.
[12]Reungjui S,Roncal CA,Mu W,et al.Thiazide diuretics exacerbate fructose-induced metabolic syndrome[J].J Am Soc Nophrol,2007,18(10):2724-2731.
[13]Bowling CB,Pitt B,Ahmed MI,et al.Hypokalemia and outcomes in patients with chronic heart failure and chronic kidney disease:Findings from propensity-matched studies[J].Circulation:Heart Failure,2010(3):253-260.

