多器官功能障礙綜合征患者腸道菌群多樣性研究
徐文秀,張 謙
(江蘇省蘇州市中醫醫院,江蘇 蘇州 215000)
臨床研究
多器官功能障礙綜合征患者腸道菌群多樣性研究
徐文秀,張 謙
(江蘇省蘇州市中醫醫院,江蘇 蘇州 215000)
目的應用PCR-DGGE技術對多器官功能障礙(MODS)患者腸道菌群多樣性進行研究,分析其與疾病的關系。方法收集15例MODS患者和15例正常對照人群的糞便樣本,提取樣本細菌總基因組DNA。根據MODS評分分成低分組(<5分)、中分組(5~10分)、高分組(≥10分)。然后對細菌總基因組DNA的16SrRNA的V3區進行PCR擴增,進行DGGE圖譜及多樣性分析,分析MODS患者及對照人群腸道菌群的相似性,并通過Shannon-Weaver(H')指數來分析樣本的條帶數、均勻度指數、多樣性指數、豐富度指數和優勢度指數。結果低分組及高分組與對照組菌群結構差異顯著;低分組腸道菌群結構的種類及數量、優勢菌種類及相對含量均明顯低于中分組。中分組與高分組腸道菌群結構比較差異無統計學意義。高分組腸道菌群的種類多于低分組,但是數量差異不大;優勢菌相對含量及種類差異顯著。結論MODS患者腸道中獨有的細菌與疾病有關,它們與MODS的關系尚需進一步探索。
PCR-DGGE;多器官功能障礙綜合征;腸道菌群
多器官功能障礙綜合征(MODS)是危重病患者的常見并發癥。Mayr等[1]對ICU危重患者死亡原因及危險因素進行分析顯示,急性MODS引起的死亡占ICU總死亡人數的47%,遠遠超過單個器官衰竭和突發的心搏驟停而居ICU死亡原因的首位。目前國內外最常用的是加拿大Marshall等[2]的MODS評分和1995年全國危重病急救醫學學術會議[3]上提出并通過的MODS診斷標準,1986年Carrico等[4]首先提出腸道是發生MODS的原動力,腸道參與創傷、燒傷和感染后的各種應激反應,是MODS的始動器官。其主要損傷腸道黏膜屏障,影響腸道動力。近年隨著分子生物學的發展,PCR-DGGE技術應用于腸道微生物的研究[5]。本研究應用PCR-DGGE技術對MODS患者腸道菌群多樣性進行了觀察,現報道如下。
1 臨床資料
1.1一般資料 收集2010年10月—2012年3月蘇州市中醫醫院重癥醫學科及蘇州大學附屬第二醫院重癥醫學科15例符合標準MODS患者的糞便標本作為MODS組,同時采集15例同期健康體檢者糞便標本作為對照組。MODS診斷符合相關診斷標準,且存在2個或2個以上系統或器官功能障礙,年齡大于18周歲,以感染為誘因。MODS組年齡(74.82±14.69)歲,對照組年齡(81.40±10.49)歲,2組年齡比較差異無統計學意義(P>0.05)。MODS組又根據MODS評分分成3組:低分組(<5分)6例,中分組(5~10分)5例,高分組(≥10分)4例。
1.2主要實驗儀器和設備 Eppendorf 5804R低溫高速離心機;Vortex-2 Genie旋渦振蕩器;DK-8D型電熱恒溫水槽;PTC-225 Peltier Thermal Cycler PCR儀;PAC3000水平電泳儀;Syngene凝膠成像系統;Nanophotometer儀;垂直流超凈工作臺;DGGE儀(The DCode TM Universal Mutation Detection System);GS-800灰度掃描儀。
1.3腸道糞便樣本采集 采樣前,將30 mL糞便收集塑料杯高壓滅菌烘干備用。用無菌塑料杯收集每個個體新鮮糞便的中后端部分。標本采集完成后用蠟膜將塑料杯杯口封閉。同時對每個個體胃腸道問題信息進行采集。采集的樣本先于冰箱凍存,并立即轉運回實驗室-70 ℃保存備用。
1.4PCR-DGGE分析 16S rRNA 基因V3高變區通用引物[6]V3F:5’-CGC CCG CCG CGC GCG GCG GGC GGG GCG GGG GCA CGG GGG GCC TAC GGG AGG CAG CAG-3’;V3R:5’- ATT ACC GCG GCT GCT GG-3’,其中CGC CCG CCG CGC GCG GCG GGC GGG GCG GGG GCA CGG GGG G為GC夾。采用Touch-down程序,94 ℃,3 min預變性;94 ℃,1 min 變性;65 ℃,1 min退火;72 ℃,1 min 延伸,之后每2個循環退火溫度就下降 1 ℃,直到退火溫度降到 55 ℃,再以此為退火溫度循環4次;72 ℃,5 min延伸;4 ℃,10 min。隨后通過對PCR產物進行Recon-condition PCR去除嵌合體以及異源雙鏈的影響。擴增產物檢驗:將擴增產物上樣于2%瓊脂糖凝膠,Gel Red染色,于0.5×TAE緩沖液中150 V電泳30 min,以50 bp DNA ladder為Marker,使用凝膠成像系統Syngene進行檢驗。之后進行DGGE凝膠制備,220 V,電泳10 min。隨后150 V,電泳5 h,電泳結束后對凝膠進行Gel-Red染色15 min,使用Bio-Rad凝膠成像儀拍照。并通過QuantityOne軟件對DGGE分子指紋圖譜進行相關分析。
2 結 果
2.1MODS患者腸道狀況分析 15例MODS樣本大部分是直接從直腸部位吸取而來,呈水樣或粥樣,部分樣本帶有少量食物殘渣、膜狀物質等。臨床體檢聽診腸鳴音結果發現腸鳴音減弱的共有5例,其中低分組為0例,中分組3例,高分組2例。15例患者中大便隱血陽性3例,低分組0例,中分組2例,高分組1例(便隱血,并出現嘔血現象)。
2.2低分組與對照組DGGE圖譜分析 低分組和對照組條帶數、均勻度指數、多樣性指數、豐富度指數和優勢度指數比較差異均有統計學意義(P均<0.05)。低分組多樣性指數與豐富度指數均低于對照組,說明對照組腸道菌群種類及數量較大;均勻度指數與優勢度指數均低于對照組,說明二者腸道優勢菌種種類及相對含量差異也較大。見表1和圖1。
2.3中分組和對照組DGGE圖譜分析 中分組和對照組條帶數、均勻度指數、多樣性指數、優勢度指數和豐富度指數比較差異均無統計學意義。提示中分組與對照組在細菌的種類和數量以及優勢菌的種類和相對含量各方面差異不明顯。見表2和圖2。
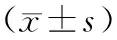
表1 低分組與對照組DGGE圖譜分析
注:①與對照組比較,P<0.05。

圖1 低分組和對照組電泳圖
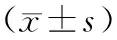
表2 中分組與對照組DGGE圖譜分析

圖2 中分組和對照組電泳圖
2.4高分組和對照組DGGE圖譜分析 高分組和對照組條帶數、優勢度指數和豐富度指數比較差異均有統計學意義(P均<0.05),而均勻度指數、多樣性指數比較差異無統計學意義。提示高分組樣本和對照組腸道菌群在種類上有明顯差異,優勢菌的種類和相對含量較豐富。見表3和圖3。
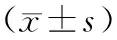
表3 高分組與對照組DGGE圖譜分析
注:①與對照組比較,P<0.05。
2.5特異性條帶克隆測序分析 選擇8條具有代表性的DGGE條帶進行切膠回收、PCR擴增、克隆和測序,測序后所得的序列和數據庫GenBank和RDP中的16SrRNA序列進行比對。顯示相似性最高的分別是類桿菌屬、不動桿菌屬、腸球菌屬和大腸桿菌。這提示MODS患者腸道中類桿菌屬、不動桿菌屬、腸球菌屬和大腸桿菌含量相對較高。見圖4。

圖3 高分組和對照組電泳圖

圖4 MODS各組與對照組電泳圖
3 討 論
腸道菌群與MODS的發生發展有著密切聯系。早在1988年,就有學者發現ICU患者大腸桿菌、脆弱擬桿菌、腸球菌普遍存在,而表皮葡萄球菌、念珠菌、假單胞菌對MOF高分有影響[7]。Marshall等[8]1993年采用含血的瓊脂和Macconkey瓊脂培養需氧菌、血瓊脂和苯乙醇瓊脂培養厭氧菌對患者胃腸道提取物進行定量培養,通過API20E系統進行定量和定性分析。該研究揭示了腸道細菌與遠距離器官感染之間的關系。研究發現,器官功能障礙的患者上消化道內容物經培養后,出現一些與上呼吸道感染有關并有時會造成尿路感染的病原微生物,如念珠菌、糞鏈球菌、假單胞菌和表皮葡萄球菌。
本研究中,16S rRNA V3區的PCR-DGGE圖譜能夠對人體腸道主要菌群組成進行區分。所有糞便標本的DGGE圖譜顯示高度的多態性,而且不同標本間的帶型均存在很大的差異。MODS低分組患者樣本與對照組以及高分組相比,在菌群組成和數量以及優勢菌的種類及相對含量各方面具有顯著差異。中分組與對照組及高分組和低分組相比,菌群結構的差異不是很明顯。這可能的原因是樣本量較小,尚不能取得更詳盡的信息。也可能提示MODS評分標準與腸道菌群結構有一定的聯系。
本研究還針對DGGE圖譜上顯示的,在MODS患者中亮度較高(即相對含量較高)以及在MODS患者中特異存在的條帶做了切膠回收克隆測序的實驗,顯示MODS患者腸道類桿菌屬、不動桿菌屬、腸球菌屬和大腸桿菌含量相對較高。提示這些菌屬在MODS患者疾病的發生發展上起到一定作用。不動桿菌屬是一種毒力較低的機會致病菌,當機體由于疾病導致免疫力低下的時候,便可引起感染,引發炎癥反應,如果控制不及時造成SIRS進而導致MODS。有研究顯示不動桿菌在肺炎、血液傳染病、膿胸等患者體內濃度很高[9]。腸球菌屬為橢圓形或圓形鏈狀排列的革蘭陽性球菌,是人和動物腸道正常菌群的一部分。毒力較低,只有在一定條件下如必須在宿主組織定植、并能抵抗機體的免疫防御機制后才能引起組織病理改變,導致感染。Hung等[10]從腎膿腫患者的體液中培養出大量大腸桿菌以及腸球菌,也提示這2種菌屬與SIRS及MODS的發生有關。通過合理使用抗生素以及飲食調節腸道菌群的組成,有可能減輕MODS患者的臨床癥狀,對于MODS患者的預防、治療和轉歸都有著重要的作用。
MODS是一類發病機制復雜的綜合征,對患者、家庭和整個社會都導致了嚴重的傷害。過去對MODS病因的研究主要集中在對炎癥反應的控制上,雖然也認識到腸道菌群的重要作用,但是多數也是通過培養法針對某些細菌做的定量、定性分析,而從總體上分析腸道菌群結構的研究并不多。前期學者多集中于益生菌對腸道菌群調節作用的研究上,而本文是從腸道菌群總體結構上的探索。再者,以人的腸道為研究對象,每個人的飲食、生活環境和宿主基因等都會影響腸道菌群結構的組成,因此本研究結果與他們的研究結果均有一定的差異。
[1] Mayr VD,Dünser MW,Greil V,et al. Causes of death and determinants of outcome in critically ill patients[J]. Critical Care,2006,10(6):R154
[2] Marshall JC,Cook DJ,Christou NV,et al. Multiple organ dysfunction score:a reliable descriptor of a complex clinical outcome[J]. Crit Care Med,1995,23(10):1638-1652
[3] 王今達,王寶恩. 多臟器功能失常綜合征病情分期診斷及嚴重程度評分標準(經廬山'95全國危重病急救醫學學術會討論通過)[J]. 中國危重病急救醫學,1995,7(6):346-347
[4] Carrico CJ,Meakins JL,Marshall JC,et al. Multiple-organ-failure syndrome[J]. Arch Surg,1986,121(2):196-208
[5] 楊曉軍,王曉紅,梁志娟. 16S rDNA測序在呼吸機相關性肺炎痰液細菌多樣性分析中的應用[J]. 中華危重病急救醫學,2014,26(5):294-299
[6] Hill JM. Vasoactive intestinal peptide in neurodevelopmental disorders:therapeutic potential[J]. Curr Pharm Des,2007,13(11):1079-1089
[7] Marshall JC,Christou NV,Horn R,et al. The microbiology of multiple organ failure:the proximal gastrointestinal tract as an occult reservoir of pathogens[J]. Archives of Surgery,1988,123(3):309-315
[8] Marshall JC,Christou NV,Meakins JL. The gastrointestinal tract. The “undrained abscess” of multiple organ failure[J]. Ann Surg,1993,218(2):111-119
[9] Jajoo M,Kumar V,Jain M,et al. Intravenous colistin administration in neonates[J]. Pediatric Infectious Disease Journal,2011,30(3):218-221
[10] Hung CH,Liou JD,Yan MY,et al. Immediate percutaneous drainage compared with surgical drainage of renal abscess[J]. Int Urol Nephrol,2007,39(1):51-55
Study on the intestinal microbial flora diversity in the patients with MODS
XU Wenxiu, ZHANG Qian
(Suzhou Hospital of Traditional Chinese Medicine, Suzhou 215000, Jiangsu, China)
Objective It is to study the intestinal microbial flora diversity in the patients with MODS by PCR-DGGE technology, and to analyze its relationship with the disease. Methods The stool samples of 15 patients with MODS and 15 healthy people were collected and the genomic NDA of the microbial flora was extracted. According to MODS scores, the patients were divided into low score group (<5), medium score group (5-10), high score group (>=10). V3 area of 16S rRNA of total genomic DNA of bacteria was chosen for PCR amplification to do DGGE profiles and diversity analysis, intestinal flora similarity was analyzed between MODS patients and control group, and through the Shannon-Weaver (H ') index the sample number of bands, evenness index, diversity index, richness index and dominance index were analyzed. Results The differences in the microorganism community structure between low score group, high score group and control group were significant. Sample amount and type of structure of intestinal flora, kind and relative content of advantage strains in low score group was significantly lower than that in medium score group, but there was no significant difference in the microorganism community structure between low score group and high score group. The kinds of intestinal flora in high score group was more than that in low score group, but the difference in quantity was not significant. The difference in kind and relative content of advantage strains was significant. Conclusion Unique intestinal microbial flora in MODS patients is related to the disease, but their relationship with the MODS remains to be further explored.
PCR-DGGE; MODS: intestinal microbial flora
10.3969/j.issn.1008-8849.2015.28.009
R0541.64
B
1008-8849(2015)28-3104-04
2014-12-30

