從藥品監管的角度分析打粉中藥存在的問題
李莉,曠吉琳,朱麗萍,高天
·藥事管理·
從藥品監管的角度分析打粉中藥存在的問題
李莉1,曠吉琳1,朱麗萍1,高天2
目的:為保證打粉中藥的安全及質量可控,并有利于監管部門對該類藥材的監管,同時為我省2015年版《中藥飲片炮制規范》收載范圍提供參考意見。方法:通過收集成都市目前市面上正在銷售的部分打粉中藥,對其生產企業所在地、是否有執行標準、用法用量等進行統計,并結合相關法規和文獻對打粉中藥存在的問題及質量不可控的原因進行分析。結果:所收集的樣本33.3%的品種未標示執行標準,標示有執行標準的品種中有50%與標示標準有出入,有部分品種無生產許可證、GMP證書,只有少數品種說明了制法/加工方法和原藥材產地。結論:藥監部門對目前市面上正在銷售的粉末類藥材監管不完善,可通過將打粉中藥收錄入《中藥飲片炮制規范》的方式來規范其生產,達到利于藥監部門監管的目的。
粉末中藥;打粉中藥;中藥飲片炮制規范
中藥材打粉是中藥飲片常用的炮制方法之一,中藥細粉是中藥臨床使用的重要飲片規格,具有使用方便,攜帶便利等優點。在中醫古書籍,以及國家、地方藥品標準中,也記載和規定了部分中藥材打粉使用的方法和標準。但是除傳統的打粉藥材外,隨著社會的發展、人們觀念的轉變及需求的不同,打粉中藥發展迅速,不僅將原來不打粉的藥材打粉,而且銷售、使用也不僅僅以藥用為目的。這樣的發展一方面方便了群眾使用中藥,對促進中醫藥產業的發展和保護公眾健康起到了積極作用。另一方面也存在著一些亟待解決的問題。我省自2012年起,開始逐步加強對打粉中藥的監管工作,但至今仍處于研究階段,相應的監管措施還不完善,需要更加深入和具體的研究以促進其發展。
1 資料與方法
1.1 資料
隨機抽取收集2014年1月至5月成都市正在銷售的打粉藥材(打粉中藥),對其說明書或標簽部分內容進行分析統計。
1.2 方法
通過收集成都市正在銷售的部分打粉藥材的信息,對其品種名稱、生產企業所在地、是否有執行
標準、用法用量、是否具有(標注)生產許可證、是否具有(標注)GMP證書、是否說明制法/加工方法、是否標示原料產地等進行分析統計,并對粉末類藥材質量不可控的原因、存在的問題進行分析和討論。
2 結果
2.1 對部分打粉中藥信息的分析
本文收集了成都市目前市面上正在銷售的9個品種,生產地包括:四川省(5個)、云南省(2個)、廣東省(1個)、重慶市(1個)。通過對收集到的9個品種的打粉中藥說明書/標簽內容進行分析發現,33.3%(構成比)的品種未標示執行標準,標示有執行標準的品種中有50%與標示標準有出入,有部分品種無生產許可證、GMP證書,只有少數品種說明了制法/加工方法和原藥材產地,具體情況詳見表1。
2.2 與傳統炮制方法、用法/用量的比較
傳統炮制方法多為凈制、干燥后切片或直接備用等,打粉中藥在其基礎上還要進行打粉操作;傳統用法的飲片一般炮制后入湯劑,而打粉中藥多數采用吞服、沖服,具體情況詳見表2。
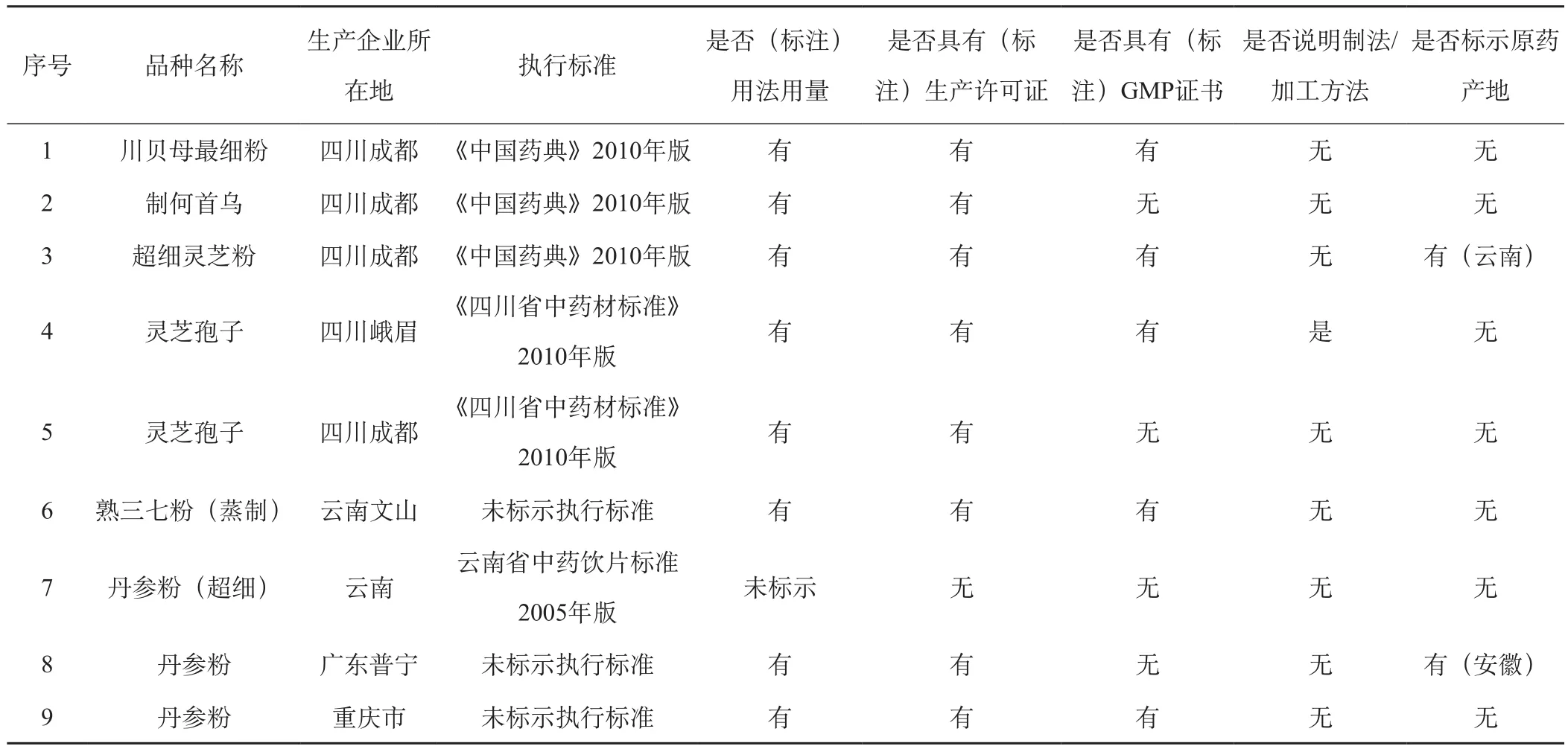
表1 部分打粉中藥信息的統計情況
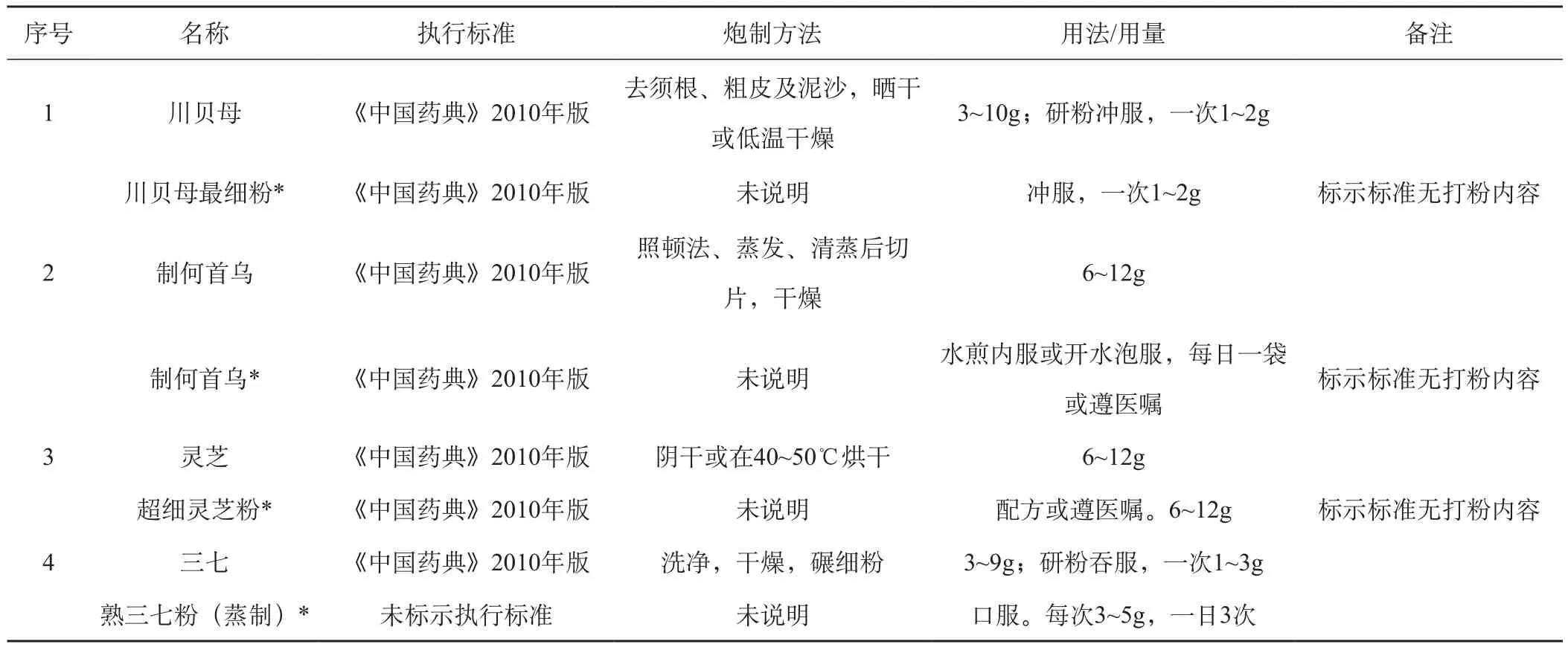
表2 與傳統方式的比較
3 討論
3.1 打粉中藥的本質為飲片
打粉中藥雖然與一般的飲片在包裝及銷售方式上有所不同,但其本質還是屬于中藥飲片,而非藥品。有很多傳統藥材就是以粉末入藥(如煎劑、散劑等),同時傳統中醫用藥也常有單方,即以一味藥組成一個藥方,如“獨參湯”,僅有人參一味藥入方。現在“打粉中藥”的應用,是以中醫藥理論為根本指導原則,以傳統用藥中的“粉末入藥”以及“單方入藥”為應用基礎的一種用藥方式。
打粉中藥只是在包裝、銷售形式上類似藥品,但與藥品不同的是它們沒有經過藥學研究、臨床研究等過程,沒有藥監部門批準的生產工藝,也沒有經過各級藥監部門的審核、審批[1]。
3.2 目前成都市的打粉藥材主要存在的問題
3.2.1 品種繁多、應用模式轉變 目前,打粉中藥不僅在大部分藥店都有銷售,而且品種繁多,既有傳統或現有標準中可以打粉使用的品種,如川貝母、三七等等,同時也涵蓋了很多傳統或現有標準中未涉及打粉的品種,包括山楂、雞內金、五靈脂、紅花、蛤蚧、山藥、西洋參等。大部分打粉中藥的服用方法與傳統用藥方式不同,炮制方法也發生了變化(如表2所示),但還是直接沿用原藥材的功能與主治,并且未進行過相關的臨床前及臨床研究。
打粉中藥材與傳統方法相比,第一,傳統方法炮制后直接入煎劑的藥材,藥材本身不會進入人體內部,而打粉中藥多數采用的吞服、沖服,是直接將藥材送入人體內;第二,打粉中藥將一部分中藥材開發為細粉、超細粉甚至更為細微的粉末,雖有利于有效成分的溶出,但同時毒性物質的溶出量也有可能增大,即增大了毒性反應發生的幾率[1]。
3.2.2 存在無標準的現象 目前,市面上除了本省生產的打粉藥材,還包括部分省外生產,如云南、廣東、重慶等。部分打粉中藥在說明書或標簽上,沒有標示執行標準,只有“藥品GMP證書編號”及“藥品生產許可證號”。不過相關企業這些證明性文件是否含有本品種的生產范圍,因為不能查看到文件原件,所以無法核實。而依據我國的藥品管理法,中藥飲片必須按照國家藥品標準或省、自治區、直轄市人民政府藥品監管部門指定的炮制規范炮制[2]。
無標準的另外一層意義在于,即使粉末類藥材有執行標準,如《中國藥典》或省級中藥飲片標準等,以目前的科學技術手段,對打粉藥材的檢測還具有一定難度。所以通過現有的技術,很難制定出有效的質量標準,不利于打粉中藥的檢測及監管。
3.2.3 標準混淆、粉末等級不明確 市面上出現的“川貝母極細粉”,在其標簽上標注的執行標準為“《中國藥典》2010年版第一部”,查閱《中國藥典》2010年版(第一部)發現,藥典上的品種名稱為“川貝母”,在其加工以及【用法】中并未提及“極細粉”,而在【用法】中僅寫到“打粉吞服”。“ 超細靈芝粉”,該品種標簽上標示的執行標準也為“《中國藥典》2010年版第一部”,但是藥典涉及的品種為“靈芝”,同樣沒有“靈芝粉”這個品種。顯然,上述兩個打粉藥材與其標示的執行標準所對應的品種具有出入。
《中國藥典2010年版》“凡例”收載有最粗粉、粗粉、中粉、細粉、最細粉、極細粉的粉末等級[3]。粉末等級對藥材的有效物質溶出、成本均有影響,所以明確粉末等級對打粉中藥的監管具有一定的意義。
3.2.4 包裝材料及原料產地 粉末藥材易吸潮,所以容易發生霉變等現象,使藥材的性質改變。
為防止變質,市面上的粉末藥材大部分都標注了儲存方式,有利于指導使用者避免不當的儲存方式造成藥材的變質。為更好地保證藥材質量,生產企業在藥材包裝上采取了很多措施。常見的藥材以塑料瓶包裝,使用者在使用時擰開瓶蓋,取出一定量后,再將瓶蓋擰緊,部分藥材瓶加了內塞,有利于藥材的密封。有部分藥材,如“川貝母最細粉”,采用袋裝[袋裝(10g/袋),一盒10袋],使密封性更佳。但是這些措施不能避免藥材包裝材料安全性的問題。因此在關注粉末藥材本身質量的同時,還應加強對其包裝材料的監管。
中藥理論中有“道地藥材”的這個概念,從一方面反應了中藥材(打粉藥材原藥)的產地不同,其粉末在質量,價格上都不同。原材料的產地無法統一規定,但是有必要加以區分,要求生產企業將原材料的產地標注在成品的標簽或說明書內,可供不同要求的使用者選擇。
3.3 數據來源分析
本文收集的數據仍有很多不足,主要表現在數據量較少,且僅限于成都市,范圍較窄等方面。需要說明的是,對打粉中藥材的監管目前處于逐步發展過程的前期。首先,本文收集的數據量雖然少,但都屬于目前市面上的常見品種,能集中的反應出打粉中藥存在的一些問題。其次,將數據收集范圍限定在成都市,主要因為成都市目前已經形成較穩定的打粉中藥市場,對該地區收集的數據進行研究具有一定的實際意義。
4 小結
除了通過分析以上收集的部分粉末類藥材的信息所發現的問題外,打粉中藥還存在以下幾個問題:各企業同品種生產工藝和標準不統一;企業營銷過程中與銷售地管理部門溝通不夠,造成各種矛盾;少部分未經批準試點的藥品生產企業,超范圍、超品種進行中藥材打粉生產,違反國家藥品管理法律法規;臨床研究仍然存在著不足和局限性等等。因此加快完善相應的法規及監管制度十分必要。
加強對打粉中藥的監管,較有效的方法是通過加強質量控制來保障它的有效性及安全性。目前還很難通過成品檢驗實現對打粉中藥的監管,但是我們可以通過監管其生產過程來控制其質量。例如將打粉中藥收錄入我省新版的“中藥飲片炮制規范”中,通過制定炮制規范的方法來規范打粉中藥生產企業的生產過程,同時為保證能夠制定出合理、有效的炮制規范,相關的藥學、藥理毒理等研究也十分重要。
[1] 華春玉.不同粒徑馬錢子粉的急性毒性實驗[J].醫藥導報,2001,20(12):776.
[2] 國家食品藥品監督管理局.中華人民共和國藥品管理法(主席令第45號)[S].2001.
[3] 國家藥典委員會.中華人民共和國藥典2010年版(第一部) [S].北京:中國醫藥科技出版社,2010.
(責任編輯:蔣淼)
Analysis of the problem existed in Traditional Chinese medicine powder from the prospect of drug supervision/
LI Li1, KUANG Ji-lin1, ZHU Li-ping1, GAO Tian2//(1.ChengduUniversity of Traditional Chinese Medicine, Chengdu 610041, Sichuan;2. Afflated Hospital of Chengdu university of Traditional Chinese Medicine, Chengdu 610072, Sichuan)
Objective:To ensure the safety and quality control of traditional Chinese medicine powder, improve the supervision and put the reference for the inclusion range of "Chinese Herbal Medicine Decoction Pieces Processing Norms".Method:Chinese traditional medicine powder on market was partly collected in Chengdu. Statistics analysis was carried out including production enterprises, execution standard, usage and dosage. And the reason for the existed problem and uncontrolled quality was analyzed in combination with regulation and literature.Result:In the samples collected, no execution standard couldn't be found in 33.3% of the samples. The labeled standard was not in accordance with the powder could be found in 50% of the samples. Some varieties had no pharmaceutical producer license and drug GMP certifcation. Only a few varieties had the indication of the processing method and the medicinal origin.Conclusion:The current supervision on selling powder by regulation department is not enough. It is suggested that TCM powder can be included in "Chinese Herbal Medicine Decoction Pieces Processing Norms" for the production standardization and better supervision of TCM powder.
Traditional Chinese medicine powder; Dafen TCM; Chinese Herbal Medicine Decoction Pieces Processing Norms
R 283, R 288
A
1674-926X(2015)02-023-03
1.成都中醫藥大學,四川 成都 610041
2.成都中醫藥大學附屬醫院,四川 成都 610072
李莉(1989-),女,碩士研究生,中藥理論與應用研究 Tel:18200338986 Email:304709021@qq.com
高天(1963-),女,主任藥師,中藥安全性研究
Tel:18980769037 Email: tutugt@163.com
2014-05-22

