艾塞那肽降低超重和肥胖患者體質量有效性與安全性的系統評價Δ
蘇 娜,徐家玥,徐 珽(四川大學華西醫院藥劑科,成都 610041)
超重和肥胖是指體內脂肪堆積過多或分布異常,通常伴有體質量增加。改善體質量的措施主要包括飲食控制、行為干預、體力活動、藥物治療和手術治療。目前,臨床用于治療肥胖的藥物主要分為非中樞性減體質量藥、中樞性減體質量藥和兼有減體質量作用的降糖藥物。胰高糖素樣肽1(GLP-1)受體激動藥不僅可以增加胰島素分泌、抑制胰高血糖素分泌,而且可以延緩胃排空,通過抑制食欲相關中樞而減少進食量。目前,國內上市的GLP-1 受體激動藥有利拉魯肽和艾塞那肽。國內外研究表明,兩藥對于超重和肥胖的2型糖尿病患者有明顯的減體質量作用[1]。艾塞那肽目前只在肥胖伴2型糖尿病的患者中推薦,并沒有作為治療單純性肥胖的推薦藥物[2]。因此,本研究采用Meta 分析的方法系統評價了艾塞那肽降低超重和肥胖患者體質量的有效性和安全性,以為臨床合理用藥提供循證依據。
1 資料與方法
1.1 納入與排除標準
納入研究類型為國內外公開發表的隨機對照試驗(RCT),語種限定為中文和英文。研究對象為超重和肥胖的成年患者,診斷標準均符合美國心臟學會(AHA)、美國心臟病學學院(ACC)和肥胖學會(TOS)的標準[2],即年齡≥18 歲,體質量指數(BMI)≥25 kg/m2的成年人,無論是否伴2型糖尿病、高血壓和高脂血癥;排除兒童、妊娠期婦女和感染人類免疫缺陷病毒(HIV)的患者。試驗組患者給予艾塞那肽治療,對照組患者給予安慰劑或者其他藥物治療。結局指標為患者體質量變化情況和不良反應發生率。
1.2 檢索策略
計算機檢索Cochrane圖書館、PubMed、Medline、EMBase、中國期刊全文數據庫、中文科技期刊數據庫和萬方數據庫。檢索時限均從建庫起至2014 年3 月。檢索詞包括“超重”“肥胖”“艾塞那肽”“Exenatide”“Overweigh”“Obesity”等。此外,追溯已納入文獻和相關綜述的參考文獻。
1.3 資料提取
文獻檢索結果以數據庫形式保存。由兩位研究者根據納入與排除標準獨立篩選文獻、提取資料并評價質量,然后交叉核對,如發生分歧,討論解決或交由第三位研究者協助裁定。
1.4 方法學質量評價
按照Cochrane 偏倚風險評估工具5.1.0 版對納入研究的方法學質量進行評價[3]。評價內容包括:①隨機分配方法;②分配方案是否隱藏;③是否對患者和實施者采用盲法;④是否對數據分析者采用盲法;⑤結果數據是否完整;⑥是否選擇性報道結果;⑦是否有其他偏倚來源。針對每項評價指標,作出“低度偏倚”“高度偏倚”或“不清楚”的判斷。
1.5 統計學方法
采用Cochrane協作網提供的Rev Man 5.3.0統計軟件進行Meta 分析。分類變量采用相對危險度(RR)為療效分析統計量,各效應量均以95%可信區間(CI)表示,并繪制森林圖,以α=0.05為檢驗水準[4]。首先,采用χ2檢驗對納入研究進行異質性檢驗(臨床異質性和方法學異質性),同時根據I2判斷異質性的大小,I2≤25%為低度異質性,25%<I2<50%為中度異質性,I2≥50%則為高度異質性[5]。若各納入研究結果間無異質性(P>0.1,I2<50%),則采用固定效應模型進行Meta 分析;反之,則采用隨機效應模型進行Meta分析。根據異質性產生原因對各研究進行亞組分析。必要時,行敏感性分析以檢驗結果的穩定性。對于無法合并的指標則進行描述性分析。
2 結果
2.1 納入研究基本信息
初檢出3 777 篇英文文獻和133 篇中文文獻,按照納入與排除標準逐層篩選,最終納入25 篇(項)RCT[6-30],其中中文文獻2篇[15,22],英文文獻23篇[6-14,16-21,23-30],合計5 307例患者。9項研究比較了艾塞那肽和安慰劑的減體質量效果[6-14],3 項研究比較了艾塞那肽和二甲雙胍的減體質量效果[15-17],1 項研究比較了艾塞那肽和格列本脲的減體質量效果[18],1項研究比較了艾塞那肽和羅格列酮的減體質量效果[19],1項研究比較了艾塞那肽和他司魯肽的減體質量效果[20],1項研究比較了艾塞那肽和西格列汀的減體質量效果[21],9項研究比較了艾塞那肽和胰島素的減體質量效果[22-30]。艾塞那肽組患者皮下注射艾塞那肽10 μg,一天2次[6-10,12-20,22-23,25-30]或者2 mg,一周1次[11,21,24];作為對照的7 組分別應用安慰劑(皮下注射,一天2 次)、二甲雙胍(500~1 000 mg,一天3 次,口服)、格列本脲(5 mg,一天3次,口服)、羅格列酮(4 mg,一天2次,口服)、他司魯肽(10 mg,一周1 次,皮下注射)、西格列汀(100 mg,一天1 次,口服)、胰島素(10~24 U/d,皮下注射)。所有研究療程為12~52 周。2項研究納入患者為不合并糖尿病的肥胖患者[6-7],1項研究納入患者類型是多囊卵巢綜合征患者[17],其余研究納入患者均為2型糖尿病患者。
2.2 納入研究方法學質量評價結果
25項RCT中,16項采用隨機數字表進行隨機分配,判定為低度偏倚[6,8-11,16-19,21-22,24,26-28,30],其他研究均僅在文中提及“隨機”而未進行詳細描述,判定為不清楚。10 項RCT 提及雙盲,判定為低度偏倚[6,8-14,18,21]。1 項RCT 對數據分析者實施盲法,判定為低度偏倚[24]。7項RCT 提及分配隱匿的方法,判定為低度偏倚[8-11,20-21,25]。25 項RCT 均未提及選擇性報道和其他偏倚,判定為不清楚。
2.3 Meta分析結果
2.3.1 體質量變化 23項RCT報道了體質量變化情況[6-14,16-29],按照對照組不同的治療措施進行亞組分析,Meta 分析結果詳見圖1。由圖1可知,艾塞那肽組患者體質量顯著低于安慰劑組[SMD=-2.06,95%CI(-2.97,-1.15),P<0.001]、胰島素組[SMD=-3.51,95%CI(-4.52,-2.51),P<0.001]、格列本脲組[SMD=-3.70,95%CI(-4.28,-3.12),P<0.001]、羅格列酮組[SMD=-1.25,95%CI(-1.71,-0.80),P<0.001]和西格列汀組[SMD=-0.71,95%CI(-0.93,-0.48),P<0.001],而與二甲雙胍組[SMD=-1.39,95%CI(-2.83,0.06),P=0.06]、他司魯肽組[SMD=0.00,95%CI(-0.14,0.14),P=1.00]比較差異無統計學意義。
2.3.2 不良反應發生率 9 項RCT 報道了不良反應發生率[8,10,15-16,20,24-25,28-29]。常見不良反應為惡心、嘔吐、腹瀉、便秘等,癥狀均較輕微,患者可以耐受。按照對照組不同的治療措施進行亞組分析,Meta 分析結果詳見圖2。由圖2 可知,艾塞那肽組患者不良反應發生率顯著高于胰島素組[RR=1.22,95%CI(1.06,1.41),P=0.006],低于他司魯肽組[RR=0.95,95%CI(0.91,0.99),P=0.02],與安慰劑組[RR=1.29,95%CI(0.85,1.96),P=0.23]、二甲雙胍組[RR=1.20,95%CI(0.78,1.85),P=0.41]比較,差異無統計學意義。
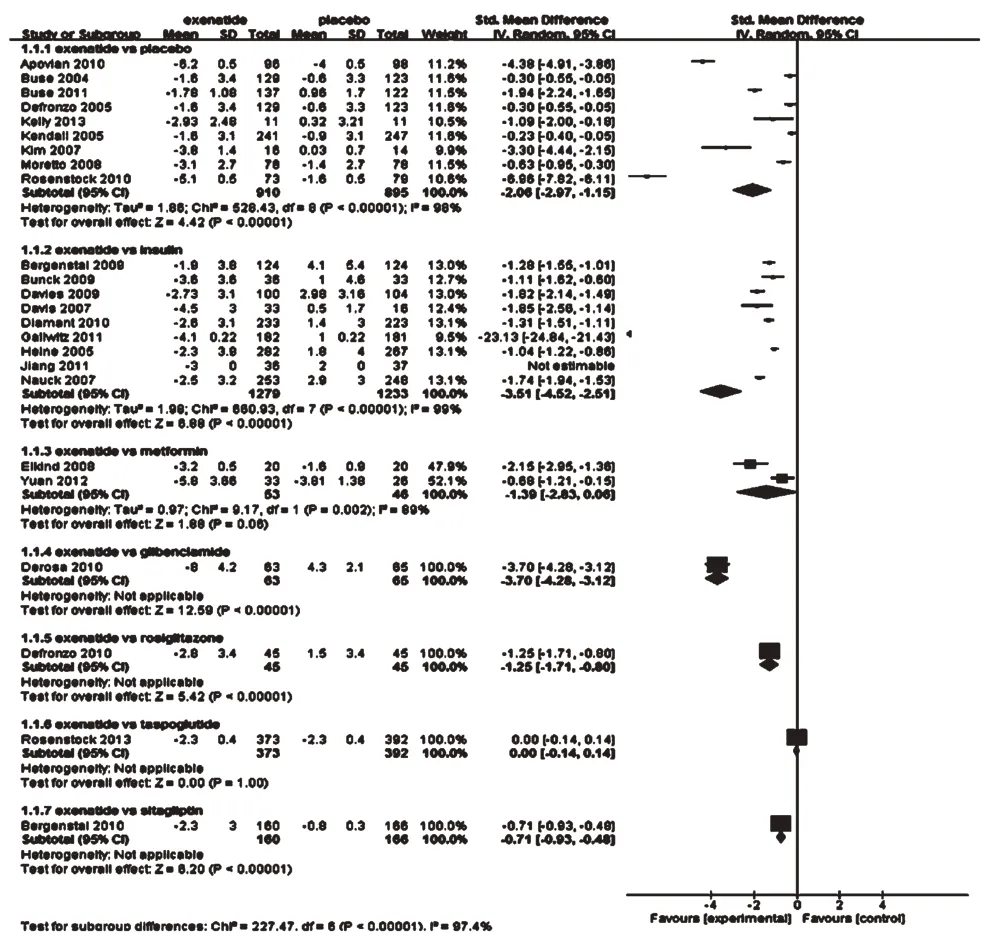
圖1 體質量減少的Meta分析森林圖Fig 1 Forest plot of Meta-analysis of the body mass
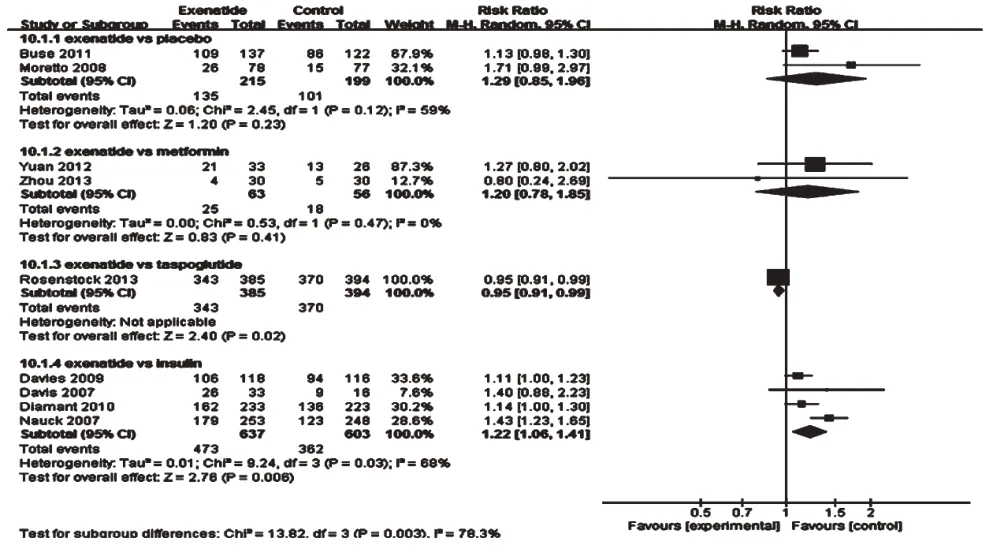
圖2 不良反應發生率的Meta分析森林圖Fig 2 Forest plot of Meta-analysis of the incidences of adverse reactions
2.4 敏感性分析
Meta分析結果顯示,I2≥50%,敏感性分析將固定效應模型改為隨機效應模型,并且根據對照組不同的治療措施作亞組分析,結果均未發生變化,說明本研究結果較為穩定。
3 討論
GLP-1 從腸內釋放入循環后可以增強葡萄糖依賴性胰島素分泌,并顯示出其他抗高血糖藥作用。艾塞那肽為GLP-1類似物,具有降低胃排空速率、促進飽食感等多種生理活性。
本研究首次針對超重和肥胖患者進行評價,納入標準并未局限于2型糖尿病患者,由于艾塞那肽說明書并未批準減質量的適應證,所以研究結論可為臨床艾塞那肽治療超重和肥胖患者提供理論依據。本研究按照RCT對照組治療措施的不同進行亞組分析,對比的治療措施包括安慰劑、胰島素、格列本脲、羅格列酮、二甲雙胍、西格列汀或其他GLP-1 類似物。結果顯示,艾塞那肽對于超重和肥胖患者減質量的治療效果顯著優于安慰劑、胰島素、格列本脲、羅格列酮和西格列汀,而與二甲雙胍、他司魯肽比較差異無統計學意義。提示艾塞那肽降低超重和肥胖患者的體質量是有效的。
安全性方面,本次Meta分析結果顯示,艾塞那肽的不良反應發生率顯著高于胰島素,低于他司魯肽,與安慰劑、二甲雙胍比較差異則無統計學意義。艾塞那肽的不良反應主要表現在消化系統,而這可能與GLP-1 類似物的作用機制有關。2009年和2010年美國食品藥品管理局(FDA)分別警告艾塞那肽注射液的急性胰腺炎風險和腎功能改變風險,而這兩個不良反應在本次評價中均未觀察到。提示艾塞那肽降低超重和肥胖患者的體質量安全性較好。
綜上所述,艾塞那肽能有效降低超重和肥胖患者的體質量,但消化系統不良反應較多。由于納入本次Meta分析的25篇文獻中23篇為國外文獻,研究對象存在種族差異,故艾塞那肽對于我國患者的長期療效和安全性尚需大樣本、高質量的RCT進一步驗證。
[1]Wilding JPH,Hardy K.New drugs for diabetes:glucagon-like peptide lanalogues[J].BMJ,2011,342(2):343.
[2]Jensen MD,Ryan DH,Apovian CM,et al.2013 AHA/ACC/TOS guideline for the management of overweight and obesity in adults:a report of the American college of cardiology/American heart association task force on practice guidelines and the obesity society[J].J Am Coll Cardiol,2014,63(25):2 985.
[3]Higgins JPT,Green S.Cochrane handbook for systematic reviews of interventions version 5.1.0[EBOL](2011-03)[2014-03].http//:www.cochrane-handbook.org.
[4]Higgins JPT,Green S.Cochrane Handbook for Systematic Reviews of Interventions Version 5.0.0[EBOL](2008-02)[2014-03].http//:www.cochrane-handbook.org.
[5]Higgins JPT,Thompson SG.Quantifying heterogeneity in a meta-analysis[J].Stat Med,2002,21(11):1 539.
[6]Kelly AS,Rudser KD,Nathan BM,et al.The effect of glucagon-like peptide-1 receptor agonist therapy on body mass index in adolescents with severe obesity:a randomized,placebo-controlled,clinical trial[J].JAMA Pediatr,2013,167(4):355.
[7]Rosenstock J,Klaff LJ,Schwartz S,et al.Effects of exenatide and lifestyle modification on body weight and glucose tolerance in obese subjects with and without pre-diabetes[J].Diabetes Care,2010,33(6):1 173.
[8]Buse JB,Bergenstal RM,Glass LC,et al.Use of twicedaily exenatide in basal insulin-treated patients with type 2 diabetes:a randomized,controlled trial[J].Ann Intern Med,2011,154(2):103.
[9]Apovian CM,Bergenstal RM,Cuddihy RM,et al.Effects of exenatide combined with lifestyle modification in patients with type 2 diabetes[J].Am J Med.2010,123(5):468.
[10]Moretto TJ,Milton DR,Ridge TD,et al.Efficacy and tolerability of exenatide monotherapy over 24 weeks in antidiabetic drug-naive patients with type 2 diabetes:a randomized,double-blind,placebo-controlled,parallel-group study[J].Clin Ther,2008,30(8):1 448.
[11]Kim D,MacConell L,Zhuang D,et al.Effects of onceweekly dosing of a long-acting release formulation of exenatide on glucose control and body weight in subjects with type 2 diabetes[J].Diabetes Care,2007,30(6):1 487.
[12]Kendall DM,Riddle MC,Rosenstock J,et al.Effects of exenatide(exendin-4)on glycemic control over 30 weeks in patients with type 2 diabetes treated with metformin and a sulfonylurea[J].Diabetes Care,2005,28(5):1 083.
[13]DeFronzo RA,Ratner RE,Han J,et al.Effects of exenatide(exendin-4)on glycemic control and weight over 30 weeks in metformin-treated patients with type 2 diabetes[J].Diabetes Care,2005,28(5):1 092.
[14]Buse JB,Henry RR,Han J,et al.Effects of exenatide(exendin-4)on glycemic control over 30 weeks in sulfonylurea-treated patients with type 2 diabetes[J].Diabetes Care,2004,27(11):2 628.
[15]周巖,吳大方,宋菲菲,等.新診斷肥胖2型糖尿病患者應用艾塞那肽的臨床觀察[J].中國藥物與臨床,2013,13(3):360.
[16]Yuan GH,Song WL,Huang YY,et al.Efficacy and tolerability of exenatide monotherapy in obese patients with newly diagnosed type 2 diabetes:a randomized,26 weeks metformin-controlled,parallel-group study[J].Chin Med J,2012,125(15):2 677.
[17]Elkind-Hirsch K,Marrioneaux O,Bhushan M,et al.Comparison of single and combined treatment with exenatide and metformin on menstrual cyclicity in overweight women with polycystic ovary syndrome[J].J Clin Endocrinol Metab,2008,93(7):2 670.
[18]Derosa G,Maffioli P,Salvadeo SA,et al.Exenatide versus glibenclamide in patients with diabetes[J].Diabetes Technol Ther,2010,12(3):233.
[19]DeFronzo RA,Triplitt C,Qu Y,et al.Effects of exenatide plus rosiglitazone on beta-cell function and insulin sensitivity in subjects with type 2 diabetes on metformin[J].Diabetes Care,2010,33(5):951.
[20]Rosenstock J,Balas B,Charbonnel B,et al.The fate of taspoglutide,a weekly GLP-1 receptor agonist,versus twice-daily exenatide for type 2 diabetes:the T-emerge 2 trial[J].Diabetes Care,2013,36(3):498.
[21]Bergenstal RM,Wysham C,Macconell L,et al.Efficacy and safety of exenatide once weekly versus sitagliptin or pioglitazone as an adjunct to metformin for treatment of type 2 diabetes(DURATION-2):a randomised trial[J].Lancet,2010,376(9 739):431.
[22]蔣建家,牟倫盼,蘇勁波,等.艾塞那肽對口服降糖藥治療欠佳的肥胖2 型糖尿病患者的療效及安全性[J].中華糖尿病雜志,2011,3(4):305.
[23]Gallwitz B,B?hmer M,Segiet T,et al.Exenatide twice daily versus premixed insulin aspart 70/30 in metformin-treated patients with type 2 diabetes:a randomized 26-week study on glycemic control and hypoglycemia[J].Diabetes Care,2011,34(3):604.
[24]Diamant M,van Gaal L,Stranks S,et al.Once weekly exenatide compared with insulin glargine titrated to target in patients with type 2 diabetes(DURATION-3):an open-label randomised trial[J].Lancet,2010,375(9 733):2 234.
[25]Davies MJ,Donnelly R,Barnett AH,et al.Exenatide compared with long-acting insulin to achieve glycaemic control with minimal weight gain in patients with type 2 diabetes:results of the helping evaluate exenatide in patients with diabetes compared with long-acting insulin(HEELA)study[J].Diabetes Obes Metab,2009,11(12):1 153.
[26]Bunck MC,Diamant M,Cornér A,et al.One-year treatment with exenatide improves beta-cell function,compared with insulin glargine,in metformin-treated type 2 diabetic patients:a randomized,controlled trial[J].Diabetes Care,2009,32(5):762.
[27]Bergenstal R,Lewin A,Bailey T,et al.Efficacy and safety of biphasic insulin aspart 70/30 versus exenatide in subjects with type 2 diabetes failing to achieve glycemic control with metformin and a sulfonylurea[J].Curr Med Res Opin,2009,25(1):65.
[28]Nauck MA,Duran S,Kim D,et al.A comparison of twice-daily exenatide and biphasic insulin aspart in patients with type 2 diabetes who were suboptimally controlled with sulfonylurea and metformin:a non-inferiority study[J].Diabetologia,2007,50(2):259.
[29]Davis SN,Johns D,Maggs D,et al.Exploring the substitution of exenatide for insulin in patients with type 2 diabetes treated with insulin in combination with oral antidiabetes agents[J].Diabetes Care,2007,30(11):2 767.
[30]Heine RJ,van Gaal LF,Johns D,et al.Exenatide versus insulin glargine in patients with suboptimally controlled type 2 diabetes:a randomized trial[J].Ann Intern Med,2005,143(8):559.

