阻抗心動描記法在感染性休克患者預后評估中的價值
張 祎,何 淼,趙 娟,趙 鵬,李志延,方 軍
(1.中國石油中心醫(yī)院重癥醫(yī)學科,河北 廊坊065000;2.中國石油中心醫(yī)院急診科,河北 廊坊065000)
感染性休克作為危重癥患者的主要死亡原因一直是重癥醫(yī)學研究的難點和熱點,病死率高達30%~60%,探討影響感染性休克預后的危險因素至關重要[1]。血流動力學監(jiān)測可準確地反映其病情的嚴重程度和生理變化。阻抗心動描記法(impedance cardio graphy,ICG)是一種無創(chuàng)血流動力學監(jiān)測方法,具有無創(chuàng)、方便、經(jīng)濟、準確、及時等優(yōu)點。本研究旨在探討ICG評價感染性休克患者預后的價值。
1 資料與方法
1.1 一般資料 選取2012年1月—2015年2月于中國石油中心醫(yī)院重癥醫(yī)學科住院進行治療的75例感染性休克患者作為研究對象,按入院28d轉(zhuǎn)歸分為存活組和死亡組。存活組35例,男性22例,女性13例,年齡55~72歲,平均(63.91±4.39)歲;其中肺部感染16例,腹腔感染6例,菌血癥6例,顱內(nèi)感染5例,其他感染2例。死亡組40例,男性25例,女性15例,年齡48~72歲,平均(65.50±5.15)歲;其中肺部感染18例,腹腔感染7例,菌血癥6例,顱內(nèi)感染6例,其他感染3例。2組性別、年齡和感染類型差異均無統(tǒng)計學意義(P>0.05),具有可比性。
1.2 診斷與排除標準 2012膿毒癥休克標準[2]:①已有明確或疑似的感染;②符合全身炎性反應綜合征標準,包括體溫>38.3℃或<36℃、心率>90次/min、呼吸頻率>20次/min、血白細胞>12×109/L或<4×109/L或幼稚型細胞>10%;③出現(xiàn)組織灌注不足和器官功能障礙,如乳酸增高、少尿、肌酐升高、血小板減少等;④血流動力學改變,充分補液后,收縮壓<90mmHg或平均動脈壓<70 mmHg或收縮壓下降超過40mmHg。排除標準:①年齡<18周歲;②大面積肺栓塞;③伴有急性心肌梗死或心源性肺水腫;④24h內(nèi)緊急手術。⑤放棄治療。
1.3 方法 所有患者診斷成立后立即予以急性生理和慢性健康(Acute Physiology and Chronic Health Evaluation,APACHE)Ⅱ評分,使用 GEM Premier3000血氣分析儀測定動脈血乳酸,并計算24h乳酸清除率,乳酸清除率=(初始乳酸-24h乳酸)/初始乳酸,應用美國ANALOGIC公司阻抗心動描記監(jiān)護系統(tǒng)監(jiān)測血流動力學參數(shù)。
1.4 觀察指標 監(jiān)測感染性休克患者血流動力學參數(shù),包括平均動脈壓(mean artery pressure,MAP)、心排出量(cardiac output,CO)、心臟指數(shù)(cardiac index,CI)、每搏排出量(stroke volume,SV)、心搏容量指數(shù)(stroke volume index,SVI)、加速指數(shù)(acceleration index,ACI)、左心室射血分數(shù)(left ventricular ejection fraction,LVEF)等。比較2組血流動力學參數(shù)、動脈血乳酸、乳酸清除率、APACHEⅡ評分。
1.5 統(tǒng)計學方法 應用SPSS 17.0軟件進行統(tǒng)計分析。計量資料比較采用t檢驗;計數(shù)資料比較采用χ2檢驗;危險因素分析采用多因素Logistic回歸分析。P<0.05為差異有統(tǒng)計學意義。
2 結(jié) 果
2.1 2組動脈血乳酸、乳酸清除率、APACHEⅡ評分比較 存活組乳酸清除率高于死亡組,APACHEⅡ評分低于死亡組,差異有統(tǒng)計學意義(P<0.05),2組初始動脈血乳酸差異無統(tǒng)計學意義(P>0.05),見表1。
表1 2組血乳酸、乳酸清除率、APACHEⅡ評分比較Table 1 Comparison of blood lactic acid,lactate clearance and APACHEⅡscores in two groups(±s)
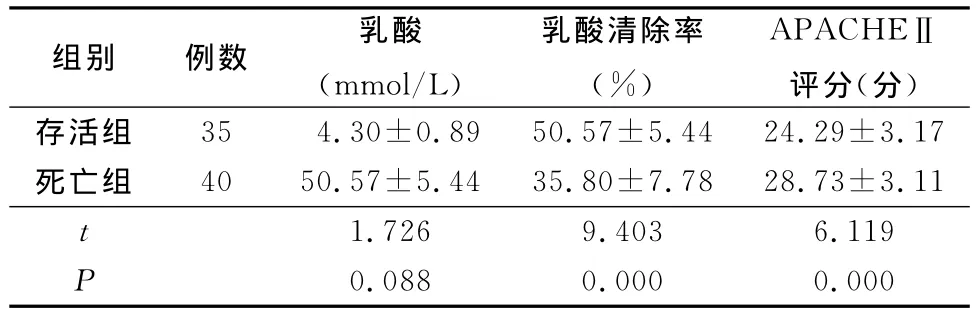
表1 2組血乳酸、乳酸清除率、APACHEⅡ評分比較Table 1 Comparison of blood lactic acid,lactate clearance and APACHEⅡscores in two groups(±s)
組別例數(shù)乳酸(mmol/L)乳酸清除率(%)APACHEⅡ評分(分)存活組35 4.30±0.89 50.57±5.44 24.29±3.17死亡組40 50.57±5.44 35.80±7.78 28.73±3.11 t 1.726 9.403 6.119 P 0.088 0.000 0.000
2.2 2組血流動力學指標比較 存活組心排出量、心臟指數(shù)、每搏排出量、心搏容量指數(shù)、左心室射血分數(shù)、加速指數(shù)高于死亡組,差異有統(tǒng)計學意義(P<0.05),2組平均動脈壓差異無統(tǒng)計學意義(P>0.05),見表2。
表2 2組血流動力學參數(shù)比較Table 2 Comparison of hemodynamics in two groups(±s)
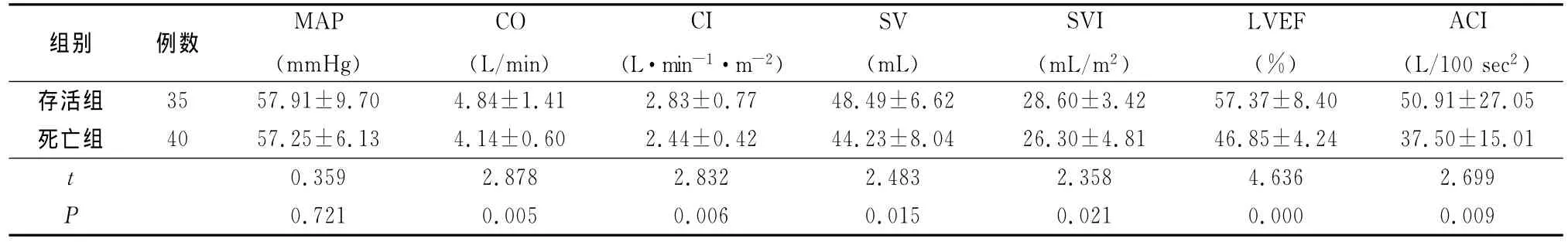
表2 2組血流動力學參數(shù)比較Table 2 Comparison of hemodynamics in two groups(±s)
組別例數(shù)MAP(mmHg)CO(L/min)CI(L·min-1·m-2)SV(mL)SVI(mL/m2)LVEF(%)ACI(L/100sec2)存活組35 57.91±9.70 4.84±1.41 2.83±0.77 48.49±6.62 28.60±3.42 57.37±8.40 50.91±27.05死亡組40 57.25±6.13 4.14±0.60 2.44±0.42 44.23±8.04 26.30±4.81 46.85±4.24 37.50±15.01 t 0.359 2.878 2.832 2.483 2.358 4.636 2.699 P 0.721 0.005 0.006 0.015 0.021 0.000 0.009
2.3 Logistic回歸分析 以患者是否死亡為因變量(死亡=1,存活=2),APACHEⅡ評分(連續(xù)變量)、乳酸清除率(連續(xù)變量)、CO(連續(xù)變量)、CI(連續(xù)變量)、SV(連續(xù)變量)、SI(連續(xù)變量)、LVEF(連續(xù)變量)、ACI(連續(xù)變量)為自變量,進行二元Logistic回歸分析,得出乳酸清除率、LVEF為感染性休克患者死亡的獨立影響因素,見表3。

表3 Logistic回歸分析Table 3 Logistic regression analysis
3 討 論
感染性休克是重癥醫(yī)學科患者最常見的死亡原因,病理生理基礎是以全身炎癥反應為基礎,導致組織灌注不足、器官微循環(huán)障礙、通透性增加、血容量減少,組織氧輸送和氧利用下降等[3]。感染性休克病死率居高不下,本研究病死率約53.3%,與目前研究基本一致,研究影響感染性休克預后的因素非常重要。
ICG建立在電傳導的基礎上,主要測量由胸主動脈和上下腔靜脈所產(chǎn)生的電流,隨著心臟的收縮與舒張,電阻抗也隨血流量變化而變化。ICG比超聲心動圖更全面,與有創(chuàng)監(jiān)測方法SWAN-GANS導管相比有良好的相關性。文獻報道,早期使用ICG監(jiān)護系統(tǒng)可以減輕患者因循環(huán)障礙和組織灌注不足引起的損害[4]。
本研究顯示存活組APACHEⅡ評分低于死亡組,乳酸清除率高于死亡組,差異有統(tǒng)計學意義,2組初始血乳酸差異無統(tǒng)計學意義;存活組通過ICG監(jiān)測獲得的CO、CI、SV、SVI、ACI、LVEF等血流動力學參數(shù)優(yōu)于死亡組,差異有統(tǒng)計學意義。心排出量是機體發(fā)生變化的早期預警;心臟指數(shù)反映心臟功能狀況;每搏排出量反映心肌收縮力指標,排除心率影響,比心排出量更能反映心臟功能;左心室射血分數(shù)是反映心臟收縮功能的重要指標;加速指數(shù)反映心臟收縮時血流在主動脈內(nèi)的最大加速度,與心排出量相比可排除血流量因素,更能反映心肌收縮力和心功能狀況[5]。提示心功能抑制的患者病死率升高。同時根據(jù)感染性休克指南要求,需要使用液體復蘇、血管收縮藥物(去甲腎上腺素)、正性肌力藥物等維持足夠的心排出量和灌注壓。通過血流動力學監(jiān)測,可以指導上述液體復蘇、血管活性藥物等的使用,隨時根據(jù)監(jiān)測結(jié)果優(yōu)化治療方案。因此,我們認為通過ICG監(jiān)測血流動力學參數(shù)在指導對癥治療的同時,有利于評價預后。本研究二元Logistic回歸分析顯示,乳酸清除率、左心室射血分數(shù)為感染性休克患者死亡的獨立影響因素。血乳酸水平可反映患者組織灌注情況,即刻血乳酸只是反映當時組織氧供與氧耗的關系,乳酸清除率可揭示組織和細胞氧代謝的動態(tài)變化情況,及時了解感染性休克患者內(nèi)環(huán)境和組織細胞代謝情況以及機體對治療的反應性,評價臨床治療的有效性,比單一的血乳酸更有意義,可作為評價感染性休克預后的獨立影響因素,這一點與目前研究一致[6-7]。APACHEⅡ評分比較客觀的反映患者生理參數(shù)的紊亂程度,已廣泛應用于危重癥患者評估,雖未能作為感染性休克預后的獨立影響因素,但本研究死亡組APACHEⅡ評分明顯高于存活組(P<0.05),因而APACHEⅡ評分也可作為判定預后的一個重要影響因素[8]。本研究得出左心室射血分數(shù)是除乳酸清除率外又一獨立影響因素。一直以來在感染性休克研究中更重視血管功能不全,即血管麻痹[9]。近期越來越多的研究顯示,感染性休克患者多合并心功能不全,且多出現(xiàn)在感染性休克的早期,感染性休克時心功能不全和血管功能不全同樣重要。感染性休克的死亡原因為心血管崩潰或頑固的低血壓。心血管系統(tǒng)在感染性休克病理生理機制中起著重要作用,近期研究為感染性休克心功能不全提供了大量的證據(jù),認為應重視心功能惡化對預后的影響[10]。心功能尤其是左心室功能是感染性休克患者血流動力學改變的重要環(huán)節(jié),文獻報道感染性休克患者會出現(xiàn)不同形式的心功能抑制,原因可能為白細胞介素(interleukin,IL)-6等炎癥因子引起心肌損傷。膿毒癥患者血清中IL-6升高,其水平與膿毒癥嚴重程度相關,IL-6可抑制心肌收縮力,與左心室收縮功能呈負相關。IL-6對心肌收縮力的抑制作用可能與抑制心肌興奮-收縮偶聯(lián)過程有關,可使心肌興奮時鈣瞬變峰值降低,使肌漿網(wǎng)釋放鈣離子減少,活化肌橋數(shù)目減少,從而造成心肌收縮力減低,左心室收縮功能受損[11]。患者左心室射血分數(shù)、心臟做功及其效率明顯下降,乳酸清除率下降,乳酸水平相對升高,組織灌注惡化,病死率升高。心排出量和每搏排出量未明顯降低時,已出現(xiàn)心肌收縮功能減低,左心室射血分數(shù)下降。感染性休克時為保持較高水平的心臟指數(shù),左心室舒張末容積增大,心室腔代償性擴大,即使每搏排出量和心率增加,心肌抑制仍是存在的,左心室射血分數(shù)呈不同程度下降。心室腔擴大認為是可逆的,一般恢復時間7~10d,但并非所有患者均可安全度過這個時期,射血分數(shù)下降程度導致病死率增加。而心肌細胞損傷導致的心肌收縮功能減低,可加重血流動力學紊亂,更促進休克和多器官功能衰竭發(fā)生,導致心功能進一步惡化,加劇對預后的不良影響。心功能不全是感染性休克患者體內(nèi)重要臟器灌注不足和死亡的主要原因。合并心功能抑制的感染性休克患者病死率為70%,而無心功能抑制的病死率只有20%。感染性休克早期,心室收縮功能下降是引起心臟對液體復蘇反應性減低的主要原因[12-13]。左心室射血分數(shù)受到心臟前后負荷、心率、心肌收縮性等多因素的影響,是多種因素綜合作用的結(jié)果,因而左心室射血分數(shù)與預后的關系明顯優(yōu)于心排出量等其他心功能指標,可作為評價感染性休克預后的獨立影響因素。ICU住院患者多高齡,合并多種基礎疾病,心臟貯備功能下降,往往不只是心功能抑制而是感染性休克基礎上合并心功能不全,此時左心室射血分數(shù)對預后的判定更為有意義,考慮這也是本研究患者病死率高的原因。
綜上所述,通過ICG監(jiān)測患者的血流動力學參數(shù),與乳酸清除率等一樣,可以達到指導治療、評價預后的作用。
[1] Glassford NJ,Eastwood GM,Bellomo R,et al.Physiological changes after fluid bolus therapy in sepsis:a systematic review of contemporary data[J].Crit Care,2014,18(6):696.
[2] Dellinger RP,Levy MM,Rhodes A,et al.Surviving Sepsis Campaign:international guidelines for management of severe sepsis and septic shock,2012[J].Intensive Care Med,2013,39(2):165-228.
[3] O'Neill R,Morales J,Jule M,et al.Early Goal-directed therapy for severe sepsis/septic shock:which components of treatment are more difficult to implement in a communitybased emergency department?[J].J Emerg Med,2012,42(5):503-510.
[4] 王華東,曹文杰,張民,等.早期液體復蘇對感染性休克患者血流動力學的影響[J].現(xiàn)代生物醫(yī)學進展,2013,13(25):4929-4931,4912.
[5] Weyer S,Menden T,Leicht L,et al.Development of a wearable multi-frequency impedance cardiography device[J].J Med Eng Technol,2015,39(2):131-137.
[6] Odom SR,Howell MD,Silva GS,et al.Lactate clearance as a predictor of mortality in trauma patients[J].J Trauma Acute Care Surg,2013,74(4):999-1004.
[7] 楊芳,閆芳.血乳酸水平和乳酸清除率對感染性休克患者預后的評估[J].實用臨床醫(yī)藥雜志,2014,18(16):44-46.
[8] 馬建齊,白靜慧,蔣雷,等,乳酸與APACHEⅡ評分對感染性休克患者預后影響的分析[J].中國醫(yī)藥導報,2013,10(31):166-168.
[9] No authors listed.Vasoplegia in septic shock(review)[J].Georgian Med News,2015,(239):56-62.
[10] Gamkrelidze M,Intskirveli N,Vardosanidze K,et al.Myocardial dysfunction during septic shock[J].Georgian Med News,2014,(237):40-46.
[11] Wong HR,Walley KR,Pettil? V,et al.Comparing the prognostic performance of ASSIST to interleukin-6and procalcitonin in patients with severe sepsis or septic shock[J].Biomarkers,2015,20(2):132-135.
[12] 馬馳騁,劉愛軍,張慧明,等.無創(chuàng)血流動力學監(jiān)測手段在重癥患者液體管理中的應用[J].海南醫(yī)學,2015,26(3):404-405.
[13] Sasai T,Tokioka H,F(xiàn)ukushima T,et al.Reliability of central venous pressure to assess left ventricular preload for fluid resuscitation in patients with septic shock[J].J Intensive Care,2014,2(1):58.

