首發(fā)抑郁癥患者邊緣系統(tǒng)PET-CT葡萄糖代謝水平及磁共振T2值變化研究
藍 杰,朱 彥,王冬青
(1.丹徒區(qū)第三人民醫(yī)院影像科,江蘇鎮(zhèn)江212003;2.江蘇大學附屬醫(yī)院影像科,江蘇鎮(zhèn)江212001)
首發(fā)抑郁癥患者邊緣系統(tǒng)PET-CT葡萄糖代謝水平及磁共振T2值變化研究
藍 杰1,朱 彥2,王冬青2
(1.丹徒區(qū)第三人民醫(yī)院影像科,江蘇鎮(zhèn)江212003;2.江蘇大學附屬醫(yī)院影像科,江蘇鎮(zhèn)江212001)
目的 探究首發(fā)抑郁癥邊緣系統(tǒng)神經(jīng)細胞的葡萄糖代謝水平及豫馳時間(T2)變化情況。方法 采用正電子發(fā)射計算機斷層顯像(PET-CT)掃描及高場MRI(T2WI序列)分別對20例健康受試者(健康組)及20例首發(fā)抑郁癥患者(首發(fā)抑郁組)進行檢查,檢測邊緣系統(tǒng)腦區(qū)的最大標準攝取值(SUVmax)及MRIT2值。結果 與健康組比較,首發(fā)抑郁組患者左側(cè)海馬和左側(cè)杏仁核的SUVmax及T2值均降低,差異有統(tǒng)計學意義(P<0.05),右側(cè)海馬杏仁核的SUVmax及T2值未出現(xiàn)變化,差異無統(tǒng)計學意義(P>0.05);與健康組比較,首發(fā)抑郁組患者左側(cè)前扣帶回的SUVmax升高,差異有統(tǒng)計學意義(P<0.05),右側(cè)前扣帶回的SUVmax及T2值未見變化,差異無統(tǒng)計學意義(P>0.05)。結論 首發(fā)抑郁癥患者的邊緣系統(tǒng)神經(jīng)細胞受損體現(xiàn)在神經(jīng)細胞的數(shù)目、完整性及對能量的攝取利用上,這些損害是抑郁癥發(fā)生發(fā)展的一個重要機制。
抑郁癥; 腦/解剖學和組織學; 體層攝影術,發(fā)射型計算機; 邊緣系統(tǒng); 葡萄糖,代謝; 病例對照研究
抑郁癥是較為常見的一種精神類疾病,嚴重影響人們的正常生活及社交,癥狀較重者有自殺傾向。首發(fā)抑郁癥患者因為初次發(fā)病,且未經(jīng)治療或復發(fā),較其他類型抑郁癥有更好的機制研究性。廣泛研究表明,首發(fā)抑郁癥與情感調(diào)節(jié)的重要系統(tǒng)——邊緣系統(tǒng)的神經(jīng)細胞功能損害有關,其損害不僅僅是神經(jīng)細胞數(shù)目與完整性的缺失,也包括完整的神經(jīng)細胞對能量攝取利用的功能改變。以往的臨床研究很難對這些改變有客觀的數(shù)據(jù)研究及合適的觀察手段。本研究通過先進的正電子發(fā)射計算機斷層顯像(PET-CT)及高場MRI設備對邊緣系統(tǒng)腦區(qū)分別進行葡萄糖代謝水平、神經(jīng)細胞數(shù)目及完整性檢測,客觀地取得大腦邊緣系統(tǒng)神經(jīng)細胞功能變化的基本資料,為首發(fā)抑郁癥患者的臨床研究及診治提供幫助。
1 資料與方法
1.1 一般資料 收集2011年4月至2014年4月江蘇省鎮(zhèn)江市丹徒區(qū)第三人民醫(yī)院及江蘇大學附屬醫(yī)院精神科門診抑郁癥患者的臨床資料,根據(jù)漢米爾頓抑郁量表評分選擇首發(fā)抑郁癥患者20例作為首發(fā)抑郁組,均未經(jīng)過抗抑郁藥物干預及電休克治療。排除標準:(1)其他精神障礙或藥物依賴;(2)患有嚴重的軀體疾病或有嚴重藥物過敏史;(3)曾患腦部器質(zhì)性疾病或其他可能影響腦部結構與功能的疾病;(4)近期使用影響腦血管功能藥物者。入選的20例患者中男9例,女11例;年齡 16~41歲,平均(27±3)歲;受教育年限9~16年,平均(14±3)年;身高150~179 cm,平均(159±14)cm;體質(zhì)量44~82 kg,平均(61±12)kg;均為右利手。另選擇同期20例健康志愿者作為健康組,均來自于醫(yī)院職工或其家屬,其中男9例,女11例;年齡22~40歲,平均(29±7)歲;受教育年限8~19年,平均(14±2)年;身高158~178 cm,平均(163±24)cm,體質(zhì)量42~82 kg,平均(56±8)kg,均為右利手。兩組性別、年齡、身高等一般資料比較,差異均無統(tǒng)計學意義(P>0.05)。本研究經(jīng)醫(yī)院倫理委員會批準,全部受試者對本研究項目知情,并簽署知情同意書。
1.2 方法
1.2.1 PET-CT掃描檢查 受試者檢查前24 h禁煙酒,12 h內(nèi)禁食,檢查前夜保證充足睡眠,需要服用苯二氮類藥物者前晚8:00之前用藥。顯像方法:每位受檢者靜脈注射18氟-氟代脫氧葡萄糖(18F-FDG)約5mCi(1Ci= 3.7×1010Bq),注射前測量血糖。注射后保持靜息狀態(tài)30min,塞耳、閉眼,以減少聲光刺激。18F-FDG用加拿大EBCO TR19型醫(yī)用回旋加速器制得,合成效率70%,18F-FDG放射化學純度大于95%。患者保持平靜呼吸,PET顯像采用3D采集模式,1個窗位,計15min。經(jīng)衰減校正后行迭代法重建,獲得橫斷、矢狀、冠狀面CT、PET及PET-CT融合圖像,層厚5mm。圖像后處理使用最新的Syngo True D VE12A工作站,所有圖像均由2~3位有經(jīng)驗的影像醫(yī)生共同閱片,對18F-FDG PET-CT顯像結果進行分析,仔細觀察解剖結構,在橫斷面上選取邊緣系統(tǒng)主要腦區(qū)結構(主要包括海馬、杏仁核及前扣帶回),勾勒感興趣區(qū)(ROI),直徑范圍5~10mm,得出最大標準攝取值(SUVmax)。所有數(shù)據(jù)統(tǒng)一光盤儲存,以便同一時間進行分析統(tǒng)計。
1.2.2 高場MRI掃描檢查 受試者由專業(yè)醫(yī)護人員對其進行檢查前的解釋及情緒安撫工作,并讓其靜坐休息30min,強調(diào)檢查時嚴格遵守檢查技師的囑咐和要求。采用SiemensMagnetom Trio Tim 3.0T高場磁共振成像系統(tǒng)及8通道頭顱專用線圈對受試者進行掃描。定位于正中矢狀面,作平行于腦干長軸的冠狀斜切面掃描。采用T2WI序列掃描,掃描參數(shù):TR 3500ms,TE 135ms,激勵次數(shù)(NEX)2,視野(FOV)230mm×230mm,矩陣256×192,層厚1.0mm,無間隔。掃描數(shù)據(jù)經(jīng)收集后存入光盤,以備在工作站中進行統(tǒng)一處理,處理過程中利用隨機LEONARDO程序進行基線、相位校正,并在邊緣系統(tǒng)主要腦區(qū)勾勒ROI,由2~3位有經(jīng)驗的影像醫(yī)生共同測量其內(nèi)平均豫弛時間(T2值)。
1.3 統(tǒng)計學處理 測得數(shù)據(jù)符合正態(tài)分布,應用Stata 12.0統(tǒng)計軟件進行數(shù)據(jù)分析,計量資料以±s表示,采用t檢驗,P<0.05為差異有統(tǒng)計學意義。
2 結 果
2.1 兩組雙側(cè)海馬SUVmax與T2值比較 與健康組比較,首發(fā)抑郁組患者左側(cè)海馬的SUVmax及T2值均出現(xiàn)下降,差異均有統(tǒng)計學意義(P<0.05)。右側(cè)海馬的SUVmax及T2值未出現(xiàn)變化,差異無統(tǒng)計學意義(P>0.05)。見表1。
表1 兩組雙側(cè)海馬SUVmax與T2值比較(±s)
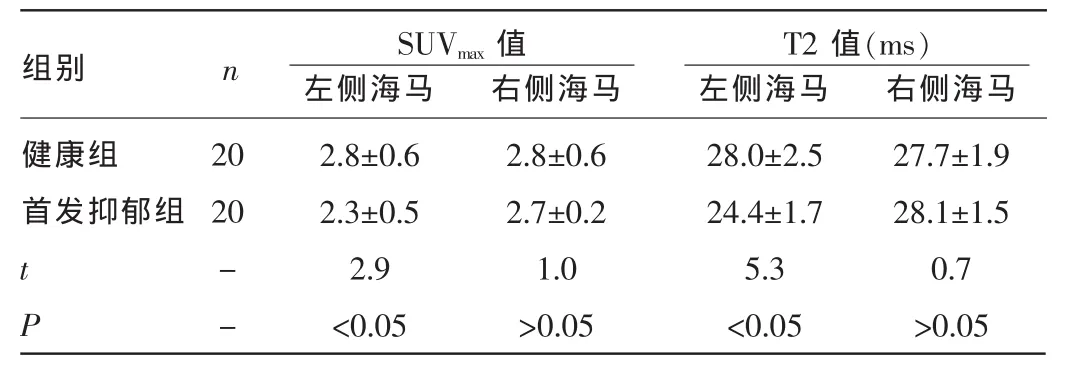
表1 兩組雙側(cè)海馬SUVmax與T2值比較(±s)
注:-表示無此項。
組別n SUVmax值左側(cè)海馬 右側(cè)海馬T2值(ms)左側(cè)海馬 右側(cè)海馬健康組首發(fā)抑郁組27.7±1.9 28.1±1.5 0.7>0.05 20 20 t P --2.8±0.6 2.3±0.5 2.9<0.05 2.8±0.6 2.7±0.2 1.0>0.05 28.0±2.5 24.4±1.7 5.3<0.05
2.2 兩組雙側(cè)杏仁核的SUVmax與T2值比較 與健康組比較,首發(fā)抑郁組患者左側(cè)杏仁核的SUVmax及T2值均下降,差異有統(tǒng)計學意義(P<0.05)。右側(cè)杏仁核的SUVmax及T2值未出現(xiàn)變化,差異無統(tǒng)計學意義(P>0.05)。見表2。
表2 兩組雙側(cè)杏仁核SUVmax與T2值比較(±s)

表2 兩組雙側(cè)杏仁核SUVmax與T2值比較(±s)
注:-表示無此項。
組別n SUVmax值左側(cè)杏仁核 右側(cè)杏仁核T2值(ms)左側(cè)杏仁核 右側(cè)杏仁核健康組首發(fā)抑郁組28.5±1.7 27.6±1.9 1.6>0.05 20 20 t P --2.9±0.4 2.2±0.6 4.3<0.05 3.1±0.6 2.9±0.3 1.3>0.05 30.4±1.8 25.6±2.0 8.0<0.05
2.3 兩組雙側(cè)前扣帶回的SUVmax與T2值比較 相對于健康組,首發(fā)抑郁組患者左側(cè)前扣帶回的SUVmax升高,差異有統(tǒng)計學意義(P<0.05)。左側(cè)前扣帶回的T2值未變化,右側(cè)前扣帶回的SUVmax及T2值未出現(xiàn)變化,差異均無統(tǒng)計學意義(P>0.05)。見表3。
表3 兩組雙側(cè)前扣帶回SUVmax與T2值比較(±s)
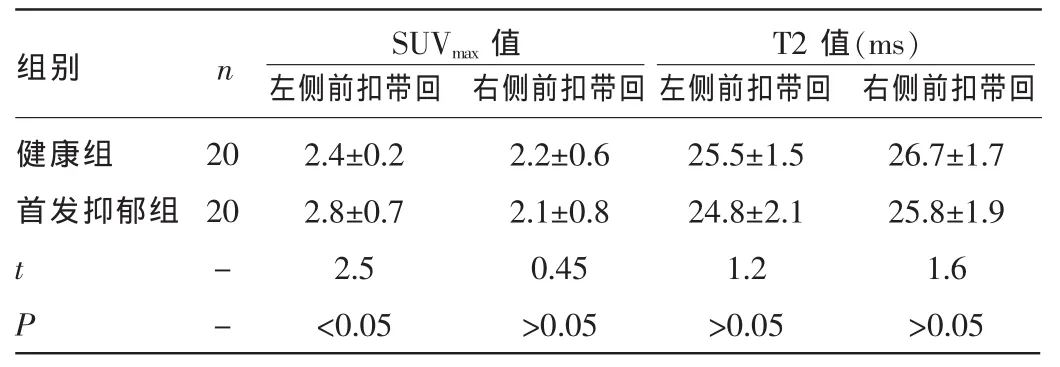
表3 兩組雙側(cè)前扣帶回SUVmax與T2值比較(±s)
注:-表示無此項。
組別n SUVmax值左側(cè)前扣帶回 右側(cè)前扣帶回T2值(ms)左側(cè)前扣帶回 右側(cè)前扣帶回健康組首發(fā)抑郁組t P 2.2±0.6 2.1±0.8 0.45>0.05 20 20 --2.4±0.2 2.8±0.7 2.5<0.05 25.5±1.5 24.8±2.1 1.2>0.05 26.7±1.7 25.8±1.9 1.6>0.05
3 討 論
3.1 PET-CT與高場MRI結合研究抑郁癥的優(yōu)勢 抑郁癥已成為如今發(fā)病率較高的精神疾病之一,其臨床表現(xiàn)以持續(xù)性的情緒低落、興趣減低為主要癥狀[1],診斷手段較為單一主觀。抑郁癥發(fā)病機制雖尚未明了,但大腦邊緣系統(tǒng)的結構功能異常是公認的疾病發(fā)生的一個重要環(huán)節(jié)[2],包括各腦區(qū)核團的形態(tài)異常、細胞代謝功能的異常及腦區(qū)之間的鏈接異常。如今研究抑郁癥患者腦結構與功能變化的手段較多,但均存在一定的劣勢。高分辨率PET-CT能夠清晰顯示出大腦各核團及重要聯(lián)絡腦區(qū)形態(tài),能夠從分子影像水平對抑郁癥的腦結構及功能進行研究[3]。高場MRI的T2值測量也是從分子層面對邊緣系統(tǒng)腦區(qū)的神經(jīng)細胞數(shù)目及完整性進行觀察[4]。將2種方法結合起來研究,能夠彌補影像研究方法中手段單一的不足,能夠分別以神經(jīng)細胞的數(shù)目、完整性及神經(jīng)細胞的功能代謝為出發(fā)點,取長補短,共同研究抑郁癥患者邊緣系統(tǒng)的影像學表現(xiàn)異常并探討可能的機制。
3.2 PET-CTSUVmax變化的意義 本研究發(fā)現(xiàn),在所選擇的邊緣系統(tǒng)中,首發(fā)抑郁組患者左側(cè)海馬、左側(cè)杏仁核的SUVmax出現(xiàn)了降低,而左側(cè)扣帶回的SUVmax則出現(xiàn)升高。SUV值代表著該細胞組織對葡萄糖的攝取量[5-6],即對能量的運用能力,一般在細胞興奮或激活狀態(tài)下有明顯升高。本組PET-CT結果提示,邊緣系統(tǒng)各個腦神經(jīng)區(qū)細胞的葡萄糖攝取出現(xiàn)了異常,表明所選ROI的神經(jīng)細胞在功能上出現(xiàn)了紊亂。左側(cè)海馬及左側(cè)杏仁核的神經(jīng)細胞對能量的利用出現(xiàn)了降低,神經(jīng)活動隨即降低,包括細胞的新陳代謝,對遞質(zhì)的攝取、運輸及信息的傳遞[7]。這些改變影響了海馬及杏仁核的情感調(diào)節(jié)功能及與其相應聯(lián)絡腦區(qū)的聯(lián)系活性,使情感調(diào)節(jié)能力下降,神經(jīng)細胞對能量的攝取降低同樣也導致了細胞本身的活性降低、代謝緩慢,從而引起抑郁癥患者對事物興趣的減低及學習記憶能力的下降,出現(xiàn)消極、健忘及自殺傾向等臨床癥狀[8]。而對于左側(cè)扣帶回的SUVmax升高,作者認為與邊緣系統(tǒng)各腦區(qū)對情感調(diào)節(jié)能力的代償有關,扣帶回具有對其他邊緣系統(tǒng)核團功能損失的一種代償、支持作用。由于多個研究已證實大腦功能存在著優(yōu)勢半球[9],故本研究發(fā)現(xiàn)的變化多出自于左側(cè)大腦半球。
3.3 高場MRI中T2值變化的意義 T2值降低在中樞神經(jīng)系統(tǒng)中代表著神經(jīng)細胞含水量減少及鐵沉積增多,細胞的壞死形成其內(nèi)鐵元素的釋放及沉積,同時細胞的枯萎凋亡引起腦區(qū)含水量的下降,側(cè)面反映了正常神經(jīng)細胞的數(shù)目及完整性[10]。本研究結果顯示,所測邊緣系統(tǒng)中只有左側(cè)海馬及左側(cè)杏仁核的T2值出現(xiàn)了明顯降低,其他腦區(qū)未出現(xiàn)明顯變化,揭示在首發(fā)抑郁癥發(fā)病中,左側(cè)海馬及左側(cè)杏仁核的神經(jīng)細胞出現(xiàn)了數(shù)目減少及完整性缺失,這些細胞的凋亡及損害導致該功能腦區(qū)的調(diào)節(jié)障礙[11]。海馬及杏仁核屬于邊緣系統(tǒng)對情感調(diào)節(jié)過程中最核心的部分,其神經(jīng)細胞損害成為邊緣系統(tǒng)功能異常的一個重要因素。由于扣帶回一定的代償功能,在早期首發(fā)抑郁癥中,其內(nèi)的神經(jīng)細胞功能變化不太明顯,隨著抑郁癥的加重或復發(fā),扣帶回神經(jīng)細胞的形態(tài)功能或許會存在較大改變,需要進一步地對各種其他類型抑郁癥進行比較研究。
結合PET-CTSUVmax及MRI中T2值變化來看,通過這些數(shù)據(jù)對首發(fā)抑郁癥進行一定程度的影像學診斷,可為臨床診斷提供一個新穎的、可靠的技術手段。研究結果同時提示,在抑郁癥的發(fā)病機制中,邊緣系統(tǒng)的左側(cè)海馬及左側(cè)杏仁核神經(jīng)細胞不僅出現(xiàn)數(shù)目及完整性的降低,同時也出現(xiàn)了對能量運用的障礙[12],這個過程是彼此相疊的,容易加劇抑郁癥的發(fā)展。
[1]Wu F,Tang Y,Xu K,et al.Whitermatter abnormalities inmedicationnaive subjectswith a single short-duration episode ofmajor depressive disorder[J].Psychiatry Res,2011,191(1):80-83.
[2]Piser TM.Linking the cytokine and neurocircuitry hypothesesof depression:a translational framework for discovery and development of novel anti-depressants[J].Brain Behav Immun,2010,24(4):515-524.
[3]HerholzK.Use of FDGPETasan imaging biomarker in clinical trialsof Alzheimer′sdisease[J].Biomark Med,2012,6(4):431-439.
[4]Weber K,Giannakopoulos P,Delaloye C,etal.Personality traits,cognition and volumetric MRIchanges in elderly patientswith early-onset depression:a2-year follow-up study[J].Psychiatry Res,2012,198(1):47-52.
[5]Zuo C,Ma Y,Sun B,etal.Metabolic imaging of bilateral anterior capsulotomy in refractory obsessive compulsive disorder:an FDGPETstudy[J]. JCereb Blood Flow Metab,2013,33(6):880-887.
[6]CaroliA,Prestia A,Chen K,etal.Summarymetrics to assess Alzheimer disease-related hypometabolic pattern with 18F-FDG PET:head-to-head comparison[J].JNuclMed,2012,53(4):592-600.
[7]Illi J,MiaskowskiC,Cooper B,etal.Association between pro-and antiinflammatory cytokinegenesand a symptom cluster of pain,fatigue,sleep disturbance,and depression[J].Cytokine,2012,58(3):437-447.
[8]Einvik G,VistnesM,Hrubos-Str?m H,etal.Circulating cytokine concentrationsarenotassociated withmajor depressive disorder in a communitybased cohort[J].Gen Hosp Psychiatry,2012,34(3):262-267.
[9]Simon NM,McNamara K,Chow CW,etal.A detailed examination of cytokine abnormalities in Major Depressive Disorder[J].Eur Neuropsychopharmacol,2008,18(3):230-233.
[10]Fox MD,Buckner RL,White MP,etal.Efficacy of transcranialmagnetic stimulation targets for depression is related to intrinsic functional connectivitywith the subgenual cingulate[J].Biol Psychiatry,2012,72(7):595-603.
[11]AlexopoulosGS,Hoptman MJ,KanellopoulosD,etal.Functional connectivity in the cognitive control network and the defaultmode network in late-lifedepression[J].JAffectDisord,2012,139(1):56-65.
[12]Yüksel C,?ngür D.Magnetic resonance spectroscopy studies ofglutamaterelated abnormalities inmood disorders[J].Biol Psychiatry,2010,68(9):785-794.
PET-CT glucosemetabolism level and magnetic resonance T2 values changes in the limbic system of first-episode depression patients
Lan Jie1,Zhu Yan2,Wang Dongqing2
(1.DepartmentofMedical Imaging,Dantu DistrictNo.3 People′s Hospital,Zhenjiang,Jiangsu 212003,China;2.Department of Medical Imaging,the Affiliated Hospital of Jiangsu University,Zhenjiang,Jiangsu 212001,China)
Objective To study the first-episode depression limbic system changesofglucosemetabolism ofnerve cells and T2 signal changes.M ethods Using PET-CT and MRI(T2WIseries)to scan 20 first episode depression patients(the first episode group)and 20 healthy examinees(the healthy group),detecting the SUVmaxand T2 valuesby MRIof the limbic systemrespectively.Results Compared to thehealthy group,the SUVmaxand T2 valuesof lefthippocampusand amygdaloid nucleusof first episode depression patientswas reduced significantly,whose difference had statistical significance(P<0.05).The SUVmaxand T2 values of righthippocampus and amygdaloid nucleus had no change.Ithad no statisticalsignificance in difference(P>0.05);The SUVmaxvalue of left anterior cingutate of first episode depression patientswas increased,whose difference had statistical signifi cance(P<0.05).Therewas no change in the SUVmaxof the rightanterior cingulate cortex or T2 value by MRI.Ithad no statistical significance in difference(P>0.05).Conclusion The nerve cells in limbic system of the first-episode depression patients have been damaged,reflecting in number,integrity of nerve cells and in take and utilization ofenergy.These damage become an importantmechanism of the developmentin depression.
Depressive disorder; Brain/anatomy&histology; Tomography,X-ray computed; Limbic system;Glucose,metabolism; Case-controlstudies
10.3969/j.issn.1009-5519.2015.09.003
A
1009-5519(2015)09-1287-03
2014-12-05)
藍杰(1977-),男,江蘇鎮(zhèn)江人,主治醫(yī)師,主要從事中樞影像診斷工作;E-mail:17712823062@189.com。
朱彥(E-mail:salary_hi@126.com)。

