40例結直腸癌肝轉移手術前應用新輔助化療效果觀察
丁祥林
結直腸癌是嚴重威脅人類生命安全的惡性腫瘤之一,據相關文獻[1]統計結果顯示,該疾病致死率在美國的所有惡性腫瘤中位居第二,而在中國則位居第五,近些年發生率逐年增長,越來越引起人們的重視。結直腸癌致死的患者中大約50%是因為腫瘤發生了轉移,這其中70%發生了肝轉移[2]。目前外科手術治療是最主要的手段,患者的5年存活率與接受手術的時間呈顯著的負相關性,但在患者初次就診時能接受根治性手術的通常不超過15%[3]。結直腸癌發展至晚期后往往病情極為復雜,此時如何增加根治性手術的切除率以及術后的復發率成為關注的焦點。有研究顯示新輔助化療能為根治性手術的實施爭取機會,但目前國內相關資料較少,筆者自2013年7月-2015年7月期間采用新輔助化療治療結直腸癌肝轉移,現將相關情況報告如下,為臨床治療提供參考。
1 資料與方法
1.1 一般資料 選取2013年7月-2015年7月期間于蘇州永鼎醫院腫瘤科收治的結直腸癌肝轉移患者共40例,其中男21例,女19例,年齡32~72歲,平均年齡(55.1±10.3)歲。腫瘤原發部位:結腸者共23例,直腸者17例,腫瘤轉移至肝后均為多發灶。新輔助化療方案:單純FOLFIRI方案者3例,FOLFOX6方案者27例,兩種方案聯合應用者10例。本研究方案經上報醫院倫理委員會審查通過后實施,所有患者在接受治療前均被告知相應的治療方案,并簽署知情同意書。
1.2 納入及排除標準 (1)患者均為首次于本院進行住院治療;(2)所有患者均為單純肝轉移,且自愿接受新輔助化療;(3)原發灶和轉移灶均行病理學診斷確診;(4)住院前均進行詳細的CT或MRI檢查并評估確認原發灶、肝轉移灶可切除;(5)患者年齡不超過75歲,且KPS評分不低于60分;(6)治療效果觀察指標明確;(7)排除患者合并有高血壓、糖尿病、心臟病等全身疾病。(8)排除合并腸穿孔、急性腸梗阻或嚴重感染等嚴重并發癥者。
1.3 方法
1.3.1 新輔助化療方案 (1)FOLFOX6方案:奧沙利鉑(85 mg/m2)靜滴2 h,d1;甲酰四氫葉酸(400 mg/m2)靜滴2 h,d1;400 mg/m25-FU靜脈推注,緊接下來2.4 g/m25-FU靜滴持續46 h,2周后重復1次以上方案。每次實施方案前30分鐘均給予患者5-HT3受體拮抗劑以減輕嘔吐反應。囑患者在治療期間避免受到冷刺激,若在治療過程中發現患者病情繼續進展或發生 Ⅳ級毒性反應則應及時終止本化療方案或更換化療方案。(2)FOLFIRI方案:國產伊立替康180 mg/m2靜滴90 min,d1,四氫葉酸鈣400 mg/m2靜滴2 h,d1,氟尿嘧啶0.4 g/m2靜推(四氫葉酸鈣之后用),氟尿嘧啶2.4 g/m2持續靜脈灌注(經化療泵灌注)46 h,每14天重復,14 d為一周期,2周后重復1次以上方案。每次實施方案前30分鐘均給予患者5-HT3受體拮抗劑以減輕嘔吐反應,若患者出現腹瀉則及時給與鹽酸洛哌丁胺膠囊,若在治療過程中發現患者病情繼續進展或發生頑固性腹瀉等嚴重不良反應則應及時終止本化療方案或更換化療方案。
1.3.2 手術方法 患者接受新輔助化療獲得手術條件后停止化療至少15 d后方可進行手術治療,開腹或腹腔鏡下切除原發灶,開腹手術切除肝轉移灶,嚴格按照無瘤原則進行手術操作,按照結直腸癌手術標準指南確定切除范圍,切除標本均送病理檢查。
1.4 治療效果評價標準 同一病灶在接受新輔助化療后2周進行復查,選擇與治療前相同的檢查方法。根據WHO提出的實體瘤治療效果評價標準(RECIST)對本資料中的患者情況進行評價,新輔助化療過程中出現的不良反應均進行記錄并分析,相關標準參照美國國家癌癥研究所提出的化療毒性分級標準進行,血清CEA若超過5.0 ng/mL則認為是陽性結果。新輔助化療效果評價結果表示:CR:目標病灶消失;PR:目標病灶至少縮小30%;PD:目標病灶增加超過20%或有新病灶發生;SD:目標病灶縮小程度未達到PR標準或增加程度未達到PD標準。有效=CR+PR。
1.5 統計學處理 采用Excel建立數據庫,使用SPSS 18.0統計軟件進行分析,計量資料采用(±s)表示,比較采用t檢驗,計數資料采用 字2檢驗,以P<0.05為差異有統計學意義。
2 結果
2.1 患者接受新輔助化療前后血清CEA、原發灶和轉移灶的變化情況比較 本資料患者接受新輔助化療(4.2±0.7)個周期,其中轉移灶治療效果獲得CR者共0例,獲得PR者共27例,獲得PD者共2例,獲得SD者共11例,新輔助化療對轉移灶有效率為67.5%(27/40)。原發灶獲得CR者共0例,獲得PR者共22例,獲得PD者共3例,獲得SD者共15例,新輔助化療對原發灶有效率55.0%(22/40)。治療前血清CEA陽性率為85.0%(34/40),接受新輔助化療后血清CEA陽性率為47.5%(19/40),新輔助化療前后血清CEA陽性率比較差異有統計學意義( 字2=5.774,P<0.05)。新輔助化療前后的原發灶平均大小、轉移灶平均大小及血清CEA值比較,差異均有統計學意義(P<0.05),見表 1。
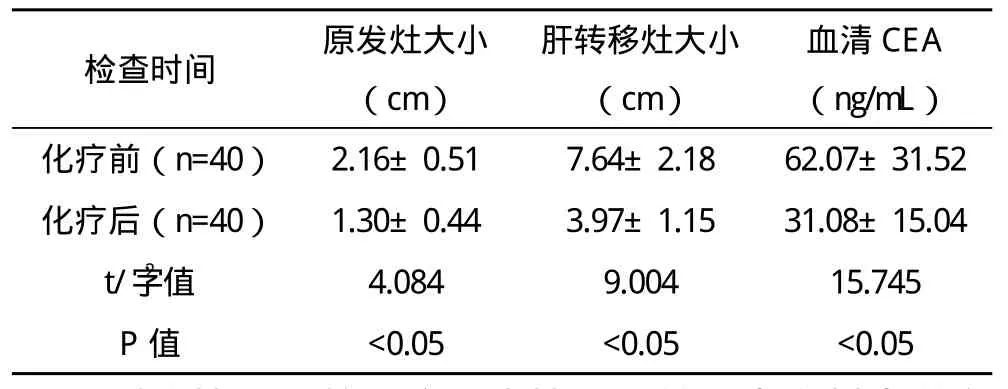
表1 新輔助化療前后血清CEA值、原發灶大小和轉移灶大小的比較(x-±s)
2.2 手術情況及并發癥發生情況比較 本資料中共有14例(35.0%)獲得根治性切除術,其中1例患者發生切口感染,1例患者發生肝功能衰竭,并發癥發生率為5.0%,無患者發生圍手術期死亡。
3 討論
結直腸癌是一種致死率較高的惡性腫瘤疾病,發生肝轉移后若不能及時接受根治性手術則患者的5年生存率為0,中位生存時間為7個月[4]。若能及時接受根治性手術則5年生存率可增加至40%~50%,中位生存時間可增長至35個月[5]。利用外科手術的方式將轉移灶切除是根治的唯一方法,但接受根治性手術有較為嚴格的適應證[6]。傳統的外科觀點認為,根治性手術僅當轉移灶被局限在半肝范圍內,且轉移灶數量低于3個,轉移灶發現時間與原發灶被切除之間時間超過12個月,未發生肝門淋巴結或其他部位的轉移,手術切緣需超過病灶邊緣1 cm等,在這樣的要求下,過去僅大約10%的患者能獲得根治性手術的機會,但這樣的情況明顯不符合現代外科手術的要求[7-9]。近些年美國肝膽胰協會提出,若對患者的術前評估認為在將轉移灶完全切除后剩余的肝組織仍能完成肝臟的正常生理功能以及相鄰的肝組織具有足夠的血流和膽道則可進行根治性手術[10]。隨著肝臟外科手術技術的發展、對手術器械的改進以及對圍手術期的管理提高等因素,目前肝轉移灶數量、分布情況以及轉移灶大小等對患者能否接受手術方面的影響越來越小[11]。Lehmann等[12]的研究結果表明,傳統手術指征的手術接受率為18.1%,擴大手術指征后手術切除率可達到29.4%,而前者術后復發率為29.7%,5年生存率為42.4%,中位生存時間45.1個月,后者術后復發率36.3%,5年生存率為50.7%,中位生存時間58.1個月,擴大手術指征后的手術接受率明顯增加(P<0.05),而復發率、5年生存率以及中位生存時間等比較差異均無統計學意義(P>0.05)。
新輔助化療是通過化療的方法來獲得降低腫瘤臨床分期的目的,從而為患者爭取到接受根治性手術的機會,同時有利于一些未被發現的微小轉移灶被清除,有利于患者預后的改善[13-14]。目前新輔助化療在進展期乳腺癌以及子宮頸癌等方面獲得了廣泛的應用,且效果較為理想[15]。本資料中選擇了FOLFOX6以及FOLFIRI兩種化療方案單用或聯合應用,其中27例(67.5%)的轉移灶體積明顯縮小,為患者增加了獲得根治性手術的機會。在臨床上,新輔助化療的應用有一定的限制,筆者認為在術前評估原發灶和轉移灶具備可切除條件或潛在可切除時方可取得較為理想的效果,而對于轉移灶被認為是不可切除者,則不適合新輔助化療,而更傾向于選擇姑息性治療。本研究資料結果顯示,新輔助化療對轉移灶有效率67.5%(27/40),對原發灶有效率55.0%(22/40)。治療前血清CEA陽性率85.0%(34/40),接受新輔助化療后血清CEA陽性率為47.5%(19/40),新輔助化療前后血清CEA陽性率比較差異有統計學意義( 字2=5.774,P<0.05),同時血清CEA值比較差異有統計學意義(t=15.745,P<0.05)。新輔助化療前原發灶平均大小(2.16±0.51)cm,化療后平均大小(1.30±0.44)cm,化療前后比較差異有統計學意義(t=4.084,P<0.05)。新輔助化療前轉移灶平均大小(7.64±2.18)cm,化療后平均大小(3.97±1.15)cm,化療前后比較差異有統計學意義(t=9.004,P<0.05)。14例(35.0%)獲得根治性切除術,其中1例患者發生切口感染,1例患者發生肝功能衰竭,并發癥發生率為5.0%,無患者發生圍手術期死亡。說明本新輔助化療方案的安全性較好,能被多數患者所接受,且能增加患者獲得根治性切除術的幾率。隨著肝臟外科手術技術的進一步發展以及新輔助化療方面研究的進一步深入,新輔助化療在改善結直腸癌肝轉移患者預后中扮演越來越重要的角色。
[1] Tamas K,Walenkamp A M,Hospers G A.Rectal and colon cancer:Not just a different anatomic site[J].Cancer Treat Rev,2015,28(2):5760-5766.
[2] Ayez N,Grünhagen D J,Verhoef C.The use of neo-adjuvant chemotherapy in patients with resectable colorectal liver metastases[J].Eur J Surg Oncol,2015,41(7):859-867.
[3] Fernandes E,Ferreira J A,Santos L L.New trends in guided nanotherapies for digestive cancers[J].J Control Release,2015,10(3):288-307.
[4] Ayez N,Radema S A,Hillegersberg R,et al.Neo-adjuvant chemotherapy followed by surgery versus surgery alone in high-risk patients with resectable colorectal liver metastases[J].BMC Cancer,2015,26(15):180-185.
[5] Bonney G K,Coldham C,Mirza D F.Role of neoadjuvant chemotherapy in resectable synchronous colorectal liver metastasis[J].J Surg Oncol,2015,111(6):716-724.
[6] Slesser A A,Khan F,Rao S.The effect of a primary tumour resection on the progression of synchronous colorectal liver metastases[J]. Eur J Surg Oncol,2015,41(4):484-492.
[7] De Felice F,Musio D,Tombolini V.Neoadjuvant chemoradiotherapy for locally advanced rectal cancer[J].World J Gastrointest Oncol,2014,15(12):438-440.
[8] Berardi R,Maccaroni E,Cascinu S.Locally advanced rectal cancer[J].World J Gastroenterol,2014,20(46):17 279-17 287.
[9] Leung U,Kuk D,Fong Y.Long-term outcomes following microwave ablation for liver malignancies[J].Br J Surg,2015,102(1):85-91.
[10] Khan K,Wale A,Chau I.Colorectal cancer with liver metastases[J].World J Gastroenterol,2014,20(35):12 391-12 406.
[11] Musters G D,Sloothaak D A,Tanis P J.Perineal wound healing after abdominoperineal resection for rectal cancer[J].Int J Colorectal Dis,2014,29(9):1151-1157.
[12] Lehmann A M,Chondrogiannis S,Rubello D.Early prediction of response by 18F-FDG PET/CT during preoperative therapy in locally advanced rectal cancer[J].Eur J Surg Oncol,2014,40(10):1186-1194.
[13] Ahmed S,Johnson K,Iqbal N.Advances in the management of colorectal cancer: from biology to treatment[J].Int J Colorectal Dis,2014,29(9):1031-1042.
[14] Bohac G C,Guaqueta D,Hartshorn K L.Disparity in the use of combined modality therapy for rectal cancer in the older adult[J].J Geriatr Oncol,2013,4(1):90-97.
[15] Schouten S B,De Bruin A F,Harst E.Is microvessel density correlated with anastomotic leakage after low anterior resection[J].Hepatogastroenterology,1900, 61(129):90-93.

