例談初中化學的計算題
強勤姣

摘要: 化學計算題能有效的考查學生的思維能力與解決問題的能力,尤其在重視解決實際問題的新課程教學中,一道綜合的化學計算題能考查學生多方面的能力。盡管化學計算題比較多,但從類型上看可以大體的分成幾個類型:化學式方面的,化合價方面的,化學方程式方面的以及溶液方面的題型。本文主要通過舉例來說明與化學式、化學方程式、溶液方面有關的計算題型。
關鍵詞:化學;計算;分類
初中化學計算的題型是比較多的,在中考中的各種題類中都會出現,無論是填空題還是選擇題都會夾著計算題,從常見的計算題看,大體將化學計算題型分為與化學式有關的,與化學方程式有關的,與溶液有關的題型。為了更好的幫助學生理清解題思路,筆者結合自身的教學實踐在此做一些歸納。
一、與化學式有關的計算
計算化學式的相對分子質量與化學式中的各種元素的質量比。
例1:C3H6O3(碳酸二甲酯)被稱為綠色的化學試劑,因為它的毒性比較低,用途十分的廣泛,能很好做有機溶劑,也能添加在燃油里。現在請你根據它的化學式計算它的相對分子質量————;并根據化學式解出它的C:H:O的質量比————;同時計算出它的氧元素的質量分數————。其實,這是比較容易的計算題,關鍵是請學生記住幾個公式:質量×原子個數(之和)→相對分子質量;相對原子質量×原子個數(之比)→各元素質量比;相對原子質量×原子個數/相對分子質量=某元素的質量分數。
例2:我們國家規定出售的尿素CO(NH2)2的質量分數在96%以上為一級品。假如現在出售1頓尿素,它的含氮元素的質量為0.44噸(雜質里沒有氮元素),請你根據以上的信息計算該尿素屬不屬于一級品?這是一道解不純物中含純物質的質量分數的計算題,只要讓學生掌握下面這個公式就行了:不純物中某元素的質量分數/純物質中該元素的質量分數×100%=不純物中含有的純物的質量分數。因此,根據這個計算原理,就能計算出這種尿素中含有的純尿素的百分含量了:先計算出純的尿素的含N的質量分數為46.7%,然后再利用上面的計算公式進行計算:44%÷46.7%=94.2%<96%,因此,它不屬于國家規定的一級品。其實,中考中的對于化學式計算方面的題目,主要是利用上面的兩個計算方法,只要學生能把握上面的幾個公式,就能輕松解題了。
二、與化學方程式有關的計算
縱觀這幾年的中考試題,試卷上關于化學方程式方面的計算題是肯定不會缺少的,有的出現在填空里,有的出現在選擇題中,還有的與實驗題結合起來考查學生,當然,最后的大比分計算題也經常見到與化學方程式有關的計算題,因此,在各種化學計算題型里,與化學方程式有關的計算還是顯得很重要的。目前,有的計算題來自高中的化學內容,也有的來自社會熱點問題,增加社會背景是主要特點。比如,有關漂白粉的形成過程,復雜的有機物燃燒,電解氯化鎂等等都屬于高中方面的知識;以藥品、最新的軍事武器為素材的題目,就是屬于社會生活熱點問題了。這類題目,一般先給出背景,再給予相關的化學方程式,只要學生能明白題中的各種信息,就能順利的解題。例:2005年5月中國登山隊員又一次的登上珠穆朗瑪峰進行高度測量,這是新中國成立以來的第二次,目的是看看珠穆朗瑪峰的高度變化情況。登山隊員在登山的過程中需要一定的能源,能向他們提供能源的是一種叫氫化鈣的物質(CaH2),這種物質與水反應能產生氫氧化鈣與氫氣,其中的氫氣就是一種清潔的能源。請你先寫出這個化學方程式?假如登山隊員利用42克的氫化鈣與足量的水進行反應,請你計算一下,能產生多少克的氫氣?這個是與社會生活有密切聯系的化學計算題,解決它的關鍵是理解題目中的信息,根據有關的化學方程式,利用CaH2的質量解出H2的質量就行了,然后再利用密度公式計算出H2的體積。這個題目并不難,但所涉及的素材與化學反應都是初中學生不熟悉的內容,這就有效的考查了學生的閱讀能力與處理信息的能力,也考查了學生利用化學方程式的計算能力,這是新課程教學改革的一個重要特點。
例2某化學學習小組欲測定從實驗室里取出來的KClO3樣品的純度,他們從實驗室里取了2.5克KClO3與0.8克的MnO2,然后將兩者混合后加熱。
三、與溶液有關的計算
與溶液有關的計算,也是中考化學計算題中的主要題型,中考題中的考查題的形式是多樣的,常常是與生產、生活相聯系的,而且很多題目是分值比較少的,穿插在填空題與選擇題中,當然也有分值較大的計算題。
例1:濃H2SO4有較強的腐蝕性,它溶解時會產生大量的熱,利用它配置稀H2SO4時要特別注意安全。請你根據下面要求進行相關的計算:現有98%的濃H2SO420克,它所含的溶
質是多少克?假如將此濃H2SO4緩慢的注入在80克的水中,得到的稀H2SO4的質量是多少克?溶質的質量分數為多少?這個題目要利用溶液稀釋前后的溶質質量不變的原理來解的。其實,這個題目并不難,它的目的是讓學生重視稀釋濃H2SO4時的操作問題。
四、溶液中的熱點問題
(一)標簽問題
此類題目主要考查學生的閱讀能力以及應用信息解決實際問題的能力。例如:下面是實驗室里常有的盛放鹽酸的試劑瓶上的標簽,請你認真閱讀標簽,然后通過計算說明,欲配置100克14%的稀鹽酸,需要這樣的鹽酸多少毫升?
鹽酸(分析純)
化學式:HCl 相對分子質量:36.5
密度:1.18克/立方厘米 質量分數:36%
這個題目的關鍵是要求學生認真的閱讀題目中的信息,然后進行思考,再利用稀釋溶液的原理來進行計算。它也是與生活實際相聯系的問題。
(二)特殊反應問題
例如:在某個溫度下,將5.6克的生石灰投入到100克飽和的澄清的石灰水里,等它們充分反應后,而且問題下降到原來的溫度時,下面說法中正確的是( ):
A溶液中的溶質的質量不變;B溶液中鈣離子的數目不變;C溶液里的沉淀質量應該是5.6克。因為氧化鈣與水是發生反應的,而且產生熱,所以,溶液中的水會減少的,但溫度恢復以后,溶液的飽和狀態沒有變,也就是說這個溶液還是飽和的,因此,溶質不會變。故選擇A。很多特殊的反應常常是中考中的熱點,要求學生在審題的時候,特別注意題中的溶液、溶質、溶劑的質量變化情況。
五、綜合的化學計算
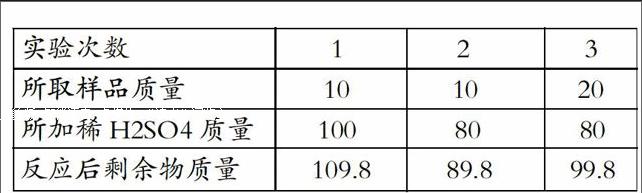
化學的綜合題,就是加強了化學知識之間的聯系,把化學式、化學實驗、溶液知識、化學方程式等等方面的內容聯系起來對學生進行考查,有的題目還出現了很多表格、圖像為信息載體的題目,它的特點就是要利用數學知識理解題意,要求學生分析圖表,分析數據,掌握題目給的各種信息,并利用化學方程式計算出相關的問題,這是考查學生綜合利用信息的能力。如,某機械廠新購進一批黃銅(銅與鋅的合金),化驗員為了測定其含銅的質量分數,將樣品加工成粉狀后置于燒杯里與稀H2SO4進行反應,已知三次實驗只有一次是黃銅樣品與稀H2SO4完全反應的。有關數據如下:
試請分析:1樣品與稀H2SO4完全反應的質量之比是多少?樣品中含有的銅的質量分數是多少?2請你計算出樣品與稀H2SO4完全反應后的溶液中的溶質的質量分數(精確到0.1%)。這是一道較為綜合性的題目,不僅要求學生知道合金中只有鋅能與稀H2SO4發生反應外,還要求學生能看懂表格,分析出數據的特點,找到哪組是恰好完全反應的,考查了學生靈活的思維能力。
總之,化學計算反映一個學生綜合運用化學知識解決實際問題的能力,因此化學計算在中考中的權重比較大。做好化學計算的分類工作,主要是為了讓學生盡快的掌握化學計算的方法,提高化學計算的能力,從而突顯減負增效的教學理念。
編輯 ∕高 偉

