尿液有形成分全自動分析儀(UF-1000i)性能評價
陳麗娟,羅俐鶯,魏權,詹燕婷
(龍巖人民醫院,福建 龍巖364000)
UF-1000i應用半導體激光流式細胞/核酸熒光染料技術,對各種有形成分的細胞膜、細胞核、細胞質進行特異性的核酸熒光染色;且具有獨立的雙檢測通道(沉渣通道和細菌通道),能快速提供 WBC、RBC、EC、CAST 和 BACT 等參數定量報告[1]。但按照CNAS:2014醫學實驗室認可準則,要求臨床實驗室在儀器投入使用前,需對分析系統進行性能驗證,要達制造廠商規定的性能要求方可使用[2],以達到實驗室標準化管理的要求,這樣才能保證實驗室檢測結果的質量。因此,筆者依據美國臨床實驗室標準化協會(CLSI)頒布的H56-A文件[3]及UF-1000i全自動尿液有形成分析儀病例研究手冊[4]和UF-1000i說明書對本院新購置待投入使用的 UF-1000i主要定量參數(RBC、WBC、EC、CAST和BACT)的批內精密度、批間精密度、準確度、攜帶污染率、線性范圍、檢測模式比對分析和生物區間參考范圍進行驗證實驗[5-7]。現報告如下。
1 材料與方法
1.1 儀器和試劑 Sysmex UF-1000i尿液有形成分全自動分析儀及原廠配套試劑和尿液有形成分質控物。
1.2 樣本來源 采用2013年9月到10月在本院住院、門診患者和健康體檢人員新鮮尿液標本,2h內完成測定[8]。
1.3 評價方法 將UF-1000i尿分析儀按使用要求調整至最佳檢測狀態,再進行如下各性能參數的驗證實驗。
1.3.1 批內精密度 選用高、中、低三個濃度水平的新鮮尿液分別于當日用UF-1000i重復測定11次,棄用第1次檢測數據,計算后10次測定結果的變異系數CV值。
1.3.2 批間精密度 用高、低兩個水平濃度的質控(按說明書要求混勻),連續測定20d,計算其變異系數CV值。
1.3.3 準確度 用高、低兩個水平濃度的質控(按說明書要求混勻),用UF-1000i連續測定5次,計算平均值,看是否在質控范圍內,質控批號:YS3017。
1.3.4 殘留率 取高濃度新鮮尿液樣本(約含RBC:5000 個/μl,BACT:10000 個/μl),混合均勻后連續測定三次,測定值分別為H1、H2、H3;再取低濃度尿樣(約含 RBC:20 個/μl,BACT:150 個/μl),連續測定3次,測定值分別為L1、L2、L3。按以下公式計算攜帶污染率:(CV%)=[(L1-L3)/(H3-L3)]×100%。
1.3.5 線性范圍 取富含紅細胞、白細胞、細菌和上皮細胞的尿樣 (RBC約10000個/μl、WBC約6000個/μl、BACT 約 10000 個/μl、EC 約 220 個/μl),以鞘液做稀釋液, 進行 1:2,1:4,1:16, 1:64,1:256(EC 稀釋度為 1:2,1:4,1:8,1:16,1:32;) 稀釋,各稀釋點均各測3次,取其均值為實測值;以稀釋計算值作為理論值。各稀釋尿樣的實測值與理論值進行線性回歸和相關分析 ,計算公式。要求a值在1±0.05 范圍內,相關系數 r≥0.975。
1.3.6 檢測模式比對 準備10份新鮮尿液樣本,濃度覆蓋生物參考區間,整個實驗在樣本老化之前完成。在手動模式和自動模式下檢測這10份樣本,每個樣本在各個模式下檢測3次,取其均值,計算手動模式和自動模式之間的結果偏差百分比。
1.3.7 生物參考區間驗證 隨機選擇40例健康人群的樣本(男女各20例),檢測結果至少90%在擬定的參考區間內,說明實驗室使用的參考區間有效。
1.4 統計軟件 用EXECEL 2010進行線性回歸和相關分析。
2 結果
UF-1000i各項參數 (RBC、WBC、EC、CAST 和BACT)檢測及統計分析結果如下:(1)批內精密度見表 1;(2)批間精密度見表 2;(3)準確度見表 3;(4)攜帶污染率見表4;(5)線性分析見表5;(6)檢測模式比對分析見表6;(7)生物區間參考范圍驗證結果見表7。
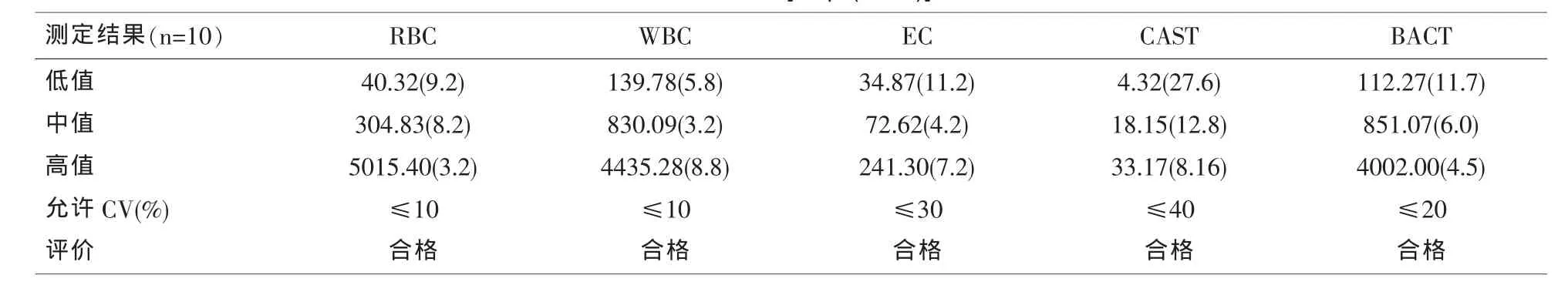
表1 批內精密度 [個/μl(CV%)]
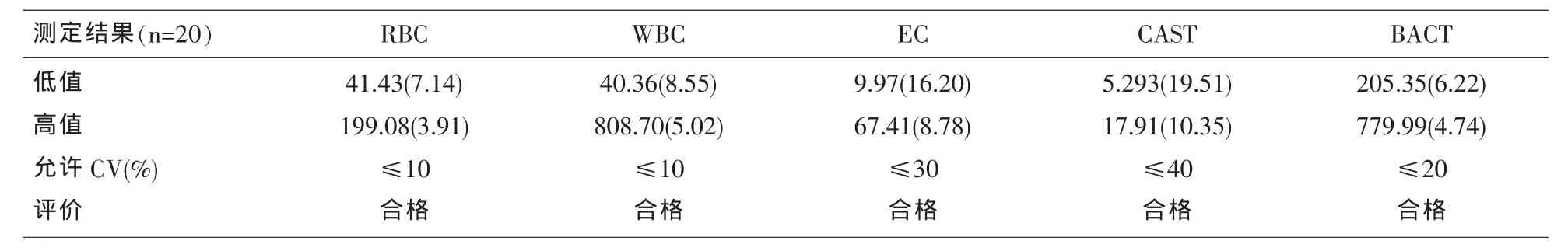
表2 批間精密度單位:[個/μl(CV%)]

表3 準確度(n=5)
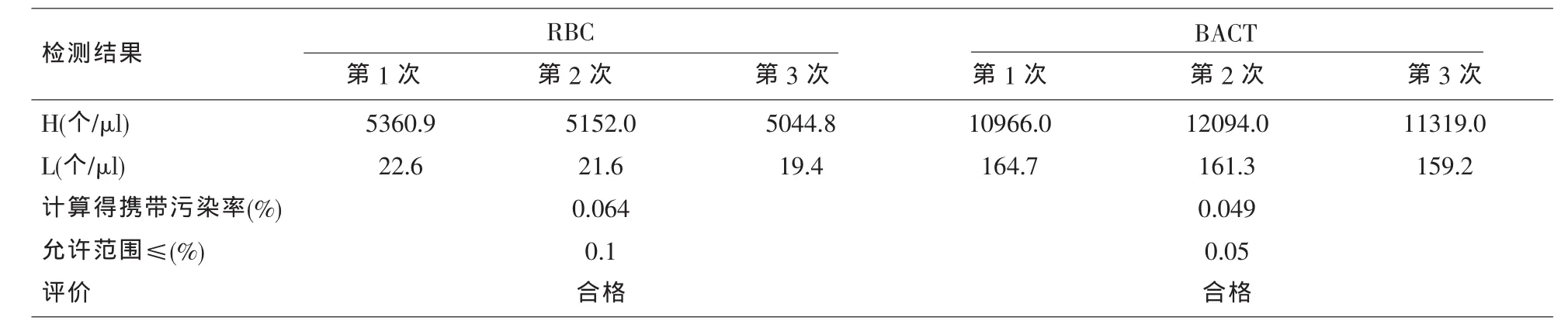
表4 攜帶污染率
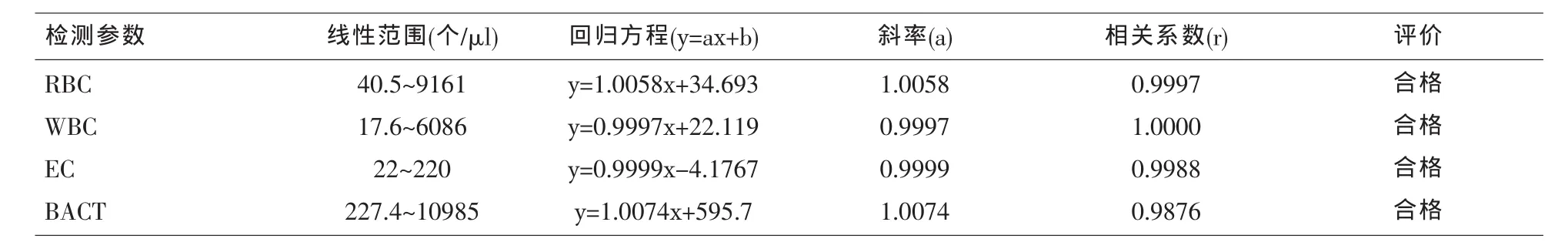
表5 線性分析
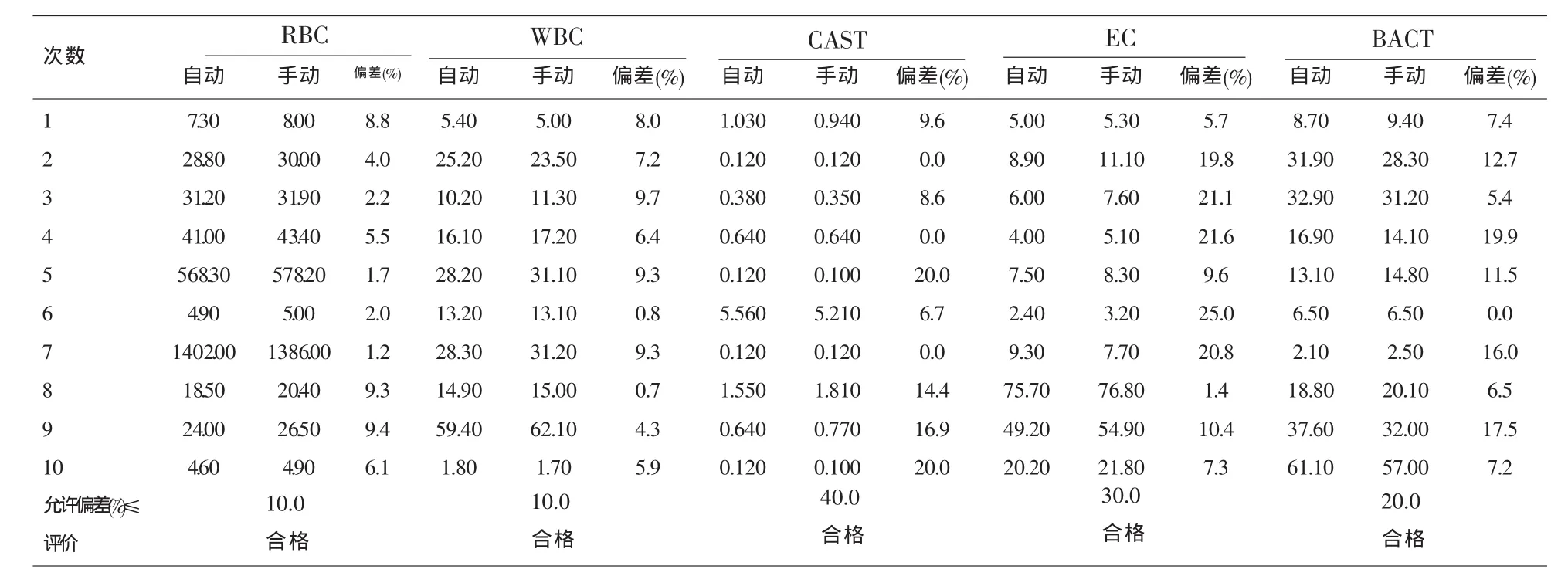
表6 檢測模式比對分析單位:(個/μl)
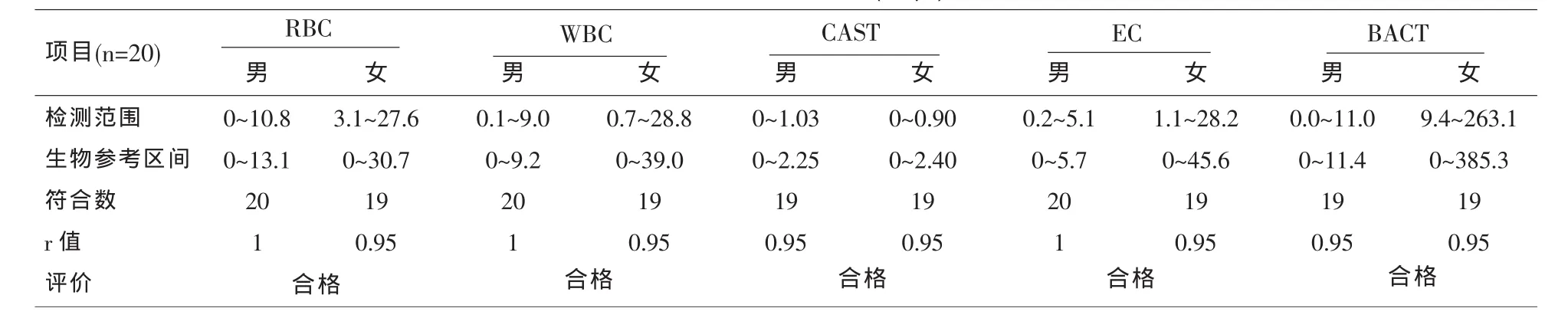
表7 生物參考區間(個/μl)
3 討論
由以上驗證結果可知,我院購進的UF-1000i 5項主要定量參數 (RBC、WBC、EC、CAST和BACT)指標的批內、批間精密度、線性、檢測模式比對、殘留率、準確度、檢測模式比對分析的性能指標均符合廠商標示的性能參數及質控品的要求[9]。本科室還同時對Sysmex公司提供的生物參考區間進行驗證, 結果 RBC 、WBC、EC、 CAST、BACT 均在要求范圍內。在線性范圍驗證上,由于紅細胞上限值的樣本難于獲得,我們通過在尿液樣本中加入適量的EDTA-K2抗凝血作為紅細胞高值樣本[10,11]。在CAST方面,我院實在難以獲得廠家高限值的樣本,所以該項目的線性未加以驗證,而是用高值的質控樣做準確度等參數的驗證。
雖然UF-1000i具有規范化、方便快捷、檢測率高的優點,但由于其基本原理仍是根據有形成分的大小及核酸量的多寡進行非形態分析,尿沉渣成分復雜,有時受干擾物質影響,且儀器的靈敏度高易受干擾,易致假陽性率高,所以其結果只能供篩選之用[12,13],不能完全取代傳統的化學檢查和尿有形成份顯微鏡檢查,比如:UF-1000i管型的假陽性率高,且不能將病理管型進一步分類,而尿管型的數量和類型對急性腎炎和某些腎外疾病[14]有重要的診斷價值[15,16]。因此,UF-1000i提供的陰性結果可以免檢,但為陽性時,必須以鏡檢復檢為準,以免引起臨床不必要的誤診。
綜上所述,我院新購進的UF-1000i尿液有形成分全自動分析儀其精密度良好,準確度高,線性等各項性能指標均符合要求,可應用于臨床尿液分析的篩查實驗。
[1]叢玉隆,馬駿龍.尿液有形成分鏡檢與自動化檢測方法學利弊和互補分析[J].中華檢驗醫學雜志,2009,32(6):609-611.
[2]中國合格評定國家認可委員會.醫學實驗室質量和能力認可準則在體液學檢驗領域的指南[S].CNAS-CL41,CNAS,2013.
[3]Clinical Laboratory Standards Institute.Body fluid analysis for cellular composition;appmved guideline[S].H56-A,CLSI,2006.
[4]油野友二.UF-1000i clinical case study[M].Japan;SYSMEX COPR0RATION,2007:18-21.
[5]何巍巍,梁曉君,潘斌,等.Sysmex UF-1000i全自動尿沉渣分析儀的性能評價分析[J].實驗與檢驗醫學,2013,31(4):405-407.
[6]潘蕓,王瑤.Sysmex UF-1000i在尿液檢測中的性能評價 [J].現代檢驗醫學雜志,2011,26(6):76-78.
[7]趙燕霞.Sysmex UF-1000i全自動尿有形成分分析儀性能評價[J].實用醫技雜志,2014,21(3):290-291.
[8]叢玉隆,馬俊龍,張時民.尿液細胞成分定量分析方法學研究[J].中華檢驗醫學雜志,2006,29(3):211-214.
[9]葉應嫵,王毓三,申子瑜.全國臨床檢驗操作規程[M].第3版.南京:東南大學出版社,2006:293-294.
[10]黃震,遲秀文,束振華.UF-1000i臨床檢測性能評價及復檢條件探討[J].現代檢驗醫學雜志,2011,26(1):76-78.
[11]李滔,汪永紅.UF-1000i全自動尿有形成分分析儀的方法學性能評價[J].長江大學學報,2013,10(18):41-44.
[12]蘇海鵬,李巖,王琳.尿液自動化檢測與尿沉渣鏡檢法在檢測管型方面的利弊和互補分析 [J].國際檢驗醫學雜志.2012,11(22):2786-2787.
[13]顧可梁.重視尿液有形成分檢查[J].國際檢驗醫學雜志,2008,29(1):1-3,7.
[14]鄭洪,梁雪冰,葉聯珍.UF-1000i尿有形成分分析儀檢測尿管型的評價[J].實用醫學雜志,2010,26(20):3814-3815.
[15]葉小英,陸敏,段厚全,等.Sysmex UF-1000i尿沉渣分析儀檢測管型的影響因素[J].實驗與檢驗醫學,2013,31(2):187-188.
[16]熊立凡,劉成玉.臨床檢驗基礎[M].第4版.北京:人民衛生出版社,2009:179-199.

