自噬在腫瘤發生、發展和治療中的作用研究進展
孔蘊源綜述 李蓉審校
(1、南昌大學第一附屬醫院;2、南昌大學基礎醫學院,江西 南昌 330001)
細胞自噬(autophagy)是細胞中細胞中降解的通路,是將細胞中受損、衰老、變性以及失去功能的蛋白質和細胞器運輸到溶酶體內,并在溶酶體內一系列酶的作用下進行消化、降解的過程[1]。自噬現象廣泛存在于各種真核細胞生物中,是細胞中高度保守的過程。其在正常的生理和病理過程中都發揮重要作用。在正常細胞中,細胞自噬在代謝調控、細胞內質量平衡,以及發育和分化過程更新中扮演的角色。細胞中存在多種自噬調節因子,使得細胞中自噬水平保持平衡狀態,繼而有利于細胞正常生理過程。但是當細胞中自噬水平發生紊亂,會導致細胞生物學功能的異常甚至導致疾病的產生。研究表明,腫瘤、神經退行性疾病、自身免疫性疾病等多種疾病與細胞自噬異常有關[2]。近年來研究表明,自噬在腫瘤發生、發展過程中存在雙重效應,既可以促進腫瘤的發生,又可以抑制腫瘤的發生,如同一把“雙刃劍”。因此,本文就自噬及其在腫瘤的發生、發展和治療中的作用做一綜述。
1 細胞自噬形成
自噬是細胞利用溶酶體降解自身細胞器和大分子物質的過程.在哺乳動物細胞中,主要存在3種不同的自噬方式:巨自噬(macroautophagy)[3]、微自噬(microautophagy)[4]和分子伴侶介導自噬(chaperone-mediated autophagy,CMA)[5]。巨自噬是指待降解物由內質網膜包繞形成自噬體,然后與溶酶體融合并降解其內容物;微自噬是指被降解物直接被溶酶體包裹并降解的過程;而CMA為胞漿內蛋白結合到分子伴侶后轉運到酶體腔中,被溶體酶消化過程。由于微自噬和CMA并沒有形成自噬囊泡的過程,而巨自噬在細胞中需要形成獨立的自噬囊泡,并且自噬囊泡的形成可以受到藥物的干預等,因此通常認為的自噬主要是指能夠形成自噬囊泡的巨自噬。
當細胞處于饑餓、高溫、低氧、激素、化療和放療等危險環境或細胞內細胞器損傷、基因突變、蛋白變性時,來源于細胞膜、內質網、高爾基體等膜結構相互聚集(起始過程);通過成核作用與細胞內大分子相結合,將細胞質或細胞器包裹形成開放的半囊泡 (囊泡延伸過程);然后在溶酶蛋白LAMP1、LAMP2、Rab7、UVRAG 等的作用下形成封閉的自噬體(成熟過程);最終,在溶酶體膜受體的介導作用下,自噬體與溶酶體相互融合形成自噬溶酶體(自噬體-溶酶體融合),并通過溶酶體降解內含物(自噬體降解過程),其降解產物然后被細胞再利用,以實現細胞本身的代謝需要和細胞器的更新(圖 1)[2]。
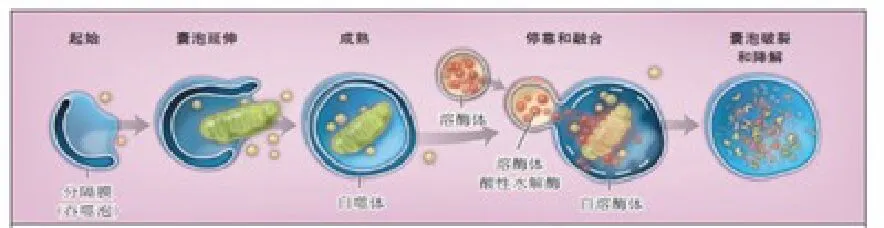
圖1 自噬形成的過程:起始→囊泡延伸→成熟→自噬體-溶酶體融合→自噬體降解。
2 調控自噬的主要信號通路
隨著對自噬研究的深入,發現多種信號通路可以調節細胞內自噬水平,目前研究比較清楚的自噬調控方式主要包括:(1)mTOR依賴的信號通路:如PI3K-ATK-mTOR信號通路[6]、LKB1-AMPK-mTOR信號通路[7,8]等;(2)mTOR非依賴的信號通路[9,10]:如Beclin1和III型PI3K形成復合物調控自噬,也可以通過Bcl2抗凋亡蛋白家族相互作用調節自噬等等。
2.1 mTOR依賴的信號通路 哺乳動物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)是一個高度保守的絲氨酸/蘇氨酸蛋白激酶,其為PI3K相關激酶家族成員,具有調節靶蛋白磷酸化的作用。mTOR在細胞中主要以兩種復合物的方式存在:分別是對雷帕霉素敏感的mTOR復合物1(mTORC1)和不敏感的mTORC2,其中mTORC1與細胞自噬關系比較密切。研究表明,mTOR是細胞中氨基酸、ATP和激素的感應器,mTOR是自噬體的形成,成熟過程中關鍵,也是多種自噬調控信號通路的匯合點[12]。研究表明,生長因子受體和配體結合后,導致蛋白激酶PI3K活化,活化的PI3K磷酸化磷脂肌醇(PI)的肌糖環D3位點從而產生PI(3,4,5)P3。PI(3,4,5)P3結合到PDK1和AKT的PH結構域并使它們轉位到細胞質膜,繼而導致AKT磷酸化,磷酸化的AKT具有激酶活性,可以是mTOR蛋白磷酸化從而激活mTORC1復合物,活化的mTORC1復合物通過激活一系列下游信號通路繼而抑制細胞自噬的產生,這一信號通路被稱為PI3K-ATK-mTOR信號通路[11]。而抑制PI3K-ATK-mTOR信號通路的任何環境都可以促進細胞自噬的產生。
另外,細胞能級狀態也可調控mTORC1復合物的活性。研究表明,蛋白細胞處于饑餓狀態時,細胞中的ATP含量明顯減少,導致ATP/AMP的比值會下降。ATP/AMP的比值下降可以通過LKB1激酶活化AMP活化蛋白激酶(AMPK),AMPK的下游底物為mTOR[12]。因此LKB1-AMPK通路也可以調控mTOR的活性繼而調控細胞中自噬的水平,被稱為LKB1-AMPK-mTOR信號通路。
2.2 mTOR非依賴的信號通路 研究表明,在細胞還還存在繞過mTOR調控細胞自噬的方式,被稱為mTOR非依賴的信號通路。其中最主要的mTOR非依賴的信號通路為beclin1-Hvps34通路,有實驗發現,Mst1(mammalian Ste20-like kinase 1)可使Beclin1 BH3結構域N-端的Thr108磷酸化,增強Beclin1與Bcl-2和/或Bcl-xL疏水溝α3螺旋間的互作,使Beclin1同源二聚體穩定,減弱Atg14L與Beclin1的結合,降低Beclin1-P13K-Atg14L復合體脂激酶Vps34的活性以抑制自噬[13],而死亡相關蛋白激酶DAPK1可以通過磷酸化Beclin1蛋白使得 Beclin1與Bcl-2和/或 Bcl-xL解離,繼而與Atg14L形成Beclin1-P13K-Atg14L-Vps34復合體脂激酶,從而達到起始自噬體形成的目的[14,15]。
3 自噬在腫瘤中的作用
在正常生理情況下,自噬可以及時清除細胞中破損或衰老的細胞器、合成錯誤或折疊錯誤的蛋白質等大分子物質,防止細胞出現異常的病態(如癌變等),同時自噬的產生的氨基酸、脂肪酸等小分子物質也可以被細胞從新利用。因此,自噬就是細胞的“備用倉庫”,對維持細胞正常生物學功能具有非常重要的作用。近年來在多種腫瘤中發現自噬的增強或減弱:一方面,自噬水平的下降也導致腫瘤的惡化和進展;另一方面,自噬增強使腫瘤細胞免受饑餓、化療、放療所導致的損傷而持續生存。因此自噬在腫瘤發生、發展過程中可能存在雙重效應,如同一把“雙刃劍”。
3.1 自噬抑制腫瘤的發生 大量研究表明,多種促進細胞自噬的相關基因在多種腫瘤細胞中缺失,或表達下降,并且在多種腫瘤細胞中也發現自噬能力低于正常細胞,表明自噬減弱與腫瘤的發生明確相關。例如有研究發現促進自噬的分子 (如Beclin1等)在人類乳腺癌、前列腺癌等細胞中缺失或表達下降[16],而在小鼠中敲除Beclin1等位基因導致小鼠多種細胞自噬水平減弱,同時癌癥發生率明顯高于Beclin1基因正常的小鼠[17]。還有實驗證明在正常組織中長期慢性地抑制細胞自噬,會激活腫瘤生成過程:比如化學致癌物誘導形成的肝癌細胞,在癌變前期的肝結節時就已經出現了自噬能力下降的現象[18,19]。由此不難看出,細胞自噬扮演了一個對抗腫瘤生成的角色。
3.2 自噬促進腫瘤的發生 自噬作為細胞本能的防衛武器,在細胞處于惡劣環境中,細胞會啟動自噬程序,使得細胞代謝降到最低,維持細胞的生存。在腫瘤細胞中,由于腫瘤細胞快速分裂增殖,需要的營養和能量比正常細胞多,但是腫瘤發生初期時的血管網絡沒有完全建立,導致營養和能量不能運輸到腫瘤組織中,這時,腫瘤細胞通過提高自噬活性防止細胞因缺乏營養而死亡。另外,當腫瘤長大發生血管崩塌時、腫瘤細胞脫離原發灶游走時等都會出現營養不足或供應中斷時,也需要腫瘤細胞增強自噬防止細胞死亡[20]。因此,很多腫瘤細胞如結腸癌、肺癌細胞及人宮頸癌細胞等均有較高的自噬潛能,這對腫瘤細胞在對抗惡劣環境過程中起到了一定的保護作用[21,22]。此外,還有實驗發現,在乳腺癌、睪丸癌、結腸癌等細胞中抑制細胞自噬后,可以觀察到了由環境壓力導致的細胞凋亡的增多[23]。
另外,在腫瘤化療、放療過程中,細胞會通過提高自噬活性及時清除大量的破損細胞器、損壞的蛋白質等有害成分,以便提供應急的底物和能量為修復受損DNA贏得時間和條件[24]。另外,自噬也使一些抗腫瘤藥物的作用減弱:例如惡性神經膠質瘤細胞經替莫唑胺處理3d后,細胞中自噬明顯增強,同時細胞的增殖受到抑制;但當藥物作用細胞7天后,細胞有開始增殖,同時自噬能力減弱,表明細胞自噬在細胞中的動態改變與細胞所處的環境有關,而這種動態變化可以防止其死亡,保護腫瘤細胞生存[25]。Wu等發現,用于前列腺癌治療的SFK(Src family kinase)抑制劑臨床療效往往不太理想,這可能與此類藥物會誘導高水平的自噬有關[26]。因此,自噬在特定情況下具有保護腫瘤細胞的作用,從而達到促進腫瘤發生、進展的目的。
4 自噬作為腫瘤的治療靶點
隨著自噬在腫瘤發生、發展中作用及其機制研究的深入。研究人員發現多種調控自噬的藥物,包括促進自噬和抑制自噬的藥物。其中部分藥物已近進入臨床實驗階段。
4.1 促進自噬的藥物 研究表明,促進自噬可以抑制細胞增殖,導致細胞凋亡,因此,靶向促進自噬的藥物具有抗腫瘤的作用。目前,最常用的抗腫瘤藥物為雷帕霉素(Rapamycin),雷帕霉素最初是作為治療移植排斥反應和抗真菌治療一種免疫抑制劑和真菌抑制藥物。近年來研究發現,雷帕霉素是一種自噬誘導劑。研究表明,雷帕霉素作用細胞短時間后,細胞自噬相關分子LC3-Ⅱ/LC3-Ⅰ比值會明顯升高,提示雷帕霉素具有促進自噬的作用。分子機制研究發現,雷帕霉素細胞中的靶蛋白為mTOR,通過與免疫親和蛋白FKBP12相結合,依附于mTOR的C末端,阻止mTOR激活,從而抑制mTORC1。由于mTORC1復合物的活化可以促進自噬,因此,雷帕霉素可以通過抑制mTORC1達到促進自噬的作用[27]。目前,雷帕霉素具有抑制多種腫瘤細胞的作用,并且其作為自噬誘導劑用于腫瘤治療的臨床實驗已經開始。另外,多種腫瘤抑制劑或分化誘導劑具有誘導細胞自噬的作用。近年來研究發現,中草藥姜黃的有效成分姜黃素可以通過多種途徑誘導細胞自噬,并能抑制細胞增殖[28]。另外,治療急性早幼粒細胞白血病的分化誘導劑全反式維甲酸可有通過誘導自噬的方式,促進癌蛋白PML/RARa蛋白的降解,繼而促進細胞分化,而抑制自噬可以抑制ATRA介導的PML/RARa蛋白的降解,并能抑制APL細胞分化。這些結果提示促進自噬具有抗腫瘤作用[29]。而靶向促進自噬的藥物可能將來可能單獨或聯合其它藥物用于腫瘤治療。
4.2 抑制自噬的藥物 有研究人員發現,在有些腫瘤細胞中,自噬誘導劑不僅不能促進腫瘤細胞死亡,還能抑制其它化學治療或放療誘導的細胞凋亡,表明抑制細胞自噬也可能用于腫瘤的治療。近年來研究發現,多種自噬抑制劑可以增強化療藥物抗腫瘤作用。抗瘧疾藥物氯喹(chloroquine)可以聯合多種化療藥物治療腫瘤。機制學研究發現,多種化療藥物如環磷酰胺、紫杉醇等具有誘導腫瘤細胞自噬的作用,而氯喹可以選擇性地進入溶酶體,通過中和溶酶體酸性環境,并能破壞后溶酶體等方式抑制細胞自噬,從而提高化療藥物對腫瘤細胞的殺傷作用[30,31]。也有研究發現組蛋白去乙酰化酶曲古抑菌肽(TSA)和伏立諾他(SAHA)具有改善笨腎上腺素誘導心肌肥大并可以通過抑制自噬達到抗腫瘤的作用[32]。還有研究發現自噬抑制劑去甲基丙咪嗪(DCMI)除了具有治療精神疾病外,還可以通過抑制自噬體和溶酶體的融合抑制化療藥物誘導的高水平自噬通路,繼而達到增強化療藥物細胞毒性的作用[33]。除此之外,現在還發現其它自噬抑制劑如3甲基腺苷(3-MA),渥曼青霉素(wortmannin),LY294002等多種自噬抑制劑,這些藥物都有可能與化療藥物聯合治療,達到增強抗腫瘤效果的作用[34,35]。
5 結語
自噬作為細胞中普遍存在的降解途徑之一,其在正常生理和病理過程中發揮重要作用。自噬在腫瘤發生、發展中具有雙重效應,一方面具有維持細胞穩態,促進衰老的細胞、病態細胞死亡多作用,另一方面自噬可以防止細胞在惡劣環境中死亡,并具有導致多種藥物治療耐藥的作用。因此,探討腫瘤中細胞中自噬的作用,并通過自噬誘導劑和自噬抑制劑干預腫瘤細胞的自噬水平,繼而達到治療腫瘤的目的,為腫瘤治療提供新的治療靶點。
[1]丁渭,張玉林,陳德喜.自噬-凋亡之后的新概念[J].中國生物化學與分子生物學報,2012,28(5):419-423.
[2]Arroyo DS,Gaviglio EA,Peralta Ramos JM,et al.Autophagy in inflammation,infection,neurodegeneration and cancer[J].Int Im-munopharmacol,2014,18(1):55-65.
[3]Feng Y,He D,Yao Z,et al.The machinery of macroautophagy[J].Cell Res,2014,24(1):24-41.
[4]Sahu R,Kaushik S,Clement CC,et al.Microautophagy of cyto solic proteins by late endosomes[J].Dev Cell,2011,20(1):131-139.
[5]Schneider JL,Suh Y,Cuervo AM.Deficient chaperone-mediated autophagy in liver leads to metabolic dysregulation[J].Cell Metab,2014,20(3):417-432.
[6]Heras-Sandoval D,Pérez-Rojas JM,Hernández-Damián J,et al.The role of PI3K/AKT/mTOR pathway in the modulation of autophagy and the clearance of protein aggregates in neurodegeneration[J].Cell Signal,2014,26(12):2694-2701.
[7]Hsu JL,Liu SP,Lee CC,et al.A unique amidoanthraquinone derivative displays antiproliferative activity against human hormone-refractory metastatic prostate cancers through activation of LKB1-AMPK-mTOR signaling pathway[J].Naunyn Schmiedebergs Arch Pharmacol,2014,387(10):979-990.
[8]Han D,Li SJ,Zhu YT,et al.LKB1/AMPK/mTOR signaling pathway in non-small-cell lung cancer[J].Asian Pac J Cancer Prev,2013,14(7):4033-4039.
[9]Dai JP,Zhao XF,Zeng J,et al.Drug screening for autophagy inhibitors based on the dissociation of Beclin1-Bcl2 complex using BiFC technique and mechanism of eugenol on anti-influenza A virus activity[J].PLoS One,2013,8(4):e61026.
[10]Castino R,Bellio N,Follo C,et al.Inhibition of PI3k class III-dependent autophagy prevents apoptosis and necrosis by oxidative stress in dopaminergic neuroblastoma cells [J].ToxicolSci,2010,117(1):152-162.
[11]Furuta S,Hidaka E,Ogata A,et al.Ras is involved in the negative control of autophagy through the class I PI3-kinase[J].Oncogene,2004,23(22):3898-3904.
[12]Gwinn DM,Shackelford DB,Egan DF,et al.AMPK phosphorylation of raptor mediates a metabolic checkpoint[J].Mol Cell,2008,30(2):214-226.
[13]Maejima Y,Kyoi S,Zhai P,et al.Mst1 inhibits autophagy by promoting the interaction between Beclin1 and Bcl-2[J].Nat Med,2013,19(11):1478-1488.
[14]Levin-Salomon V,Bialik S,Kimchi A.DAP-kinase and autophagy[J].Apoptosis,2014,19(2):346-356.
[15]Eisenberg-Lerner A,Kimchi A.PKD is a kinase of Vps34 that mediates ROS-induced autophagy downstream of DAPk[J].Cell Death Differ,2012,19(5):788-797.
[16]Laddha SV,Ganesan S,Chan CS,et al.Mutational landscape of the essential autophagy gene BECN1 in human cancers[J].Mol Cancer Res,2014,12(4):485-490.
[17]Brech A,Ahlquist T,LotheRA,et al.Autophagy in tumour suppression and promotion[J].Mol Oncol,2009,3(4):3366-3375.
[18]Cuervo AM,Autophagy:In sickness and in health[J].Trends Cell Biol,2004,14(2):70-77.
[19]Jin S,p53,Autophagy and tumor suppression [J].Autophagy,2005,1(3):171-173.
[20]Lock R,Debnath J.Extracellular matrix regulation of autophagy[J].Curr Opin Cell Biol, 2008,20(5):583-588.
[21]Kanazawa T,Germano IM,Komata T,et al Role of autophagy in temozolomide-induced cytotoxicity for malignant glioma cells[J].Cell Death Differ,2004,11(4):448-457.
[22]Wu Z,Chang PC,Yang JC,et al.Autophagy blockade seneitizes prostate cancer cells towards Src family kinase inhibitors[J].Genes Cancer 2010,1(1):40-49.
[23]Maiuri MC,Zalckvar E,Kimchi A,et al.Self-eating and selfkilling:crosstalk between autophagy and apoptosis[J].Nat Rev Mol Cell Biol,2007,8(9):741-752.
[24]Li X,Fan Z.The epidermal growth factor receptor antibody cetuximab induces autophagy in cancer cells by downregulating HIF-1alpha and Bcl-2 and activating the beclin 1/hVps34 complex[J].Cancer Res,2010,70(14):5942-5952.
[25]潘強.替莫唑胺耐藥的惡性膠質瘤細胞系耐藥特性演變的研究[D],碩士研究生學位論文,2010.
[26]Wu Z,Chang PC,Yang JC,et al.Autophagy Blockade Sensitizes Prostate Cancer Cells towards Src Family Kinase Inhibitors[J].Genes Cancer,2010,1(1):40-49.
[27]Chiarini F,Evangelisti C,McCubrey JA,et al.Current treatment strategies for inhibiting mTOR in cancer[J].Trends Pharmacol Sci,2015,36(2):124-135.
[28]Xiao K,Jiang J,Guan C.Curcumin induces autophagy via activating the AMPK signaling pathway in lung adenocarcinoma cells[J].J Pharmacol Sci,2013,123(2):102-109.
[29]Isakson P,Bjoras M,Boe SO,et al.Autophagy contributes to therapy-induced degradation of the PML/RARA oncoprotein[J].Blood,2010,116(13):2324-2331.
[30]Tang MC,Wu MY,Hwang MH,et al.Chloroquine enhances gefitinib cytotoxicity in gefitinib-resistant nonsmall cell lung cancer cells[J].PLoS One,2015,10(3):e0119135.
[31]Duffy A,Le J,Sausville E,et al.Autophagy modulation:a target for cancer treatment development[J].Cancer Chemother Pharmacol,2015,75(3):439-447.
[32]Cao DJ,Wang ZV,Battiprolu PK,et al.Histone deacetylase(HDAC)inhibitors attenuate cardiac hypertrophy by suppressing autophagy[J].PNAS,2011,108(10):4123-4128.
[33]RossiM1,Munarriz ER,BartesaghiS,etal.Desmethylclomipramine induces the accumulation of autophagy markers by blocking autophagic flux[J].J Cell Sci,2009,122(Pt18):3330-3339.
[34]Coker-Gurkan A,Arisan ED,Obakan P,et al.Inhibition of autophagy by 3-MA potentiates purvalanol-induced apoptosis in Bax deficient HCT 116 colon cancer cells[J].Exp Cell Res,2014,328(1):87-98.
[35]Ren Y,Huang F,Liu Y,et al.Autophagy inhibition through PI3K/Akt increases apoptosis by sodium selenite in NB4 cells[J].BMB Rep,2009,42(9):599-604.

