鐵粉吸氧腐蝕系列實驗的設計及應用
徐泓+朱敏+魏明貴
摘要:依據鐵的吸氧腐蝕原理,使用鐵粉、碳粉、食鹽水等試劑和常規玻璃儀器以及數字實驗技術,開發了空氣中氧氣含量的測定、鐵氧化過程的能量變化、鐵粉的吸氧腐蝕、影響化學反應速率因素等系列實驗設計,并應用于教學實踐,可充分發揮吸氧腐蝕的教育價值及其教學功能。
關鍵詞:鐵粉;吸氧腐蝕;系列設計;實驗探究
文章編號:1005–6629(2015)4–0063–04 中圖分類號:G633.8 文獻標識碼:B
吸氧腐蝕是生活中最常見的金屬腐蝕形式,其存在一方面對生活中金屬資源(尤其是鐵)造成大量浪費,在建筑、醫療等許多方面給人類帶來很多不利的影響;另一方面利用吸氧腐蝕原理研發的食品脫氧劑、暖寶寶等產品,又給人類生活帶來了安全和便捷。中學化學教學中有很多內容涉及吸氧腐蝕,本文從正面、積極的視角,利用鐵的吸氧腐蝕開發出空氣中氧氣含量的測定、鐵氧化過程中的能量變化、鐵粉的吸氧腐蝕、影響化學反應速率因素等幾個系列實驗,通過教師在教學中的實踐應用,充分發揮這一教學資源的教育價值和實驗教學的功能。
1 空氣中氧氣含量的測定
利用紅磷燃燒測定空氣中氧氣含量的實驗一直是我國初中化學教材中的經典實驗,但該實驗在原理上由于當紅磷在密閉容器中不再燃燒時,仍會有3.45%~7.6%的氧氣殘留[1,2],即紅磷燃燒不能完全耗盡空氣中的氧氣;在操作上由于當燃著的紅磷在伸入瓶中的一瞬間,瓶內空氣膨脹,會排出相當一部分空氣,影響測量的科學性和準確性[3]。而文獻顯示[4,5,6]:以還原鐵粉為主的脫氧劑,短時間內可除去密閉容器中氧氣,使食品處于無氧狀態(O2濃度0.01%以下),說明鐵的吸氧腐蝕幾乎能耗盡密閉裝置中的氧氣。因此,可利用脫氧劑吸收氧氣的原理,即鐵的吸氧腐蝕設計實驗以測量空氣中氧氣含量。
1.1 實驗設計及過程
連接裝置如圖1所示,檢驗氣密性。實驗時先將濾紙裁成長方形,大小以剛好能附著在250mL廣口瓶內側一圈為宜,用膠頭滴管吸取約4mL 1 mol/L NaCl溶液使濾紙浸潤并粘附在廣口瓶內側。燒杯中倒入與廣口瓶凈容積相當的水,打開止水夾,用洗耳球使導管內充滿水,并夾緊止水夾。稱取2.0g還原鐵粉、2.5g活性炭粉(本實驗使用的是上海申鶴化學品有限公司生產的分析純還原鐵粉和啟東申鶴化學品有限公司生產的化學純活性炭,下同),并攪拌均勻。將廣口瓶橫放,一邊轉動,一邊將鐵粉和碳粉混合物倒入廣口瓶內壁,盡可能使其較均勻地附著在廣口瓶內壁的濾紙上,并迅速塞緊瓶塞。約4分鐘后打開止水夾,會看到水迅速進入廣口瓶,稍后可觀察到燒杯內水的體積減少約1/5,可得出氧氣約占空氣體積的1/5。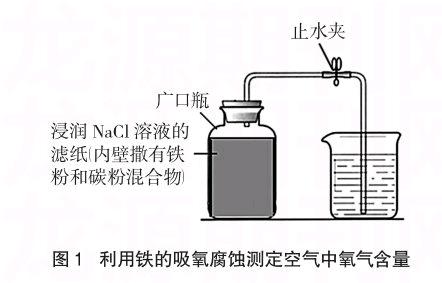
1.2 實驗優點
(1)原理科學,利用鐵的吸氧腐蝕能幾乎耗盡體系中的氧氣的原理。
(2)裝置簡單,與現行初中化學教材中紅磷燃燒實驗裝置基本相似。
(3)原料易得,都為中學化學實驗中常見藥品,且用量少。
1.3 應用說明
本實驗可應用于初中化學“空氣中主要成分”相關內容的教學中,可用于演示實驗,也可用于學生課后探究(自制食品脫氧劑)。教學中可先通過食品脫氧劑創設教學情境,說明脫氧劑的主要成分和作用,以此開展實驗教學引導學生得出空氣中氧氣含量的結論,最后用鐵的生銹簡化其原理為[7]:4Fe+3O2=2Fe2O3,既不違背其科學性,也符合學生認知水平。
2 鐵的氧化過程中的能量變化
能量觀是中學化學的核心觀念之一,通過放熱反應和吸熱反應說明化學反應中伴隨能量變化是高中化學的必修內容。現行教材中的有關放熱反應是利用金屬鎂或鋁與鹽酸反應實驗開展教學的,現象雖較明顯,但實驗的趣味性不強。筆者利用還原鐵粉、碳粉組成的吸氧腐蝕系統設計如下實驗。
2.1 實驗設計及過程
稱取2.0g還原鐵粉、2.5g活性炭粉,攪拌均勻,用濾紙包好。滴入約1mL 1 mol/L NaCl溶液使濾紙包潤濕,此時用手輕輕搓揉濾紙包,明顯感覺濾紙包發燙。用溫度計或溫度傳感器測量得到隨時間變化而溫度發生變化的曲線,如圖2(筆者實驗時環境溫度即起始溫度為20.8℃)所示,最高溫度可接近70℃。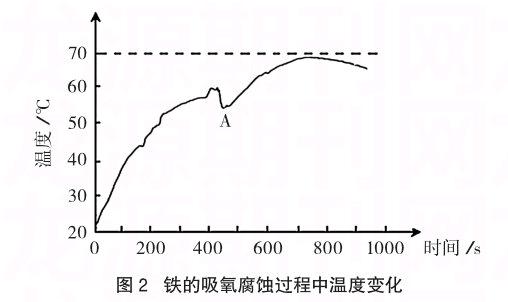
2.2 實驗優點
(1)操作簡單,現象明顯,尤其是溫度變化給學生較強的沖擊力。
(2)數字化實驗的應用使實驗從定性到半定量化。
(3)密切聯系生活,能說明暖寶寶的工作原理,引導學生選擇使用合格產品以防止使用過程中可能造成的燙傷。
2.3 應用說明
本實驗可應用于高中化學必修2模塊中有關“化學反應與能量變化”的教學,可用于演示實驗,也可用于學生課后探究(自制“暖寶寶”)活動。教學中可從生活中暖寶寶的使用引入,利用上述實驗幫助學生感知放熱反應及其應用,同時通過溫度傳感器幫助學生初步認識從定性到半定量的研究方法,加深對鐵與氧氣、水反應過程中能量變化的認識:2Fe(s)+3/2O2(g)+xH2O(l)=Fe2O3·xH2O(s),ΔH<0。其中圖2中A點是對濾紙包輕輕搓揉后,使結塊的混合物松散增大了反應物接觸面積所致。若不斷搓揉濾紙包,曲線會更不規則,但能使反應溫度上升更高。本實驗還可滲透情感態度價值觀的教育。
3 鐵粉的吸氧腐蝕
吸氧腐蝕是學生學習過程中的一個難點,尤其是對在中性或弱酸性條件下,由鐵、碳組成的原電池的正極電極反應難以理解,大多數學生常常認為是H2O中H+參與得電子,即發生析氫腐蝕。為增強實驗的直觀性,突出氧氣參與反應這一特點,設計如下實驗。
3.1 實驗設計及過程
裝置如圖3所示,用膠頭滴管吸取約4mL 1 mol/L NaCl溶液使濾紙浸潤并粘附在廣口瓶內側。稱取2.0g還原鐵粉、2.5g活性炭粉,攪拌均勻,倒入廣口瓶并迅速放入氧氣傳感器探頭并塞緊瓶塞,輕輕轉動廣口瓶,使鐵粉和碳粉混合物盡可能均勻附著在廣口瓶內壁。同時開始采集氧氣含量數據,約3分鐘后瓶內氧氣含量降至0.5%以下,約5~6分鐘即可使瓶內氧氣含量降至0.1%,10分鐘左右降為零,隨時間變化氧氣含量變化如圖4中帶“▲”的曲線。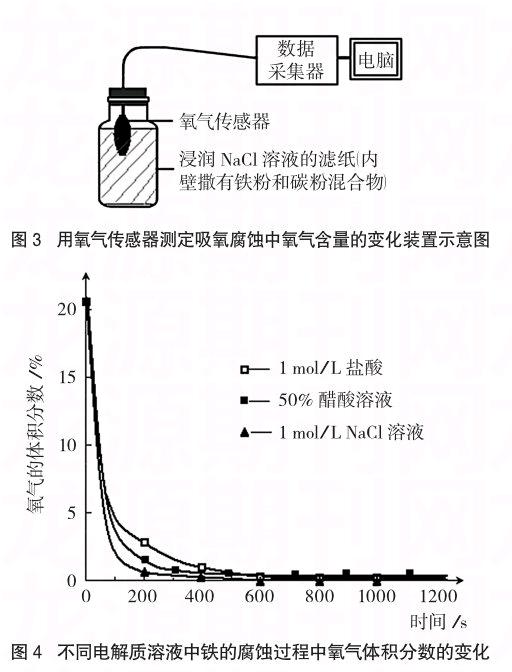
3.2 實驗優點
(1)現象直觀,便于學生認識到氧氣在中性或弱酸性條件下均參與了正極反應,即發生:O2+2H2O+4e-=4OH-。
(2)探究味更濃,有利于學生在實驗中學會控制變量,如鐵粉和碳粉不變,僅改變電解質溶液,探究不同條件下鐵的腐蝕。
(3)趣味性更強,讓學生感受數字實驗帶來的便捷。圖4曲線顯示,無論是在中性介質(NaCl溶液)中,還是弱酸性介質(稀鹽酸或稀醋酸)中,裝置內氧氣含量均減少,說明鐵均可以發生吸氧腐蝕。
3.3 應用說明
本實驗可應用于高中化學選修4“化學反應原理”模塊中有關“金屬的腐蝕”教學,可用于課堂演示或學生課后的探究活動,如用1 mol/L鹽酸和50%醋酸溶液代替氯化鈉溶液同樣顯示氧氣含量下降(如圖4中分別帶“□”和“■”的曲線),且用壓強傳感器測出此時瓶內壓強減小,排除氧氣含量下降并非由于產生H2所致,說明在該酸性條件下鐵仍然以發生吸氧腐蝕為主。還可以繼續探究在Na2CO3溶液、NaHCO3溶液等其他電解質溶液中是否會加快金屬的腐蝕?是否也會發生吸氧腐蝕?多大pH條件下主要發生析氫腐蝕。實驗有助于幫助學生理解中性或弱酸性條件下金屬發生吸氧腐蝕這一教學難點,讓學生體會實驗技術的進步對于化學學科學習和發展的促進作用。
4 影響化學反應速率的因素
利用上述3.1實驗中鐵的吸氧腐蝕實驗還可進一步探究影響化學反應速率(鐵的腐蝕速率)的因素。
4.1 實驗設計及過程
先完成上述3.1實驗,得到如圖5中曲線①(橫坐標為時間,縱坐標為氧氣含量)。其他條件不變,將稱量并混合好的鐵粉、碳粉用濾紙包好,以減小其與瓶中空氣的接觸面積,用1 mol/L NaCl溶液浸潤濾紙包再放入相同廣口瓶中,同時開始采集氧氣含量數據,得到如圖5中曲線②。
4.2 實驗優點
(1)圖示形式直觀,有助于學生感受到接觸面積和氧氣濃度等因素對鐵的腐蝕速率的影響,進而形成相關認知。
(2)有利于體現宏觀、符號、曲線等表征元素在本節內容教學中的價值,加強學生對非連續文本的理解。
(3)有利于教師在教學中應用POD(預測-觀察-解釋)教學策略,即先讓學生預測不同接觸面積時鐵發生吸氧腐蝕時氧氣含量的變化快慢,再通過數字實驗觀察現象,最后解釋并形成結論,同時滲透控制變量的研究方法。
4.3 應用說明
本實驗可應用于高中化學選修4“化學反應原理”模塊中有關“化學反應速率的影響因素”教學。首先讓學生預測在鐵粉和碳粉混合物以不同方式放入瓶內后,瓶中氧氣含量的變化曲線;再借助于數字化實驗手段形成圖形并對比;最后進行分析解釋,得出結論。同時,同一曲線的變化趨勢也體現了氧氣濃度對腐蝕速率的影響,即隨反應時間的增長,曲線越來越平緩,說明反應速率越來越慢。
此外還可以通過上述實驗設計編制相應探究性試題,以電化學、化學反應速率、金屬性質、化學反應能量變化等知識為考查內容,突出對學生實驗能力和科學探究能力的考查。已有很多老師編制出相關內容的優質試題[8,9],其中2014年安徽省高考理綜第28題在借鑒PISA試題編制理念的基礎上,以金屬的腐蝕為情境[10],設計的科學探究題較為經典。
參考文獻:
[1]章永軍.利用傳感器分析空氣中氧氣含量測定的誤差[J].化學教與學,2011,(7):92~93.
[2]楊承印等.密閉容器中殘余氧含量測定的思考[J].化學世界,2010,(11):652~655.
[3]朱華英,劉懷樂.空氣里氧氣含量的測定實驗值得改進[J].教學儀器與實驗,2005,(7):25.
[4]吳建文等.脫氧劑量的研究和應用[J].食品科學,2002,(5):148.
[5]賴軒.脫氧劑在食品保鮮中的作用機理、應用與開發[J].廣東科技,2008,(5):60.
[6]徐泓.利用“食品脫氧劑”測定空氣中氧氣含量的系列設計[J].化學教育,2010,(11):71~72.
[7] Just Breathe: The Oxygen Content of Air [J]. Journal of Chemical Education,2001,(4):512A~512B.
[8]譚宗俊,張莉.鋼鐵吸氧腐蝕速度的探究題[J].化學教學,2010,(9):79~80.
[9]但世輝,李斌.一道關于“鐵的吸氧腐蝕”的原創題[J].化學教學,2012,(5):61~63.
[10]夏建華. PISA科學評價對編制化學科學探究題的啟迪[J].化學教學,2014,(9):67.

