分子印跡電化學發光分析
李素萍關懷民徐國寶*,4童躍進*
(福建師范大學化學與化工學院1,材料科學與工程學院2,福建省高分子材料重點實驗室3,福州 350007)4(中國科學院長春應用化學研究所電分析化學國家重點實驗室,長春 130022)
評述與進展
分子印跡電化學發光分析
李素萍1關懷民2,3徐國寶*1,4童躍進*1
(福建師范大學化學與化工學院1,材料科學與工程學院2,福建省高分子材料重點實驗室3,福州 350007)4(中國科學院長春應用化學研究所電分析化學國家重點實驗室,長春 130022)
分子印跡電化學發光兼具分子印跡技術及電化學發光方法兩者的優點,即高靈敏度、高選擇性、可控性好、易于微型化和操作簡單等特點。近幾年來在生物仿生傳感器、有害農藥殘留物質及食品安全監測等方面具有廣泛的應用。本綜述簡要介紹分子印跡電化學發光傳感器及分子印跡固相萃取電化學發光的概況,并對其今后的研究趨勢進行展望。
分子印跡;電化學發光;綜述
1 引 言
電化學發光(Electrochemiluminescence,ECL)是通過電化學激發反應產生發光的現象[1]。與其它分析技術相比,ECL具有靈敏度高、可控性好、線性范圍寬、裝置簡單、成本低等優點。近年,電化學發光的研究得到了蓬勃發展。商品化的電化學發光免疫分析和DNA探針分析被廣泛應用于醫療診斷、食品安全、生物戰試劑檢測以及環境監測等多種領域[2]。電化學發光還被用做高效液相色譜、毛細管電泳以及微流控芯片的檢測器,用于檢測眾多的共反應物,特別是含有氨基的各種物質[3~5]。
分子印跡技術(Molecularly imprinted technology,MIT)是一種以目標分子(模板分子或印跡分子)為模板,合成對該分子具有特異性識別功能的聚合物的技術。MIT最早起源于免疫學,1931年,前蘇聯科學家Polyakov[6]首次提出“分子印跡”這一概念。該技術最初是從受體-抗體相互作用得到啟發,融合了高分子化學、分子識別技術、仿生物學等形成的。而標志“分子印跡”萌芽的是1949年Dickey提出的“專一性吸附”概念。經過80多年的發展,分子印跡聚合物這一概念演變成包含了各式各樣的有機高分子,極大地豐富了分子印跡的研究內容。MIT的研究核心內容則是分子印跡聚合物(Molecularly imprinted polymer,MIP)[7,8],通過MIP的特異性識別位點可以實現了從非生物活體獲得“抗體”[9]。與其它傳統的傳感器相比,分子印跡傳感器[10~12]具有對目標分子高度專一識別性,此外其在機械穩定性和熱穩定性方面也不遜色于化學傳感器,已經廣泛應用于藥物分析[13]、環境有害物質痕量分析[14,15]、固相萃取[16,17]和色譜分離[18]等各個研究領域。
隨著生命科學技術、材料科學和現代分析檢測手段的深入研究,分子印跡電化學傳感器在各方面都得到了更加廣泛的應用。盡管如此,分子印跡電化學傳感器畢竟發展時間較短,還有諸如電流效率通常較低和檢測信號較弱等很多問題等待研究者進一步解決。
ECL在靈敏度和可控性方面具有獨特的優勢,而MIP在特異性識別方面具有獨特的優勢,將二者有機結合起來,構建新型的MIP-ECL檢測方法用于分析領域將是一個活躍的研究方向。因此本綜述將簡要介紹分子印跡電化學發光近幾年的研究進展,并對其進行展望。
2 分子印跡-電化學發光傳感器的發展與應用
目前,MIP-ECL傳感器已在檢測殘留痕量農藥[19~22]、毒品[23,24]、藥物[25]、雙酚 A[26]、氨基酸[27]和蛋白質[28,29]等方面顯現出了特有的優點。以下將簡要闡述該傳感器的應用。
2.1 蛋白質的檢測
蛋白質是一類重要的生物大分子,是生命的物質基礎。如血紅蛋白是血紅細胞中運載氧氣和二氧化碳分子保持身體血液酸堿平衡的一類重要含鐵蛋白質。在臨床上,血紅蛋白的濃度與地中海貧血、白血病、心臟疾病等的診斷密切相關。因此,精確定量檢測血紅蛋白水平在臨床上有著重要的應用。至今為止,已應用如光譜、電化學方法和化學發光以及ELISA多種檢測分析方法來檢測。應用分子印跡技術能夠創建比天然受體更能承受極端環境條件如高溫、高壓及極端pH值等的合成受體。因此應用分子印跡技術檢測蛋白質的方法在近十多年來也受到了研究者們的密切關注[30~34]。Wu等[30]基于分子印跡技術在血紅蛋白模板存在下電化學聚合丙烯酰胺構建血紅蛋白電化學傳感器。以鐵氰化鉀作為表征印跡膜的探針,該MIP電極顯現出了對模板分子特異的識別性能和高的靈敏度。Kan等[32]以共價法將血紅蛋白嫁接于功能化后的磁性Fe3O4納米顆粒表面,再通過溶膠凝膠表面印跡聚合制得核殼微納米磁性分子印跡聚合物。該印跡聚合物對目標分子的吸附量在pH 6.5條件下達到10.5 mg/g,相較于非印跡聚合物高出了4.6倍。
相較于以上各種技術的發展,Zhou等[28]基于磁性分子印跡聚合物(MMIPs)作為捕獲探針制備單抗體“三明治”型電化學發光免疫傳感器用于檢測血紅蛋白。他們首先在磁性Fe3O4納米顆粒表面以溶膠凝膠法及表面印跡技術合成MMIPs,并將抗體修飾于Ru@SiO2@Au納米復合材料上,作為與目標分子結合的標記物。當目標分子富集于MMIPs上后,帶有ECL信號標記的抗體與目標分子相結合。最后,通過磁場作用將制備好的“三明治”型免疫復合物修飾于絲網印刷碳電極上,在最優條件下進行ECL測試。該傳感器線性范圍為0.1~4×104μg/L,檢出限(S/N=3)為0.023 μg/L。相比于傳統的雙抗體三明治型電化學發光免疫傳感器,該傳感器具有以下優點:(1)MMIP捕獲探針成本相對比較低,易量產,且克服了普通抗體捕獲探針易失活等不利因素;(2)該探針易固定在電極上,也容易通過施加和移除磁場來洗脫掉,所以,該傳感器能夠簡單的生產和再生;(3)該探針比普通探針具有更多識別的結合位點,使得MMIPs能夠富集溶液中超痕量的抗原,極大地增強了檢測靈敏度。
Zhou等[29]在上述技術基礎上,應用溶膠凝膠法和表面分子印跡及抗原決定基法印跡技術在磁性Fe3O4納米顆粒表面合成以人類免疫球蛋白 G (Human IgG)為模板的磁性分子印跡聚合物(MMIPs),將該MMIPs作為捕獲探針構建了檢測人類免疫缺陷病毒1型抗體(anti-HIV-1)的“三明治”型電化學發光免疫傳感器,如圖1所示。其中,抗原決定基印跡法是應用假模板進行印跡,即用Human IgG代替anti-HIV-1作為印跡模板,Human IgG具有與anti-HIV-1相同的Fc區以及不同的Fb區,當anti-HIV-1在MMIPs上富集后,不同的Fb區可以用掩蔽劑進行掩蔽。作者應用MMIPs代替HIV-1抗原作為捕獲探針,辣根過氧化物酶(HRP)修飾的 HIV-1 (HRP-HIV-1)作為傳感器的標記物,當目標分子anti-HIV-1富集于MMIPs上后與溶液中的標記物相結合形成“三明治”型免疫復合物。最后,通過磁場作用將其修飾于絲網印刷碳電極上,結合HRP在魯米諾-雙氧水(luminol-H2O2)ECL系統中催化作用,檢測魯米諾的發光強度,從而實現目標分子的檢測。首先,該傳感器應用了假模板進行印跡,假模板易得,成本相對較低;其次,聚合得到的MMIPs易量產,且能夠通過洗脫模板重復使用,大大降低了免疫傳感器的成本;最后,ECL檢測方法的應用,增強了傳感器的靈敏度,得到了抗體稀釋度為1∶20000~1∶50的檢測范圍和1∶60000(S/N=3)的檢出限。在人血清樣本的檢測中結果表明,所研制的“三明治”型免疫傳感器比單獨的MMIPs的抗干擾能力更強,主要是因為抗原抗體的高度專一識別能力,使其選擇性更好。該方法具備制備簡單、成本較低、靈敏度和選擇性高等優點,在生化分析領域具有潛在應用價值。
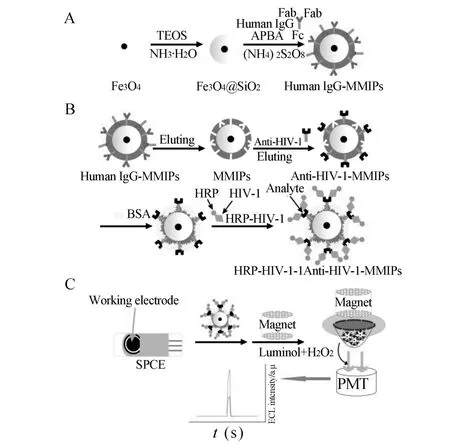
圖1 檢測anti-HIV-1的“三明治型”MIP-ECL免疫傳感器構建過程[29]Fig.1 Procedure for constructing a MIP-ECL immunosensor and the determination of anti-human immunodeficiency virus-1(HIV-1)[29]
2.2 農藥的檢測
農藥殘留等問題一直是全球關注的食品安全問題。檢測方法的簡便快速和經濟高效一直是分析領域研究的目標,MIP-ECL方法的出現為農藥檢測提供了一種新的有效方法。
Li等[19]構建MIP-ECL傳感器用于超痕量異丙隆除草劑(IPU)的檢測,該檢測主要是基于目標分子IPU與葡萄糖氧化酶(GOD)標記的IPU(GOD-IPU)間的競爭反應。作者以IPU為模板在金電極上電聚合鄰氨基酚單體合成分子印跡膜。用IPU將印跡孔穴屏蔽后,將其浸漬于GOD-IPU的溶液中,得到GOD-IPU替代IPU的分子印跡膜。再將其浸漬于樣品溶液中,樣品溶液中的IPU與MIP膜上GOD-IPU發生競爭反應。待反應后,分子印跡膜上殘留的GOD-IPU催化葡萄糖產生雙氧水,與魯米諾反應,增強電化學發光信號。當GOD-IPU分子被樣品中IPU分子取代后,電化學發光強度減少。因此,可以根據該電化學發光信號的減弱,定量分析模板分子IPU的濃度。基于葡萄糖氧化酶的催化作用,該傳感器的電化學發光信號增強,具有靈敏度和選擇性高、響應快、檢出限低等優點。該法的檢測范圍為9×10-11~5.1×10-9mol/L,檢出限為3.78×10-12mol/L。與檢測IPU的其它方法相比,檢出限更低。在應用該傳感器檢測水溶液樣品時,回收率達到98.5%~102.1%。

圖2 用于檢測GA3的ECL-MIP傳感器的構建過程[22]Fig.2 Procedure to construct a MIP-ECL sensor and determination of gibberellin A3(GA3)[22]
Li等[22]基于赤霉素A3(GA3)和羅丹明B(RhB)標記的GA3(RhB-GA3)在分子印跡膜上的競爭結合反應構建檢測GA3的新型MIP-ECL傳感器,如圖2所示。作者在金電極上用電聚合法以鄰苯二胺作為單體,GA3作為模板分子進行印跡得到印跡膜。用 GA3將印跡孔穴屏蔽后,將其浸漬于 RhB-GA3的溶液中,得到RhB-GA3替代GA3的分子印跡膜,將此電極應用于GA3的檢測。樣品中GA3與電極上的RhB-GA3競爭反應后,分子印跡膜上殘余的RhB-GA3被電化學氧化產生RhB氧化產物。該氧化產物能夠與溶液中的溶解氧反應生成過氧化物離子自由基(),過氧化物與魯米諾反應,極大地提高金電極上魯米諾電化學發光信號。當RhB-GA3被樣品中GA3分子取代后,電化學發光強度減小。因此,可以根據該電化學發光信號的減弱,定量分析GA3的濃度。該傳感器的檢測濃度范圍1×10-11~3×10-9mol/L,檢出限為3.45×10-12mol/L。相對于GA3濃度1000倍的Na+、Ca2+、Mg2+、S、Cl-和C,500倍的葡萄糖、蔗糖、谷氨酸、Fe2+、Al3+和Zn2+,300倍的Cu2+和Hg2+都未能影響GA3產生的ECL信號。檢測啤酒樣品時,實驗回收率達到96.0% ~103.2%。該傳感器具有靈敏度高、選擇性好和響應快等優點。
除以上方法外,Li等[21]應用納米顆粒表面印跡結合電化學發光方法選擇性識別磺酰脲類除草劑甲基噻吩磺隆(TFM)。作者在功能化后的SiO2納米顆粒表面進行TFM分子印跡,后用沉積法在玻碳電極表面修飾上印跡的核殼SiO2納米球。在印跡膜表面,作者用HF將SiO2球刻蝕得到多孔結構印跡膜。目標分子TFM在印跡膜上結合時能夠觀察到魯米諾的電化學發光現象,且相比于空白,結合上目標分子的ECL強度增強了2.7倍。這是由于TFM在堿性條件下分解產生CO2,CO2能夠與溶液中溶解氧還原生成的OOH-反應生成能夠分解成不同的過氧化物自由基,如這些強氧化性的自由基加速了魯米諾的氧化反應,從而增強了魯米諾的發光強度。因此,可以應用該現象來構建對TFM有特異識別的傳感器。多孔印跡膜的應用增加了膜上電子的傳輸,且目標分子TFM在反應中增強了魯米諾的發光效應,因此該傳感器不僅印跡效率得到了提高,靈敏度也相應增強。它的檢測范圍為5.0×10-10~1.0×10-7mol/L,檢出限為0.32 nmol/L。其具有經濟、高靈敏度、快速、特異性識別及穩定性良好等優點,在檢測磺酰脲類除草劑的應用上具有潛在的應用價值。
2.3 毒品的檢測
ECL曾被用于毒品檢測,能檢測到nmol濃度水平,但在原位氣體檢測領域該靈敏度仍是不夠。為了提高檢測的靈敏度和選擇性,文獻[23,24]應用ECL固態電極結合溶膠凝膠分子印跡法構建檢測毒品的分子印跡電化學發光傳感器。該類傳感器制備過程可分為兩步:一是先將電化學發光物質用Nafion和多壁碳納米管復合材料固定在玻碳電極上,形成第一層膜;二是在已修飾上發光物質膜的表面再修飾一層分子印跡溶膠凝膠聚合物薄膜。如Han等[23]應用該法制備了用于檢測甲基苯丙胺的MIP-ECL傳感器,在1.0×10-10~1.0×10-14mol/L濃度范圍內線性良好,檢出限為4.0× 10-15mol/L。該傳感器極高的靈敏度使其能在封閉的容器中通過氣體來檢測到毒品。為了驗證該傳感器的選擇性,他們將TPA、L-色氨酸、L-絡氨酸、甘氨酸、L-蘇氨酸、海洛因以及嗎啡等加入樣品溶液中,進行干擾實驗,發現即使這些干擾物的濃度比目標分子的濃度(0.10 nnol/L)高100倍,仍沒有ECL信號干擾,該傳感器具有良好的選擇性。
3 分子印跡固相萃取-電化學發光分析
除了在電極上直接或者間接修飾MIP用于ECL檢測,還可將MIP作為固相萃取吸附劑進行預處理樣品,用于ECL檢測雙酚 A[26]、萊克多巴胺[35]、酚酞[36]、氯霉素[37]、食物殘留有機物[38]和氨基酸[39]等。MIP作為萃取的吸附劑,不僅融合了MIP的專一識別性能,還填補了傳統固相萃取劑對復雜樣品難分離的缺點。
Wang等[35]基于萊克多巴胺(RAC)對Ru(bpy)2+3-DBAE體系ECL信號的猝滅作用,以RAC作為模板,聚乙二醇為致孔劑,環氧樹脂為功能單體,在鐵芯攪拌子表面印跡。當洗脫掉致孔劑與模板后得到識別RAC的MIP攪拌子。一定轉速下該攪拌子在樣品溶液中吸附萃取目標分子,后經解吸附處理得到純化的目標分子溶液用于ECL檢測。由于RAC對-二丁基乙醇胺(DBAE)體系ECL的猝滅作用,RAC濃度在1.0×10-10~5.0×10-8mol/L范圍與ECL強度呈現良好的線性關系,檢出限為3.5× 10-12mol/L。他們將攪拌子吸附萃取法與MIP及ECL相結合,能選擇性快速識別分析物,富集能力強,靈敏度高,抗干擾能力好。該方法達到良好的檢測目的,也拓寬了分子印跡技術與ECL方法在食品安全分析領域的應用。
Guo等[38]基于孔雀綠對luminol體系的ECL具有抑制效應,以孔雀綠為模板,選用甲基丙烯酸作為功能單體,二甲基丙烯酸二乙醇酯作為交聯劑,偶氮二異丁腈作為引發劑制備分子印跡聚合物。經過研碎,過篩,得到粒徑大小為32~96 μm的MIP顆粒,以其為萃取材料,自制固相萃取小柱。通過自制萃取小柱對樣品純化富集分析物,對MIP上吸附的目標分子進行解吸附處理后用于ECL檢測。因孔雀綠對Luminol的ECL具有抑制作用,因此可以根據ECL強度對分析物進行定量分析。該分子印跡固相萃取小柱的干擾實驗表明,該方法具有較強的抗干擾能力。ECL檢測結果表明,該方法的靈敏度較高,檢出限為6×10-12mol/L。作者應用經典整體柱法制備印跡聚合物,用于自制固相萃取小柱,成本相對較低,萃取效率高;結合ECL檢測分析物,提高了檢測的靈敏度,且相對于色譜分析技術,降低了儀器成本。
4 用于構建MIP-ECL傳感器的電化學發光體系
4.1 魯米諾-H2O2體系
魯米諾(Luminol)電化學發光通常在堿性溶液中,在過氧化氫存在的情況下,以電化學氧化的方式發生。但現已有研究表明,魯米諾可以在多種實驗條件下產生電化學發光,如不同的溶劑、氧氣或者過氧化氫存在或不存在的情況,不同的電極和有Br-和Cl-等其它物質共存的情況。在已構建的MIP-ECL傳感器中,主要應用到的發光體系有:(1)在Luminol-H2O2系統中通過目標分子上修飾酶[19,22,28]催化底物產生H2O2,H2O2與Luminol反應增強ECL信號;(2)Luminol發光系統中,通過目標分子對Luminol的直接作用,增強[21]或者抑制[38]luminol發光;(3)在Luminol-H2O2系統中,目標分子在MIP孔洞上的結合與否,增加或減少電子傳遞,從而實現目標分子的定量檢測[20]。
4.2體系
5 展 望
分子印跡電化學發光分析近年來得到較快發展,但是與其它分子印跡分析相比,分子印跡電化學發光是一個新興的研究方向,研究報道還相對較少,還需要在以下方面開展深入研究:(1)目前電化學發光分析中,使用的電位相對較高,會影響分子印跡材料的穩定性,需要發展更加穩定的分子印跡材料或研發低電位下發光的體系;(2)發展透光性好的分子印跡材料和新型信號放大技術,以提高檢測靈敏度;(3)發展在水溶液中具有良好識別能力的分子印跡材料;(4)針對有些常用電化學發光體系在堿性條件下發光強度好的特點,發展在堿性條件下具有良好識別能力和穩定性的分子印跡材料;(5)引進新的電化學發光體系和分子印跡方法,拓寬分子印跡電化學發光分析應用范圍;(6)研制便攜的電化學發光檢測裝置等。分子印跡和電化學發光具有廣泛的應用范圍[41,42]、良好的發展和應用前景。
1 XU Guo-Bao,DONG Shao-Jun.Chinese J.Anal.Chem.,2001,29(1):103-108
徐國寶,董紹俊.分析化學,2001,29(1):103-108
2 Hu L Z,Xu G B.Chem.Soc.Rev.,2010,39(8):3275-3304
3 Yin X B,Dong S J,Wang E.TrAC,Trends Anal.Chem.,2004,23(6):432-441
4 Wei H,Wang E.TrAC Trends Anal.Chem.,2008,27(5):447-450
5 Kong D X,Lin B,Han Y,Zheng X,Zhou X,Li Q,Chi Y,Chen G N.Electrochim.Acta,2014,123:111-116
6 Polyakov M V.Zh.Fiz.Khim.,1931,2:799-805
7 Li W,Li S J.Adv.Polym.Sci.,2007,206:191-210
8 Bossi A,Bonini F,Turner A P,Piletsky S A.Biosens.Bioelectron.,2007,22(6):1131-1137
9 Mosbach K,Ramstrom O.Nat.Biotechnol.,1996,14(2):163-170
10 Andersson L I.J.Chromatogr.B,2000,745(1):3-13
11 Guan G J,Liu B H,Wang Z Y,Zhang Z P.Sensors,2008,8(12):8291-8320
12 Suriyanarayanan S,Cywinski P J,Moro A J,Mohr G J,Kutner W.Top.Curr.Chem.,2012,325:165-265
13 Gurler B,Ozkorucuklu S P,Kir E.J.Pharm.Biomed.Anal.,2013,84:263-268
14 Sergeyeva T A,Piletsky S A,Brovko A A,Slinchenko E A,Sergeeva L M,El'skaya A V.Anal.Chim.Acta,1999,392 (2-3):105-111
15 Li H D,Guan H M,Dai H,Tong Y J,Zhao X N,Qi W J,Majeed Saadat,X G B.Talanta,2012,99:811-815
16 Chianella I,Piletsky S A,Tothill I E,Chen B,Turner A P F.Biosens.Bioelectron.,2003,18(2-3):119-127
17 Peng Y,Xie Y,Luo J,Nie L,Chen Y,Chen L,Du S,Zhang Z P.Anal.Chim.Acta,2010,674(2):190-200
18 Cheong W J,Yang S H,Ali F.J.Sep.Sci.,2013,36(3):609-628
19 Li S,Tao H,Li J P.Electroanalysis,2012,24(7):1664-1670
20 Li X,Li J,Yin W,Zhang L.J.Solid State Electrochem.,2014,18(7):1815-1822
21 Li H F,Xie C G,Fu X C.Sens.Actuators,B,2013,181:858-866
22 Li J P,Li S H,Wei X P,Tao H L,Pan H C.Anal.Chem.,2012,84(22):9951-9955
23 Han C F,Shang Z Y,Zhang H H,Song Q J.Anal.Methods,2013,5(21):6064-6070
24 SHANG Zhe-Yi,HAN Chao-Feng,SONG Qi-Jun.Chinese J.Anal.Chem.,2014,42(6):904-908
商哲一,韓超峰,宋啟軍.分析化學,2014,42(6):904-908
25 Wu B,Wang Z,Xue Z,Zhou X,Du J,Liu X,Lu X.Analyst,2012,137(16):3644-3652
26 Jiang X H,Ding W J,Luan C L.Can.J.Chem.,2013,91(8):656-661
27 DING Zhao-Yun,LI Chun-Yang,SONG Qi-Jun.Chinese J.Anal.Chem.,2013,41(10):1543-1548
丁照云,李春陽,宋啟軍.分析化學,2013,41(10):1543-1548
28 Zhou J,Gan N,Hu F,Li T,Zhou H,Li X,Zheng L.Sens.Actuators,B,2013,186:300-307
29 Zhou J,Gan N,Li T,Hu F,Li X,Wang L,Zheng L.Biosens.Bioelectron.,2014,54:199-206
30 Wu S,Tan W,Xu H.Analyst,2010,135(10):2523-2527
31 Whitcombe M J,Chianella I,Larcombe L,Piletsky S A,Noble J,Porter R,Horgan A.Chem.Soc.Rev.,2011,40(3): 1547-1571
32 Kan X,Zhao Q,Shao D,Geng Z,Wang Z,Zhu J J.J.Phys.Chem.B,2010,114(11):3999-4004
33 Kan X,Xing Z,Zhu A,Zhao Z,Xu G,Li C,Zhou H.Sens.Actuators,B,2012,168:395-401
34 Toshifumi T,Takayuki H.Org.Biomol.Chem.,2008,6(14):2459-2467
35 Wang S,Wei J,Hao T T,Guo Z Y.J.Electroanal.Chem.,2012,664:146-151
36 Guo Z,Hao T,Shi L,Gai P,Duan J,Wang S,Gan N.Food Chem.,2012,132(2):1092-1097
37 HAO Ting-Ting,XIE Wen-Ting,LI Qin-Fen,GUO Zhi-Yong.Chinese J.Anal.Lab.,2012,31(2):105-108
郝婷婷,謝文婷,李琴芬,郭志勇.分析試驗室,2012,31(2):105-108
38 Guo Z,Gai P,Hao T,Wang S,Wei D,Gan N.J.Agric.Food.Chem.,2011,59(10):5257-5262
39 Lu J,Ge S,Wan F,Yu J.J.Sep.Sci.,2012,35,320-326
40 LI Hai-Juan,HAN Shuang,HU Lian-Zhe,XU Guo-Bao.Chinese J.Anal.Chem.,2009,37(11):1557-1565
李海娟,韓雙,胡連哲,徐國寶.分析化學,2009,37(11):1557-1565
41 FU Cong,LI Jian-Ping.Chinese J.Anal.Chem.,2014,42(3):315-319
傅聰,李建平.分析化學,2014,42(3):315-319
42 SUN A-Long,ZHENG Xing-Wang.Chinese J.Anal.Chem.,2014,42(8):1220-1224
孫阿龍,鄭行望.分析化學,2014,42(8):1220-1224
This work was supported by the National Natural Science Foundation of China(Nos.21274022,21175126)
Molecular Imprinting Electrochemiluminescence Analysis
LI Su-Ping1,GUAN Huai-Min2,3,XU Guo-Bao*1,4,TONG Yue-Jin*1
1(College of Chemistry and Chemical Engineering,Fujian Normal University,Fuzhou 350007,China)
2(College of Materials Science and Engineering,Fujian Normal University,Fuzhou 350007,China)
3(Fujian Key Laboratory of Polymer Materials,Fuzhou 350007,China)
4(State Key Laboratory of Electroanalytical Chemistry,Changchun Institute of Applied Chemistry, Chinese Academy of Sciences,Changchun 130022,China)
Molecularly imprinted electrochemiluminescence method combines the advantageous properties of molecularly imprinted polymer and electrochemiluminescence,such as high sensitivity,good selectivity,good controllability, easy miniaturization and simple operation. In recentyears, molecularly imprinted electrochemiluminescence has
much attention in the fields of biomimetic sensors,hazardous pesticide residue detection,and food safety monitoring,etc.In this review,the research progresses of molecularly imprinting electrochemiluminescence sensors and the applications of molecularly imprinted polymers as solid phase extraction matrices in electrochemiluminescence analysis have been summari
zed,and the future research trends have been proposed.
Molecular imprinting;Electrochemiluminescence;Review
14 August 2014;accepted 10 November 2014)
2014-08-14收稿;2014-11-10接受
本文系國家自然科學基金資助項目(Nos 21274022,21175126)
*E-mail:guobaoxu@ciac.ac.cn;tongyuejin@fjnu.edu.cn
10.11895/j.issn.0253-3820.140694

