促紅細胞生成素對外傷性顱腦損傷大鼠神經絲的保護作用
劉健,高佳星,汪葉松
(1.四川省綿陽市人民醫院 腦外科,四川 綿陽 621000;2.四川省綿陽市人民醫院 婦產科,四川 綿陽 621000;3.浙江大學醫學院附屬第二醫院 腦外科,浙江 杭州 310000)
?
促紅細胞生成素對外傷性顱腦損傷大鼠神經絲的保護作用
劉健1,高佳星2,汪葉松3
(1.四川省綿陽市人民醫院 腦外科,四川 綿陽 621000;2.四川省綿陽市人民醫院 婦產科,四川 綿陽 621000;3.浙江大學醫學院附屬第二醫院 腦外科,浙江 杭州 310000)
目的 觀察促紅細胞生成素(erythropoietin EPO)對創傷性顱腦損傷(traumatic brain injury,TBI)大鼠腦皮質中神經絲的影響,并探討其意義。方法 45只Wistar大鼠按隨機原則分為9組,正常對照組、顱腦損傷組(各組于建模后6、12、24、72 h取標本),EPO處理組(各組于建模后6、12、24、72 h取標本),每組5只,采用Myneurolab腦立體定向儀和Benchmark顱腦損傷撞擊器制作創傷性顱腦損傷模型。應用免疫組化法觀察上述時間點損傷灶周圍皮層神經絲的形態改變,Western blot檢測各時間點中神經絲蛋白H(neurofilament H,NF-H)的表達變化。結果 免疫組化結果顯示:正常對照組NF-H含量豐富,呈棕黃色絲狀結構,在腦皮質的大椎體細胞層、小椎體細胞層,海馬區,胼胝體中表達尤為明顯,而顱腦損傷組于腦外傷后6 h見NF-H較正常組稀疏,部分結構中斷,6~24 h內可見神經絲數目進一步減少,排列紊亂加重,至24 h破壞程度達到高峰,72 h時上述情況有所緩解,外傷后EPO處理組神經絲數量在各個時間點均比外傷組多,且排列較外傷組整齊。神經絲的密集程度在12 h達到高峰,然后逐漸降低。Western blot顯示:與正常組相比,顱腦損傷組損傷后 6h可見 NF-H 的表達減少(P<0.05)。6~12 h內NF-H蛋白表達持續減少(P<0.05),24 h 后達最低值(P<0.01),72 h時升高(P< 0.05)。但與顱腦損傷各組比較,EPO處理組NF-H的表達升高(P<0.05)。結論 EPO對腦具有保護作用,其可能機制為抑制神經絲蛋白降解。
促紅細胞生成素;創傷性腦損傷;神經絲
顱腦損傷發生率居高不下,目前護腦藥物療效不確切,尋找新的治療藥物成為當務之急[1]。神經絲三聯蛋白NF-L,NF-M,NF-H,是神經細胞的骨架蛋白,對于維持神經細胞的結構穩定,信號轉導,軸漿運輸等方面有重要作用。神經細胞骨架在腦損傷后15 min即可在損傷灶同側及對側檢測到有輕微的形態改變,并在24 h內降解逐漸加重[2]。通常在腦損傷后,三聯蛋白中神經絲蛋白H(neurofilament H,NF-H)的降解最為嚴重,因此常將其作為評價早期腦損傷程度的標志物[3]。近年來,多項細胞和動物實驗證實促紅細胞生成素(erythropoietin,EPO)可以減輕腦損傷,發揮神經保護作用,但其保護機制尚未完全明確[4]。美國國立衛生研究院(NIH)等多處研究機構進行臨床試驗的驗證EPO能否減輕顱腦損傷以及幫助患者獲得康復[5]。對于EPO的腦保護作用的研究多有報道[6-10],腦損傷后神經絲降解這一重要的病理生理機制的論述也常見,而對于EPO對神經絲的保護作用及其機制卻鮮有研究。因此,本文旨在觀察促紅細胞生成素對創傷性顱腦損傷(traumatic brain injury,TBI)大鼠腦皮質中神經絲的影響,并探討其意義。
1 材料與方法
1.1 實驗動物及分組 SPF級健康雄性Wistar 大鼠45只,8周齡,體質量(220±20)g,許可證號2003-0004,由湖北省疾控中心提供。按隨機原則分為9組,正常對照組、顱腦損傷組(各組于建模后6、12、24、72 h取標本),EPO處理組(各組于建模后6、12、24、72 h取標本),每組各5只,本實驗遵循《實驗動物保護條例》。
1.2 主要儀器及耗材 大鼠腦立體定向儀,電動顱鉆、BenchmarkTM電磁顱腦損傷撞擊器(美國Myneurolab公司);明膠海綿、骨蠟(武漢大學人民醫院);LS-50HJ不銹鋼壓力鍋(廣州罡然機電設備有限公司);MSE微量電子天平(上海亞津電子科技有限公司);GT10-1臺式高速離心機(北京時代北利離心機有限公司);DZF-6050干燥箱(北京北方利輝試驗儀器設備有限公司);GSS/DSS不銹鋼切片架(北京桑翌實驗儀器研究所);YD-202A切片機(廣州晟龍實驗儀器有限公司);OLYMPUS BX51顯微鏡(上海澤仕光電科技有限公司);水浴箱(常州中捷實驗儀器制造有限公司);SW-CJ-2D超凈工作臺(深圳市超杰實驗儀器有限公司);電化學發光(ECL)系統(美國Pierce公司)。
1.3 主要試劑 EPO[沈陽三生制藥股份有限公司,國藥準字(2000)沈三生s-01號];NF-H 鼠抗人多克隆抗體(Santa Cruz公司,sc-56575);辣根過氧化物酶(HRP)標記羊抗鼠二抗、SP 試劑盒、DAB 顯色試劑盒(武漢博士德);GAPDH(Santa Cruz 公司);4%多聚甲醛、PBS液(武漢大學基礎醫學院);胰蛋白酶(美國Amresco公司)。
1.4 方法 顱腦損傷模型的建立[11]:將實驗大鼠在室溫(23±2) ℃,濕度60%~80%的環境中適應性喂養2 d,用新配制的10%水合氯醛(4 mL/kg體質量) 腹腔注射麻醉,俯臥位,頭部固定于腦立體定向儀上,沿中線剪開頭皮,暴露右頂骨,用牙科鉆在冠狀縫后 1.5 mm、矢狀線旁2.5 mm處鉆孔并擴大為一直徑5 mm骨窗,注意保持硬腦膜完整。正常對照組骨窗造好后用骨蠟封閉,然后縫合頭皮。顱腦損傷組用同樣方法制造骨窗,然后用BenchmarkTM電磁顱腦損傷撞擊器撞擊硬腦膜(深度為2.0 mm,撞擊面直徑2.0 mm,撞擊速度為4 m/s),致右頂葉腦挫裂傷,保持硬腦膜完整,骨蠟封閉骨窗。造模好后供給飼料和飲水,分籠飼養。
EPO處理組如上方法造模成功后10 min,大鼠腹腔注射EPO,劑量為5000 U/kg,然后分籠飼養,常規供給飼料和飲水。
術后未見死亡大鼠,外傷后6、12、24、72 h時間段處死大鼠5只,取大鼠腦組織。
1.5 檢測指標 Western blot檢測NF-H的表達:將組織樣品按每10 mg組織加入 50 μL裂解液的比例加入裂解液,用玻璃勻漿器在冰浴中勻漿,直至組織充分裂解。裂解后10000 r/min 4 ℃ 離心5 min,取上清。取適量上清加入5×SDS loading buffer,沸水煮5~10 min 冷卻至室溫后上樣電泳。分別配制8%和12%的PAGE膠,各樣品取等量上樣電泳。GAPDH用12%的PAGE 膠;NF-H 用8%的PAGE分離膠。80 V電壓開始電泳,待溴酚藍跑過積層膠后將電壓升高至120 V,根據預染marker顯示,判斷目的蛋白充分分離后,停止電泳。以同一樣品中各目的蛋白OD值/GAPDH OD值的比值作為檢測蛋白的相對含量。用 Image-Pro Plus 6.0軟件進行圖象分析。
免疫組化法觀察NF-H的表達:把本實驗中固定好的的腦部石蠟切片置于65 ℃烘箱中,烘片2 h,脫蠟至水,用 PBS(pH7.4)沖洗3次,每次5 min;高壓熱修復;室溫下孵育;甩去PBS液,一抗1:200濃度稀釋,4 ℃過夜;甩去PBS液,用的二抗,濃度1:200每張切片加50~100 μL稀釋液,室溫下孵育30~60 min;顯色;自來水沖洗,復染,0.1%鹽酸分化,PBS沖洗返藍;切片經過梯度酒精(70%~100%)脫水干燥,透明,封固。PBS液代替一抗作為陰性對照。在200倍鏡下拍照觀察各組NF-H表達變化情況。
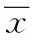
2 結果
2.1 NF-H的免疫組化結果 正常對照組 NF-H的免疫組化結果:NF-H在組織切片上含量豐富,呈棕黃色絲狀結構,在腦皮質的大椎體細胞層、小椎體細胞層,海馬區,胼胝體中表達尤為明顯。NF-H在大椎體細胞層中,大部分呈微細平行的絲狀排列,少部分交織成網狀(見圖1)。

圖1 正常對照組NF-H的免疫組化結果(×200)Fig.1 The immunohistochemical results of NF-H in normal control group(×200)
顱腦損傷組NF-H的免疫組化結果:腦外傷后6 h見神經絲較正常組稀疏,部分結構中斷,6~24 h內可見神經絲數目進一步減少,排列紊亂加重,至24 h破壞程度達高峰,72 h時上述情況有所緩解(見圖2)。

圖2 大鼠創傷性顱腦損傷后不同時間NF-H的免疫組化結果(×200)Fig.2 The immunohistochemical results of NF-H after traumatic brain injury at different time(×200)
EPO處理組的免疫組化結果:EPO 處理組與正常對照組相比,神經絲數量減少。但是在各個時間點均比外傷組的數量多,且排列較外傷組整齊。神經絲的密集程度在12h達到高峰,然后逐漸降低(見圖3)。

圖3 大鼠創傷性顱腦損傷使用EPO后不同時間NF-H的免疫組化結果(×200)Fig.3 The immunohistochemical results of NF-H after given EPO in rats with traumatic brain injury at different time(×200)
2.2 NF-H的Western blot免疫印跡結果 與對照組比較,顱腦損傷各組腦損傷后6 h即可見NF-H的表達減少(P<0.05)。6 h至12 h內NF-H蛋白表達持續性減少,24 h 后達最低值(P<0.01)。72 h時升高,但差異仍具有統計學意義(P< 0.05)。與顱腦損傷相同時間點比較,EPO處理組顯著提高了NF-H的表達(P<0.05),見表1。
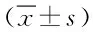
表1 Western blot檢測NF-H蛋白表達量Tab.1 The expression levels of NF-H protein detected by Western ±s)
**P<0.01,*P<0.05,與對照組比較,compared with control group;#P<0.05,與TBI組比較,compared with TBI group
3 討論
近年來,多項體內外實驗證實促紅細胞生成素可以發揮神經保護作用,目前研究表明其機制可能為:減少興奮性氨基酸毒性的作用、抗氧化作用、抗炎作用、抗凋亡作用、穩定細胞代謝、促進血管形成等[11]。神經絲三聯蛋白NF-L,NF-M,NF-H,是神經細胞的骨架蛋白,對于維持神經細胞的結構穩定、信號轉導、軸漿運輸等起重要作用。神經絲蛋白的降解會導致神經細胞的崩解,信號傳導障礙,及神經細胞功能紊亂,宏觀則表現為神經功能的缺失。國外研究表明NC證實腦損傷后NF-H的表達量會有明顯改變[12-14]。
本實驗將NF-H作為評價早期腦損傷的指標。和對照組比較:免疫組化表明,腦損傷后神經絲結構發生紊亂,損傷后6 h即可見神經絲較正常組稀疏,部分結構中斷,6~24 h內可見神經絲排列紊亂加重,至24 h破壞程度達到高峰;Western blot表明6、12、24、72 h各時段顱腦損傷組均較對照組NF-H量減少(P<0.01)。由此提示神經絲在腦損傷后會發生降解,且在早期即有明顯的改變。將腦損傷組和EPO處理組比較:腦損傷使用EPO之后,神經絲排列較外傷組整齊,神經絲的密集程度在12 h達到高峰,然后逐漸降低;Western blot表明各時段用藥組均較外傷組NF-H數量多(P<0.05),且在12 h和24 h更加明顯(P<0.01)。以上結果提示EPO具有保護細胞骨架抑制其降解的功能。尤其需要注意的是外傷用藥后12 h的神經絲更加密集,神經絲蛋白的表達量也是用藥后的最高值,表明EPO早期的腦保護作用更強。由于原發性腦損傷主要是由于受傷本身及傷后早期的病理生理演變所致,結合本實驗可以進一步推測EPO通過抑制神經絲蛋白的降解,從而對原發性腦損傷有較好的減輕作用。
本實驗通過腦立體定向儀和電磁顱腦損傷撞擊器制作創傷性顱腦損傷模型,致傷部位、范圍、深度、撞擊速度等參數都進行數字化設定,避免了常規顱腦損傷模型中的致傷程度不一致,重復性差的缺陷,較精確地模擬了臨床創傷性顱腦損傷的致傷特點,為實驗研究奠定了基礎。本試驗將NF-H作為評價腦損傷程度的指標,檢測不同的干預措施對NF-H的形態和量的改變,來評價干預措施對腦的影響。同時設定不同的觀察時間點,有利于進一步明確NF-H的變化趨勢。NF-H作為評價腦損傷程度的指標已經被廣泛使用,敏感性好,特異性高,同時通過免疫組化檢測的圖像直觀清晰,具有其他檢測指標無法替代的優勢。
綜上所述,創傷性顱腦損傷后,給予外源性EPO能抑制神經絲降解,達到保護神經作用。其通過何種途徑發揮抑制作用則需要進一步研究。
[1] Siren A,Fratelli M,Brines M,et al.Erythropoietin prevents neuronal apoptosis after cerebral ischemia and metabolic stress[J].Proc Natl Acad Sci,2001,98(7):4044-4049.
[2] 劉玲,董強.缺血性神經元損害中非谷氨酸依賴的鈣離子毒性機制,神經損傷與功能重建[J],2007,2(3):133-138.
[3] Zhang Y,Xiong Y,Mahmood A,et al.Therapeutic effects of erythropoietin on histological and functional outcomes following traumatic brain injury in rats are independent of hematocrit[J].Brain Res,2009,1294(9):153-164.
[4] 王雙坤,劉佰運,郝淑煜,等.創傷性腦損傷的動物實驗模型[J].中國交通醫學雜志,2005,19(4):327-329.
[5] Siren A,Fratelli M,Brines M,et al.Erythropoietin prevents neuronal apoptosis after cerebral ischemia and metabolic stress[J].Proc Natl Acad Sci,2001,98(7):4044-4049.
[6] Pina NC,Detloff MR,Bobroski WF,et al.Cytoskeletal protein degradation and neurodegener- ation evolves differently in males and females following experimental head injury[J].Exp Neurol, 2003,180(1):55-73.
[7] Saatman KE,Creed J,Raghupathi R,et al.Calpain as a therapeutic target in traumatic brain injury[J].Neurotheraputics,2010,7(1):31-42.
[8] Sinor AD,Greenberg DA.Erythropoietin protects cultured cortical neurons,but not astroglia,from hypoxia and AMPA toxicity[J].Neurosci Lett,2000,290(3):213-215.
[9] Ruscher K,Freyer D,Karsch M,et al.Erythropoietin is a paracrine mediator of ischemic tolerance in the brain:evidence from an in vitro mode1[J].J Neurosci,2002,22(23):10291-10301.
[10] Kumral A,Genc S,Ozer E,et al.Erythropoietin down regulates Bax and DP5 pro-apoptotic gene expression in neonatal hypoxic-ischemic brain injury[J].Biol Neonate,2005,89(3):205-210.
[11] 王雙坤,劉佰運,郝淑煜,等.創傷性腦損傷的動物實驗模型[J].中國交通醫學雜志,2005,19(4):327-329.
[12] Brines M,Cerami A.Erythropoietin-mediated tissue protection:reducing collateral damadge from the primary injury response[J].J Inter Med,2008,264(5):405-432.
[13] Nagai A,Nakagawa E,Choi HB,et al.Erythropoietin and erythropoietin receptors in human CNS neurons,astrocytes,microglia,and oligodendrocytes grown in culture[J].J Neuropathol Exp Neurol,2001,60(4):386-392.
[14] Grasso G,Sfacteria A,Cerami A,et al.Erythropoietin as a tissue-protective cytokine in brain injury:what do we know and where do we go?[J].Neuroscientist,2004,10(2):93-98.
(編校:王儼儼)
Neuroprotective effect of EPO on neurofilaments in rats with traumatic brain injury
LIU Jian1,GAO Jia-xing2,WANG Ye-song3
(1.Department of Neurosurgery, Mianyang City People’s Hospital, Mianyang 621000, China; 2.Department of Obstetrics and Gynecology, Mianyang City People’s Hospital, Mianyang 621000, China; 3.Department of Cerebral Surgery, The Second Affiliated Hospital of Zhejiang University School of Medicine, Hangzhou 310000, China)
ObjectiveTo observe the erythropoietin (EPO) on neurofilaments in rats traumatic brain injury(TBI) and its significance.Methods45 Wistar rats were divided into nine groups: normal control group, brain injury(6, 12, 24, 72 h after brain injury), and EPO treatment after brain injury(6, 12, 24, 72 h after brain injury).The Myneurolab of stereotactic apparatus and the Benchmark of traumatic brain injury impactor were used to produce TBI model.The morphologic changes of neurofilament were observed by immunohistochemistry in lesion peri cortex,and the expressions of neurofilament H(NF-H) were detected by Western blot at the above time points.ResultsThe immunohistochemistry result showed that in normal control group, NF-H was abundant in tissue section with the tan filamentous structure, and existed in big cones, small cones, hippocampus, especially obvious in corpus callosum of cerebral cortex layer; in brain injury group, NF-H was sparse with part of the structure interrupted after traumatic brain injury of 6h, further nerve filament number reduced with disordered arrangement after 6~24 h, the damage reached its peak after 24 h, and the above situation eased after 72 h.The number of neurofilaments in EPO treatment group at each time point was higher than that in brain injury group after trauma, arranged neatly and the intensity of neurofilament reached the peak at 12 h, then gradually reduced.Western blot result showed that compared with normal group, the expression of NF-H reduced after traumatic brain injury of 6h (P<0.05), within 6~12 h NF-H protein expression persistent decrease (P< 0.05), reached the lowest after 24 h (P<0.01), and elevated after 72 h (P<0.05).But compared with groups of brain injury, the expression of NF - H decreased in EPO treatment group (P<0.05). Conclusion EPO has a neuroprotective effect, and its possible mechanism is to inhibit the degradation of neurofilament protein.
traumatic brain injury; erythropoietin;neurofilaments
2012年浙江省醫藥衛生科技計劃(2012KYB096)
劉健,男,本科,主治醫師,研究方向:腦外傷,E-mail:lj1104881684@163.com。
R3
A
1005-1678(2015)02-0063-04

