預處理條件及金屬離子改性對H-MOR分子篩的DME羰基化性能影響
趙娜,牛君陽,劉亞華,譚猗生,李新剛
(1 天津大學化工學院,天津化學化工協同創新中心,天津 300072; 2 中國科學院山西煤炭化學研究所,煤轉化國家重點實驗室,山西 太原 030001)
引 言
乙醇是一種新型清潔燃料,市場需求量逐年增加。目前乙醇的生產主要有兩大類:一類是已工業化的發酵法[1];另一類是化學合成法,包括乙烯水合法[2]、甲醇同系化法[3-4]、合成氣直接合成法[5-6]。然而3 種化學合成法存在生產成本高,設備易腐蝕等問題,所以迫切需要開發出綠色乙醇合成新工藝。
H-MOR 分子篩具有八元環(8-MR)和十二元環(12-MR)孔道結構,且富含Br?nsted 和Lewis酸。Iglesia 等[7-10]研究發現,H-MOR 分子篩具有較高的DME 羰基化活性及產物MA 的選擇性,這一發現引起了眾多研究者的關注。研究表明,DME 羰基化反應主要在H-MOR 分子篩的8-MR內進行:DME 先在B 酸位上吸附、解離產生甲氧基中間體,然后由吸附在L 酸位上的CO 進攻甲氧基的C—O 鍵,形成乙酰基過渡態,此為反應的速控步驟。該路徑有反應條件溫和、產物乙酸甲酯選擇性高的特點。
據此,本課題組[11-12]近期通過“DME 羰基化制MA-MA 加氫制乙醇”兩個反應串聯式耦合,建立了一個高效、環保的乙醇合成新體系,采用該反應路徑后,產物中只有乙醇和甲醇。此外由于該體系使用沸石分子篩與Cu/ZnO 耦合催化劑,相比傳統的催化劑具有價格便宜、無腐蝕性、反應條件溫和等特點,具有廣闊的應用前景。其中,“MA 加氫制乙醇”反應體系使用的Cu 基催化劑在工業催化加氫領域已經相當成熟[13-14],而“DME 羰基化制MA”反應體系卻存在8-MR 內的活性位有限,導致DME的轉化效率難以提高,且催化劑的穩定性差,易失活等亟需突破的瓶頸。研究發現金屬Cu 離子改性后H-MOR 分子篩催化劑的DME 羰基化活性明顯提高[12]。
本文采用H-MOR 分子篩為DME 羰基化反應的催化劑,分別考察不同預處理條件、不同反應溫度對催化劑催化活性及穩定性的影響,以確定最佳的H-MOR 預處理條件及最適宜的反應溫度。繼而采用離子交換法制備Cu[12,15-16]、Ni[17]、Fe[18]、Co[19]等不同金屬離子改性后的H-MOR 催化劑樣品,并對各個金屬改性后的催化劑樣品進行DME 羰基化活性測試,探究經過不同金屬離子改性后,絲光沸石分子篩的DME 轉化率和產品中MA 的選擇性的變化情況,并以Cu 改性后的H-MOR 分子篩來探究預處理時不同還原溫度對催化劑催化活性的影響。
1 實驗部分
1.1 催化劑制備
催化劑制備所需要的原料包括:商業氫型絲光沸石(Tosoh Corporation,SiO2/Al2O3=18)、硝酸銅(Cu(NO3)2·3H2O)、硝酸鎳(Ni(NO3)2·6H2O)、硝酸鐵(Fe(NO3)3·9H2O)、硝酸鈷(Co(NO3)2·6H2O),以上4 種金屬硝酸鹽均購買于天津市光復科技發展有限公司,純度為分析純。
金屬離子改性的H-MOR 催化劑的制備采用離子交換法,稱取5 g H-MOR 加入收三口燒瓶中,然后加入250 ml 濃度恰為0.1 mol·L-1硝酸銅的溶液;70℃恒溫水浴鍋中磁力攪拌6 h,過濾洗滌后,將樣品于110℃的恒溫干燥箱中干燥12 h,重復交換3 次后,將干燥好的樣品置于管式爐中在N2氣氛(30 ml·min-1)下500℃ (5℃·min-1)焙燒2 h,得收的樣品標記為IE-Cu。按照同樣的方法,進行不同金屬硝酸鹽溶液的離子交換,得收的樣品按不同金屬元素分別標記為 IE-Ni、IE-Fe、IE-Co 等。
1.2 分析測試儀器
X 射線粉末衍射實驗是采用德國布魯克斯AXS技術有限公司的D8-Focus 型X 射線衍射分析儀測試,輻射源為CuKα(波長=0.15418 nm),掃描范圍為5°~50 °,掃描步長為0.02 °,操作電壓電流分別為:40 kV,40 mA。
H-MOR 的表面形貌特征由日本Hitachi 公司 S-4800 型場發射掃描電子顯微鏡(FE-SEM)進行測試,操作電壓電流分別為:3 kV,8 mA。
TG/DTA 分析在美國 Perkin-Elmer Diamond TG/DTA 型熱分析儀器上測試,樣品用量3 mg,空氣流速100 ml·min-1,測試溫度范圍25~700℃(10℃·min-1)。
微孔比表面積測試實驗在美國康塔公司生產的Quantachrome Autosorb-1 型物理吸附儀上進行,樣品測試前在300℃脫氣預處理10 h,繼而在-196℃下進行氮氣吸附/脫附測試。樣品總比表面積、微孔比表面積、微孔體積采用t-方法(t-method)進行計算,微孔平均孔徑采用SF 方法進行計算。
1.3 催化劑活性測試評價
1.3.1 DME 羰基化反應測試步驟
(1)裝置氣密性檢查:將500 mg 催化劑(0.15~0.27 nm)加入反應管中,連接好反應器后,通入N2,背壓至2 MPa 時,N2流量應為零,且經過1 h 后示數不變,則裝置氣密性良好。
(2)催化劑原位還原:在氫氣氣氛450℃下還原10 h,再在氮氣氣氛500℃,脫水處理2 h,最后降溫至180℃。若為新鮮H-MOR,則直接在氮氣氣氛下500℃預處理2 h 即可。
(3)背壓反應:通入原料氣(DME/CO/N2),背壓至1.5 MPa,在180℃條件下或者其他溫度條件下進行二甲醚羰基化反應。
(4)產物檢測:采用氣相色譜在線檢測,反應尾氣進入氣相色譜A(GC-9860)的HP-1 型高分離度氣相色譜柱(30 m×0.32 mm×0.25 μm)進行在線采樣分析,采用FID 型檢測器,分析尾氣中的DME和產物MA;從A 流出的尾氣經過冷阱冷凝液化后流入氣相色譜B(GC-9860)的TDX-01 填充柱,采用TCD 檢測器,對N2、CO 等無機氣體以及副產物CO2等進行在線分析,氣相色譜 B 還安裝有HP-PLOT/Q 毛細管柱(30 m×0.53 mm×40 μm),采用氫FID 型檢測器,在線檢測分析反應尾氣中是否有CH4等C1~C5副產物。
1.3.2 產物定性分析 分別利用原料氣體、含氧有機化合物液相標準樣、無機標氣來確定DME、MA、Methanol 及EA 等在氣相色譜儀的色譜柱中的出峰時間。
1.3.3 計算 DME 轉化率,產物MA、Methanol、EA 選擇性的計算方法:
DME 某時刻轉化率按式(1)進行計算
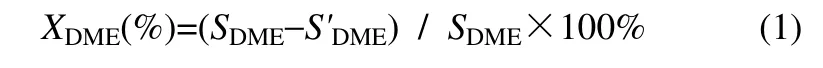
式中,XDME為DME 在某時刻的轉化率,%;SDME為原料氣中DME 的峰面積數值,μV·s;S'DME為反應中某時刻尾氣中DME 的峰面積數值,μV·s;產物MA、Methanol、EA 某時刻選擇性按式(2)進行計算
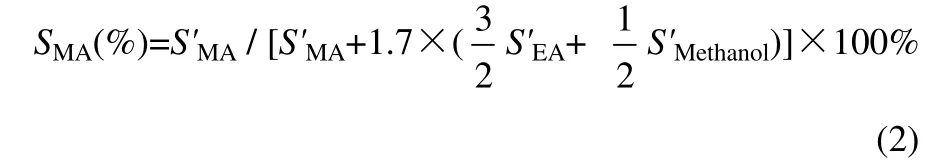
式中,SMA、SEA、SMethanol分別為MA、EA、Methanol 在某時刻的選擇性,%;S'MA、S'EA、S'Methanol分別是反應中某時刻尾氣中MA、EA、Methanol的峰面積數值,μV·s。
2 結果與討論
2.1 樣品的表征
圖1 是H-MOR 催化劑的掃描電鏡圖片。如圖所示,催化劑樣品顆粒粒徑比較均勻,主要呈不規則的實心棱柱狀,顆粒與顆粒之間的堆疊較為緊密。且顆粒粒徑較常規分子篩的粒徑要小,結合BET 數據,發現H-MOR 催化劑的比表面積為380 m2·g-1,微孔比表面積為334 m2·g-1,微孔體積為0.172 cm3·g-1,微孔的平均孔徑為0.59 nm,平均顆粒尺寸為43.5 nm,而傳統的絲光沸石分子篩的顆粒尺寸約為2~4 μm[20]。與傳統的絲光沸石分子篩相比,本文中所考察的分子篩顆粒尺寸較小,因此其微孔孔道的長度變短,縮短了物質的擴散路徑,推測此結構有利于反應的傳質。

圖1 H-MOR 樣品的SEM 照片Fig.1 SEM images of H-MOR
2.2 預處理條件對樣品羰基化性能的影響
依據羰基化反應機理[21-22],水與DME 分子在B 酸性位存在競爭吸附,不利于反應的進行。此外,在反應形成甲氧基中間體后,分子篩中的水分子會與甲氧基反應形成甲醇,形成H2O+Z-CH3CH3OH+Z-H 間的動態平衡,不利于CO 與甲氧基的反應,而且產生的水也會使催化劑中毒,因此在活性測試前要對H-MOR 催化劑進行高溫吹掃預處 理,脫除分子篩中吸附的水分子。
表1 給出了不同溫度和時間在氮氣氣氛預處理條件下,H-MOR 催化劑的DME 羰基化轉化率。對比第1 組與第2、3、4 組數據發現,未經處理的催化劑樣品活性僅為2.9%,預處理(除水)后,催化劑的活性明顯提高。500℃時的DME 羰基化轉化率達20.5%,明顯高于300℃的轉化率,說明較高的預處理溫度更有利于樣品中水分和其他雜質的脫除,以消除H2O 的對CO 的競爭吸附,有利于DME 羰基化反應的進行。但在500℃繼續延長預處理時間,對DME 羰基化轉化率的影響作用不大,說明2 h的時間已足夠脫出分子篩中的水分。所以本著節約能耗,減少反應時間等問題,最終選用氮氣氣氛500℃處理2 h 作為DME 羰基化反應催化劑H-MOR 的預處理條件。

表1 不同預處理條件下H-MOR 樣品的DME 轉化率Table 1 DME conversion over H-MOR sample under different pretreatment conditions
2.3 不同反應溫度對樣品活性的影響
在確定了適宜的催化劑預處理條件后,用一系列溫度梯度進行DME 羰基化反應活性測試。圖2給出了在不同反應溫度下的DME 轉化率隨時間的變化趨勢,發現H-MOR 催化劑的DME 羰基化轉化率隨反應溫度的升高而顯著提高,但高溫反應時,色譜檢測收少量副產物甲烷產生,而在其他較低的反應溫度則未發現甲烷,說明此時副反應產生的概率增加,且催化劑穩定性差,經誘導期后則快速失活。而在低溫180℃時經約3 h 的誘導期,DME 轉化率達收19.6%,且整個反應過程催化活性基本保 持穩定,8 h 后DME 轉化率仍為20.2%,表明H-MOR 催化劑在180℃反應時催化活性比較穩定,無副反應發生,催化劑的壽命延長。
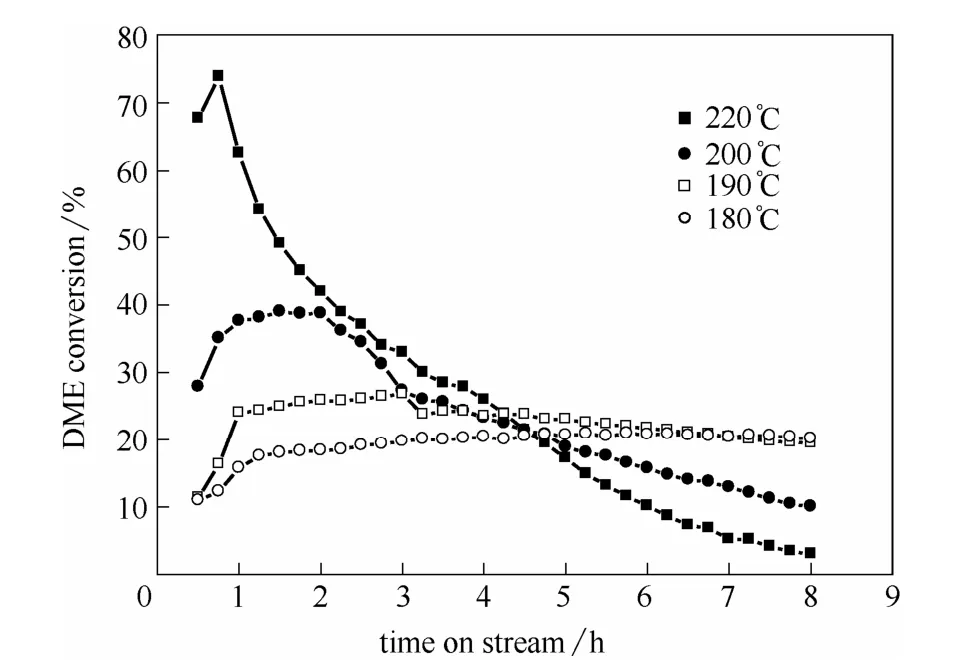
圖2 不同反應溫度下商業H-MOR 樣品的活性趨勢圖Fig.2 DME carbonylation plotted against time on stream over commercial H-MOR sample at different temperatures
為探究催化劑失活原因[23],對不同反應溫度后的催化劑樣品進行熱重分析,圖3 為新鮮H-MOR和不同反應溫度后H-MOR 催化劑的TG 曲線,新鮮H-MOR 催化劑在300℃前有一段明顯失重,主要認為是由于H-MOR 分子篩孔道中吸附的水分子在升溫過程中脫除造成的。而180 和190℃反應后催化劑樣品的TG 曲線與新鮮催化劑的TG 曲線相近,失重率略大于新鮮樣品,認為高出新鮮催化劑的部分主要由反應過程中吸附在分子篩孔道中的小分子脫除造成。隨著反應溫度升高,在220℃反應后催化劑樣品的TG 曲線上可明顯觀察收三段失重峰:180℃前為第一失重階段,失重率為11.8%,認為是分子篩孔道中的水以及其他低沸點物質的脫除引起的;180~350℃為第二失重階段,失重率為6.1%,一般把這部分失重是歸結為形成在催化劑樣品上的“軟積炭”脫除導致的;350~670℃為第三失重階段,失重率分為9.6%,由于這部分溫度較高,把這部分歸結為“硬積炭”的脫除,主要失重物質為芳香族化合物,約占積炭總量的60%以上。結合不同反應溫度下的活性數據證實,隨著反應溫度升高而導致催化劑穩定性變差的主要原因是因為積炭的生成,反應溫度越高,副反應發生的概率越大,因而催化劑產生的積炭量越多,催化劑穩定性越差,導致催化劑快速失活。在低溫180℃時,DME 轉化率不高,但整個反應過程穩定性好,且副反應發生概率小,MA 選擇性大于95%。鑒于催化劑工業應用時穩定性及產物選擇性的要求,最終選取180℃為最適宜的催化反應溫度。
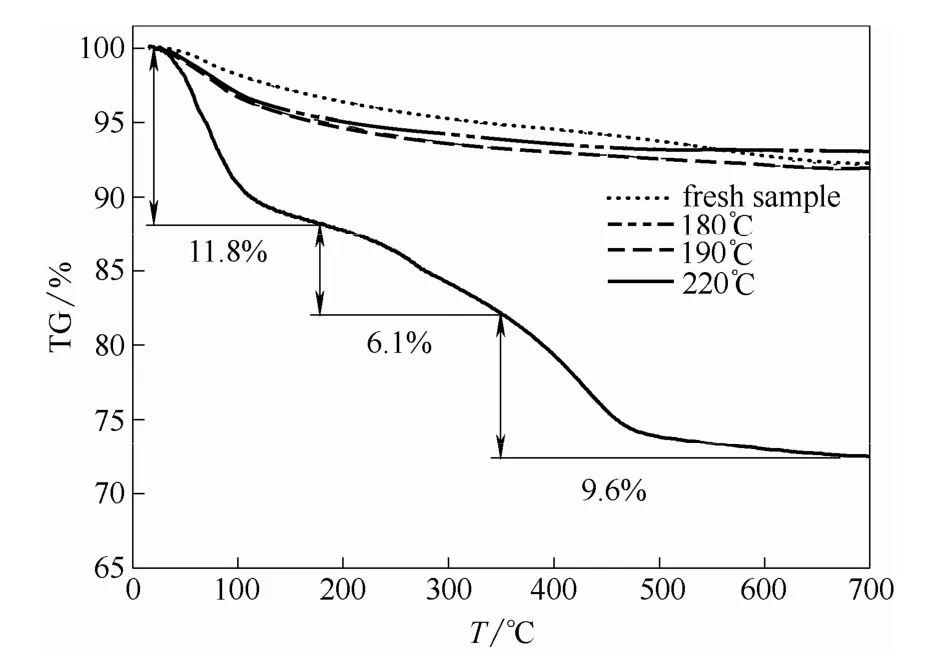
圖3 新鮮樣品和不同反應溫度反應后樣品的TG 曲線Fig.3 TG curves of fresh sample and samples after reaction at different temperatures
2.4 金屬離子改性對H-MOR 分子篩DME 羰基化性能的影響
根據Iglesia 等[7-10]提出的二甲醚羰基化機理,在羰基化反應過程中,首先是DME 吸附在催化活性位上,形成甲氧基,然后CO 分子進攻甲氧基,形成乙酰類物質,在這個過程中涉及CO 分子的活化和吸附。金屬離子的引入,可能有利于CO 分子的吸附,不僅可以有效地斷裂甲氧基物種中的C—O 鍵,又能促進CO 分子的非解離吸附。基于此,將幾類有利于CO 分子非解離吸附的金屬離子Cu、Ni、Fe、Co 等采用離子交換法交換收H-MOR 分子篩上,制得的催化劑樣品分別標記為IE-Cu、IE-Ni、IE-Fe、IE-Co。

圖4 樣品的XRD 譜圖Fig.4 XRD patterns of samples
2.4.1 XRD 結果分析 首先,對制得的IE-Cu、IE-Ni、IE-Fe、IE-Co 等催化劑樣品進行X 射線衍射實驗,圖4 為不同金屬離子改性催化劑樣品的XRD譜圖。根據特征峰的位置,發現離子交換后催化劑 樣品的主要物相仍為 H-MOR(PDF 卡片號:#49-0924),說明金屬離子改性后催化劑仍然保留了H-MOR 分子篩的基本骨架結構特征。對比圖4 a、b、d、e 的XRD 衍射峰曲線發現,催化劑交換Co、Cu、Ni 離子后,X 射線衍射峰強度變強,其中IE-Ni催化劑的衍射峰的強度變化最為明顯。而IE-Fe 催化劑的衍射峰強度明顯下降,并伴隨新的衍射峰出現,判斷為Fe3O4物相(PDF 卡片號:#65-3107)的衍射峰,認為這是由于大部分Fe 未進入分子篩骨架,而是以Fe3O4的形式分散在在分子篩表面。
2.4.2 DME羰基化活性測試 對改性后H-MOR 分子篩進行DME 羰基化活性測試,圖5 為改性后H-MOR分子篩的DME轉化率隨反應時間進行的變化趨勢圖。以新鮮H-MOR 的DME 轉化率隨時間的變化趨勢為基準,可以明顯地發現,IE-Co與IE-Fe催化劑的DME 的轉化率明顯下降,兩者的活性趨勢走向在誘導期和穩定期幾乎相同,但IE-Co 催化劑的穩定性優于IE-Fe催化劑。而IE-Cu 與IE-Ni 催化劑的DME羰基化活性加強,IE-Cu 催化劑的DME轉化率可高達36.9%(2 h),8 h 后DME 轉化率為26.7%,IE-Ni 催化劑DME 轉化率約為26.4%,并在整個反應過程中羰基化活性穩定,表明Ni 的加入不僅提高了催化劑DME 羰基化活性,同時也提升了催化劑穩定性,延長了催化劑的壽命。根據計算,4 種金屬離子改性后催化劑的MA 的選擇性均大于91%。
Zhan 等[24]探究了Cu 離子價態對DME 羰基化活性的影響,研究結果發現Cu2+在室溫時對CO 的吸附能力就較弱,Cu+在反應溫度時與CO 的相互作用較強,導致CO 解離吸附十分困難,而Cu0在反應條件下與CO 的相互作用較弱,因此Cu0與H+的協同作用能更好地提高H-MOR 催化劑DME 羰基化活性。所以對IE-Cu 催化劑進行還原,探究還原溫度對DME 羰基化活性的影響。根據1.3.1(2)催化劑原位還原的步驟分別在300 與450℃對IE-Cu 催化劑進行預處理,然后進行DME 羰基化活性測試,如圖5 中()與(▲)曲線所示,300 與450℃兩溫度下DME 轉化率曲線變化趨勢相相同,經過短暫的誘導期后轉化率分別為29.6%與36.9% (3 h),8 h 后轉化率下降收25.1%與26.7%。研究結果說明,隨著預處理溫度提高,IE-Cu 催化劑的羰基化活性提高(約7.2%)。推測這是因為在高的還原溫度下Cu2+更多地被還原為低價Cu 物種,從而提高了DME 羰基化反應活性。
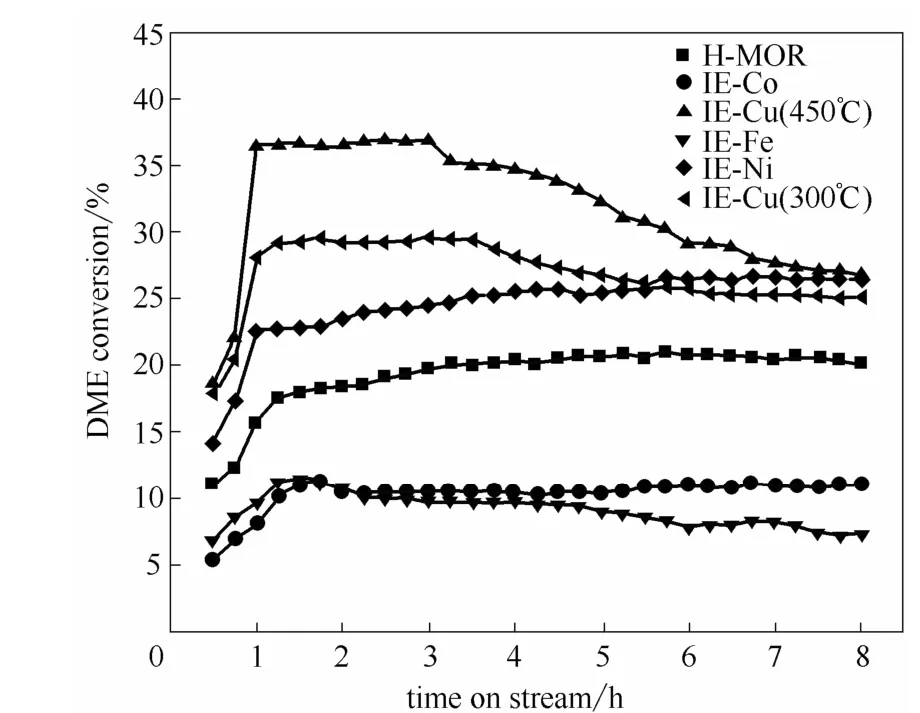
圖5 金屬離子改性后H-MOR 的DME 轉化率趨勢圖Fig.5 DME carbonylation plotted against time on stream over different metal cation modification H-MOR samples
3 結 論
本文主要對商業H-MOR 分子篩的DME 羰基化活性測試條件進行了優化,包括催化劑預處理條件(溫度和時間)及反應溫度等。最終篩選出H-MOR的最佳預處理條件為N2氣氛下500℃預處理2 h,以有效除去分子篩上中吸附的水分和其他雜質;并根據不同反應溫度下DME 羰基化的活性測試,發現催化劑的反應溫度與活性成正比,與穩定性成反比, 180℃是最佳的反應溫度。然后利用離子交換法制備金屬改性的H-MOR 催化劑,根據DME 羰基化活性測試結果發現,IE-Co 和IE-Fe 催化劑的DME 羰基化轉化率降低,IE-Cu 和IE-Ni 催化劑的DME 羰基化轉化率提高,IE-Cu 催化劑的DME 轉化率高達36.9%,約為新鮮H-MOR 催化劑的兩倍。綜合以上4 種金屬改性后H-MOR 催化劑DME 羰基化活性考察結果,IE-Cu 催化劑的DME 羰基化活性最高,為此以IE-Cu 催化劑為基礎,繼續考察了還原溫度對催化劑活性的影響,發現高的還原溫度(450℃)下催化劑的活性較高,分析可能是由于高溫下金屬Cu2+被更多地還原為低價Cu 物種,有利于提高DME 羰基化反應速率。
[1]Cardona C A, Sánchez ó J.Fuel ethanol production: process design trends and integration opportunities [J].Bioresource Technology, 2007, 98(12): 2415-2457.
[2]Atkins M P, Smith D J H, Westlake D J.Montmorillonite catalysts for ethylene hydration [J].Clay Miner., 1983, 18: 423-429.
[3]Novotny M.Pre-pressuring methanol-cobalt with carbon monoxide in homologation of methanol[P]: US , 4283582.1981-8-11.
[4]Francoisse P B, Thyrion F C.Methanol to ethanol by homologation: kinetic approach [J].Industrial & Engineering Chemistry Product Research and Development, 1983, 22(4): 542-48.
[5]Ichikawa M, Fukushima T.Mechanism of syngas conversion into C2-oxygenates such as ethanol catalysed on a SiO2-supported Rh-Ti catalyst [J].Journal of the Chemical Society, Chemical Communications, 1985, (6): 321-323.
[6]Mei D, Rousseau R, Kathmann S M, Glezakou V A, Engelhard M H, Jiang W, Wang C M, Gerber M A, Stevens D J.Ethanol synthesis from syngas over Rh-based/SiO2catalysts: a combined experimental and theoretical modeling study [J].Journal of Catalysis, 2010, 271(2): 325-342.
[7]Cheung P, Bhan A, Sunley G J, Iglesia E.Selective carbonylation of dimethyl ether to methyl acetate catalyzed by acidic zeolites [J].Angewandte Chemie International Edition, 2006, 45(10): 1617- 1620.
[8]Bhan A, Allian A D, Sunley G J, Law D J, Iglesia E.Specificity of sites within eight-membered ring zeolite channels for carbonylation of methyls to acetyls [J].Journal of the American Chemical Society, 2007, 129(16): 4919-4924.
[9]Cheung P, Bhan A, Sunley G J, Law D J, Iglesia E.Site requirements and elementary steps in dimethyl ether carbonylation catalyzed by acidic zeolite [J].Journal of Catalysis, 2007, 245(1): 110-123.
[10]Bhan A, Iglesia E.A link between reactivity and local structure in acid catalysis on zeolites [J].Accounts of Chemical Research, 2008, 41(4): 559-567.
[11]Li X G, San X G, Zhang Y, Ichii T, Meng M, Tan Y, Tsubaki N.Direct synthesis of ethanol from dimethyl ether and syngas over combined H-mordenite and Cu/ZnO catalysts [J].ChemSusChem, 2010, 3(10): 1192-1199.
[12]Yang G H, San X G, Jiang N, Tanaka Y, Li X, Jin Q, Tao K, Meng F, Tsubaki N.A new method of ethanol synthesis from dimethyl ether and syngas in a sequential dual bed reactor with the modified zeolite and Cu/ZnO catalysts [J].Catalysis Today, 2011, 164(1): 425-428.
[13]Claus P, Lucas M, Lücke B, Berndt T, Birke P.Selective hydrogenolysis of methyl and ethyl acetate in the gas phase on copper and supported group Ⅷ metal catalysts [J].Applied Catalysis A: General, 1991, 79(1): 1-18.
[14]Kenvin J C, White M G.Supported catalysts prepared from mononuclear copper complexes: catalytic properties [J].Journal of Catalysis, 1992, 135(1): 81-91.
[15]Zhang X, Li Y P, Qiu S B, Xu Q.Synthesis of methyl acetate by dimethyl ether carbonylation over Cu/HMOR: effect of catalyst preparation method [J].Chinese Journal of Chemical Physics, 2013,26(1): 77-82.
[16]Zhang X, Li Y P, Qiu S B, Wang T J, Ma L L, Zhang Q, Ding M Y.Effect of calcination temperature on catalytic activity and textual property of Cu/HMOR catalysts in dimethyl ether carbonylation reaction [J].Chinese Journal of Chemical Physics, 2013, 26(2): 220-224.
[17]Wegman R W.Vapour phase carbonylation of methanol or dimethyl ether with metal-ion exchanged heteropoly acid catalysts [J].Journal of the Chemical Society, Chemical Communications, 1994, (8): 947-948.
[18]Sardesai A, Tartamella T, Lee S.Synthesis of hydrocarbons fromdimethyl ether: selectivities towards light hydrocarbons [J].Fuel Science & Technology International, 1996, 14(5): 703-712.
[19]Inui T, Phatanasri S, Matsuda H.Highly selective synthesis of ethene from methanol on a novel nickel-silicoaluminophosphate catalyst [J].Journal of the Chemical Society, Chemical Communications, 1990, (3): 205-206.
[20]Xue H, Huang X, Ditzel E, Zhan E, Ma M, Shen W.Dimethyl ether carbonylation to methyl acetate over nanosized mordenites [J].Industrial & Engineering Chemistry Research, 2013, 52(33): 11510-11515.
[21]Zecchina A, Geobaldo F, Spoto G, Bordiga S, Ricchiardi G, Buzzoni R, Petrini G.FTIR investigation of the formation of neutral and ionic hydrogen-bonded complexes by interaction of H-ZSM-5 and H-mordenite with CH3CN and H2O: Comparison with the H-NAFION superacidic system [J].The Journal of Physical Chemistry, 1996, 100(41): 16584-16599.
[22]Boronat M, Martínez-Sánchez C, Law D, Corma A.Enzyme-like specificity in zeolites: a unique site position in mordenite for selective carbonylation of methanol and dimethyl ether with CO [J].Journal of the American Chemical Society, 2008, 130(48): 16316-16323.
[23]Liu Y, Zhao N, Xian H, Cheng Q, Tan Y, Tsubaki N, Li X.Facilely synthesized H-mordenite nano-sheet assembly for carbonylation of dimethyl ether [J].ACS Applied Materials & Interfaces, 2015, 7: 8398-8403.
[24]Zhan H, Huang S, Li Y, Lv J, Wang S, Ma X.Elucidating the nature and role of Cu species in enhanced catalytic carbonylation of dimethyl ether over Cu/H-MOR [J].Catalysis Science & Technology, 2015, (5): 4378-4389.DOI: 10.1039/C5CY00460H.

