30例自體外周造血干細胞移植治療多發性骨髓瘤的療效及預后因素評價
王 婷 劉 輝 李江濤 馮 茹 田 園 邢保利 許曉東 裴 蕾 寧尚勇
Ting WANG,Hui LIU,Jiangtao LI,Ru FENG,Yuan TIAN,Baoli XING,Xiaodong XU,Lei PEI,Shangyong NING
·論著·
30例自體外周造血干細胞移植治療多發性骨髓瘤的療效及預后因素評價
王婷劉輝李江濤馮茹田園邢保利許曉東裴蕾寧尚勇
目的:對30例多發性骨髓瘤(multiple myeloma,MM)患者經自體外周造血干細胞移植(autologous hematopoietic stem cell transplantation,APBSCT)治療后的臨床療效進行評估,并分析可能影響預后的因素。方法:30例MM患者有2例復發行2次APBSCT,因此共計移植32例次。移植前予常規聯合化療(11例含萬珂),化療聯合G-CSF動員APBSC,選擇以馬法蘭為基礎的預處理方案,d0天回輸。結果:動員后患者采集的單個核細胞(MNC)中位數為6.41×108/kg,CD34+細胞4.75×106/kg。APBSCT后中位中性粒細胞和血小板重建時間分別為9.5天和11天。APBSCT后CR和VGPR率分別為37.5%和34.4%,中位生存期(overall survival,OS)為67.27個月,中位無進展生存期(progression-free survival,PFS)為29.77個月,其中CR組、PR組中位PFS分別為29個月、20個月,VGPR組中位PFS未達到,CR+VGPR組與PR組PFS比較P=0.025。萬珂組和非萬珂組CR率分別為63.6%和23.8%(P= 0.034),萬珂組中位OS及PFS均未達到,非萬珂組中位PFS為22個月(P=0.045)。結論:硼替佐米誘導序貫APBSCT可獲得更長的無病生存。APBSCT作為MM誘導緩解后的強化治療,緩解率高,且移植后獲得VGPR以上反應的患者PFS獲益。
多發性骨髓瘤自體外周造血干細胞移植硼替佐米
Ting WANG,Hui LIU,Jiangtao LI,Ru FENG,Yuan TIAN,Baoli XING,Xiaodong XU,Lei PEI,Shangyong NING
Correspondence to:Hui LIU;E-mail:liuhui8140@126.com
Department of Hematology,Ministry of Health Beijing Hospital,Beijing 100730,China
隨著社會老齡化進展,多發性骨髓瘤(multiple myeloma,MM)發病率逐步上升,已成為血液系統高發腫瘤疾病。既往治療主要以常規化療為主(如VAD、MP、MPT等),但療效并不盡人意。隨著新型靶向藥物(如硼替佐米、沙利度胺、雷那度胺)的出現及大劑量馬法蘭后序貫自體外周造血干細胞移植(autologous hematopoietic stem cell transplantation,APBSCT)的應用,患者的預后明顯改善,延長了無進展生存時間(PFS)和總生存(OS),取得了較好療效。現就30例進行自體APBSCT的患者進行回顧性研究與分析。
1 材料與方法
1.1一般資料
以2000年2月至2014年9月收集北京醫院血液科接受APBSCT的30例MM患者為研究對象;30例患者中男性17例,女性13例,中位年齡56(36~69)歲。其中2例因復發進行二次移植,因此共進行APBSCT共計32例次。參照國際骨髓瘤工作組(International Myeloma Working Group,IMWG)的制定標準[1]。
1.2方法
1.2.1誘導化療移植前中位誘導化療次數5.5次(2~12)。11例患者化療方案中含有硼替佐米(bortezomib)(萬珂,Velcade)(11/30,36.7%),即萬珂組,包括PCD(硼替佐米、環磷酰胺、地塞米松)、PAD(硼替佐米、脂質體阿霉素、地塞米松)、PD(硼替佐米、地塞米松)。非萬珂組(19/30,63.3%)采用傳統方案,包括MP(馬法蘭、潑尼松)、VAD(長春新堿、阿霉素、地塞米松)等。
1.2.2干細胞動員、采集、保存和回輸采用化療聯合重組人粒細胞集落刺激因子(rhG-CSF)動員外周造血干細胞(APBSC)。方案[2]:CTX 1.0~1.2 g/m2·d× 2d,VP-16 300~500 mg×2d。化療后當外周血WBC計數降至1×109/L后開始予rhG-CSF 300 μg/d皮下注射,WBC>4×109/L、PLT>50×109/L時開始采集。COBE血細胞分離機持續采集2~3天,每次采集循環血量8 000~12 000 mL。APBSC懸液加入等量保護液(血漿和二甲基亞砜組成),程序降溫,-196℃液氮保存。40℃水浴箱中1 min內解凍后快速回輸。
1.2.3預處理方案及維持治療在32例次移植中,24例次患者采用馬法蘭(M)200 mg/m2,4例次采用馬法蘭140 mg/m2加VP-16 1 000 mg加司莫司汀(BCNU)200 mg,另外4例因患者年齡偏大或采集的CD34+細胞計數偏少,采用馬法蘭(M)140 mg/m2。移植后26例患者采用口服沙利度胺(Thalidomide,反應停)維持治療,劑量75 mg~150 mg,1例患者因末梢神經炎較重,采用干擾素維持治療,3例患者間斷采用MP、VAD等方案化療(較早期患者)。
1.2.4療效評判本研究中所有MM患者療效評價均參照IMWG療效標準[1]。具體分為完全緩解(CR)、非常好的部分緩解(VGPR)、部分緩解(PR)、疾病穩定(SD)及疾病進展(PD)。觀察指標:CR率、總反應率(CR+VGPR)、總生存率(OS)及無進展生存率(PFS)。隨訪方式以住院、門診及電話等為主。隨訪截止日期為2014年9月30日。
1.3統計學處理
采用SPSS 16.0軟件進行統計學分析。Kaplan-Meier曲線方法進行生存分析,P值檢驗采用Log rank檢驗單因素分析,P<0.05為有統計學意義。
2 結果
2.1基本臨床特征
分型:IgG 20例,IgA 6例,IgD 2例,輕鏈lambda 型2例。按Durie-Salmon進行臨床分期:ⅡA期5例,ⅢA期18例,ⅢB期7例。
2.2外周血干細胞采集
32例次動員后采集到的中位單個核細胞數(MNC)為6.41×108/kg(3.37×108/kg~12.78×108/kg),中位CD34+細胞數為4.75×106/kg(0.98×106/kg~49.1× 106/kg)。其中萬珂組采集到的CD34+細胞平均值為6.28×106/kg,非萬珂組11.49×106/kg(P=0.160)。
2.3造血功能重建
32例次APBSCT后中位中性粒細胞重建(中性粒細胞>0.5×109/L)時間為9.5(8~13)天,中位血小板重建時間(血小板>20×109/L,且能脫離輸血支持的維持5天以上)11(8~14)天。其中萬珂組與非萬珂組中位中性粒細胞重建時間為11天和9天(P=0.055),兩組血小板重建時間分別為12天和11天(P=0.329)。
2.4療效評價
2.4.1治療反應率32例次患者APBSCT后共有12例獲得CR(12/32,37.5%),11例獲得VGPR(11/32,34.4%),9例獲得PR(9/32,28.1%),總有效率(CR+ VGPR)為71.9%。萬珂組11例次中7例獲得CR(7/ 11,63.6%),3例獲得VGPR(3/11,27.3%),1例獲得PR(1/11,9.1%),總有效率為90.9%。21例次非萬珂組中有5例獲得CR(5/21,23.8%),8例獲得VGPR(8/ 21,38.1%),8例獲得PR(8/21,38.1%),總有效率為61.9%(表1)。其中萬珂組與非萬珂組之間CR率、VGPR率、PR率之間P值分別為0.034、0.66和0.098。2.4.2生存評價1)總體生存評價30例患者中有2例失訪,可評價病例共28例。中位隨訪時間52 (1~140)個月,總體中位OS為67.27(7~133)個月,總體中位PFS為29.77(1~105)個月。2)硼替佐米應用對生存的影響萬珂組11例,非萬珂組17例,萬珂組9例患者目前生存,僅2例死亡,中位OS及PFS均未達到。非萬珂組12例死亡,5例死亡,中位OS為50(18~120)個月,中位PFS為22(1~105)個月。兩組OS比較P=0.362,PFS比較P=0.045(圖1)。3)移植后反應情況對生存的影響按照移植后反應率進行分組,CR組、PR組中位OS分別為58個月、37個月,VGPR組中位OS未達到,3組間OS比較P=0.13,CR+VGPR組與PR組P=0.056。CR組、PR組中位PFS分別為29個月、20個月,VGPR組中位PFS未達到,3組間PFS比較P=0.056,CR+VGPR組與PR組P=0.025(圖2)。

表1 移植后反應情況 例Table 1 Reaction rates after APBSCT

圖1 誘導方案含萬珂組與非萬珂組PFS曲線Figure 1 PFS curves of Velcade and non-Velcade regimen groups
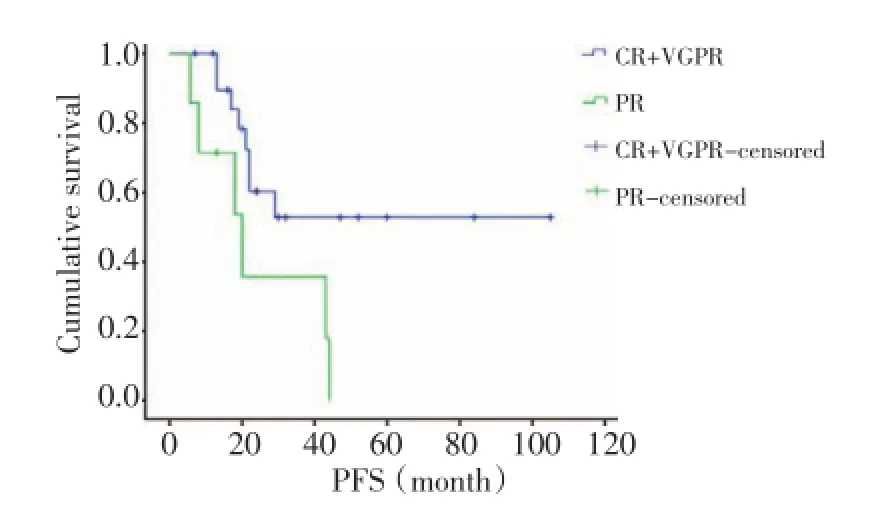
圖2 移植后CR+VGPR組、PR組PFS曲線Figure 2 PFS curves in CR+VGPR and PR groups after APBSCT
3 討論
多發性骨髓瘤老年人多發,傳統治療方案效果欠佳,生存期短,預后不佳。近年來,隨著APBSCT的廣泛開展以及技術的成熟、支持治療的完善,多數患者能夠獲得高質量的治療反應,OS和(或)PFS獲益。汪娟等[3]對27例MM患者進行分析,移植后CR率達到70.4%;李燕郴等[4]研究提示ASCT可明顯延長患者的OS,對PFS也有延長趨勢:部分患者甚至有可能獲得臨床治愈[5]。同時,隨著新型靶向藥物的加入,在含有硼替佐米的誘導方案后序貫ASCT,可進一步優化ASCT,顯著改善預后。梁賾隱等[6]研究中,16例接受硼替佐米誘導方案的患者進行序貫APBSCT,序貫移植組及單純化療組患者2年OS率分別為100.0%和66.0%(P=0.029)。鄒德慧等[7]認為新藥聯合ASCT可獲得高質量的治療反應,延長患者的PFS 和OS時間,這些均為MM治療開啟新篇章。
本研究中APBSCT后患者也同樣獲得良好的治療反應,32例次患者中37.5%的患者在APBSCT后達到CR,34.4%獲得VGPR,VGPR以上的總有效率(CR+VGPR)達到了71.9%,其中萬珂組更是高達90.9%。Moreau等[8]、Ladetto等[9]研究表明,對治療的反應程度及治療后的緩解情況與患者的生存息息相關,高質量的治療反應可以顯著延長PFS甚至OS時間。Martinez-Lopez等[5]研究中,移植后獲得CR、nCR、VGPR和PR的患者12年的0S率分別為35%,22%,16%和16%,且CR超過11年的患者中復發率極低,提示移植后CR能夠獲得更長的無病生存,且被治愈的可能性很大。本研究中,CR+VGPR組與PR 組OS比較P=0.056,雖然目前沒有統計學差異,可能與樣本量偏少、隨訪時間過短有關。而兩組間PFS比較P<0.05,具有統計學上的顯著性差異,提示移植后獲得CR和VGPR的患者相較僅獲得PR的患者,無病生存時間更長,生活質量更高,同時PFS的延長很有可能帶來更低的復發率,從而有可能使得OS延長,隨著后期的病例擴充和隨訪時間的延長,將有可能獲得統計學顯著性差異。
本研究參照IMWG推薦選擇誘導方案[10],其中11例含有硼替佐米。新藥的加入從各個方面為預后的改善做出卓越貢獻。首先,Oakervee等[11]、李娟等[12]研究均提示含有萬珂的方案并不影響干細胞動員和采集。本研究萬珂組與非萬珂組采集到的CD34+細胞平均值之間(P=0.160)。無顯著統計學差異。且兩組間中位中性粒細胞重建時間為11天和9天(P= 0.055),兩組血小板重建時間分別為12天和11天(P= 0.329),均無顯著性差異,與文獻報道一致。說明使用萬珂在保證干細胞采集數量的同時,對其質量沒有造成影響,從而保證了造血重建的時間,減少因重建時間延長、植活失敗導致的嚴重感染和致命出血發生。其次,應用萬珂對治療反應率也起到提升作用。本研究中,萬珂組CR率為63.6%,VGPR率為27.3%。而非萬珂組CR率、VGPR率分別為23.8%和38.1%,兩組間CR率P=0.034,具有統計學意義。這說明應用萬珂可以帶來更深層次和更高質量的緩解,這為APBSCT后OS和PFS的獲益奠定了堅實基礎。第三,在近幾年一些有關萬珂用于誘導方案的隨機對照或回顧性臨床研究中,萬珂對生存預后的改善所起到的作用已經嶄露頭角。Sonneveld等[13]、Cavo等[14]、Harousseau等[15]隨機臨床研究中,萬珂組OS和PFS均優于傳統方案誘導組。同樣,本研究中,萬珂組僅2例患者死亡,中位OS及中位PFS均未達到。非萬珂組12例死亡,5例生存,中位OS和PFS分別為50個月(P=0.362)和22個月(P=0.045),兩組間PFS有顯著統計學差異,提示誘導方案中含有萬珂的患者可以在PFS獲益。雖然兩組OS之間P>0.05,但從曲線走勢上可以看出萬珂組具有一定優勢。目前統計學無差異可能與樣本量過少、隨訪時間過短、萬珂組患者出現終點事件少有關。
總之,新藥和APBSCT在MM治療中的應用在不斷發展,一方面,APBSCT可在誘導化療的基礎上獲得更高的有效率及高質量的緩解率,延長PFS,改善生活質量,并可能降低復發率,進一步延長OS。同時硼替佐米等新藥加入移植前后的誘導治療可進一步優化APBSCT,提高CR率,使患者更大程度地獲益。
1 Kyle RA,Rajkumar SV.Criteria for diagnosis,staging,risk stratification and response assessment of multiple myeloma[J].Leukemia,2009,23(1):3-9.
2 Liu H,Chang NB,Li JT,et al.Analysis of therapeutic effect and prognosis of autologous peripheral stem cell transplanation for 21 patients with multiple myeloma[J].Journal of Clinical Hematology,2011,24(3):145-147.[劉輝、常乃柏、李江濤,等.自體外周造血干細胞移植治療21例多發性骨髓瘤的臨床療效及預后因素評價[J].臨床血液學雜志.2011,24(03):145-147.]
3 Wang J,Fu ZZ,Wu DP,et al.Retrospective analysis on therapeutic effect of autologous hematopoietic stem cell transplantation in multiple myeloma patients[J].National Medical Journal of China,2013,93(2):114-118.[汪娟,傅琤琤,吳德沛,等.自體造血干細胞移植治療多發性骨髓瘤的回顧性療效分析[J].中華醫學雜志,2013,93 (2):114-118.]
4 Li YC,Wang GR,Geng CY,et al.Chinese multiple myeloma patients at high risk benefit more from autologous stem cell transplantation[J].Journal of Leukemia&Lymphoma,2013,22(11):645-649.[李燕郴,王國蓉,耿傳營,等.自體造血干細胞移植可使中國高危多發性骨髓瘤患者獲益更多[J].白血病淋巴瘤,2013,22(11):645-649.]
5 Martinez-Lopez J,Blade J,Mateos MV,et al.Long-term prognostic significance of response in multiple myeloma after stem cell transplantation[J].Blood,2011,118(3):529-534.
6 Liang ZY,Ren HY,Cen XN,et al.Bortezomib-based chemotherapy for patients with multiple myeloma:a single center experience[J]. Chinese Journal of Hematology,2014,35(3):225-230.[梁賾隱,任漢云,岑溪南,等.硼替佐米為基礎的化療方案治療多發性骨髓瘤患者的療效及預后因素分析[J].中華血液學雜,2014,35(3):225-230.]
7 Zou DH,Sui WW,Yi SH,et al.Analysis of the efficacy and prognosis on first-line autologous hematopoietic stem cell transplantation of patients with multiple myeloma[J].Chinese Journal of Hematology,2013,34(4):299-303.[鄒德慧,隋偉薇,易樹華,等.一線自體造血干細胞移植治療多發性骨髓瘤療效及預后因素分析[J].中華血液學雜志,2013,34(4):299-303.]
8 Moreau P,Attal M,Pégourié B,et al.Achievement of VGPR to induction therapy is an important prognostic factor for longer PFS in the IFM 2005-01trial[J].Blood,2011,117(11):3041-3044.
9 Ladetto M,Pagliano G,Ferrero S,et al.Major tumor shrinking and persistent molecular remissions after consolidation with bortezomib,thalidomide,and dexamethasone in patients with autografted myeloma[J].J Clin Oncol,2010,28(12):2077-2084.
10 Cavo M,Rajkumar SV,Palumbo A,et al.International Myeloma Working Group consensus approach to the treatment of multiple myeloma patients who arecandidates for autologous stem cell transplantation[J].Blood,2011,117(23):6063-6073.
11 Oakervee H,Popat R,Cavenagh JD.Use of bortezomib as induction therapy prior to stem cell transplantation in frontline treatment of multiple myeloma:impact on stem cell harvesting and engraftment[J].Leuk Lymphoma,2007,48(10):1910-1921.
12 Li J,Liu JR,Huang PH,et al.Efficacy and safety of bortezomib-based induction regimen before autologous hematopoietic stem cell transplantation in patients with multiple myeloma[J].2012,51(4):279-283.[李娟,劉俊茹,黃蓓暉.含硼替佐米的誘導化療序貫自體造血干細胞移植治療多發性骨髓瘤的療效和安全性[J].中華內科雜志.2012,51(4):279-283.]
13 Sonneveld P,Schmidt-Wolf IG,van der Holt B,et al.Bortezomib induction and maintenance treatment in patients with newly diagnosed multiple myeloma:results of the randomized phase III HOVON-65/ GMMG-HD4 trial[J].J Clin Oncol,2012,30(24):2946-2955.
14 Cavo M,Tacchetti P,Patriarca F,et al.Bortezomib with thalidomide Plus dexamethasone compared with thalidomide plus dexamethasone as inductiontherapy before,and consolidation therapy after,double Autologous stem-cell transplantation in newly diagnosed multiple myeloma:a randomised phase 3 study[J].Lancet,2010,376(9758):2075-2085.
15 Harousseau JL,Attal M,Avet-Loiseau H,et al.Bortezomib plus Dexamethasone is superior to vincristine plus doxorubicin plus dexamethasoneasinductiontreatmentpriortoautologous stem-cell transplantation in newly diagnosed multiple myeloma:results of the IFM 2005-01 phase III trial[J].J Clin Oncol,2010,28 (30):4621-4629.
(2014-10-30收稿)
(2014-12-30修回)
(編輯:楊紅欣)

王婷專業方向為血液科常見疾病診治及自體造血干細胞移植。
E-mail:wangting9798@126.com
Analysis of therapeutic effects and prognostic factors of autologous peripheral stem-cell transplantation for 30 patients with multiple myeloma
Objective:To evaluate the clinical efficiency and prognostic factors of autologous peripheral blood stem cell transplantation(APBSCT)in 30 cases of multiple myeloma(MM).Methods:Two of the 30 patients received the second treatment of APBSCT because of relapse after the first treatment.Thus,a total of 32 case-times of APBSCT were studied.Combination chemotherapy was inducted regularly before APBSCT(11 patients used bortezomib as an induction drug),and chemotherapy combined with the G-CSF regimen was used to mobilize peripheral blood stem cells.Preconditioning was based on melphalan.Results:Mononuclear cells in harvest were 6.41×108/kg,and CD34+cells in harvest were 4.75×106/kg.The median times of neutrophil and platelet engraftment were 9.5 and 11 d,respectively.The complete remission(CR)and very good partial remission(VGPR)rates were 37.5%and 34.4%after APBSCT,respectively.The median overall survival(OS)was 67.27 months in all patients,and the median progression-free survival (PFS)was 29.77 months.The median PFS rates were 29 and 20 months in the patients who achieved CR and PR,respectively,and the median PFS was not observed in the patients who achieved VGPR.Statistical differences in PFS were detected between the CR+VGPR and PR groups(P=0.025).The CR rates were 63.6%and 23.8%in the bortezomib(bortezomib-based chemotherapy)and non-bortezomib groups(P=0.034),respectively.The median OS and PFS were not obtained in the bortezomib group,whereas the median PFS was 22 months in the non-bortezomib group(P=0.045).Conclusion:MM patients treated with bortezomib-based chemotherapy followed byAPBSCT had prolonged PFS.APBSCT can improve the response and survival of MM patients.
multiple myeloma,autologous peripheral stem cell transplantation,bortezomib
10.3969/j.issn.1000-8179.20142174
衛生部北京醫院血液科(北京市100730)
劉輝liuhui8140@126.com

