分子探針:提速癌癥診斷的新工具
賀曉鵬
結(jié)構(gòu)可控先進(jìn)功能材料及其制備教育部重點實驗室,華東理工大學(xué)化學(xué)與分子工程學(xué)院,上海 200237
*論著——精準(zhǔn)醫(yī)療*
分子探針:提速癌癥診斷的新工具
賀曉鵬
結(jié)構(gòu)可控先進(jìn)功能材料及其制備教育部重點實驗室,華東理工大學(xué)化學(xué)與分子工程學(xué)院,上海 200237
癌癥的快速、準(zhǔn)確血液診斷是國際生命健康領(lǐng)域亟待解決的科學(xué)問題。然而,現(xiàn)有臨床診斷技術(shù)存在操作流程繁復(fù)、技術(shù)要求高、耗時長且成本昂貴等缺陷。發(fā)展可用于快速捕捉血液癌標(biāo)志物的簡易、經(jīng)濟(jì)型診斷新工具逐漸成為國內(nèi)外學(xué)術(shù)研究熱點。分子探針具備構(gòu)建簡易、響應(yīng)快、成本低的優(yōu)勢,其傳統(tǒng)應(yīng)用領(lǐng)域為環(huán)境檢測與細(xì)胞、活體標(biāo)記等。近年來,靈敏探測血液癌標(biāo)志物的分子探針創(chuàng)制,形成了一個多學(xué)科交叉的新興領(lǐng)域。該文簡要綜述了相關(guān)領(lǐng)域研究團(tuán)隊對此類分子探針的構(gòu)筑策略,并結(jié)合相關(guān)癌標(biāo)志物的“快速檢測”實例展現(xiàn)了探針的醫(yī)學(xué)潛能,旨在為分子探針的多元化發(fā)展提供新的研究思路,期待通過獨特化學(xué)技術(shù)與臨床醫(yī)學(xué)的有機(jī)結(jié)合,實現(xiàn)對癌癥血液診斷的提速和低成本化。
癌癥;血液標(biāo)志物;分子探針;分子診斷;熒光
長期以來,癌癥嚴(yán)重威脅著人類的生命健康。由于人類對癌癥的發(fā)生、發(fā)展及復(fù)發(fā)機(jī)制尚未有系統(tǒng)性認(rèn)識,而傳統(tǒng)的臨床手術(shù)、放化療法和近年興起的免疫治療技術(shù)尚需完善,癌癥仍是全球致死率最高的人類重大疾病之一[1]。癌癥的早期診斷與治療可顯著提高患者的生存期,但受臨床癌標(biāo)志物特異性不高,尤其是現(xiàn)有癌檢測手段技術(shù)繁復(fù)、耗時長、原材料昂貴等局限,癌的精準(zhǔn)、快速診斷仍是生命科學(xué)領(lǐng)域亟待解決的關(guān)鍵科學(xué)問題。因此,開發(fā)簡易、高效的癌癥診斷工具,對于癌患者的術(shù)前化驗、術(shù)中判斷和術(shù)后監(jiān)控具有重要意義。
癌細(xì)胞所分泌特異標(biāo)志物的血液化驗是目前大規(guī)模體檢的首選技術(shù),它不但可規(guī)避磁共振與活檢等手段所帶來的輻射、肌體創(chuàng)傷與高成本,還可為癌癥的早期診斷提供高通量的普篩平臺。然而,現(xiàn)有臨床化驗技術(shù)(如酶聯(lián)免疫吸附測定、免疫發(fā)光、聚合酶鏈?zhǔn)椒磻?yīng)等)具有一定的局限性,操作繁復(fù)(反復(fù)的孵育、封閉、擴(kuò)增與洗滌步驟),耗時長且價格昂貴(需聯(lián)用多種成本較高的抗體、基因序列等生化試劑)。于是,發(fā)展可更高效、快速捕捉血液標(biāo)志物的經(jīng)濟(jì)型診斷工具,是當(dāng)前學(xué)術(shù)界的研究熱點。
區(qū)別于傳統(tǒng)生化手段對待測物的標(biāo)記需求,分子探針(即可用于研究與其余分子或結(jié)構(gòu)相互作用的原子與分子)往往可“自帶”一種“關(guān)開信號”,可經(jīng)由與待測物的共價或非共價作用產(chǎn)生一種“免標(biāo)記”(即無需對待測物進(jìn)行標(biāo)記)的信號改變,從而實現(xiàn)對待測物的定量分析。這一檢測原理具備操作便捷、響應(yīng)快、成本低等優(yōu)勢。分子探針的傳統(tǒng)應(yīng)用領(lǐng)域為環(huán)境檢測與細(xì)胞、體內(nèi)(熒光)標(biāo)記等[2]。隨著上述臨床診斷學(xué)問題的日益凸顯,構(gòu)建可用于靈敏、快速捕捉血液癌標(biāo)志物的分子探針,逐漸成為了一個獨特的交叉學(xué)科研究方向,為傳統(tǒng)的分子探針領(lǐng)域注入了新的活力。這一新興方向涉及化學(xué)、化工與材料學(xué)家對分子探針的設(shè)計加工,同時涵蓋生物與醫(yī)學(xué)家對探針的臨床實踐與優(yōu)化指導(dǎo),通過多學(xué)科協(xié)同創(chuàng)新為人類的生命健康謀求福祉。
基于上述學(xué)科背景,該文從分子設(shè)計、合成與材料復(fù)合組裝等方法學(xué)層面簡要綜述相關(guān)領(lǐng)域科研團(tuán)隊對癌標(biāo)志物分子探針的構(gòu)筑策略,并結(jié)合其相關(guān)臨床樣品“快速檢測”實例展現(xiàn)此類探針的醫(yī)學(xué)價值,期待通過獨特分子工程技術(shù)與臨床醫(yī)學(xué)導(dǎo)向的有機(jī)結(jié)合,實現(xiàn)對血液癌標(biāo)志物臨床診斷的提速。
1 分子探針構(gòu)建及血清癌標(biāo)志物檢測
1.1 分子探針構(gòu)建策略概要
分子探針的組成主要包含一類可與待測物(生物小分子或大分子)產(chǎn)生特異相互作用的識別基團(tuán)和一類可經(jīng)由識別產(chǎn)生信號的報告基團(tuán)。探針的作用模式可以是共價的化學(xué)反應(yīng),也可以是非共價的結(jié)合作用(圖1):當(dāng)識別基團(tuán)與報告基團(tuán)偶聯(lián)后,后者的信號被關(guān)閉,隨后經(jīng)探針與標(biāo)志物的快速結(jié)合打斷關(guān)閉機(jī)制,報告基團(tuán)的信號被“開啟”。此外,還可通過分子組裝手段獲得材料復(fù)合型分子探針(圖2):經(jīng)由信號基團(tuán)與一種特殊材料基底的組裝形成復(fù)合探針材料,隨后通過與標(biāo)志物的識別產(chǎn)生信號。
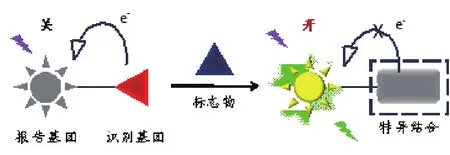
圖1 小分子探針的標(biāo)志物檢測原理Fig. 1 Detection mechanism of small-molecule probes for biomarkers
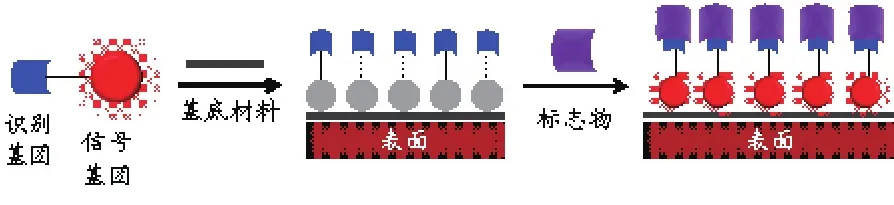
圖2 材料復(fù)合分子探針的標(biāo)志物檢測原理Fig. 2 Detection mechanism of material-based molecular probes for biomarkers
1.2 小分子探針
α-酮戊二酸(α-KG)是體內(nèi)代謝途徑中重要的氮素運(yùn)載體之一,與急性髓樣白血病密切相關(guān)[3]。基于酮與肼的高反應(yīng)活性,合成了含肼識別基團(tuán)的熒光分子探針,通過分子內(nèi)電荷轉(zhuǎn)移機(jī)制淬滅熒光。當(dāng)α-KG與肼反應(yīng)后,探針的熒光被選擇性開啟,進(jìn)一步應(yīng)用微流池體系[4]與脂質(zhì)體包裹策略[5]實現(xiàn)了對血清中α-KG的快速定量(10-20 min;圖3a)。芳香胺N-乙酰轉(zhuǎn)移酶2(NAT2)主要分布于肝臟與結(jié)腸,其功能紊亂與多種癌癥相關(guān)[6]。為了屏蔽生物背景光,發(fā)展了一種可在近紅外波段(>780 nm)發(fā)射熒光的分子探針,并引入芳香胺基團(tuán),通過電子轉(zhuǎn)移機(jī)制淬滅熒光。當(dāng)NAT2對探針的芳香胺位點進(jìn)行乙酰化修飾后,探針熒光在短時內(nèi)顯著增強(qiáng)(圖3a),應(yīng)用這一探針初步實現(xiàn)了對肝組織勻漿中NAT2的熒光檢測,將進(jìn)一步驗證其臨床血液檢測能力[7]。此外,還發(fā)展了一種稀土元素(Tb3+)配位的芳香胺衍生物,當(dāng)發(fā)生NAT2催化的乙酰化作用后,探針可產(chǎn)生100倍的發(fā)光增強(qiáng),且熒光壽命達(dá)到1 ms以上[8]。
除上述基于化學(xué)反應(yīng)的分子探針,拓展了基于分子折疊的探針原型。環(huán)氧化酶-2(COX-2)的表達(dá)量可隨癌癥的進(jìn)程而顯著提升,但在正常組織內(nèi)極少表達(dá)[9]。將一種可與COX-2高親和力結(jié)合的抑制劑分子與熒光團(tuán)通過長柔性鏈連接,構(gòu)建了可在水環(huán)境中產(chǎn)生疏水折疊,并通過電子轉(zhuǎn)移機(jī)制淬滅熒光的分子探針(圖3b)。COX-2與抑制劑的結(jié)合可選擇性快速展開分子折疊(30 min),產(chǎn)生強(qiáng)熒光發(fā)射。此類分子探針被應(yīng)用于癌細(xì)胞與正常細(xì)胞的區(qū)分[10],以及癌組織、炎癥組織和正常組織的熒光辨別[11],為熒光指導(dǎo)手術(shù)提供了新的方法,同時為癌患的COX-2血液檢測提供了便捷工具。核酸是重要的生命信息分子,許多核酸物質(zhì)也被認(rèn)為是有效的腫瘤標(biāo)志物。基于這一背景,設(shè)計合成了以多肽為核酸受體,含有雙芘基團(tuán)的堆疊為激基締合物的折疊分子探針,通過與胞內(nèi)核酸的結(jié)合,締合物折疊被打開,產(chǎn)生單個芘基的熒光[12]。進(jìn)一步構(gòu)建了一種光致變色型折疊探針,當(dāng)探針折疊時無法通過光照對其進(jìn)行結(jié)構(gòu)調(diào)控,而與核酸結(jié)合后探針不但熒光發(fā)生增強(qiáng),且光致變色性能被激活,為核酸標(biāo)志物的檢測提供了多元化的信號輸出[13]。
聚集誘導(dǎo)發(fā)光(AIE)是指將弱熒光的分子通過聚集誘導(dǎo)熒光增強(qiáng)[14]。利用這一機(jī)制,將可靶向識別癌細(xì)胞標(biāo)志物蛋白(如溶酶體蛋白跨膜β4等)的多肽與可發(fā)射紅光的AIE信號基團(tuán)偶聯(lián),實現(xiàn)了對癌細(xì)胞表面跨膜受體標(biāo)志物的靶向、短時檢測(圖3c)[15,16]。應(yīng)用相同原理,構(gòu)建了一種酶剪切型AIE探針,通過堿性磷酸酶對探針磷酸化部位的剪切游離AIE基團(tuán),從而實現(xiàn)聚集發(fā)光,探針還被驗證可在血清中高靈敏檢測上述標(biāo)志物[17]。此外,利用超分子組裝和多信號標(biāo)記策略,實現(xiàn)了對肺癌潛在標(biāo)志物神經(jīng)激肽-1受體(NK1R)的血清檢測。設(shè)計了一種磁/光兩性的超分子多肽探針(圖3d),當(dāng)探針與NK1R識別后可從二維結(jié)構(gòu)解聚成一維結(jié)構(gòu),從而釋放熒光與磁性的雙重信號[18]。利用熒光信號實現(xiàn)了對肺癌細(xì)胞表面NK1R的選擇性標(biāo)記,并進(jìn)一步利用磁信號迅速地將肺癌患者的血清樣本從正常人群中分離出來(2 min),為肺癌的診斷試劑發(fā)展提供了新的思路。

圖3 小分子癌標(biāo)志物探針工作原理示意圖Fig. 3 Detection mechanism of small-molecule probes for cancer biomarkers
1.3 材料復(fù)合探針與器件
癌細(xì)胞通常會表達(dá)及分泌一些特殊的糖蛋白與糖蛋白受體,可作為癌癥診斷的標(biāo)志物。針對肝癌細(xì)胞表面脫唾液酸糖蛋白受體(ASGPr),設(shè)計構(gòu)建了一系列熒光開啟型與電化學(xué)活性探針體系。石墨烯是一種單原子厚度的碳材料,其獨特的光電性能吸引了學(xué)術(shù)界廣泛的研究興趣[19]。利用石墨烯的熒光淬滅與分子富集效應(yīng),將糖熒光分子與石墨烯通過π-堆疊、靜電作用等有序自組裝,簡易構(gòu)筑了糖鋪層分布,且熒光淬滅的石墨烯復(fù)合探針,應(yīng)用此類探針實現(xiàn)了對于高表達(dá)ASGPr肝癌細(xì)胞的靶向特異性、短時熒光“關(guān)開”標(biāo)記(30 min;圖2)[20]。進(jìn)一步發(fā)現(xiàn)可利用糖與ASGPr識別后的內(nèi)吞效應(yīng),構(gòu)建具備細(xì)胞靶向性的糖分子探針,用于細(xì)胞內(nèi)容物的選擇性探測[21,22]。還拓展應(yīng)用此類熒光復(fù)合材料,實現(xiàn)了對阿爾茨海默癥鼠腦切片的快速“免清洗”標(biāo)記,標(biāo)記時間(30 min)比傳統(tǒng)免疫熒光標(biāo)記技術(shù)降低24倍,標(biāo)記成本降低1000倍[23]。同樣,基于石墨烯與硫磺素的復(fù)合材料,實現(xiàn)了對鼠腦脊髓液中老年斑的熒光標(biāo)記與光熱治療,即利用石墨烯的近紅外光吸收性質(zhì),實現(xiàn)了此類材料對老年斑沉淀的降解[24]。
此外,構(gòu)建了電活性基團(tuán)標(biāo)記的糖分子探針,并與一種石墨烯覆蓋的自制絲網(wǎng)印刷電極復(fù)合,通過簡便的電化學(xué)技術(shù)實現(xiàn)了對高表達(dá)ASGPr肝癌活細(xì)胞的靈敏捕捉[25,26]。值得注意的是,此類電化學(xué)器件僅需一臺可攜式電化學(xué)工作站聯(lián)用一臺個人筆記本電腦即可完成對癌細(xì)胞的檢測,為癌癥的家庭式小型化檢測儀器發(fā)展提供了研發(fā)思路。端粒酶可通過對DNA復(fù)制的修復(fù)增加細(xì)胞分裂次數(shù),且在絕大多數(shù)癌細(xì)胞中表達(dá),是一種潛在的癌標(biāo)志物。構(gòu)建了一種基于卟啉與石墨烯的復(fù)合電極,并實現(xiàn)了對低至十個癌細(xì)胞中端粒酶的定量[27]。此外,通過熒光“關(guān)開”的方法實現(xiàn)了對端粒酶的檢測,分別利用多孔硅納米顆粒[28]與納米金顆粒[29]為核心材料并負(fù)載熒光標(biāo)記的核酸片段,得到熒光關(guān)閉的信號,隨后通過端粒酶對核酸片段的催化延長(增加熒光團(tuán)與核心材料的間距)恢復(fù)被淬滅的熒光。近期探索研究中,制備了糖分子層覆蓋的金納米顆粒,并應(yīng)用顆粒與凝集素之間的識別效應(yīng),構(gòu)建了一種糖基金顆粒與凝集素聚合的超分子結(jié)構(gòu),進(jìn)一步通過凝集素與肝癌糖蛋白類標(biāo)志物甲胎蛋白異質(zhì)體(AFP-L3)的競爭結(jié)合解聚超分子體系,通過聚合—解聚過程的吸收光信號變化實現(xiàn)了肝癌患者血清的快速診斷(5 min),并實現(xiàn)了肝癌與肝炎病患和正常人血清的準(zhǔn)確區(qū)分(未發(fā)表成果)。修飾的金納米顆粒還可被用于監(jiān)控肺癌病人所呼出的氣體癌標(biāo)志物,為癌癥的快速、簡易診斷提供了獨特見解[30]。
2 結(jié)論與展望
隨著臨床需求的日益增長,發(fā)展可快速、準(zhǔn)確對癌癥進(jìn)行血液診斷的經(jīng)濟(jì)型工具是當(dāng)今多學(xué)科交叉的研究熱點。血液診斷的優(yōu)勢在于規(guī)避影像學(xué)與組織活檢等技術(shù)對于人體的創(chuàng)傷,并可高通量地對大規(guī)模樣品進(jìn)行篩查。然而現(xiàn)有技術(shù)存在操作繁、耗時長、成本高等顯著缺陷,且國外技術(shù)壟斷嚴(yán)重,于是發(fā)展我國自主知識產(chǎn)權(quán)的高效癌癥診斷工具迫在眉睫。該文簡要綜述了相關(guān)領(lǐng)域科研團(tuán)隊近年來在發(fā)展癌標(biāo)志物分子探針領(lǐng)域的研究進(jìn)展。從小分子、超分子與材料復(fù)合探針等層面闡述了探針構(gòu)建策略,進(jìn)一步結(jié)合對癌標(biāo)志物的檢測實例展示了分子探針的快速檢測性能。
分子探針的主要優(yōu)勢在于構(gòu)建簡易(合成與材料復(fù)合成本均低于現(xiàn)有生化試劑),免標(biāo)記(無需對待測品反復(fù)免疫標(biāo)記),尤其是響應(yīng)快(最快幾分鐘內(nèi)即可獲得信號),有望成為新一代的疾病診斷工具,實現(xiàn)快速和低成本的癌癥診斷。當(dāng)然,目前所發(fā)展的分子探針原型仍有待系統(tǒng)性的臨床實驗驗證,作者對分子探針的未來發(fā)展方向作如下展望:
(1)實現(xiàn)分子探針體系的標(biāo)準(zhǔn)化制備,有利于導(dǎo)向我國自主知識產(chǎn)權(quán)診斷試劑盒的研發(fā);
(2)緊密與醫(yī)學(xué)結(jié)合,進(jìn)行臨床的“多中心、大樣本和雙盲”血液化驗,充分驗證探針的醫(yī)學(xué)價值;
(3)合理設(shè)立對照組,實現(xiàn)對于癌癥的精準(zhǔn)、快速診斷。
致謝 感謝田禾教授對于本文的提議與審核
(References)
[1] Siegel R, Ma J, Zou Z, Jemal A. Cancer statistics[J]. Ca: A Cancer Journal for Clinicians, 2014, 64:9-29.
[2] Kim H N, Guo Z, Zhu W, et al. Recent progress on polymer-based fluorescent and colorimetric chemosensors[J]. Chemical Society Reviews, 2011, 40:79-93.
[3] Ward P S, Patel J, Wise D R, et al. The common feature of leukemia-associated IDH1 and IDH2 mutations is a neomorphic enzyme activity converting α-ketoglutarate to 2-hydroxyglutarate[J]. Cancer Cell, 2010, 17:225-234.
[4] Jin P, Jiao C, Guo Z, et al. Rational design of a turnon fluorescent sensor for α-ketoglutaric acid in a microfluidic chip[J]. Chemical Science, 2014, 5:4012-4016.
[5] He Y, Guo Z, Jin P, et al. Optimizing the chemical recognition process at a fluorescent chemosensor for α-ketoglutarate[J]. Industrial & Engineering Chemistry Research, 2015, 54:2886-2893.
[6] Walker K, Ginsberg G, Hattis D, et al. Genetic polymorphism in N-acetyltransferase (NAT): population distribution of NAT1 and NAT2 activity[J]. Journal of Toxicology and Environmental Health, Part B, 2009,12:440-472.
[7] Wang X, Cui L, Zhou N, et al. A highly selective and sensitive near-infrared fluorescence probe for arylamine N-acetyltransferase 2 in vitro and in vivo[J]. Chemical Science, 2013, 4:2936-2940.
[8] Terai T, Kikuchi K, Urano Y, et al. A long-lived luminescent probe to selectively detect arylamine N-acetyltransferase (NAT) activity of cells[J]. Chemical Communications, 2012, 48:2234-2236.
[9] Tucker O N, Dannenberg A J, Yang E K, et al. Cyclooxygenase-2 expression is up-regulated in human pancreatic cancer[J]. Cancer Research, 1999, 59:987-990.
[10] Zhang H, Fan J, Wang J, et al. An off-on COX-2-specific fluorescent probe: targeting the Golgi apparatus of cancer cells[J]. Journal of the American Chemical Society.,2013,135:11663-11669.
[11] Zhang H, Fan J, Wang J, et al. Fluorescence discrimination of cancer from inflammation by molecular response to COX-2 enzymes[J]. Journal of the American Chemical Society,2013, 135:17469-17475.
[12] Wu J, Zou Y, Li C, et al. A molecular beacon for the ratiometric sensing of nucleic acids. Journal of the American Chemical Society[J]. 2012, 134:1958-1961.
[13] Liu K, Wen Y, Shi T, et al. DNA gated photochromism and fluorescent switch in a thiazole orange modified diarylethene[J]. Chemical Communications, 2014,50:9141-9144.
[14] Ding D, Li K, Liu B, et al. Bioprobes based on AIE fluorogens[J]. Accounts of Chemical Research, 2013,46:2441-2453.
[15] Huang Y, Hu F, Zhao R, et al. Tetraphenylethylene conjugated with a specific peptide as a fluorescence turnon bioprobe for the highly specific detection and tracing of tumor markers in live cancer cells[J]. Chemistry an European Journal, 2014, 20:158-164.
[16] Hu F, Huang Y, Zhang G, et al. Targeted bioimaging and photodynamic therapy of cancer cells with an activatable red fluorescent bioprobe. Analytical Chemistry, 2014,86:7987-7995.
[17] Liang J, Kwok RTK, Shi H, et al. Fluorescent light-up probe with aggregation-induced emission characteristics for alkaline phosphatase sensing and activity study[J]. ACS Applied Materials and Interfaces, 2013, 5:8784-8789.
[18] Wu J, Zou R, Wang Q, et al. A peptide probe for thedetection of neurokinin-1 receptor by disaggregation enhanced fluorescence and magnetic resonance signals[J]. Scientific Reports, 2014, 4:6487.
[19] Novoselov K S, Geim A K, Morozov S V, et al. Electric field effect in atomically thin carbon films[J]. Science,2004, 306:666-669.
[20] Zhang H L, Wei X L, Zang Y, Fluorogenic probing of specific recognitions between sugar ligands and glycoprotein receptors on cancer cells by an economic graphene nanocomposite[J]. Advanced Materials, 2013,25:4097-4101.
[21] Li K B, Zang Y, Wang H, et al. Hepatoma-selective imaging of heavy metal ions using a ‘clicked’galactosylrhodamine probe[J]. Chemical Communications,2014, 50:11735-11737.
[22] Shi D T, Zhou D, Zang Y, et al. Selective fluorogenic imaging of hepatocellular H2S by a galactosyl azidonaphthalimide probe[J]. Chemical Communications,2015, 51:3653-3655.
[23] He X P, Deng Q, Cai L, et al. Fluorogenic resveratrolconfined graphene oxide for economic and rapid detection of Alzheimer’s disease[J]. ACS Applied Materials and Interfaces, 2014, 6:5379-5382.
[24] Li M, Yang X, Ren J, et al. Using graphene oxide high near-infrared absorbance for photothermal treatment of Alzheimer’s disease[J]. Advanced Materials, 2012, 24:1722-1728.
[25] Li Z, Deng S S, Zang Y, et al. Capturing intercellular sugar-mediated ligand-receptor recognitions via a simple yet highly biospecific interfacial system[J]. Scientific Reports, 2013, 3:2293.
[26] He X P, Zhu B W, Zang Y, et al. Dynamic tracking of pathogenic receptor expression of live cells using pyrenyl glycoanthraquinone-decorated graphene electrodes[J]. Chemical Science, 2015, 6:1996-2001.
[27] Wu L, Wang J, Feng L, et al. Label-free ultrasensitive detection of human telomerase activity using porphyrinfunctionalized graphene and electrochemiluminescence technique[J]. Advanced Materials, 2012, 24:2447-2452.
[28] Qian R, Ding L, Ju H. Switchable fluorescent imaging of intracellular telomerase activity using telomeraseresponsive mesoporous silica nanoparticle[J]. Journal of the American Chemical Society[J]. 2013, 135:13282-13285.
[29] Qian R, Ding L, Yan L, et al. A robust probe for lighting up intracellular telomerase via primer extension to open a nicked molecular beacon[J]. Journal of the American Chemical Society[J]. 2014, 136:8205-8208.
[30] Peng G, Tisch U, Adams O, et al. Diagnosing lung cancer in exhaled breath using gold nanoparticles[J]. Nature Nanotechnology, 2009, 4:669-673.
《糖尿病新世界》雜志稿約

《糖尿病新世界》是國家衛(wèi)生和計劃生育委員會主管,全國衛(wèi)生產(chǎn)業(yè)企業(yè)管理協(xié)會主辦的專業(yè)性學(xué)術(shù)期刊,中國核心數(shù)據(jù)期刊(遴選)數(shù)據(jù)庫收錄期刊、中國期刊全文數(shù)據(jù)庫收錄期刊、中文科技期刊數(shù)據(jù)庫收錄期刊。國內(nèi)統(tǒng)一刊號:CN 11-5019/R;國際刊號:ISSN 1672-4062,郵發(fā)代號82-120,定價10元。
本刊服務(wù)于醫(yī)學(xué)創(chuàng)新研究、醫(yī)療事業(yè)改革和廣大醫(yī)療工作者。堅持“創(chuàng)造性、科學(xué)性、指導(dǎo)性、實用性”的辦刊方針,貫徹黨和國家的衛(wèi)生方針政策,貫徹理論、實踐與交流相結(jié)合的方針。本刊長期面向全國征集醫(yī)學(xué)學(xué)術(shù)論文,在本刊發(fā)表的論文可獲得國家級繼續(xù)教育學(xué)分。
【辦刊宗旨】
本刊堅持“傳播我國糖尿病醫(yī)療的重大成果,促進(jìn)中外糖尿病領(lǐng)域的技術(shù)交流”為辦刊宗旨,為有效提高我國糖尿病的診治水平打造一個良好的傳播和交流平臺。
【主要欄目】
論著、醫(yī)藥論壇、衛(wèi)生經(jīng)濟(jì)、醫(yī)院管理、科研專欄、臨床應(yīng)用、護(hù)理天地、指南解讀、病例報告、專題筆談。
【讀者對象】
醫(yī)療衛(wèi)生科研院所、醫(yī)學(xué)院校、醫(yī)療機(jī)構(gòu)、藥品企業(yè)、醫(yī)療衛(wèi)生管理部門、社團(tuán)組織和醫(yī)藥相關(guān)行業(yè)的科研、臨床、醫(yī)護(hù)、教育、管理人員為主要服務(wù)對象。
聯(lián)系電話:010-65060551
投稿郵箱:bianjibu@tnbxsj.com
網(wǎng) 站:www.tnbxsj.com
Molecular probes: new-generation tools for the accelerated diagnosis of cancer
HE Xiaopeng
Key Laboratory for Advanced Materials & Institute of Fine Chemicals, School of Chemistry and Molecular Engineering, East China University of Science and Technology, Shanghai 20023
The rapid yet accurate diagnosis of cancer is a critical issue that poses a great challenge worldwide in the field of life science. However, current clinical biochemical techniques have flaws in terms of complicated conducting procedures, high technical requirement, long detection time and high cost. The development of simpler and more economic tools for the fast blood tests of cancer biomarkers has become a major focus of the academy. Molecular probes have merits in sensing applications owing to their conciseness in construction, fast response and low cost. Their conventional application areas involve environmental analysis and cellular/in vivo imaging. In recent years, the development of molecular probes suitable for probing cancer biomarkers has become a vividly new multidisciplinary research field. Here we summarize the construction strategies of these probes and highlight their diagnostic efficiency for cancer biomarkers. This article aims at spurring the diversification of simple and effective molecular probes for the detection cancer biomarkers, accelerating the progress of cancer blood tests by the combination of chemical techniques with medicinal science.
cancer; blood biomarker; molecular probe; molecular diagnosis; fluorescence
R730.58
A
10.11966/j.issn.2095-994X.2015.01.03.04
2015-07-30;
2015-10-01
國家重點基礎(chǔ)研究發(fā)展計劃(973計劃)項目(2013CB733700)
賀曉鵬,副研究員,研究方向為醫(yī)學(xué)導(dǎo)向的化學(xué)糖生物學(xué),電子信箱:xphe@ecust.edu.cn
引用格式:賀曉鵬.分子探針:提速癌癥診斷的新工具[J].世界復(fù)合醫(yī)學(xué),2015,1(3):207-211

