HPLC同時測定多種食品添加劑的不確定度評定
馬麗,代科,曾婷,黃仕穩,鞠鶴鵬
(廣州軍區疾病預防控制中心,廣東廣州510507)
HPLC同時測定多種食品添加劑的不確定度評定
馬麗,代科,曾婷*,黃仕穩,鞠鶴鵬
(廣州軍區疾病預防控制中心,廣東廣州510507)
建立高效液相色譜(HPLC)法測定灌裝紅腰豆中苯甲酸、山梨酸、糖精鈉含量的不確定度方法。通過建立數學模型,確定影響不確定度的因素,分析各不確定度對實驗結果的影響。樣品中苯甲酸、山梨酸、糖精鈉含量測定的合成標準不確定度分別為0.028 7、0.017 3、0.127 9 mg/kg,擴展不確定度分別為0.057 4、0.034 7、0.255 8 mg/kg。本研究方法可為HPLC法測定灌裝紅腰豆中苯甲酸、山梨酸、糖精鈉含量的不確定度評估提供參考。
HPLC;測量不確定度;食品添加劑;合成標準不確定度;擴展不確定度
近年來,以防腐劑、甜味劑以及香精為代表的食品添加劑已經被大量的運用到食品生產加工和方便食品當中[1]。因此在中國,這些食品添加劑被食品安全標準限制,這對于食品檢驗工作提出了較高的要求,尤其對于這些含量較低的物質,檢測結果的真實性更是至關重要,測量不確定度能很好的反映測量結果的質量,因此對于不確定的研究具有一定意義。
我國于1999年制定了中華人民共和國計量技術規范JJF1059—99《測量不確定度評定與表示》[2]。根據國際通用計量學基本術語,測量不確定度的定義為:表征合理地賦予被測量之值的分散性與測量結果相聯系的參數[3]。在實驗測量結果中,由于測量誤差的存在,而對被測量值不能確定的程度,表示誤差可能存在的范圍,表征結果的可信賴程度,它能更加準確的體現測量結果的分散性。
本研究根據國標GB/T 23495-2009[4]《食品中苯甲酸、山梨酸和糖精鈉的測定(HPLC)》相關要求和方法,對測量過程中可能影響測量結果的因素進行不確定度評價和分析。
1材料和方法
1.1儀器與試劑
Waterse2695HPLC:美國Waters公司;Waters2998二極管陣列檢測器,Empower software色譜工作站;AB204-L萬分之一電子天平:METTLER TOLEDO;FJ-200高速分散均質機:上海標本模型廠;SIGMA 3K15離心機:德國;KQ-600型數控超聲波清洗器:昆山市超聲儀器有限公司。
苯甲酸鈉、山梨酸鉀、糖精鈉;乙酸鋅、乙酸銨、亞鐵氰化鉀均為分析純;甲醇為色譜純。
1.2色譜條件
色譜柱:XBridge C18柱,250 mm×4.6 mm,5 μm;流動相:甲醇+乙酸銨溶液(0.02 mol/L)=15∶85,乙酸銨溶液:稱取1.56 g標準品,用純水定容至1 000 mL;流速:1 mL/min;檢測波長:230 nm;進樣量:10 μL。
1.3溶液的配制
1.3.1標準溶液的配制
1.3.1.1苯甲酸、山梨酸、糖精鈉標準儲備液配制
準確稱取苯甲酸鈉0.236 0 g、山梨酸鉀0.268 0 g、糖精鈉0.170 2 g,分別加水溶解并定容至200 mL。所得標準儲備液濃度均為1 mg/mL。
1.3.1.2苯甲酸、山梨酸、糖精鈉標準稀釋液配制
各取苯甲酸、山梨酸標準儲備液1 mL于2個100 mL容量瓶中,加水定容至刻度,兩種溶液每毫升相當于含標準品10 μg。另取糖精鈉標準儲備液1 mL于10 mL容量瓶中,加水定容至刻度。此溶液每毫升相當于含糖精鈉100 μg。
1.3.1.3單標的配置
分別吸取苯甲酸、山梨酸、糖精鈉標準稀釋液各1.0 mL于3個25 mL容量瓶中,定容至刻度,3種單標溶液的濃度分別為苯甲酸0.4 μg/mL、山梨酸0.4μg/mL、糖精鈉4.0 μg/mL。
1.3.1.4混合標準使用液的配置
準確吸取不同體積的苯甲酸、山梨酸、糖精鈉標準稀釋液于6個10 mL容量瓶中,用水定容至刻度,搖勻,配置成苯甲酸、山梨酸濃度分別為0.02、0.30、0.40、0.50、0.80、1.00 μg/mL,糖精鈉濃度為2.00、3.00、4.00、5.00、8.00、10.0 μg/mL的混合標準溶液。
1.3.2樣品的處理
1.3.2.1樣品制備及預處理
取灌裝紅腰豆作為檢驗樣品,將樣品搗碎,再經高速組織均質機均質備用。
1.3.2.2樣品前處理方法
準確稱取2.500 g上述預處理好的樣品于小燒杯中,用20 mL水分數次清洗小燒杯將樣品移入25 mL容量瓶中,超聲震蕩提取5 min,取出過后加入2 mL亞鐵氰化鉀溶液,搖勻,再加入2 mL乙酸鋅溶液,搖勻,用水定容至刻度。移入離心管中,4000r/min離心5min,吸出上清液,經0.45 μm微孔濾膜過濾,濾液待上機分析。
1.4測定方法
儀器打開預熱,按實驗條件平衡30 min以上,待基線平穩后,樣品依次進樣,以其單標液峰保留時間為依據定性,記錄各峰面積值。
1.5測定結果
單標溶液結果苯甲酸、山梨酸、糖精鈉峰保留時間分別為6.502、8.338、7.341 min。
2數學模型與不確定度計算公式
2.1數學模型
2.1.1工作曲線
苯甲酸、山梨酸、糖精鈉的標準曲線分別為y= 5 323.0x+1 485.8(R2=0.999 956)、y=96 297.7 x-754.1(R2=0.999 981)、y=4 078.0 x-2 314.7(R2=0.999 915)。
2.1.2樣品中的苯甲酸、山梨酸、糖精鈉計算公式
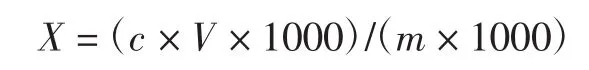
式中:X為樣品中待測組分含量,(g/kg);c為由標準曲線得出的樣液中待測物的濃度,(mg/mL);V為樣品定容體積,mL;m為樣品質量,g。
2.1.3樣品中苯甲酸、山梨酸、糖精鈉計算結果
由標準曲線可得出:①樣品溶液中苯甲酸、山梨酸、糖精鈉的濃度分別為0.254、0.214、1.64 μg/mL;②加標樣品溶液中苯甲酸、山梨酸、糖精鈉濃度分別為0.641、0.600、5.37 μg/mL;③定容體積為25 mL,樣品質量為2.5 g,因此可得知樣品中苯甲酸、山梨酸、糖精鈉的含量分別為2.54、2.14、16.4 mg/kg。
2.2測量相對不確定度計算公式[6]
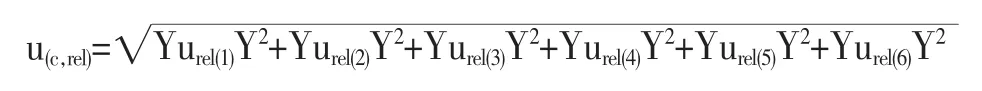
式中:u(c,rel)為樣品中苯甲酸/山梨酸/糖精鈉濃度的相對不確定度;urel(1)為苯甲酸/山梨酸/糖精鈉標準溶液及配制引起的相對不確定度;urel(2)為標準溶液的濃度-峰面積值擬合的工作曲線求苯甲酸/山梨酸/糖精鈉含量時產生的相對不確定度;urel(3)為重復測定樣品產生的相對不確定度,即A類不確定度;urel(4)為試樣稱量引入的相對不確定度;urel(5)為樣品溶液定容體積引入的相對度;urel(6)為加標回收率引起的相對不確定度。
3測量相對不確定度各分量的計算
3.1標準溶液配制引起的相對不確定度(以苯甲酸0.5μg/mL、山梨酸0.5μg/mL、糖精鈉5.0μg/mL配制為例)urel(1)由以下6個分量組成。
3.1.1標準品稱量引起的相對不確定度urel,w(標)
主要包括標準品純度、天平稱量示值以及天平稱量重復性引起的不確定度[5]。
3.1.1.1標準品純度引入的不確定度uw(標a)
苯甲酸、山梨酸、糖精鈉標準品的純度分別為:99.0%、99.8%、99.9%,假定分布區間為0.05%,取K=,則相對不確定度:苯甲酸=0.000 29,山梨酸= 0.000 29,糖精鈉=0.000 29。
3.1.1.2天平稱量準確性引起的不確定度uw(標b)
AB204-L電子天平,檢定證書給出的最大允差為0.000 2 g,假設為均勻分布,則u(標b)=0.000 2/31/2= 0.000 115 g。
3.1.1.3天平稱量重復性的不確定度uw(標c)
AB204-L電子天平,檢定證書給出的重復性誤差為±0.001 1 g,假設為均勻分布,則uw(標c)=0.001 1/31/2= 0.000 635 g。
3.1.1.4天平稱量引起的相對不確定度
uw(標)=[(uw(標a))2+(uw(標b))2+(uw(標c))2]1/2,則苯甲酸、山梨酸、糖精鈉稱量引起的相對標準不確定度分別為0.003 0、0.0026、0.00413.1.2200mL量瓶(V1)的相對不確定度urel,v1(標)包括3部分:(1)量瓶體積的不確定度,根據常用玻璃量器計量檢定規定[6]可知,A級200mL量瓶的允差為±0.15mL,按均勻分布換算成標準偏差為0.087 mL;(2)定容時的估讀誤差,用該容量瓶重復吸取蒸餾水10次,并稱量計算標準偏差為0.020 mL;(3)量瓶和溶液的溫度與校正時的溫度不同引起的體積不確定度[7],但是實驗室環境溫度大致在25℃,容量瓶的校準溫度為20℃,則環境溫度引起的不確定度為
以上3項合成得出
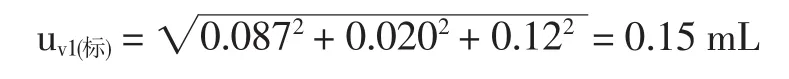
200mL量瓶(V1)的相對不確定度:urel,v1(標)=0.000 75
3.1.31mL移液管體積(V2)的相對不確定度urel,v2(標)
包括3個部分:(1)移液管體積的不確定度,根據常用玻璃量器計量檢定規定可知,A級1 mL移液管的允差為±0.007 mL,按均勻分布換算成標準偏差為;(2)吸取溶液時讀數誤差,估計為±0.005 mL,按均勻分布換算成標準偏差為0.005/;(3)移液管和溶液溫度與校正時溫度不同引起的體積不確定度為(實際溫差為5℃,水的體積膨脹系數為2.1×10-4/℃),移液管因環境溫度校正不同引起的體積不確定度為61 mL。
以上3項合成得出:
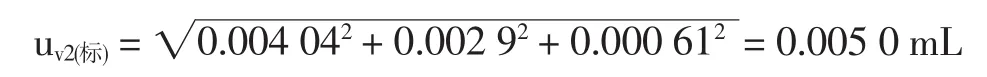
1mL移液管(V2)的相對不確定度:urel,v2(標)=0.0050 3.1.4100 mL(糖精鈉為10 mL)容量瓶體(V3)的相對不確定度urel,v3(標)
按100mL計算,包括3部分:(1)量瓶體積的不確定度,根據常用玻璃量器計量檢定規定可知,A級100 mL量瓶的允差為±0.10 mL,按均勻分布換算成標準偏差為;(2)定容時的估讀誤差,用該容量瓶重復吸取蒸餾水10次,并稱量計算標準偏差為0.018 mL;(3)量瓶和溶液的溫度與校正時的溫度不同引起的體積不確定度為100×2.1×10-4×5/
以上3項合成得出:
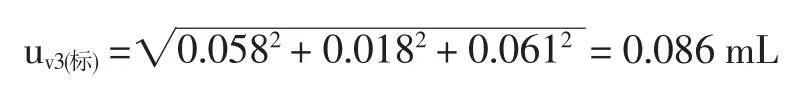
100mL量瓶(V3)的相對不確定度:urel,v3(標)=0.000 86 3.1.51 mL移液管吸取標準稀釋液的體積(V4)的相對不確定度urel,v4(標)
如“4.1.3”計算,urel,v4(標)=0.005 0。
3.1.610mL容量瓶的體積(V5)的不確定度urel,v5(標)
包括3部分:(1)量瓶體積的不確定度,根據常用玻璃量器計量檢定規定可知,A級10 mL量瓶的允差為±0.02 mL,按均勻分布換算成標準偏差為0.012 mL;(2)定容時的估讀誤差,用該容量瓶重復吸取蒸餾水10次,并稱量計算標準偏差為0.006 mL;(3)量瓶和溶液的溫度與校正時的溫度不同引起的體積不確定度為
以上3項合成得出:
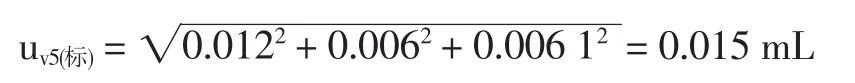
10mL量瓶(V5)的相對不確定度:urel,v5(標)=0.001 5
綜上所述,
苯甲酸、山梨酸、糖精鈉標準溶液及配制引起的相對不確定度分別為0.007 9、0.007 8、0.006 9
3.2苯甲酸/山梨酸/糖精鈉標準工作曲線擬合引起的不確定度
工作曲線數據表如表1、表2、表3所示。
urel(1)計算公式表示為:
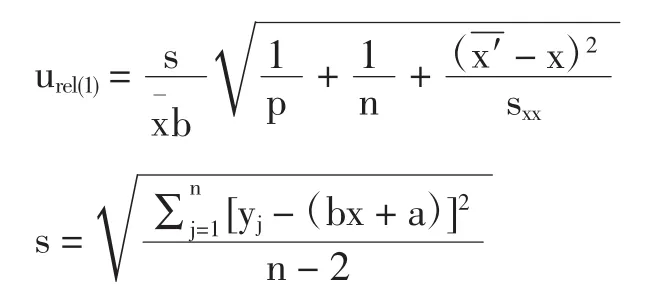
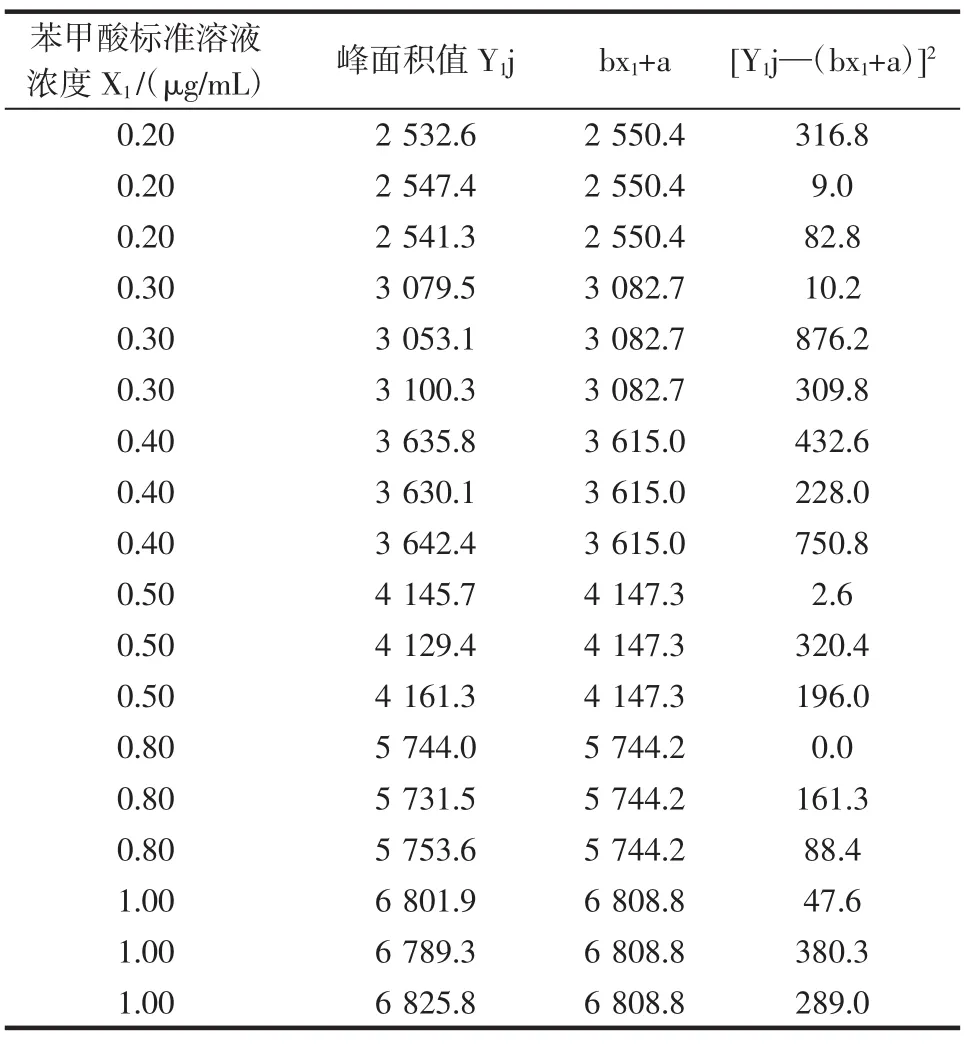
表1 苯甲酸濃度的不確定度工作曲線數據Table 1Benzoic acid concentration of working curve data uncertainty
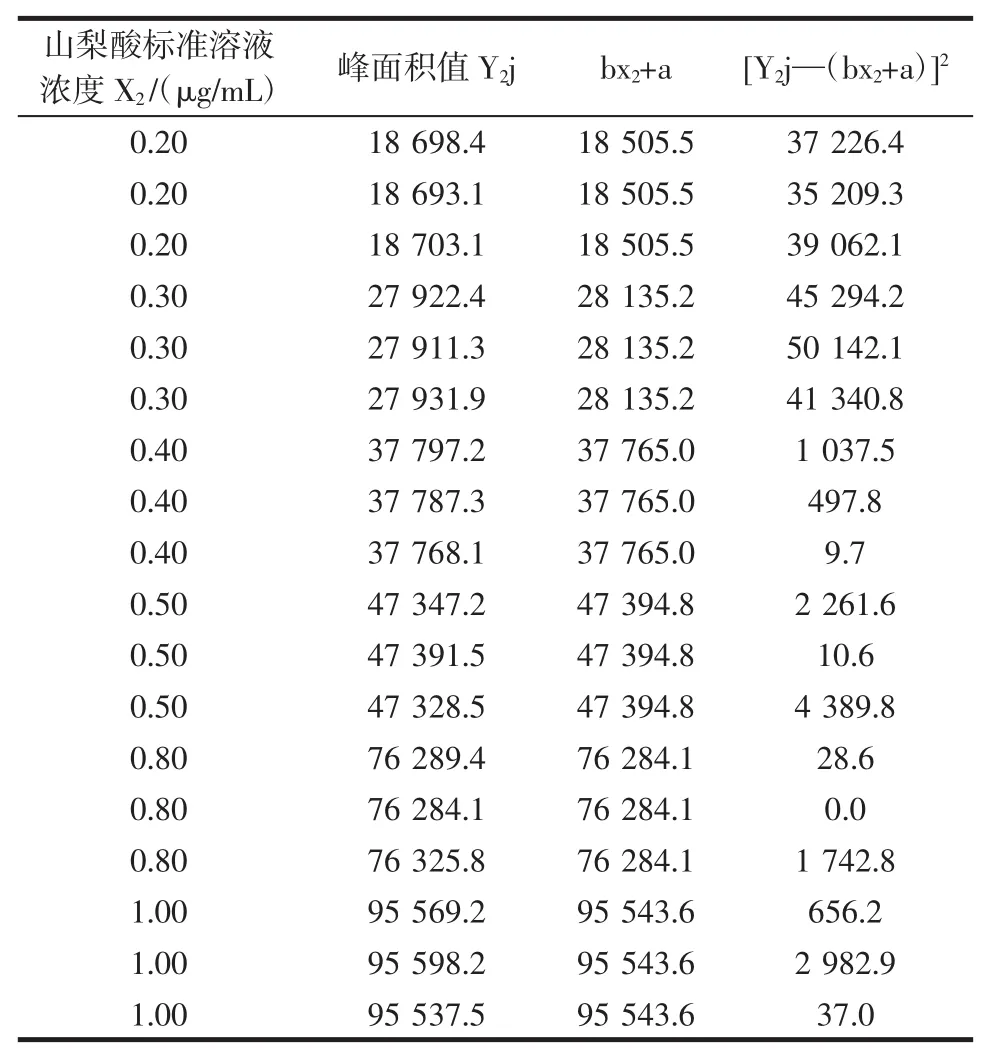
表2 山梨酸濃度的不確定度工作曲線數據Table 2The uncertainty of sorbic acid concentration in the working curve data

式中:n為測試標準溶液次數,n=6×3=18;P為測試樣品溶液次數,P=7為各標準溶液濃度的平均值,x苯=0.533,x山=0.533,x糖=5.33;x′為樣品溶液濃度的平均值;b為工作曲線的斜率,b苯=5323.0,b山=96 297.7,b糖=4 078.0。
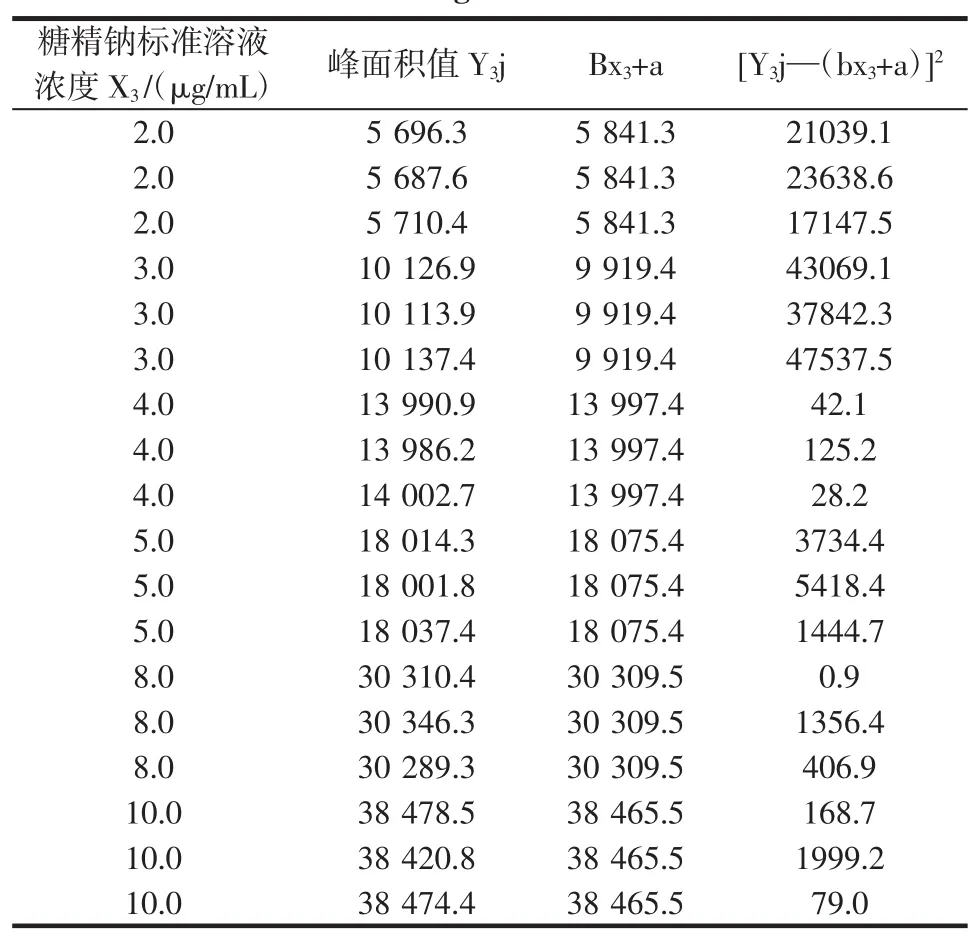
表3 糖精鈉濃度的不確定度工作曲線數據Table 3The uncertainty of saccharin sodium concentration in the working curve data
7次測量所得樣品中苯甲酸濃度分別為:0.254、0.255、0.252、0.254、0.257、0.255、0.254 μg/mL,平均濃度為0.254 μg/mL;山梨酸濃度均為0.214 μg/mL,平均濃度為0.214 μg/mL;糖精鈉濃度分別為1.642、1.644、1.635、1.637、1.637、1.640、1.643、1.640 μg/mL,平均濃度為1.640 μg/mL。
樣品中苯甲酸、山梨酸、糖精鈉的含量為x苯= 0.254×25/2.5=2.54 mg/kg;x山=0.214×25/2.5=2.14 mg/kg;x糖=1.640×25/2.5=16.40 mg/kg。

3.3高效液相色譜儀測量重復性引起的不確定度(即A類不確定度urel(3))即重復測定樣品產生的相對不確定度數據見“1.5.3”項。單次測量相對不確定度
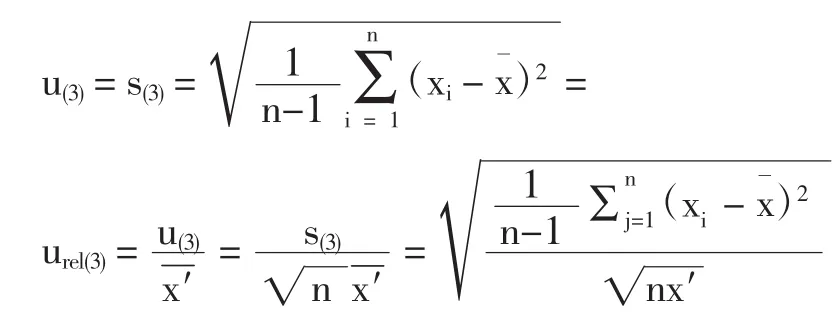
則苯甲酸、山梨酸、糖精鈉單次測量引起的不確定度分別為0.002 1、0.000 30、0.000 81
3.4樣品稱量引入的相對不確定度urel(4)
主要由電子天平稱量準確性引起的不確定度uw(標b)和稱量重復性的不確定度uw(標c),分別按“4.2.1.2”和“4.2.1.3”計算,則urel(4)=0.000 26
3.5樣品溶液定容體積引入的不確定度urel(5)
本次試驗樣品溶液定容采用的是25 mL容量瓶,25 mL容量瓶的相對不確定度urel(5)主要包括三個部分:①容量瓶體積的不確定度u(5)1,根據JJG196-2006計量檢定規程,25 mL量瓶允許誤差為±0.03 mL,按三角分布,則;②容量瓶重復性引入的不確定度u(5)2:屬A類不確定度,由實驗數據統計得u(5)1=0.021mL;③容量瓶因溫度不同產生的不確定度u(5)3,在空調條件下,設室溫為(25±2)℃,溶劑水的體積膨脹系數為2.1×10-4℃-1,按照矩形分布,包含因子,則環境溫度引入的不確定度為u(5)3=0.006 1。
合成以上三項得

3.6回收率產生的相對標準不確定度urel(6)[8]:
3.6.1苯甲酸回收率測得的結果:為95.99%、95.92%、97.41%、97.29%、95.99%、96.11%、97.07%,平均回收率為96.54%。回收率產生的不確定度為u(6)l=,回收率相對標準不確定度為=u(6)l/P%=0.007 1。
3.6.2山梨酸為96.46%、96.72%、96.45%、96.72%、96.60%、96.54%、96.48%,平均回收率為96.57%。回收率產生的不確定度u(6)l=0.001 2,回收率相對標準不確定度為=u(6)l/P%=0.001 2。
3.6.3糖精鈉為93.00%、93.08%、93.15%、93.36%、93.28%、92.99%、93.29%,平均回收率為93.16%。回收率產生的不確定度=0.0015,回收率相對標準不確定度為=u(6)l/P%=0.0016。
4苯甲酸/山梨酸/糖精鈉相對合成標準不確定度
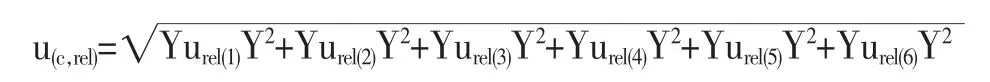
苯甲酸、山梨酸、糖精鈉相對合成標準不確定度分別為0.011 3、0.008 1、0.007 8
5擴展不確定度分析
合成標準不確定度u(c)=u(c,rel)×,u(c)l=0.0113×2.54= 0.028 7 mg/kg;u(c)l=0.008 1×2.14=0.017 3 mg/kg;u(c)l=0.007 8×16.40=0.127 9 mg/kg
取置信概率P=95%,則置信區間K=2,擴展不確定度U=u(c)×K=u(c,rel)×x×K,U苯=0.011 3×2.54×2= 0.057 4 mg/kg;U山=0.008 1×2.14×2=0.034 7 mg/kg;U糖=0.007 8×16.40×2=0.255 8 mg/kg
6結論
1)影響本實驗測量結果的主要因素為標準溶液的配制、標準曲線以及回收率,其中標準溶液的配制影響最大,而在這一過程中標準品的稱量和移液管移取溶液所占比重最大。
2)本試驗同時評定同一樣品的3種成分含量測定結果的不確定度,從試驗結果分析,糖精鈉的測量不確定度較大,苯甲酸、山梨酸次之,最大的影響因素是標準溶液的配制。
[1]Bergamo,A B,Fracassi,J A,Jesus,D P.Simultaneous determination of aspartame,cyclamate,saccharin and acesulfame-K in soft drinks and tabletop sweetener formulations by capillary electrophoresis with capacitively coupled contactless conductivity detection[J]. Food Chemistry,2010,124(4):1714-1717
[2]國家質量技術監督局.JJF1059-1999測量不確定度評定與表示[S].北京:中國計量出版社,2000
[3]Intematioual Standards Organization.GUM:Guide to the Expresionof Uncertainty in Measurement[S].Is0 Geneva Switzerland,1995
[4]中國標準化研究院.GB/T 23495-2009食品中苯甲酸、山梨酸、糖精鈉的測定(高效液相色譜法)[S].北京:中國標準出版社,2009
[5]楊玳,黃舒麗.原子吸收光譜法測定魚油中鎘的不確定度評定[J].食品與藥品,2012,28(3):128-131
[6]苗愛東,王彥宗.高效液相色譜法測定甲硝唑片中甲硝唑含量的不確定度分析[J].解放軍醫藥雜志,2012,24(1):33-34
[7]國家質量技術監督局.JJGl96-2006常用玻璃量器檢定規程[S].北京:中國計量出版社,2006
[8]莫連峰,陳瑩.HPLC法測定阿咖酚散含量的測量不確定度評定[J].中國藥品標準,2010,11(4):921-922
The Evaluation of Measurement Uncertainty for Varieties of Food Additives by HPLC Synchronously
MA Li,DAI Ke,ZENG Ting*,HUANG Shi-wen,JU He-peng
(Centers for Disease Control and Prevention of Guangzhou Military Region,Guangzhou 510507,Guangdong,China)
To establish a method of uncertainty evaluation for the determination of benzoic acid,sorbic acid and soluble saccharin from the red beans by HPLC.By establishing a mathematical model to determine the factors affecting the uncertainty and the analysis of the effect of the uncertainty of the experimental results.Results showed determination of benzoic acid,sorbic acid,soluble saccharin content in the sample of the synthetic standard uncertainty were 0.028 7,0.017 3,0.127 9 mg/kg,the expanded uncertainty were 0.057 4,0.034 7,0.255 8 mg/kg.This method can be used in HPLC determination of benzoic acid,sorbic acid and soluble saccharin in the red beans of uncertainty evaluation.
HPLC;easurement ncertainty;food additives;synthetic standard uncertainty;expanded uncertainty
10.3969/j.issn.1005-6521.2015.11.008
2013-12-12
馬麗(1971—),女(漢),高級工程師,本科,從事食品理化檢驗工作。
曾婷,碩士研究生,助理研究員。

