圖像引導體部伽瑪刀治療的臨床應用效果
齊文杰 康 靜 波朱奇張騫劉偉海軍總醫院腫瘤診療中心,北京100048
圖像引導體部伽瑪刀治療的臨床應用效果
齊文杰康靜波朱奇▲張騫劉偉
海軍總醫院腫瘤診療中心,北京100048
目的探討圖像引導體部伽瑪刀治療的臨床應用效果。方法收集海軍總醫院2013年10月~2014年10月應用圖像引導伽瑪刀治療的60例不同種類和部位腫瘤患者,觀察近期(12周)的治療效果。選出其中2例典型患者分別運用重復定位尺和圖像引導擺位,并對兩種擺位方法產生的誤差進行比較。結果治療12周,顯效42例,有效9例,無變化3例,進展3例,總有效率為85%。圖像引導伽瑪刀治療患者擺位誤差明顯優于重復定位尺引導伽瑪刀的擺位誤差,差異有統計學意義(P<0.05)。結論圖像引導體部伽瑪刀在原有伽瑪刀的精確定位框架基礎上提高了治療精度,降低了擺位誤差及靶區運動所引起的誤差,是體部伽瑪刀治療技術與圖像引導系統一次完美結合,是體部伽瑪刀治療精度的一次質的飛躍,屬于全新的伽瑪刀治療模式,值得廣泛推廣應用。
圖像引導;體部伽瑪刀;定位框架;擺位誤差
腫瘤放射治療時的等中心位置的誤差(包括擺位誤差、器官運動和變形、機械相關誤差等)是影響放射治療精確度的主要原因,也是考慮計劃靶區(planning target volume,PTV)的主要因素[1]。圖像引導放射治療(image guided radiation therapy,IGRT)是近十幾年來逐步發展起來的腫瘤放射治療新技術[2],圖像引導影像設備與放射治療設備相結合,采用先進的圖像掃描和數據處理方法,對腫瘤靶區在治療前進行精確定位,糾正擺位誤差,實現實時定位跟蹤,大大提高了放射治療的精確度,降低了對患者腫瘤靶區周圍正常組織及重要臟器和敏感組織的放射性損傷。通過對誤差數據的分析,總結造成誤差的原因和規律,為臨床醫師、物理師提供了腫瘤靶區勾畫外放的理論依據。海軍總醫院(以下簡稱“我院”)應用引進圖像引導體部伽瑪刀于臨床,共治療60例患者,現結合圖像引導體部伽瑪刀結構特性和臨床應用效果報道如下:
1 資料與方法
1.1一般資料
選擇2013年10月~2014年10月于我院接受圖像引導體部伽瑪刀治療的患者60例。患者均經病理學、CT、MRI或PET/CT等影像學確診。其中男36例,女24例;年齡21~82歲,中位年齡49歲;肺癌32例,肝癌11例,腹膜轉移瘤8例,盆腔腫瘤9例。60例患者功能狀態評分(KPS)≥70分,且患者本人和家屬均知情同意、自愿參加并配合治療。患者全程采用圖像引導體部伽瑪刀治療,圖像引導拍片后圖像能較為清晰的與經治療計劃軟件進行圖像處理定位初始圖像后生成的數字重組透視圖像配準。
1.2方法
我院所用圖像引導體部伽瑪刀系統設備為深圳奧沃國際公司生產的OUR-QGD型三維立體定向伽瑪射線體部伽瑪刀系統,在此基礎上加裝激光定位系統和江蘇瑞爾醫療科技有限公司的IGPS-V型圖像引導系統,實現圖像引導體部伽瑪刀治療模式。
1.2.1 CT模擬定位使用Philips Brilliance big ball CT行體部伽瑪刀治療定位。患者均采取仰臥位,采用真空負壓袋塑形固定體位,雙臂根據病灶位置情況放置于身體兩側或自然上舉置于頭頂,囑咐患者全身放松、平靜呼吸。利用激光定位系統根據病灶大概位置在患者體表找出合適位置粘貼體表配準標記點。并用皮膚墨水在患者體表、真空負壓袋上做好標記,囑咐患者保護好身體上的標記線不要清洗,以備重復擺位時使用。并根據需要口服顯影劑和(或)高壓注射造影劑。然后用螺旋CT 2 mm薄層掃描,獲得定位CT圖像,并通過網絡系統將定位CT圖像資料傳輸至圖像引導伽瑪刀治療計劃系統(TPS)。
1.2.2治療計劃設計依據定位CT圖像資料,制訂三維立體定位治療計劃。由負責治療方案的醫師勾畫腫瘤靶區、臨床靶區和計劃靶區,根據病灶部位、腫瘤體積給出合適的總治療劑量和單次分割劑量。腫瘤靶區等劑量曲線一般范圍在50%~70%,治療在腫瘤靶區基礎上向外擴1~1.5 cm。物理師依據醫師制定的治療方案對腫瘤靶區進行優化劑量分布,使得等劑量曲線包繞95%臨床靶區體積,保護靶區周圍重要敏感器官在放射耐受劑量范圍以下,治療醫師和物理師通過劑量-體積直方圖共同進行評估。肺癌單次治療劑量為350~500 cGy/次,治療次數9~12次;肝癌單次治療劑量300~450 cGy/次,治療次數10~11次;腹膜后淋巴結和盆腔腫瘤單次治療劑量300~420 cGy/次,治療次數10~11次。連續治療或先隔日觀察3次后再連續治療,總劑量在12~21 d完成。治療計劃經由物理師、主治醫師雙方審核簽字后傳輸至圖像引導體部伽瑪刀治療工作站;再由主治醫師與治療技師進行首次交接確認簽字后開始進入治療階段。
1.2.3治療擺位與圖像配準首先從伽瑪刀控制系統調取治療患者治療計劃,進入激光對準界面,然后治療技師進入機房擺位。首次治療擺位由一名醫師和兩名治療技師完成,并交接注意事項。后續治療擺位由2名治療技師依據患者定位時做的體表標記線、負壓袋上標記線,采用激光燈分別由X、Y、Z三個方向調整床位和患者體位,使激光定位線與患者初始定位的體表標記線、負壓袋上標記線完全吻合,囑咐患者全身放松、平靜呼吸,不要變換體位狀態。并告知患者治療室內對講系統和應急防護安全開關的使用方法,如有不適立即通過對講系統及時告知醫務人員。治療技師完成擺位后退出治療室,點擊床位定位按鈕、啟動IGRT,在IGRT控制臺打開圖像引導系統,進行X射線立體平面拍片,根據治療計劃軟件經過CT圖像處理生成的數字重組透視圖像和選擇的體內感興趣區(ROI)進行圖像引導拍片,獲得二維-三維(2D-3D)圖像,把選擇的此組配準位置圖像與患者初始CT定位圖像經治療計劃圖像處理后獲得的數字重組透視圖像進行配準,要求配準誤差≤1 mm。完成配準后,再次核對患者姓名、性別、年齡、治療部位、體位、處方劑量、醫囑要求等信息,核對無誤后打開伽瑪刀治療控制臺治療開關,對靶點進行順序治療。治療中通過監視屏幕觀察患者治療中狀況,并通過對講系統與患者進行實時溝通,及時發現患者不適或機器運行狀況,出現問題及時妥善解決。治療前、中、后要與患者進行深度溝通,提高患者對治療設備和醫務人員的信任度,消除顧慮和緊張情緒,保證治療順利、安全完成。
1.2.4測量擺位誤差并糾正為了獲得有效的驗證數據,經過與患者商談后取得患者同意,在正式進行圖像引導體部伽瑪刀治療前,對2例典型患者首次擺位用重復定位尺和激光定位圖像引導兩種方法分別進行擺位,并記錄兩組數據。在用兩種擺位方法首次擺位后和擺位誤差糾正后進行3次IGRT圖像引導掃描,得出2D-3D圖像與計劃CT圖像處理初始定位圖像后生成的數字重組透視圖像進行配準,圖像配準先用自動配準,但是如果出現自動配準失敗或因種種原因干擾導致數字重組透視圖像不夠清晰的情況時要結合手動進行配準而縮小擺位誤差,IGRT配準處理系統計算出靶區的X、Y、Z三維方向的位置偏移數據。圖像引導伽瑪刀的操作系統在治療前進行床位定位,目的是通過移動治療床來達到患者位置與初始定位位置相吻合,從而達到配準要求。床位定位和圖像引導掃描可交叉多次重復,對配準后的數據進行校正、驗證,使剩余擺位誤差值最終達到要求(≤1mm)。之后治療技師以初始CT定位圖像處理生成的數字重組透視圖像為依據觀察配準效果,并結合手動配準進行微調。并在治療記錄單中記錄擺位誤差與圖像引導糾正后誤差數據。2例患者全程治療累計擺位20次,掃描60次。掃描誤差數值<1mm方可開始治療。
1.3觀察指標
近期療效在圖像引導伽瑪刀治療后3個月按照WHO標準客觀評分[3],正常組織急性反應按照RTOG標準評價[4]。總有效=顯效+有效。
1.4統計學方法
采用統計軟件SPSS 15.0對數據進行分析,正態分布計量資料以均數±標準差(±s)表示,兩組間比較采用t檢驗;計數資料以率表示,采用χ2檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1近期療效觀察
治療12周,60例患者按照WHO標準客觀評分[3]進行療效評價,其中顯效42例,有效9例,無變化3例,進展3例,總有效率為85%。
2.2 2例典型患者重復定位尺擺位和圖像引導擺位誤差比較
結果顯示:圖像引導伽瑪刀擺位誤差明顯優于重復定位尺伽瑪刀擺位方法的擺位誤差,差異有統計學意義(P<0.05)。見表1。
表1 重復定位尺擺位X、Y、Z軸誤差和圖像引導糾正后誤差比較(mm,±s)
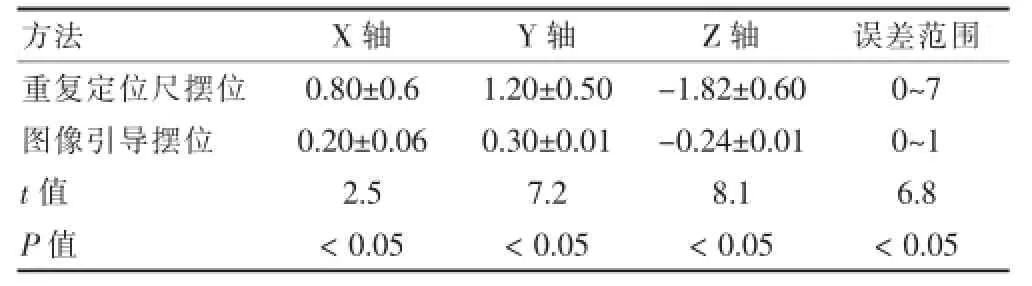
表1 重復定位尺擺位X、Y、Z軸誤差和圖像引導糾正后誤差比較(mm,±s)
?
2.3急性放射不良反應
急性放射性肺炎7例、急性食管炎4例、骨髓抑制9例、急性放射性腸炎3例。以上急性放射副作用按照RTOG標準[3]均屬于1~2級,未見3級不良反應。
3 討論
現代放射治療已經進入精確放療時代,要求放射治療要有更高的準確性[5],影像引導放療是精確放射治療的一種實現方式,而圖像匹配是影像引導的核心技術[6]。近年來,隨著科學技術的進步,各種放射治療新設備、新技術不斷被開發出來,解決的焦點問題是精度、準確性、單次高劑量、降低腫瘤靶區周圍正常組織受照劑量。體部伽瑪刀是在這樣的指導前提下應運而生,并經過十多年的臨床實踐取得較好成果。深圳奧沃國際公司生產的OUR-QGD型三維立體定向伽瑪射線體部伽瑪刀治療系統是運用多源動態旋轉聚焦技術,伽瑪射線能夠高度聚焦在指定治療靶區,使得靶區等劑量曲線非常陡峭。從而可以達到腫瘤靶區局部高劑量、降低周圍正常組織劑量、保護周圍重要臟器的治療目的。與普通放療比較其大大提高了單次劑量,減少了分割次數,縮短了總的療程。
體部伽瑪刀的多次治療重復擺位是利用伽瑪刀重復定位尺與治療床、患者構成立體坐標系框架,患者每次治療的重復擺位依據是患者體表標記在X、Y、Z方向的初始定位初始定位坐標值參數(X、Y、Z)和重復定位尺(N形尺)在定位床上的初始定位數據,通過擺位技術員擺位時進行數據核對來實現重復擺位的。這種方法不能監測到腫瘤在患者體內位置的移位,即不能做到精確校正腫瘤在放射治療時的等中心位置的誤差。體部伽瑪刀治療的這種傳統的體部框架定位方式精度的不確定性很大,患者在接受治療的重復擺位過程中其重復擺位框架所能夠解決的僅僅是靜止靶區的劑量適形問題,難以嚴格控制定位精度和保證腫瘤靶區、臨床靶區和計劃靶區的治療處方劑量的準確性,這些問題在很大程度上限制了體部伽瑪刀治療的適應癥范圍,也給臨床醫師和物理師對治療方案的制定和治療劑量的優化造成了諸多困難。
腫瘤患者在接受普通體部伽瑪刀治療的過程中受到腫瘤的治療位置和腫瘤的形狀會因生理性臟器的運動隨時發生變化、治療技術的擺位誤差等影響,導致普通體部伽瑪刀治療精確性明顯不足,治療靶區劑量及腫瘤局部控制率也不夠理想;并且因為上述原因發生放射不良反應的概率較大。導致上述誤差的因素主要是系統誤差和隨機誤差。其中系統誤差主要由設備本身導致,而隨機誤差則和患者及操作人員技術密切關聯[7-10]。引起這些變化的原因包括[11-12]:①分次間的擺位誤差,人體并非剛性結構,不同身體部位、臟器間存在相對運動能力,即使應用體位固定裝置(負壓袋、腹部束帶)來固定體位,也不可能在每次擺位時做到與計劃體位完全一致,存在數毫米甚至更大的擺位誤差;整個治療過程中患者體重的減輕或增加、腫瘤的退縮、胸、腹水的增、減等情況同樣會帶來擺位誤差;②腫瘤與周圍正常器官的移位和變形,包括分次間靶區移位和分次內靶區運動及變形。③機器設備的不穩定性造成的誤差,治療機和激光燈的定位誤差;治療中治療床的升降、左右移動的機械誤差、負壓袋漏氣、變形導致患者體位移動等;④患者身上的體表標記線太寬或不夠清晰、體表皮膚松弛也會帶來誤差,技術人員的擺位不當,使患者治療體位存在隨機誤差。由于伽瑪刀等劑量曲線在靶區和正常組織之間形成的陡峭的劑量梯度變化,一旦靶區及周圍正常組織位置發生變化,則不可避免地會引起劑量學的改變。因此,如何保證和控制伽瑪刀治療的準確性仍是醫生、技師及物理師共同關注的問題。
體部伽瑪刀作為精確放療的一種立體定向放射治療設備,要能實施符合立體定向的精確要求和規范的治療,精確的圖像引導定位是必不可缺的。圖像引導定位、配準替代或結合體部框架定位,是大部分體部伽瑪刀放療醫生和物理師長期以來所期待的[13-14]。為了解決原有普通體部伽瑪刀治療中靶區位置受多種因素影響,而導致治療中腫瘤位置發生位置變化不確定等問題,除了不斷提高治療技師擺位技術減少人為誤差外,還必須嚴格按照規定驗證維修機械誤差,并同時將影像設備與普通體部伽瑪刀設備相結合,是國產體部伽瑪刀技術發展和保障伽瑪刀治療質量的一次質的飛躍。通過這一技術不僅僅解決了這些棘手問題,而且這也必將成為推動體部伽瑪刀治療技術進一步推廣使用、得到廣泛肯定的技術指標和理論依據。
圖像引導體部伽瑪刀治療技術的實現途徑是將千伏級X射線成像設備集成在體部伽瑪刀設備上,運用激光燈與治療床上標記點、負壓固定袋上標記點及患者體表初始定位標記點構成人工重復擺位的依據,替換原有的體部伽瑪刀定位框架和重復定位尺(N形尺),減少X、Y、Z方向人為的操作誤差。IGPS放置于伽瑪刀機身外部前側,兩個X射線管固定于地面,形成對稱的雙投影交角成像幾何。治療技師每次治療前,完成治療擺位后經由治療控制臺進行床位定位,IGPS在定位中心點對治療靶區進行掃描定位,通過數據優化計算出剩余誤差并通過移動治療床完成治療靶區的圖像配準。開始治療前再運用圖像引導系統拍攝圖像與治療計劃對體部伽瑪刀CT初始定位圖像進行圖像處理后形成的數字重組透視圖像配準。每次治療前或(和)治療中采集相關的影像學信息來確定治療靶區和重要器官的結構、位置是否與治療前計劃的靶區一致[15],從而引導此次及后繼的治療。旨在治療前或在治療中對因各種原因而造成的擺位誤差進行及時的校正和配準,保證將處方劑量準確、無誤地給予到由醫師、物理師共同確定的腫瘤治療區域,從而真正達到精確治療的目的。X射線立體平面成像是一種很有效的IGPS定位技術,具有以下特點[13]:①精準度高;②拍片成像使用的劑量低;③重復定位時間短;④能進行治療前患者定位驗證和治療中靶區運動情況跟蹤。基于上述特點其與體部伽瑪刀結合成為嚴格控制靶區精準度的重要手段。普通體部伽瑪刀的重復擺位模式最直接的缺點是不能及時發現種種原因導致的體表標記點、體內病灶的位移而造成的靶區誤差,而圖像引導體部伽瑪刀通過影像學的圖像配準恰恰糾正了這個誤差。本研究通過對我院60例患者的臨床應用實踐,并通過對2例典型病例首次擺位用重復定位尺和激光定位圖像引導兩種方法分別進行擺位,發現圖像引導體部伽瑪刀治療的擺位誤差遠遠低于普通體部伽瑪刀的擺位誤差(P<0.05)。但是由于此種方法用于臨床的時間較短,病例數積累的較少,還有待于進一步的驗證。
[1]孫文澤,宋麗萍,馬軍,等.圖像引導下放射治療中心型非小細胞肺癌的配準范圍、配準方式及靶區外放的研究[J].中南大學學報:醫學版,2013,38(2):133.
[2]Xing L,Thorndyke B,Schreibmann E,et al.Overview of image-guided radiation therapy[J].Medical Dosimetry,2006,31(2):91-112.
[3]孫燕.內科腫瘤學[M].北京:人民衛生出版社,2001:640-673,994-997.
[4]Cox JD,Stetz J,Pajak TF.Toxicity criteria of the Radiation Therapy Oncology Group(RTOG)and the European Organization for Research and Treatment of Cancer(EORTC)[J].Int JRadiat Oncol Biol PhyS,1995,31:1341-1346.
[5]刑立剛,于金明.PET/CT功能影像引導非小細胞肺癌精確放療研究進展[J].實用腫瘤學雜志,2012,26(1):1-5.
[6]EmilianoS,Patrick D,Richard J,etal.Patient-specific threedimensional concomitant dose from cone beam computed tomography exposure in image-guided radiotherapy[J].Int JRadiat Oncol Biol Phys,2012,83(1):419-426.
[7]秦永輝,趙春櫻,王若崢,等.圖像引導調強放療在食管癌治療的應用[J].新疆醫科大學學報,2012,35(3):282-287.
[8]崔恩萍,汪志,唐虹,等.應用模擬定位機測量食管癌調強放療中的擺位誤差[J].醫療裝備,2012,25(2):10-12.
[9]劉凱,秦永輝,王多明,等.胸段食管癌圖像調強放療的擺位誤差和近期療效評價[J].新疆醫科大學學報,2013,(1):21-25.
[10]王風琴.千伏級CBRT在食管癌調強放療擺位中的應用[J].浙江臨床醫學,2012,(9):1039-1040.
[11]Rietzel E,Pan T,Chen GT,etal.Four-dimensional computed tomography:image formation and clinicalprotocol[J]. Med Phys,2005,32(4):874-889.
[12]戴建榮,胡逸民.圖像引導放療的實現方式[J].中華放射腫瘤學雜志,2006,15(2):132-135.
[13]付東山,黎維娟.體部伽瑪刀圖像引導技術的發展[J].中國醫療設備雜志,2014,29(9):6.
[14]閆云宇,翟福山,王安峰,等.圖像引導下大分割放療對局部晚期非小細胞肺癌患者血清腫瘤標志物及轉移侵襲相關指標的影響研究[J].中國醫藥導報,2013,10(32):42-44,47.
[15]Mackie TR,Kapatoes J,Ruchala K,et al.Image guidance for percise conformal radiotherapy[J].Int JRadiat Oncol Biol Phys,2003,56(1):89-105.
Clinical app lication effect of image-guided body gamm a knife treatment
QIWenjie KANG Jingbo ZHU Qi▲ZHANG Qian LIUWei
Tumor Diagnosis and Treatment Center,Navy General Hospital,Beijing 100048,China
Objective To expound the clinical application effect of the image-guided body gamma knife.M ethods From October 2013 to October 2014,in Navy General Hospital,60 patients with different types and locations tumor were selected,the treatment effect after treated 12 weeks of them was observed.2 typical cases chosen from them were given repeated positioning ruler and laser positioning image guided placement respectively,and the errors caused by two kinds of placementmethod were compared.Results After the treatment 12 weeks,42 caseswere excellent,9 cases were effective,3 cases were no-change,3 caseswere advance,total effective rate was 85%.Errors of laser positioning image guided placement were better than that of positioning ruler guided placement,the differences were statistically significant(P<0.05).Conclusion Image-guided body gamma knife treatment can improved the precision of the treatment based on the accurate positioning with original gamma knife framework,and reduce the positioning error and the error caused by targetmotion.It is perfect combination with whole-body gamma knife treatment techniques and Image guided system,a qualitative leap on the accuracy of body gamma knife treatment,a new mode of gamma knife treatment,and it isworth to popularize and applicated widely.
Image guided;Body gamma knife;Positioning framework;Positioning error
R730.55
A
1673-7210(2015)05(a)-0132-04
2015-01-07本文編輯:蘇暢)

