深圳市頭孢曲松低敏淋病奈瑟菌株耐藥基因分析
張麗君 王峰 莫俊鑾 彭毅
深圳市頭孢曲松低敏淋病奈瑟菌株耐藥基因分析
張麗君 王峰 莫俊鑾 彭毅
目的 了解penA、ponA、porB和mtrR突變與深圳市淋球菌對頭孢曲松敏感性降低的相關性。方法 收集2009—2011年深圳市淋球菌臨床分離株296株,采用瓊脂稀釋法篩選出頭孢曲松低敏株[MIC(0.06~0.50)μg/ml]53株。將頭孢曲松低敏菌株以及按照1∶1抽樣原則隨機抽取的53株高敏菌株,共計106株淋球菌作為試驗菌株。對所有菌株penA、ponA、porB和mtrR基因進行PCR擴增以及DNA測序分析。結果1株淋球菌的青霉素結合蛋白2(penicillin-binding protein 2,PBP2,由penA基因編碼)具有鑲嵌樣結構(MIC 0.125 0 μg/ml),對剩余105株淋球菌PBP2的氨基酸序列分析,共得到16個不同的氨基酸模式。模式ⅩⅢ、ⅩⅧ、ⅩⅩⅩⅧ對應的頭孢曲松MIC值相對較高(MIC50均為0.062 5 μg/ml),而模式Ⅱ的頭孢曲松MIC值相對較低(MIC50為0.008 0 μg/ml)。mtrR、porB以及ponA突變在頭孢曲松低敏組和高敏組中的發生率,差異無統計學意義(均P>0.05)。結論 PBP2鑲嵌樣結構可能不是深圳市淋球菌對頭孢曲松敏感性降低的主要原因,非鑲嵌樣PBP2 500~580位多個氨基酸突變產生的不同氨基酸模式聯合mtrR、porB以及ponA突變在誘導淋球菌對頭孢曲松敏感性降低中可能有意義。
淋病奈瑟球菌;頭孢曲松;DNA突變分析;微生物敏感性試驗;抗藥性,微生物
淋病是我國主要的性傳播疾病,據統計,2012年全國淋病發病達91853例,其中廣東省以16.77/10萬的發病率在全國31個省自治區直轄市中位居第三[1]。頭孢曲松作為我國治療淋病的首選藥物之一,臨床雖少見治療失敗的病例,但頭孢曲松低敏淋球菌菌株的出現,應引起重視。頭孢曲松屬于β內酰胺類抗生素,具有良好的親水性,易透過細菌外膜的膜孔,作用于青霉素結合蛋白(penicillin-binding protein,PBP)靶位。淋球菌對頭孢曲松耐藥主要由染色體介導,多數研究主要關注3個方面:①抗生素作用靶位點的改變,主要是penA基因編碼的PBP2以及ponA基因編碼的PBP1改變,影響抗生素與淋球菌的結合產生耐藥;②porB基因編碼細菌細胞膜孔蛋白的改變,導致膜通透性降低產生耐藥;③mtrR外排系統的改變,導致細菌外排作用增強產生耐藥。我們對2009—2011年淋球菌臨床分離株penA、ponA、porB和mtrR基因進行分析,試圖了解本市淋球菌對頭孢曲松敏感性降低的分子機制。
材料和方法
1.菌株來源:所有淋球菌菌株均來自2009—2011年深圳市淋球菌耐藥監測項目。從全市5個區的34家規范化性病實驗室中抽取16家作為監測點收集樣本,收集時間為每年的7~10月份,收集對象為門診就診的疑似淋病患者。樣本經革蘭染色涂片鏡檢、Thayer Martin(TM)培養基分離培養純化、氧化酶試驗、糖發酵試驗鑒定后洗脫于脫脂牛奶中,-70℃低溫保存。
2.藥敏試驗:所有菌株按照CLSI標準[2]經瓊脂稀釋法測定頭孢曲松的最小抑菌濃度(MIC)。每批試驗均由標準菌株(WHO G、WHO L、WHO J、ATCC 49226)作質控。
3.菌株篩選:按照WHO西太平洋區耐藥監測指南的解釋標準[3],篩選頭孢曲松低敏[MIC(0.06~0.50)μg/ml]淋球菌菌株,按照1∶1抽樣原則隨機抽取(SPSS 17.0軟件)等量高敏(MIC≤0.03 μg/ml)淋球菌菌株,作為試驗菌株進行penA、ponA、porB和mtrR基因分析。
4.DNA提取、PCR擴增及測序:采用QIAamp? DNA Mini Kit試劑盒進行DNA提取;由上海英濰捷基貿易有限公司合成引物分別對penA(2 040 bp)[4]、ponA(205 bp)[5]、porB(754 bp)[6]和mtrR(401 bp)[5]基因進行PCR擴增,引物序列見表1。擴增產物經瓊脂糖凝膠電泳鑒定后送上海英濰捷基貿易有限公司測序。
5.penA、ponA、porB和mtrR氨基酸序列分析:利用MEGA 4軟件將序列拼接后與標準株FA 1090的相關基因進行比對分析,分析可能存在的突變位點;同時將PBP2的氨基酸序列與青霉素敏感的淋病奈瑟菌(LM 306)、腦膜炎奈瑟菌(MC 58)、多糖奈瑟菌(NCTC 11858)、灰色奈瑟菌(NCTC 10294)、深黃/干燥奈瑟菌(1654/1659)、灰質奈瑟菌(NCTC8263)的PBP2比較,分析可能存在的鑲嵌樣結構;利用Cn3D 4.1軟件以PBP2晶體結構為基礎,分析氨基酸突變[4-6]。
6.統計學分析:采用SPSS17.0軟件對實驗數據進行分析。對突變位點與淋球菌對頭孢曲松敏感性降低的相關性采用χ2檢驗進行分析,α=0.05。
結果
1.藥敏試驗結果:共收集296株淋球菌,未發現頭孢曲松耐藥菌株,頭孢曲松低敏菌株有53株,低敏率為17.91%(53/296)。
2.PBP2氨基酸模式分析:106株淋球菌臨床分離株的PBP2氨基酸序列分析,共得到17個不同模式。其中,氨基酸模式X具有鑲嵌樣結構僅包含1株菌株,該株菌的頭孢曲松MIC值為0.125 μg/ml。剩余16個非鑲嵌樣結構模式中,模式ⅩⅧ數量最多為23株,其次為模式ⅩⅢ22株,模式ⅩⅩⅩⅧ13株,模式Ⅱ12株,模式ⅩⅪ10株。總的來說,包含菌株數量較多的氨基酸模式對應的頭孢曲松MIC值分布具有多樣性,其中模式ⅩⅢ、ⅩⅧ、ⅩⅩⅩⅧ對應的頭孢曲松MIC值相對較高(MIC50均為0.062 μg/ml),而模式Ⅱ所含菌株對應的頭孢曲松MIC值相對較低(MIC50為0.008 μg/ml)。見表2。
3.PBP2突變位點分析:具有鑲嵌樣結構的氨基酸模式X與LM 306(基因庫編號M32091)相比,共有59個氨基酸位點發生改變,大部分位點位于青霉素轉肽酶結構域(81.4%,48/59),其改變了氨基酸片段與多糖奈瑟菌、灰色奈瑟菌、深黃/干燥奈瑟菌PBP2重組后的特異性片段的一致性高達88.1%(52/59)。除氨基酸模式X外,其余16個模式共發現15位氨基酸位點的改變,分別是插入突變345D、 573N,置換突變 A501,F504,A510,A516,H541,G542,V548,P551,P552,K555,I556,I566,A574,其中345 D以及A510V、A516G的發生率均為100%,大部分的氨基酸突變存在于PBP2轉肽酶的500~557位氨基酸。MIC值相對較高的三個模式均存在501位點的氨基酸突變,而MIC值相對較低的模式Ⅱ不存在。具有A501突變的78株淋球菌菌株頭孢曲松MIC值的分布為(0.002~0.500)μg/ml,隨MIC值的增加,其置換率也在上升,3株頭孢曲松MIC值為0.5 μg/ml的菌株均具有A501和P551突變。A501突變在頭孢曲松低敏株中(82.7%,43/52)和高敏株中(66.0%,35/53)的發生率差異無統計學意義(χ2=3.811,P>0.05)。而具有H541突變的13株菌頭孢曲松MIC值的分布為(0.002~0.250)μg/ml,隨MIC值的增加,其突變率在降低,該突變在頭孢曲松低敏株中(5.8%,3/52)和高敏株中(18.9%,10/53)的發生率差異有統計學意義(χ2=4.151,P<0.05)。其他突變位點未觀察到類似的趨勢變化。見表3。
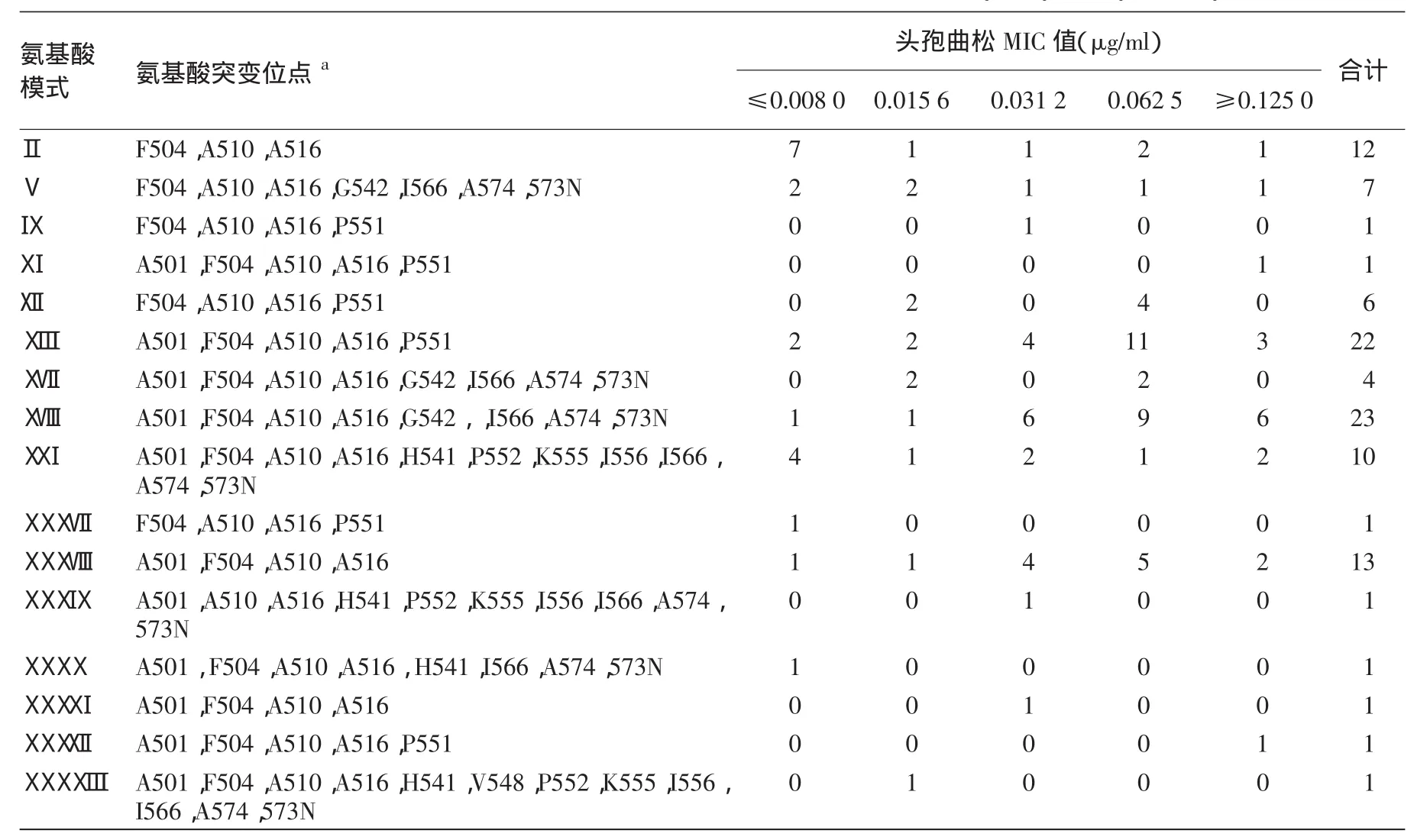
表2 不同PBP2氨基酸模式菌株對應的頭孢曲松最小抑菌濃度(MIC)分布(菌株數)
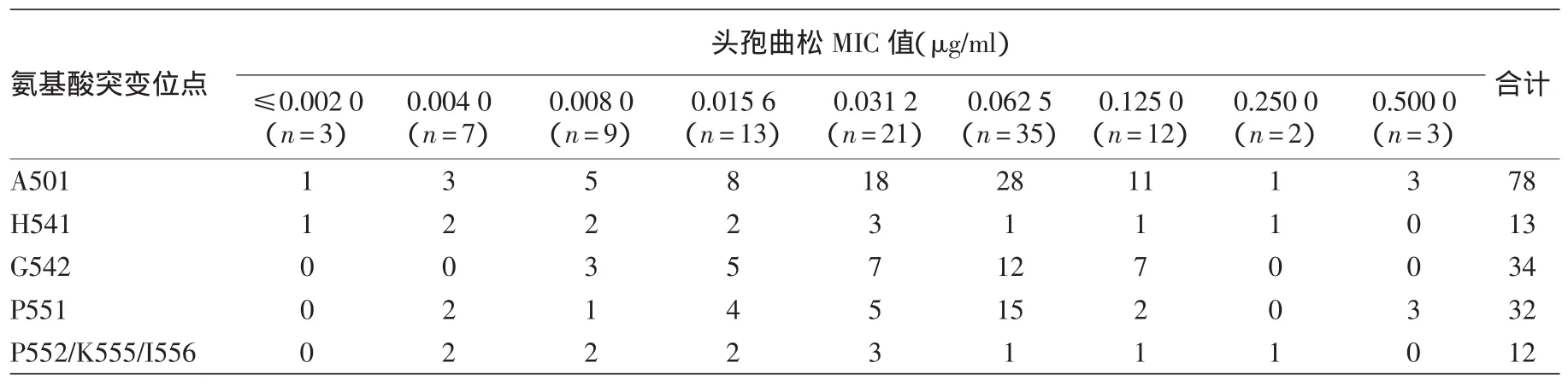
表3 含不同氨基酸突變位點菌株對應的頭孢曲松最小抑菌濃度(MIC)分布(菌株數)
Cn3D 4.1軟件對PBP2的晶體結構進行分析,其中A501突變靠近β內酰胺類藥物結合區,P551、G542以及H541突變則距離β內酰胺類藥物結合區較遠。
4.mtrR、porB和ponA突變分析:106株菌的mtrR、porB和ponA突變在頭孢曲松低敏株與高敏株中未見明顯差異。除1株高敏株外,105株菌ponA基因編碼的PBP1均存在L421P突變。99株菌porB基因編碼孔蛋白的101和102位點存在非同義置換,在低敏株中,以G101K和A102D最多見(31/53,58.5%),其次為G101D(14/53,8.5%),G101K和A102G(3/53,11.3%),G101K和A102N(3/53,11.3%)。高敏株中分別為G101K和A102D(26/53,58.5%),G101D(16/53,8.5%),G101K和A102G(5/53,11.3%),G101K和A102N(1/53,11.3%)。101和102位點的突變模式在低敏株與高敏株間的發生率差異無統計學意義(均P>0.05)。
共94株菌在mtrR啟動子區的反向重復序列中存在單核苷酸(A)缺失突變,其中低敏株49株(49/ 53,92.5%),高敏株45株(45/53,84.9%)。54株菌在mtrR編碼區具有A39T或者G45D突變,其中低敏株 24株(24/53,45.3%),高敏株 30株(30/53,56.6%)。兩處突變在低敏株和高敏株中發生率差異無統計學意義(均P>0.05)。
討論
penA、mtrR、porB、ponA 4個基因中,關注最多的是penA基因改變引起的PBP2氨基酸序列的改變。PBP2由penA基因(全長1 752 bp)編碼,其單體由兩個決定域組成,PBP二聚化決定域(71~221殘基)和PBP轉肽酶決定域(263~557殘基)[7]。研究認為PBP2轉肽酶決定域的鑲嵌樣結構[8-9]參與誘導淋球菌對頭孢曲松敏感性的降低以及對頭孢曲松的高度耐藥。但是,我們并未得出相似結論,106株淋球菌PBP2分析僅發現1株菌具有鑲嵌樣結構(MIC為0.125 μg/ml),該菌的鑲嵌樣結構是由與多糖奈瑟菌、灰色奈瑟菌、深黃/干燥奈瑟菌以及淺黃奈瑟菌相似的片段組成,其氨基酸模式與日本和澳大利亞之前報道[10-11]的對頭孢曲松低敏的菌株的鑲嵌樣結構模式X的序列一致,并不含有345位點的氨基酸插入,表明其結構并不是由氨基酸插入或置換引起,而由鄰近物種淺黃奈瑟菌、灰色奈瑟菌等對青霉素天然耐藥的共生細菌將耐藥基因部分或全部水平傳遞給病原菌所形成。由于本次研究僅發現1株菌具有鑲嵌樣結構,因此我們推測鑲嵌樣結構并不是導致深圳市淋球菌對頭孢曲松敏感性下降的主要原因[12],PBP2非鑲嵌樣結構的改變可能具有更重要的意義。值得一提的是,對該菌株的多抗原序列分型(N.gonorrhoeae-multi antigen sequence typing,NG-MAST)結果顯示該型別(ST 5308)被香港報道過[13],考慮到深圳與香港毗鄰,人員交往密切以及該株菌對頭孢曲松較高的MIC值,也應引起我們的重視。
對剩余105株淋球菌非鑲嵌樣結構的PBP2進行分析,共發現16個不同的氨基酸模式,包括9個已被報道[7-8]的和7個新發現的,表明深圳市頭孢曲松低敏淋球菌菌株的PBP2蛋白存在較高的多樣性,這可能與菌株本身具有的高多態性有關。大部分包含菌株數量較多的氨基酸模式對應頭孢曲松的MIC值范圍較廣,僅少量模式與頭孢曲松的MIC值相關。主要的6個氨基酸模式ⅩⅧ、ⅩⅢ、ⅩⅩⅩⅧ、ⅩⅪ、Ⅱ、Ⅴ中模式ⅩⅧ、ⅩⅢ對應的頭孢曲松MIC值相對較高,而模式Ⅱ的頭孢曲松MIC值相對較低,與文獻報道相一致[5,10,14]。值得注意的是模式ⅩⅩⅩⅧ為本次研究新發現,對應的頭孢曲松MIC值也相對較高。
我們對PBP2相關突變位點(A501V、P551S、G542S及345)以及mtrR、porB、ponA進行分析,發現大部分頭孢曲松低敏淋球菌菌株的這些基因均存在與文獻報道一致的突變位點[5,14-16],其中A501V位點的突變率隨著菌株MIC值的增加呈上升趨勢,在3株頭孢曲松MIC值為0.5 μg/ml的菌株中的突變率為100%,且在模式II中不存在。但是該突變位點以及其他的突變位點在兩組菌株中所占的比例,差異無統計學意義,因為這些突變位點同時也存在余本研究的高敏株中。我們推測原因可能有以下方面:①WHO西太平洋區耐藥監測指南在CLSI標準的基礎上增加了淋球菌對頭孢曲松敏感性降低折點的判定,即將MIC為(0.06~0.50)μg/ml的淋球菌判定為頭孢曲松低敏菌株,目前本地區淋球菌耐藥監測顯示大部分的菌株對頭孢曲松的MIC值都集中在0.06 μg/ml折點附近,這種菌株MIC值的非均勻分布,可能導致分析數據具有一定的偏倚;②mtrR基因編碼的是轉錄阻遏蛋白,其作用是使細菌外排能力增強,而porB基因編碼的是淋球菌的外膜孔蛋白,兩者均介導的是細菌的非特異性耐藥機制,因此,這兩個基因的突變可能不是導致淋球菌對頭孢曲松敏感性降低的關鍵因素;③本研究我們只對mtrR、porB、ponA三種基因的部分序列以及penA基因進行了測序分析,可能存在其他位點的突變或其他不確定的耐藥基因參與了淋球菌對頭孢曲松的敏感性降低。
綜上所述,PBP2鑲嵌樣結構并不是導致深圳地區淋球菌對頭孢曲松敏感性降低的主要原因,PBP2模式ⅩⅧ、ⅩⅢ、ⅩⅩⅩⅧ包含菌株對應的頭孢曲松的MIC值較高,而模式Ⅱ的頭孢曲松MIC值相對較低,推測非鑲嵌樣PBP2 500~580位多個特定位點氨基酸突變的聯合作用可能與淋球菌對頭孢曲松敏感性的降低具有一定的相關性,還需要進一步了解深圳地區淋病奈瑟菌對頭孢曲松敏感性降低的分子機制。
[1]國家衛生和計劃生育委員會.2013中國衛生統計年鑒[M/ OL].北京:中國協和醫科大學出版社,2014[2015-04-10].http:// www.moh.gov.cn/htmlfiles/zwgkzt/ptjnj/year2013/index2013.html.
[2]Clinical and Laboratory Standards Institute(CLSI).Performance Standards for Antimicrobial Susceptibility Testing:Nineteenth InformationalSupplement.CLSIdocumentM100-S19[S]. Villanova,PA,USA:CLSI,2009.
[3]World Health Organization(WHO).Sensitivity testing of Neisseria gonorrhoeae:Methodologies for use by participants in the WHO Western Pacific regional surveillance programme[C]//WHO. WHO/WPRO Regional Antimicrobial Surevillance Working Group Meeting Proceedings,Manila,1992.Manila,Philippines:WHO Regional Office for the Western Pacific,1992:33-34.
[4]Osaka K,Takakura T,Narukawa K,et al.Analysis of amino acid sequences of penicillin-binding protein 2 in clinical isolates of Neisseria gonorrhoeae with reduced susceptibility to cefixime and ceftriaxone[J].J Infect Chemother,2008,14(3):195-203.
[5]Lee SG,Lee H,Jeong SH,et al.Various penA mutations together with mtrR,porB and ponA mutations in Neisseria gonorrhoeae isolates with reduced susceptibility to cefixime or ceftriaxone[J].J Antimicrob Chemother,2010,65(4):669-675.
[6]Tanaka M,Nakayama H,Huruya K,et al.Analysis of mutations within multiple genes associated with resistance in a clinical isolate of Neisseria gonorrhoeae with reduced ceftriaxone susceptibility that shows a multidrug-resistant phenotype[J].Int J Antimicrob Agents,2006,27(1):20-26.
[7]Spratt BG.Hybrid penicillin-binding proteins in penicillinresistant strains of Neisseria gonorrhoeae[J].Nature,1988,332(6160):173-176.
[8]Unemo M,Golparian D,Nicholas R,et al.High-level cefiximeand ceftriaxone-resistant Neisseria gonorrhoeae in France:novel penA mosaic allele in a successful international clone causes treatment failure[J].Antimicrob Agents Chemother,2012,56(3): 1273-1280.
[9]Tomberg J,Unemo M,Ohnishi M,et al.Identification of amino acidsconferring high-levelresistance to expanded-spectrum cephalosporins in the penA gene from Neisseria gonorrhoeae strain H041[J].Antimicrob Agents Chemother,2013,57(7):3029-3036.
[10]Whiley DM,Limnios EA,Ray S,et al.Diversity of penA alterations and subtypes in Neisseria gonorrhoeae strains from Sydney, Australia,that are less susceptible to ceftriaxone[J].Antimicrob Agents Chemother,2007,51(9):3111-3116.
[11]Ito M,Deguchi T,Mizutani KS,et al.Emergence and spread of Neisseriagonorrhoeae clinicalisolatesharboringmosaic-like structure of penicillin-binding protein 2 in Central Japan[J]. Antimicrob Agents Chemother,2005,49(1):137-143.
[12]蔣法興,其木格,錢革,等.頭孢曲松低敏的淋球菌中青霉素結合蛋白2氨基酸替代或插入模式研究[J].中華皮膚科雜志, 2008,41(7):451-454.
[13]Lo JY,Ho KM,Lo AC.Surveillance of gonococcal antimicrobial susceptibility resulting in early detection of emerging resistance[J]. J Antimicrob Chemother,2012,67(6):1422-1426.
[14]Liao M,Gu WM,Yang Y,et al.Analysis of mutations in multiple loci of Neisseria gonorrhoeae isolates reveals effects of PIB,PBP2 and MtrR on reduced susceptibility to ceftriaxone[J].J Antimicrob Chemother,2011,66(5):1016-1023.
[15]Whiley DM,Goire N,Lambert SB,et al.Reduced susceptibility to ceftriaxone in Neisseria gonorrhoeae is associated with mutations G542S,P551S and P551L in the gonococcal penicillin-binding protein 2[J].J Antimicrob Chemother,2010,65(8):1615-1618.
[16]賴維,龔子鑒,黃朝偉,等.抑制性消減雜交結合基因芯片研究淋球菌耐頭孢曲松的分子機制[J].中華皮膚科雜志,2008,41(5):288-291.
Analysis of antibiotic resistance genes inNeisseria gonorrhoeaestrains with decreased sensitivity to ceftriaxone from Shenzhen city
Zhang Lijun,Wang Feng,Mo Junluan,Peng Yi.Clinical Laboratory for Pathogen Detection, Shenzhen Center for Chronic Disease Control,Shenzhen 518020,China
< class="emphasis_italic">Corresponding author:Wang Feng,Email:biowangfeng@163.com
Wang Feng,Email:biowangfeng@163.com
ObjectiveTo analyze the relationship ofpenA,ponA,porBandmtrRgene mutations with the reduced sensitivity to ceftriaxone inN.gonorrhoeaeisolates from Shenzhen city.MethodsA total of 296 clinical isolates ofN.gonorrhoeaewere collected in Shenzhen city from 2009 to 2011.The agar dilution method was used to estimate the sensitivity of theseN.gonorrhoeaeto ceftriaxone.Totally,53 strains with reduced sensitivity to ceftriaxone(minimum inhibitory concentration(MIC):0.06-0.50 μg/ml)were identified,and 53 strains with high sensitivity to ceftriaxone were randomlyselectedfromtheremainingstrainsandservedasthe controlgroup.PCRwasperformedto amplifythepenA,ponA,porBandmtrRgenes from the 106 isolates followed DNA sequencing.ResultsThe mosaic structure of the penicillinbindingprotein2(PBP2)gene(penAgene)wasfoundinonlyone isolate witha ceftriaxone MICof0.1250 μg/ml.Amino acid sequence analysis of the remaining 105 isolates yielded 16 different amino acid patterns.The MICs of ceftriaxone were relatively high(0.062 5 μg/ml)inN.gonorrhoeaestrains harboring the amino acid patternsⅩⅢ,ⅩⅧorⅩⅩⅩⅧ, but relatively low(0.008 0 μg/ml)in those harboring the amino acid patternⅡ.No significant differences were observed in the frequency ofmtrR,porBor ponA gene mutations betweenN.gonorrhoeaeisolates with reduced sensitivity to ceftriaxone and those with high sensitivity(all P>0.05).Conclusions The mosaic structure of PBP2 may be not the primary reason for reduced sensitivity ofNeisseria gonorrhoeaeto ceftriaxone in Shenzhen,while different amino acid patterns produced by various mutations in amino acid residues at positions 500-580 in the non-mosaic PBP2,together withmtrR,porBandponAmutations,may play more important roles in the reduced sensitivity.
Neisseria gonorrhoeae;Ceftriaxone;DNA mutational analysis;Microbial sensitivity tests;Drug resistance,microbial
10.3760/cma.j.issn.0412-4030.2015.10.006
深圳市衛生計生系統科研項目(201401071)
518020深圳市慢性病防治中心病原檢驗科
王峰,Email:biowangfeng@163.com
2014-11-10)
(本文編輯:尚淑賢)

