維生素K2對大鼠主動脈鈣化的作用研究
姜曉宇,張東海,呂安林,李寰,邱翠婷,馬曉磊,郭顯,李珊
維生素K2對大鼠主動脈鈣化的作用研究
姜曉宇,張東海,呂安林,李寰,邱翠婷,馬曉磊,郭顯,李珊
目的:探討維生素K2對大鼠血管鈣化形成及氧化應(yīng)激損傷的作用。
方法:24只大鼠隨機(jī)分為4組:對照組、6周鈣化組、12周鈣化組和6周鈣化+6周維生素K2組。采用華法林誘導(dǎo)大鼠體內(nèi)血管鈣化形成。分別通過茜素紅S染色法和鄰甲酚肽絡(luò)合酮比色法檢測4組大鼠主動脈組織鈣結(jié)節(jié)形成情況及鈣沉積含量;活性氧檢測試劑盒(二氫乙啶)檢測大鼠主動脈組織活性氧陽性細(xì)胞數(shù);透射電子顯微鏡檢測大鼠血管平滑肌細(xì)胞線粒體形態(tài)變化。
結(jié)果:6周及12周兩個鈣化組大鼠主動脈有鈣結(jié)節(jié)形成,鈣沉積含量及活性氧水平均顯著高于對照組(P均<0.01);6周鈣化+6周維生素K2組大鼠與兩個鈣化組相比,上述各指標(biāo)均顯著降低,差異均有統(tǒng)計學(xué)意義(P均<0.01)。兩個鈣化組大鼠血管平滑肌細(xì)胞線粒體腫脹,結(jié)構(gòu)模糊不清,胞質(zhì)內(nèi)空泡變性;6周鈣化+6周維生素K2組大鼠血管平滑肌細(xì)胞體積與對照組比較無明顯變化,胞質(zhì)內(nèi)未見空泡變性。
結(jié)論:華法林誘導(dǎo)血管鈣化形成與氧化應(yīng)激損傷有關(guān),氧化應(yīng)激損傷可造成細(xì)胞超微結(jié)構(gòu)損傷。維生素K2可能通過減輕血管平滑肌細(xì)胞氧化應(yīng)激損傷,改善血管鈣化。
動脈鈣化;氧化應(yīng)激;活性氧;線粒體
Methods: A total of 24 rats were divided into 4 groups: ①Control group, ②6-week calcifcation group, ③12-week calcifcation group and ④6-week calcifcation + 6-week VK2group; n=6 in each group. The arterial calcifcation was induced by warfarin (WFN) treatment. The calcium nodule and deposition in rat’s theaortic artery were detected by Alizarin red staining and o-cresolphthalein complexone method, the reactive oxygen species (ROS) were measured by DHE probe staining and the morphological changes of mitochondria in smooth muscle cells were detected by transmission electron microscopy.
Results: Calcifcation nodule formed in both 6-week and 12-week calcifcation groups, the calcifcation deposition and ROS were higher than Control group, P<0.01. Compared with both calcification groups, the above indexes were decreased in 6-week calcifcation + 6-week VK2group, P<0.01. Both calcifcation groups showed mitochondria swelling with unclear structure and cytoplasm vacuoles degeneration in vascular smooth muscle cells. The vascular smooth muscle cell volumes were similar between Control group and 6-week calcification + 6-week VK2group, and no cytoplasm vacuoles degeneration was observed.
Conclusion: Warfarin induced aortic calcifcation is related to oxidative stress injury which may cause the ultra-
micro structural damage in smooth muscle cells; VK2may reduce the oxidative stress injury and improve the condition of vessel calcifcation in experimental rats.
(Chinese Circulation Journal, 2015,30:1101.)
動脈鈣化是2型糖尿病、慢性腎臟病和慢性炎癥性疾病患者中普遍存在的血管病變。回顧性分析發(fā)現(xiàn)[1],70歲以上健康絕經(jīng)后女性中90%以上存在動脈鈣化。在Framingham研究中[2],平均年齡為6l歲的男性和女性受試者中動脈鈣化發(fā)生率分別為68%和57%。慢性腎臟病患者中動脈鈣化患病率比健康人群高45倍[3]。因此,動脈鈣化的預(yù)防和治療對于原發(fā)病的進(jìn)展和預(yù)后具有重要臨床意義。動脈鈣化形成的確切機(jī)制尚不清楚。有研究發(fā)現(xiàn),活性氧簇(ROS)的產(chǎn)生能夠通過促進(jìn)細(xì)胞核表達(dá)的成骨轉(zhuǎn)錄因子Runx2升高,α-平滑肌肌動蛋白表達(dá)量降低,血管平滑肌細(xì)胞(VSMC)由收縮表型向具有分泌功能的成骨樣細(xì)胞表型轉(zhuǎn)化,促發(fā)鈣化形成[4]。因此,動脈鈣化與氧化應(yīng)激密切相關(guān)[5,6]。而華法林干預(yù)大鼠后,研究證實能成功誘導(dǎo)大鼠動脈鈣化模型的建立[7]。故本研究通過華法林誘導(dǎo)建立大鼠體內(nèi)血管鈣化模型,在此基礎(chǔ)上觀察維生素K2治療對大鼠體內(nèi)血管鈣化形成、活性氧表達(dá)、線粒體形態(tài)變化的影響,探討維生素K2對大鼠血管鈣化形成及氧化應(yīng)激損傷的作用。
1 材料與方法
動物與試劑:2013-11至2014-11選取清潔級10周齡Sprague-DaWley雄性大鼠24只,重約120~150 g(軍隊實驗動物使用許可證SYXK軍2010-046,購自第四軍醫(yī)大學(xué)動物實驗中心)。實驗大鼠在普通鼠籠單只飼養(yǎng)(第四軍醫(yī)大學(xué)口腔實驗動物中心,SPF級別),實驗協(xié)議經(jīng)第四軍醫(yī)大學(xué)實驗動物倫理委員會批準(zhǔn)。華法林和維生素K2分別溶解在玉米油中,均勻拌入飼料中,飼料經(jīng)鈷60照射消毒。茜素紅S 產(chǎn)自美國Sigma公司;活性氧檢測試劑盒(S0033)購自中國碧云天生物公司;鈣沉積含量鄰甲酚肽絡(luò)合酮比色試劑盒購自北京中生北控生物公司。
實驗動物分組[7]:24只大鼠隨機(jī)分為對照組、6周鈣化組、12周鈣化組和6周鈣化+ 6周維生素K2組,每組6只。對照組投喂正常飼料;兩個鈣化組投喂含華法林(3 mg/g)的飼料;6周鈣化+ 6周維生素K2組在投喂6周含華法林飼料的基礎(chǔ)上給予含維生素K2(100 μg/g)飼料喂養(yǎng)6周。
大鼠主動脈組織鈣化形成情況檢測: (1)茜素紅S染色:取石蠟切片脫蠟后,磷酸鹽緩沖液清洗3次,晾干后,在組織面滴加1 g/L的茜素紅S(pH 6.3),室溫下5~10 min,用蒸餾水沖洗3次,淡綠染色20~30 s,蒸餾水浸洗3次,中性樹膠封片,顯微鏡下觀察鈣結(jié)節(jié)被染成深紅色[8]。(2)主動脈組織鈣沉積含量檢測:取雙側(cè)頸總動脈晾干后稱重,剪碎置于1.5 ml EP管中,加入超過10倍(wt /體積)10%甲酸,4℃過夜,鈣沉積含量檢測前,1006.2 g離心10 min,取上清液用于各組主動脈組織鈣沉積含量檢測[7]。
華法林成功誘導(dǎo)大鼠血管鈣化模型的鑒定標(biāo)準(zhǔn)[7]:茜素紅S染色法檢測鈣化形成,鈣化組大鼠鈣結(jié)節(jié)形成。同時鄰甲酚肽絡(luò)合酮比色法進(jìn)行鈣沉積含量定量檢測,鈣化組大鼠主動脈組織鈣沉積含量較對照組顯著升高,且差異有統(tǒng)計學(xué)意義。
大鼠主動脈組織ROS檢測:取大鼠腹主動脈,迅速制備冰凍切片。加入適當(dāng)體積稀釋好的無血清培養(yǎng)基與ROS熒光探針——二氫乙啶(DHE)探針,37℃孵箱中孵育20 min,無血清培養(yǎng)基洗滌3次。激光共聚焦顯微鏡下觀察并拍照[6]。
大鼠VSMC線粒體形態(tài)學(xué)檢測:取腹主動脈,剝?nèi)ネ饽ぜ敖Y(jié)締組織后,縱剖血管成片狀,平鋪切成約2 mm3大小的組織塊,2.5%戊二醛4℃固定24 h,脫水后純樹脂浸透2 h包埋,30℃聚合爐中聚合1 d,甲苯胺藍(lán)染色,光鏡定位,用鉆石刀切片,附到銅網(wǎng)上,醋酸雙氧鈾染色,避光25~30 min,用蒸餾水沖洗3次,檸檬酸鉛染色,6~7 min,蒸餾水沖洗3次。透射電子顯微鏡觀察線粒體形態(tài)改變并拍照[9]。
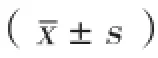
2 結(jié)果
4組大鼠主動脈組織鈣化形態(tài)學(xué)、鈣沉積含量及ROS檢測(圖1、圖2):6周鈣化組和12周鈣化組大鼠主動脈有鈣結(jié)節(jié)形成,鈣沉積含量分別為(9.38±0.867)μg/g和(14.41±0.506)μg/g,與對照組[(0.24±0.071)μg/g]相比顯著升高,差異有統(tǒng)計學(xué)意義(P均<0.01)。6周鈣化+6周維生素K2組大鼠主動脈也有鈣結(jié)節(jié)形成,鈣沉積含量為(5.75±0.465)μg/g,較兩個鈣化組顯著降低, 差異有統(tǒng)計學(xué)意義(P均<0.01)。
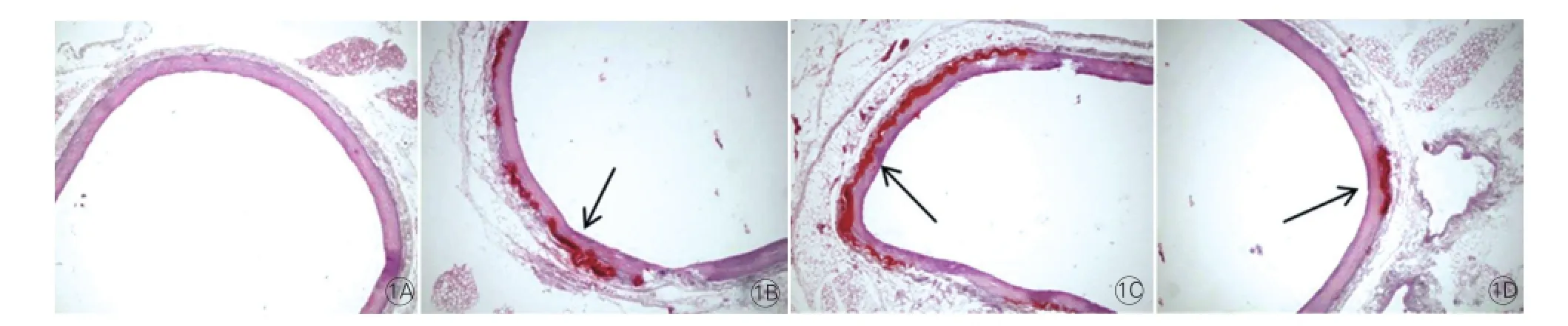
圖1 普通光學(xué)顯微鏡觀察茜素紅S染色法檢測4組大鼠主動脈組織鈣結(jié)節(jié)形成情況(n=6)
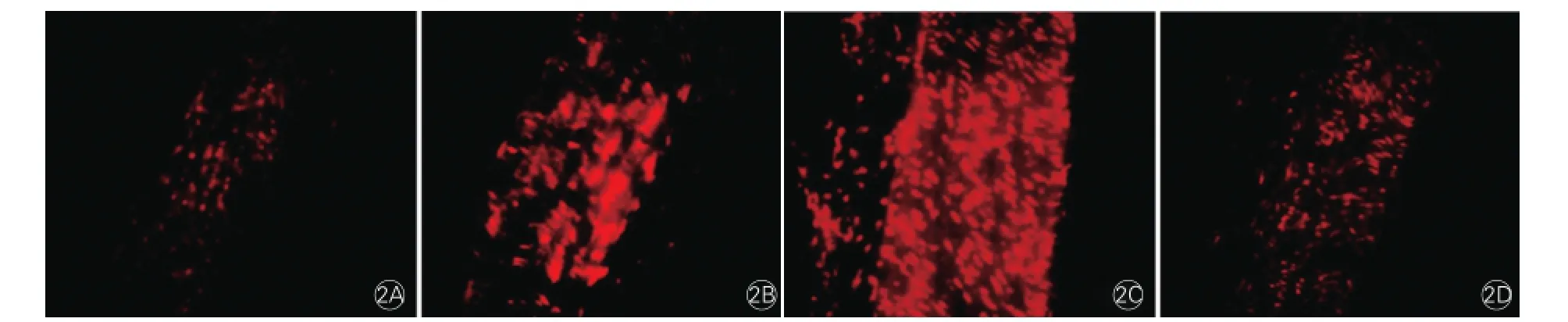
圖2 激光共聚焦顯微鏡觀察4組大鼠主動脈組織中活性氧表達(dá)情況(n=6)
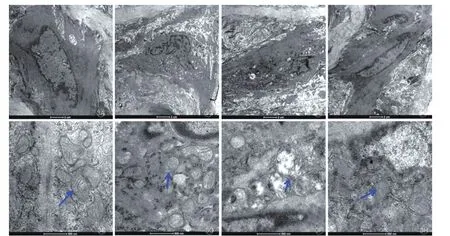
圖3 透射電子顯微鏡觀察4組大鼠主動脈組織中線粒體形態(tài)改變(n=6)
6周鈣化組和12周鈣化組大鼠主動脈組織中ROS陽性組織水平[分別為(15.7±1.59)和(28.6±2.16)]均較對照組(4.5±0.64)顯著升高,差異具有統(tǒng)計學(xué)意義(P均<0.01)。6周鈣化+ 6周維生素K2組大鼠主動脈組織中ROS陽性組織水平(11.7±1.97)較兩個鈣化組顯著降低,差異有統(tǒng)計學(xué)意義 (P均<0.01)。
4組大鼠VSMC線粒體形態(tài)學(xué)檢測 (圖3):對照組大鼠VSMC呈圓形或橢圓形,細(xì)胞膜及核輪廓清晰,胞質(zhì)內(nèi)細(xì)胞漿豐富,胞漿內(nèi)有豐富的線粒體,包膜完整,嵴清晰可見,核大,核型不整,染色質(zhì)均勻分布,可見核仁。與對照組比較,6周鈣化組及12周鈣化組大鼠VSMC細(xì)胞皺縮變小,部分細(xì)胞器發(fā)生崩解,釋放凋亡小體,線粒體腫脹變大,結(jié)構(gòu)變得模糊不清,胞質(zhì)內(nèi)出現(xiàn)空泡變性。與對照組比較,6周鈣化+6周維生素K2組大鼠VSMC體積無明顯變化,細(xì)胞器減少,可見線粒體腫脹,核略增大,核染色質(zhì)分布欠均勻,可見核仁,有少量凋亡細(xì)胞。
3 討論
導(dǎo)致動脈鈣化發(fā)病率升高的因素較多,包括高膽固醇血癥、高血壓、2型糖尿病、終末期腎病床旁透析等,這些因素均與氧化應(yīng)激相關(guān)[10,11]。大量研究證實,血管鈣化灶附近ROS表達(dá)升高[3,11-14]。而Westhofen等[15]研究發(fā)現(xiàn),維生素K通過維生素K環(huán)氧化物還原酶復(fù)合體-1(VKORC1L1)介導(dǎo)細(xì)胞內(nèi)抗氧化作用,HEK293T細(xì)胞過表達(dá)VKORC1L1基因且經(jīng)氧化劑2,4-二甲氧基-1,4-奈醌干預(yù)后,與對照組相比ROS水平降低。本研究通過動脈鈣化形態(tài)學(xué)及鈣沉積含量檢測,觀察華法林誘導(dǎo)大鼠體內(nèi)血管鈣化形成情況。華法林干預(yù)后兩個鈣化組大鼠主動脈組織中有鈣結(jié)節(jié)形成,鈣沉積含量較對照組顯著升高,成功建立大鼠體內(nèi)血管鈣化模型[16];維生素K2干預(yù)后鈣結(jié)節(jié)形成及鈣沉積含量較兩個鈣化組均顯著降低。為進(jìn)一步觀察鈣化形成后氧化應(yīng)激損傷水平,我們檢測了4組大鼠主動脈組織ROS水平。結(jié)果顯示:兩個鈣化組大鼠主動脈組織ROS陽性水平較對照組均增加(P<0.01),且隨著鈣化時間延長,ROS陽性水平進(jìn)一步升高。6周鈣化形成基礎(chǔ)上給予維生素K2干預(yù)后的大鼠主動脈ROS陽性水平顯著降低,同時主動脈鈣化形態(tài)學(xué)和鈣沉積含量與兩個鈣化組比較均顯著減少。本研究結(jié)果與Wei等[17]研究報道一致,明確了在動脈鈣化發(fā)生、發(fā)展過程中存在氧化應(yīng)激損傷。
眾所周知,氧化應(yīng)激可引起抗凋亡蛋白B細(xì)胞淋巴瘤/白血病-2的表達(dá)下調(diào)。而生物體內(nèi)線粒體損傷后,線粒體膜電位破壞,繼而出現(xiàn)ROS生成增多、鈣超載及凋亡等現(xiàn)象。維生素K2干預(yù)是否提高線粒體膜電位,從而降低ROS水平、鈣超載及凋亡表達(dá),目前尚未見相關(guān)報道。本研究通過透射電鏡觀察到,兩個鈣化組大鼠VSMC線粒體腫脹變大,結(jié)構(gòu)變得模糊不清,胞質(zhì)內(nèi)出現(xiàn)空泡變性。而經(jīng)維生素K2治療后線粒體雖腫脹,但胞質(zhì)內(nèi)未見空泡變性。這進(jìn)一步明確了動脈鈣化發(fā)生、發(fā)展過程中存在氧化應(yīng)激損傷。鈣化組大鼠VSMC超微結(jié)構(gòu)線粒體腫脹、部分溶解,進(jìn)而造成細(xì)胞凋亡。炎癥或機(jī)械損傷可導(dǎo)致VSMC凋亡,釋放基質(zhì)囊泡和凋亡小體,凋亡小體成為鈣化晶核,促發(fā)鈣沉積[18]。氧化應(yīng)激損傷是否通過凋亡途徑促進(jìn) VSMC 鈣化形成還有待進(jìn)一步深入研究。
本研究觀察到,大鼠主動脈組織鈣化形成與氧化應(yīng)激損傷有關(guān),氧化應(yīng)激損傷可造成細(xì)胞超微結(jié)構(gòu)改變,如線粒體腫脹和溶解。而維生素K2干預(yù)后鈣化組大鼠VSMC氧化應(yīng)激損傷減輕,線粒體腫脹和溶解改善。本課題組細(xì)胞學(xué)實驗進(jìn)一步證實,ROS作為第二信使激活VSMC中成骨轉(zhuǎn)錄因子Runx2的表達(dá),由具有收縮表型的VSMC向成骨樣細(xì)胞轉(zhuǎn)變并促使鈣化形成[19]。因此,氧化應(yīng)激損傷可能是動脈鈣化的重要發(fā)病機(jī)制之一,維生素K2為動脈鈣化的治療提供了新的方向。
[1] Schulz E, Arfai K, Liu X, et al. Aortic calcification and the risk of osteoporosis and fractures. J Clin Endocrinol Metab, 2004, 89: 4246-4253.
[2] Wilson PW, Kauppila LI, O'Donnell CJ, et al. Abdominal aortic calcific deposits are an important predictor of vascular morbidity and mortality. Circulation, 2001, 103: 1529-1534.
[3] Chowdhury UK, Airan B, Mishra PK, et al. Histopathology and morphometry of radial artery conduits: basic study and clinical application. Ann Thorac Surg, 2004, 78: 1614-1621.
[4] Liberman M, Bassi E, Martinatti MK, et al. Oxidant generation predominates around calcifying foci and enhances progression of aortic valve calcification. Arterioscler Thromb Vasc Biol, 2008, 28: 463-470.
[5] Roman-Garcia P, Barrio-Vazquez S, Fernandez-Martin JL, et al. Natural antioxidants and vascular calcification: a possible benefit. J Nephrol, 2011, 24: 669-672.
[6] Sage AP, Tintut Y, Demer LL. Regulatory mechanisms in vascular calcification. Nat Rev Cardiol, 2010, 7: 528-536.
[7] Schurgers LJ, Spronk HM, Soute BA, et al. Regression of warfarininduced medial elastocalcinosis by high intake of vitamin K in rats. Blood, 2007, 109: 2823-2831.
[8] Lau WL, Leaf EM, Hu MC, et al. Vitamin D receptor agonists increase klotho and osteopontin while decreasing aortic calcification in mice with chronic kidney disease fed a high phosphate diet. Kidney Int, 2012, 82: 1261-1270.
[9] 王英, 王梅. 高磷誘導(dǎo)大鼠血管平滑肌細(xì)胞鈣化及其電鏡表現(xiàn). 首都醫(yī)科大學(xué)學(xué)報, 2009, 30: 521-524.
[10] Basta G, Schmidt AM, De Caterina R. Advanced glycation end products and vascular inflammation: implications for accelerated atherosclerosis in diabetes. Cardiovasc Res, 2004, 63: 582-592.
[11] Maziere C, Salle V, Gomila C, et al. Oxidized low density lipoprotein increases RANKL level in human vascular cells. Involvement of oxidative stress. Biochem Biophys Res Commun, 2013, 440: 295-299. [12] Miller JD, Chu Y, Brooks RM, et al. Dysregulation of antioxidant mechanisms contributes to increased oxidative stress in calcific aortic valvular stenosis in humans. J Am Coll Cardiol, 2008, 52: 843-850.
[13] Boraldi F, Garcia-Fernandez M, Paolinelli-Devincenzi C, et al. Ectopic calcification in beta-thalassemia patients is associated with increased oxidative stress and lower MGP carboxylation. Biochim Biophys Acta, 2013, 1832: 2077-2084.
[14] Brodeur MR, Bouvet C, Barrette M, et al. Palmitic acid increases medial calcification by inducing oxidative stress. J Vasc Res, 2013, 50: 430-441.
[15] Westhofen P, Watzka M, Marinova M, et al. Human vitamin K 2,3-epoxide reductase complex subunit 1-like 1 (VKORC1L1) mediates vitamin K-dependent intracellular antioxidant function. J Biol Chem, 2011, 286: 15085-15094.
[16] Li H, Tao HR, Hu T, et al. Atorvastatin reduces calcification in rat arteries and vascular smooth muscle cells. Basic Clin Pharmacol Toxicol, 2010, 107: 798-802.
[17] Wei Q, Ren X, Jiang Y, et al. Advanced glycation end products accelerate rat vascular calcification through RAGE/oxidative stress. BMC Cardiovasc Disord, 2013, 13: 13.
[18] Proudfoot D, Skepper JN, Hegyi L, et al. Apoptosis regulates human vascular calcification in vitro: evidence for initiation of vascular calcification by apoptotic bodies. Circ Res, 2000, 87: 1055-1062.
[19] 邱翠婷, 呂安林, 李寰, 等. 鈣磷誘導(dǎo)大鼠血管平滑肌細(xì)胞鈣化的機(jī)制研究. 中國循環(huán)雜志, 2015, 1: 64-67.
Effect of Vitamin K2on Theaortic Artery Calcification in Experimental Rats
JIANG Xiao-yu, ZHANG Dong-hai, LV An-lin, LI Huan, QIU Cui-ting, MA Xiao-lei, GUO Xian, LI Shan.
Department of Cardiology, Xijing Hospital, Fourth Military Medical University, Xi’an (710032) Shaanxi, China
Co-corresponding Authors: LV An-lin, Email: lvanlin@fmmu.edu.cn and LI Huan, Email: lihuan816@yahoo.com
Objective: To explore the effects of Vitamin K2(VK2) on theaortic artery calcifcation and oxidative stress injury in experimental rats.
Arterial Calcifcation; Oxidative stress; Reactive oxygen species; Mitochondria
2015-06-12)
(編輯:朱柳媛)
國家自然科學(xué)基金(81170256);陜西省科技計劃項目(2009K13-01)
710032 陜西省西安市,中國人民解放軍第四軍醫(yī)大學(xué)第一附屬醫(yī)院 心內(nèi)科(姜曉宇、呂安林、李寰、邱翠婷、馬曉磊、郭顯、李珊);陜西銅川市人民醫(yī)院 心內(nèi)科(張東海)
姜曉宇 碩士研究生 主要從事動脈鈣化及機(jī)制研究 Email: muyuanj99@163.com 通訊作者:呂安林 Email: lvanlin@fmmu.edu.cn;
李寰 Emal: lihuan816@yahoo.com
R54
A
1000-3614(2015)11-1101-05
10.3969/j.issn.1000-3614.2015.11.016

