IVF晚卵泡期孕酮持續高水平對于妊娠結局的影響
譚小軍,黃向紅,劉佶,彭婀娜,蔣云山
(湖南省湘潭市中心醫院,湘潭 411100)
在行體外受精-胚胎移植(IVF-ET)助孕治療時,往往需要對患者進行控制性卵巢刺激(COS),但不同卵巢反應性的患者在使用促性腺激素釋放激素激動劑(GnRH-a)、卵泡刺激素(FSH)時,刺激的多卵泡發育可能使血清孕酮(P)水平在卵泡晚期出現持續升高[1]。國內有研究報道,P在注射人絨毛膜促性腺激素(HCG)日>1.205ng/ml(4.41nmol/L)是判斷升高的節點[2],晚卵泡期P水平的升高不利于胚胎移植在生殖領域已經有共識[3],一般認為HCG日P水平>4.41nmol/L時應取消移植周期。按照我院生殖中心診療經驗和處理習慣,對本研究中HCG 日P>4.41nmol/L 的患者,在與患者及家屬充分溝通后,均取消新鮮胚胎移植,行全胚冷凍,日后擇期行凍融胚胎復蘇移植。亦有國內學者認為在卵巢低、中、高反應患者中判斷P 升高的節點并不相同[3],國外有研究報道將P水平升高定義為HCG注射日P水平>2.93~7.32nmol/L[4-6],因此單純根據HCG 日P水平的升高預測妊娠結局可能不夠客觀和全面,P 水平的上升程度、持續時間與IVF妊娠結局是否有關尚存在爭議。在我院生殖中心之前的臨床診療中,發現晚卵泡期P>2.93nmol/L可能對IVF 妊娠結局產生不利影響,結合文獻查閱,此次研究我們將2.93nmol/L 作為P 水平升高的閾值,通過回顧性分析在我院生殖中心接受IVFET 治療的不育癥患者的臨床資料,探討注射HCG日與注射前兩日P>2.93nmol/L 水平并持續高水平與妊娠結局的相關性,為胚胎移植提供參考。
資料與方法
一、研究對象及分組
回顧性分析2010年1月至2013年12月在我院生殖中心接受第一周期IVF-ET 治療的不育癥患者1 520例。納入標準:年齡20~35歲,月經周期28~35 d,HCG 日P<4.39 nmol/L,獲卵6~15枚,均完成了新鮮周期胚胎移植,至少隨訪至妊娠28周。不育原因:輸卵管因素、排卵障礙、男方因素、原因未明不育癥、免疫性不育。排除子宮內膜異位癥、移植日因子宮內膜過薄取消周期的患者,以及單側或雙側卵巢占位性病變或切除的患者。
按注射HCG 前2d及注射日的血清P 水平分為3組,A 組:3日P均≤2.93nmol/L(n=1 128)、B組:任意兩日P>2.93nmol/L(n=307)、C 組:連續3dP>2.93nmol/L(n=85),比較各組間移植后14d 血清HCG 陽性率、臨床妊娠率、繼續妊娠率和妊娠丟失率。按照實驗設計,注射HCG 前2d及注射日中單一日P水平>2.93nmol/L不納入實驗分組,本次實驗無單一日P水平>2.93nmol/L者。
二、研究方法
IVF-ET 卵巢刺激方案:采用GnRH-a(達菲林,3.75mg/支,博福-益普生,法國)短效長方案,在黃體中期即月經第20~21天開始降調節[7]。降調14~20d 后根據患者情況給予促性腺激素(Gn)150~300 U,Gn 采用基因重組人卵泡刺激素(rFSH,默克-雪蘭諾,德國)和(或)注射用尿促卵泡素(麗申寶,珠海麗珠),根據陰道超聲監測卵泡發育情況和血中雌二醇(E2)濃度調整藥物劑量[8]。所有患者于注射HCG 前兩日及注射日監測P 水平,當60%卵泡直徑≥18mm 時,于當晚注射HCG(珠海麗珠)或重組HCG(艾澤,默克-雪蘭諾,德國),34~36h 后經陰道超聲引導下穿刺取卵,行常規IVF,根據胚胎發育形態學標準[9]對胚胎進行評級,第2天細胞數≥4個,第3天細胞數≥6個,形態評級為Ⅰ級或Ⅱ級的胚胎,為優質胚胎。3d后行常規胚胎移植,剩余的優質胚胎冷凍保存。胚胎移植后行常規黃體支持。
三、隨訪
分別于胚胎移植后14d、28d、63d,妊娠20w、妊娠28w、分娩時行復診或隨訪,復診內容包括:血β-HCG、P水平,陰道或腹部超聲檢查孕囊個數及位置,常規產前檢查情況等。所納入患者無失訪者。移植后14d血清HCG 水平陽性(>10 U/L)者為生化妊娠[10],28d行陰道超聲檢查顯示孕囊及胎心搏動者為臨床妊娠[11],妊娠≥28w為繼續妊娠,已確定臨床妊娠但未達到繼續妊娠的為妊娠丟失[12]。P及HCG 測定采用羅氏化學發光定量法,檢測試劑盒由美國貝克曼庫爾特有限公司提供。
四、統計學處理
結 果
一、3組患者一般情況比較
3組患者年齡、體重指數(BMI)、基礎FSH、不育年限比較,差異無統計學意義(P>0.05)(表1)。
二、3組患者促排卵情況比較
3組患者獲卵數、受精數、可利用胚胎數及移植胚胎數比較,差異無統計學意義(P>0.05)(表2)。
三、3組患者妊娠結局的比較
1 520例患者中988例生化妊娠,667例臨床妊娠,562例繼續妊娠,其中421例單胎分娩,141例雙胎分娩;妊娠丟失105例(含自然流產、宮外孕等),妊娠丟失的原因與胚胎質量、宮腔盆腔環境、體內激素水平、宮頸機能等相關。生化妊娠率為65.0%(988/1 520),總 臨 床 妊 娠 率 為43.88% (667/1 520),總繼續妊娠率為36.97%(562/1 520)。各組的生化妊娠率、臨床妊娠率和繼續妊娠率比較見表3。C組的生化妊娠率明顯低于A、B 兩組,差異有統計學意義(P<0.05);B、C 組的臨床妊娠率和繼續妊娠率較A 組有逐漸下降的趨勢,但各組間比較差異無統計學意義(P>0.05)。3組患者的妊娠丟失率比較,差異亦無統計學意義(P>0.05)。
表1 各組患者一般情況比較(±s)
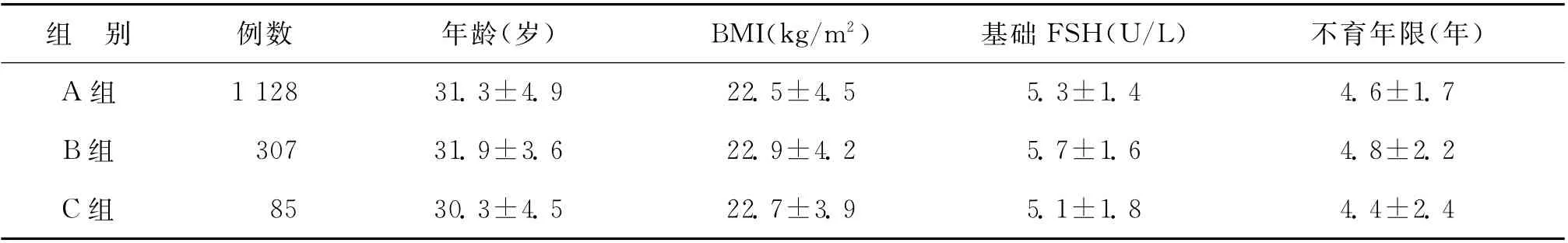
表1 各組患者一般情況比較(±s)
組 別 例數 年齡(歲) BMI(kg/m2) 基礎FSH(U/L) 不育年限(年)A 組1 128 31.3±4.9 22.5±4.5 5.3±1.4 4.6±1.7 B組 307 31.9±3.6 22.9±4.2 5.7±1.6 4.8±2.2 C組85 30.3±4.5 22.7±3.9 5.1±1.8 4.4±2.4
表2 各組患者促排卵情況比較[(±s)]

表2 各組患者促排卵情況比較[(±s)]
組 別 例數 獲卵數(枚) 受精數(枚) 可利用胚胎數(枚) 移植胚胎數(個)A 組 1 128 12.35±4.18 10.02±3.25 7.53±2.38 2.15±0.43 B組 307 12.89±4.12 9.86±3.26 7.81±2.52 2.23±0.48 C組 85 12.73±3.74 10.14±3.41 7.68±2.76 2.33±0.4 6

表3 各組患者妊娠結局比較[n(%)]
討 論
P對早期妊娠的影響主要是使子宮內膜從增殖期轉化為分泌期,為受精卵著床做準備。IVF-ET周期中晚卵泡期P 持續高水平已經被證實對妊娠結局不利[3],這可能與內膜容受性和卵泡發育不同步有關[13],但其升高的具體機制目前尚不明確。卵巢的自身反應性以及Gn的使用劑量可能是晚卵泡期P水平升高并持續的關鍵因素[14]。本研究中,晚卵泡期P水平持續3d>2.93nmol/L 組的患者生化妊娠率顯著低于其他兩組,再一次驗證了晚卵泡期P持續高水平不利于胚胎著床,但該組患者的臨床妊娠率和繼續妊娠率與其他兩組比較并無顯著性差異,提示P的持續高水平可能對最終的臨床妊娠率和妊娠維持影響并不大。國內外一些機構的研究報道推測晚卵泡期P 持續高水平對于卵母細胞質量以及優質胚胎形成的影響并不明顯[15-16],晚卵泡期P持續高水平可能對胚胎著床造成影響,這可能與子宮內膜的種植窗提前,子宮內膜容受性下降,內膜發育和胚胎著床不同步等因素有關[17]。國內目前比較公認的觀點是,HCG 注射日P≥2.93~7.32nmol/L時需要考慮取消新鮮周期移植[18]。本研究對HCG 注射前2日和注射日P水平進行動態監測,晚卵泡期P 水平持續3d>2.93nmol/L 的C組最終獲得29.41%的繼續妊娠率,雖然與其他兩組比較有下降的趨勢,但并無顯著性差異,提示臨床上不能僅僅通過晚卵泡期P 水平來預測助孕治療的妊娠結局,需要根據不同患者的情況綜合判斷是否取消或繼續給予新鮮周期胚胎移植。
綜上所述,晚卵泡期血清P持續高水平可能影響胚胎著床,但對臨床妊娠率和妊娠維持的影響并不明顯。臨床上對于卵巢不同反應性的患者,促性腺激素使用劑量不盡相同,僅僅從P水平的高低與否來預測妊娠結局可能不夠客觀全面,需要綜合判斷不同患者的情況以指導確定下一步診療方案。對于已經出現的晚卵泡期P持續高水平患者,需對患者情況進行綜合評價后決定是否繼續進行鮮胚移植,或改行囊胚移植或凍融胚胎移植。因為本研究為回顧性分析,樣本來源于就診人群,可能存在選擇偏倚,客觀性和準確性尚有待提高。
[1] Bosch E,Labarta E,Crespo J,et al.Circulating progesterone levels and ongoing pregnancy rates in controlled ovarian stimulation cycles for in vitro fertilization:analysis of over 4000cycles[J].Hum Reprod,2010,25:2092-2100.
[2] 郭悅,楊菁,蔡晶,等.晚卵泡期孕酮水平提前上升相關因素分析及其發生機制的新探討[J].生殖與避孕,2013,33:456-462.
[3] 徐蓓,李舟,章漢旺,等.血清孕酮升高對卵巢不同反應者體外受精-胚胎移植結局的影響[J].生殖醫學雜志,2013,22:685-691.
[4] Bosch E,Valencia I,Escudero E,et al.Premature luteinization during gonadotropin-releasing hormone antagonist cycles and its relationship with in vitro fertilization outcome[J].Fertil Steril,2003,80:1444-1449.
[5] Xu B,Li Z,Zhang H,et al.Serum progesterone level effects on the outcome of in vitro fertilization in patients with different ovarian response:an analysis of more than 10,000 cycles[J].Fertil Steril,2012,97:1321-1327.
[6] Van Vaerenbergh I,Fatemi HM,Blockeel C,et al.Progesterone rise on HCG day in GnRH antagonist/rFSH stimulated cycles affects endometrial gene expression[J/OL].Reprod Biomed Online,2011,22:263-271.
[7] 田莉,吳丹,沈浣.長、短效GnRH 激動劑在控制性超排卵長方案中應用效果比較[J].中國婦產科臨床雜志,2009,10:413-415,453.
[8] 范靜,姜宏,王雪梅,等.卵泡中晚期添加HMG 對體外受精-胚胎移植結局的影響[J].重慶醫學,2014,43:563-565.
[9] 莊廣倫.現代輔助生殖技術[M].北京:人民衛生出版社,2005:240-241.
[10] 任秀蓮,劉平.著床失敗、生化妊娠和流產是一碼事嗎?[J].生殖醫學雜志,2014,23:191-197.
[11] 劉愛蘭,張增芳.經腹超聲與經陰道超聲雙向檢查在早期妊娠診斷中的價值[J].醫學影像學雜志,2013,23:1445-1447.
[12] 饒騰子.影響IVF結局的臨床因素分析及IVF 成功抱嬰預測模型初步探討[D].南方醫科大學,2012.
[13] 王麗娟,胡曉東,莫美蘭,等.HCG 注射日孕酮水平和體外受精-胚胎移植妊娠結局的關系探討[J].中國優生與遺傳雜志,2013,21:116-118,140.
[14] 陳念念,李予,王文軍,等.體外受精-胚胎移植后早期妊娠丟失的相關風險因素分析[J].國際婦產科學雜志,2011,38:455-457.
[15] Hofmann GE,Bergh PA,Guzman I,et al.Premature luteinization is not eliminated by pituitary desensitization with leuprolide acetate in women undergoing gonadotrophin stimulation who demonstrated premature luteinization in a prior gonadotrophin-only cycle[J].Hum Reprod,1993,8:695-698.
[16] Melo MA,Meseguer M,Garrido N,et al.The significance of premature luteinization in an oocyte-donation programme[J].Hum Reprod,2006,21:1503-1507.
[17] Bourgain C,Devrory P.The endometrium in stimulated cycles for IVF[J].Hum Reprod Update,2003,9:515-522.
[18] 劉芳,李麗,王興玲,等.HCG 日血清激素水平對供精體外受精妊娠結局的影響[J].中國婦幼保健,2013,28:94-98.

