傷寒沙門菌質粒pR ST98對細菌生物膜形成能力及毒力的影響
傷寒沙門菌質粒pRST98對細菌生物膜形成能力及毒力的影響
劉珍,闕鳳霞,李嫄淵,吳淑燕,黃瑞
(蘇州大學醫學部病原生物學系,江蘇 蘇州 215123)
摘要:目的探討傷寒沙門菌質粒pRST98對鼠傷寒沙門菌和大腸埃希菌生物膜形成能力及毒力的影響。方法將傷寒沙門菌質粒pRST98接合轉移導入鼠傷寒沙門菌和大腸埃希菌,制備單個游離懸浮狀態下的細菌菌液;將接合導入質粒pRST98前、后的受試菌分別在相同條件下形成生物膜,制備生物膜狀態下的菌液。浮游細菌與生物膜形成細菌調節至同一濃度后分別與CT26細胞進行黏附侵襲、血清殺菌以及抗巨噬細胞吞噬實驗,比較不同狀態下受試菌毒力的差異。結果傷寒沙門菌質粒pRST98能夠促進鼠傷寒沙門菌和大腸埃希菌形成生物膜;黏附實驗顯示除大腸埃希菌外,鼠傷寒沙門菌在生物膜狀態下對CT26細胞的黏附力明顯增強,形成生物膜的細菌對CT26細胞的侵襲力明顯下降;生物膜狀態的鼠傷寒沙門菌和大腸埃希菌在兔血清和豚鼠血清中的存活率均高于浮游狀態;生物膜狀態下的鼠傷寒沙門菌在巨噬細胞內的存活率明顯高于浮游狀態下的細菌。結論質粒pRST98能夠促進鼠傷寒沙門菌和大腸埃希菌形成生物膜;生物膜的形成能促進細菌對細胞的黏附,同時抑制細菌對細胞的侵襲力;增強細菌抵抗血清殺菌及巨噬細胞吞噬的能力。
關鍵詞:傷寒沙門菌,質粒pRST98;鼠傷寒沙門菌;大腸埃希菌;生物膜;毒力
中圖分類號:
文章編號:1673-8640(2015)10-1033-06R378.2
文獻標志碼:A
DOI:10.3969/j.issn.1673-8640.2015.10.017
Abstract:ObjectiveTo investigate the influence of Salmonella typhi plasmid pRST98 on bacterial biofilm formation and virulence. MethodsSalmonella typhi plasmid pRST98 was conjugated into Salmonella typhimurium and Escherichia coli to form Salmonella typhimurium/pRST98 and Escherichia coli/pRST98. These bacteria were cultured under suitable conditions to form biofilm. The planktonic bacteria were prepared. Biofilm bacteria and planktonic bacteria were adjusted to the same concentration then carried on adhesion and invasion experiments with CT26,anti-serum killing experiments and anti-macrophage phagocytosis experiments to compare virulence in different states. ResultsSalmonella typhi plasmid pRST98 can advance biofilm formation of Salmonella typhimurium and Escherichia coli, and biofilm promoted all bacterium adhesion capabilities to CT26 except for Escherichia coli. The biofilm formation of Salmonella typhimurium and Escherichia coli decreased invasion capabilities to CT26 . The survival rates of Salmonella typhimurium and Escherichia coli in biofilm were higher than the bacteria in planktonic states for rabbit serum and guinea pig serum. Salmonella typhimurium survival rate within macrophages in biofilm state was significantly higher than that under planktonic state. Conclusions Plasmid pRST98 can promote the biofilm formation of Salmonella typhimurium and Escherichia coli. Biofilm formation promotes adhesion to cells while inhibiting invasion capability,and enhances anti-serum killing and anti-macrophage phagocytosis.
基金項目:江蘇省自然科學基金面上項目(BK2011286)
作者簡介:劉珍, 女, 1985年, 碩士, 技士,主要從事細菌生物膜形成的研究。
通訊作者:黃瑞, 聯系電話:0512-65880973。
收稿日期:(2014-12-10)
The influence ofSalmonellatyphiplasmid pRST98on bacterial biofilm formation and virulenceLIUZhen,QUEFengxia,LIYuanyuan,WUShuyan,HUANGRui.(DepartmentofPathogenicBiology,MedicalCollege,SoochowUniversity,JiangsuSoochow215123,China)
Key words:Salmonellatyphi; Plasmid pRST98;Salmonellatyphimurium;Escherichiacoli; Biofilm; Virulence

細菌生物膜(biofilm,BF)是指細菌在生長過程中,附著在有生命或無生命體表面形成的由細菌及其分泌的水合性基質所組成的膜樣復合物[1]。在微生物感染的防治和研究領域,細菌生物膜已引起臨床醫生和科研人員的極大關注。據美國國家健康研究所報道,大約80%人類細菌性感染由生物膜中的細菌引起[2]。
鼠傷寒沙門菌是一種常見的人畜共患病原菌[3]。有數據顯示沙門菌生物膜與肝癌和膽囊癌的發生有相關性[4];大腸埃希菌黏附于導尿管表面或尿道上皮細胞表面形成生物膜,是導尿管相關尿路感染(catheter-associated urinary tract infection,CAUTI)最重要的原因[5]。
傷寒沙門菌質粒pRST98是本實驗室在一次暴發于我國的傷寒流行中分離鑒定的一個獨有的傷寒沙門菌質粒。既往研究證實該質粒除編碼抗藥性外還能增強宿主菌的毒力[6]。此外pRST98還是一種接合性質粒,在自然環境和實驗室條件下均可以進入到鼠傷寒沙門菌和大腸埃希菌內,對疾病和耐藥性的傳播具有非常重要的作用[6]。因此,我們選取這2種細菌作為宿主菌,探索此質粒對宿主細菌生物膜形成能力的影響,同時比較2種細菌在形成生物膜后細菌毒力的差異。
材料和方法
一、菌株與細胞株
鼠傷寒沙門菌標準毒株χ3306(簡稱χ3306)及弱毒株χ3337(簡稱χ3337,由χ3306消除其質粒后得到)由美國亞利桑那州立大學生命科學學院的Roy Curtiss Ⅲ教授惠贈;鼠傷寒沙門菌χ3337/pRST98(簡稱χ3337/pRST98)是將傷寒沙門菌質粒pRST98接合轉移導入χ3337中形成的接合子;本實驗室保存的大腸埃希菌K12W1485不含質粒,系經實驗室誘變僅在染色體上有利福平耐藥基因的、無性菌毛的雌性菌(以E.coli表示);將傷寒沙門菌質粒pRST98經接合轉移導入E.coli中得到的接合子E.coliK12W1485/pRST98(以E.coli/pRST98表示)。
小鼠結腸癌細胞系CT26細胞購自上海中國科學院細胞庫。J774A.1細胞購自上海中國科學院細胞庫。
二、主要儀器和試劑
PHILIPS xL-20型掃描電子顯微鏡(荷蘭菲利浦公司);TCS-SP2型共聚焦激光掃描顯微鏡(德國Leica公司)。兔血清(nomal rabbit serum, NRS)和豚鼠血清(guinea pig serum, GPS)分別分離自5只健康雌兔和5只健康豚鼠的血液,取血后4 ℃靜置過夜,離心收集血清,混合過濾除菌并做無菌試驗后分裝備用。
三、實驗方法
1. 傷寒沙門菌質粒pRST98的接合轉移質粒pRST98的接合轉移參照文獻[7]進行。以攜帶pRST98的耐藥傷寒桿菌為供體,χ3337和E.coli為受體,選擇培養基為中國藍培養基含100 μg/mL利福平和供體菌上某一耐藥標志的抗菌藥物,如20 μg/mL克拉霉素 、15 μg/mL卡那霉素、25 μg/mL四環素、25 μg/mL氨芐西林和25 μg/mL萘夫西林等。將供、受體菌分別接種于3 mL LB肉湯中,37 ℃振蕩培養6 h,按等比例接種于0.5 mL新鮮LB肉湯中。由于接合性質粒具有在不同溫度時接合頻率不同的特點,故選擇37 ℃和26 ℃ 2種溫度混合培養3 h,取0.1 mL此菌液做適當稀釋后均勻涂布于上述相應的選擇性中國藍培養基,并同時作供、受體菌對照。37 ℃培養24或48 h后選擇接合子并進行血清學、生化反應鑒定并作藥敏試驗和質粒電泳檢測。比較pRST98結合前、后細菌生物膜的形成情況以及有無生物膜對待檢菌毒力和抵抗力的影響。受試菌為導入質粒pRST98前、后的同一株細菌。
2. 浮游細菌的制備將保存于-80 ℃的受試菌接種于3 mL LB液體培養基,37 ℃培養過夜后轉移至血平板活化。將細菌接種至SS培養基37 ℃培養過夜,用接種環挑取無色傷寒沙門菌單菌落,分區劃線接種于LB固體培養基平板,37 ℃培養過夜,做生化和血清學鑒定后用于實驗。每次使用前在LB平板上劃線接種后,挑取單個菌落至3 mL LB液體培養基,培養至對數生長期。細菌定量方法參照文獻[8]進行。
3. 生物膜狀態菌液的制備LB肉湯培養過夜至對數生長期后,在600 nm下測定吸光度(A600 nm)值,檢測菌液濃度;同時做平板菌落計數,計算菌落形成單位(colony-forming unit,CFU)。將菌液濃度調整致1×1010CFU/mL,分別將等量待測菌加入含0.1%葡萄糖的LB肉湯后, 加入24孔板,每孔1 mL,24孔板用封口膜密封后培養3 d形成成熟生物膜。
4. 細菌黏附、侵襲力的檢測CT26細胞用含10% 胎牛血清的RPMI1640常規培養,胰酶消化后離心,調整細胞濃度為1.5×105CFU/mL,24孔板1 mL/孔,5% CO2、37 ℃平衡12 h待用。浮游細菌在A600 nm下測定菌液濃度,同時做平板菌落計數,計算CFU,調整菌液濃度。生物膜中的細菌使用超聲作用20 min,將其中的細菌釋放出來,并調整細菌濃度。將受試菌按感染復數(multiplicity of infection,MOI)=100∶1加入細胞培養板,450×g離心10 min,繼而在5% CO2、37 ℃條件下共培養1 h,用磷酸鹽緩沖液(phosphate buffered saline,PBS)洗3次,加入預冷的細胞裂解液裂解細胞。裂解后的各組細胞做平板菌落計數檢測CFU,48 h后觀察并計數。細菌黏附力(%)=黏附細菌數/每孔加入細菌總數×100。細菌的侵襲力檢測方法基本同上,只是細菌與細胞共同孵育1 h后,棄去菌液并用PBS輕柔洗3遍,然后每孔加入含100 μg/mL阿米卡星的RPMI1640培養液,以殺死未侵入胞內的細菌,作用3 h后按上法進行細胞內活菌計數。細菌侵襲率(%)=細胞內細菌數/細胞內外細菌總數×100。
5. 血清殺菌實驗為區別血清殺菌過程中補體經典途徑與旁路途徑的不同作用,將血清置于50 ℃水浴15 min,以滅活大多數參與旁路途徑(another complement pathway, ACP)的成分,并將全血清和1∶10稀釋的血清用于實驗。將浮游細菌和生物膜狀態的細菌調整濃度至1×104CFU/mL。分別吸取浮游菌和來自生物膜中的菌液20 μL,各自加入含0.2 mL相應血清的試管和不含血清的普通肉湯管。根據預實驗結果,選37 ℃ 2 h為殺菌的作用條件。用CFU計算存活細菌數。以上實驗重復3次,每份樣品均做2次,取其平均值。細菌存活率(%)=血清作用后CFU/對照組CFU×100。
6. 抗巨噬細胞吞噬實驗將生物膜狀態和浮游狀態下的受試菌濃度調整至1×107CFU/mL待用。J774A.1細胞用含10%胎牛血清的RPMI1640培養基維持培養(含100 μg/mL鏈霉素和100 μg/mL青霉素)。實驗時用胰酶消化貼壁生長的J774A.1細胞,使其分散,用不含抗菌藥物的培養液洗滌細胞3次,血細胞計數板計數后將細胞濃度調整至5×105個/mL,分別加入6孔板,每孔1 mL。37 ℃、5% CO2條件下平衡1 h。將1 mL不同狀態的受試菌加入到各孔中,在37℃、5% CO2條件下與細胞共作用1 h。用含100 μg/mL阿米卡星的RPMI1640培養液離心洗滌3次以除去胞外菌,重新懸浮于含100 μg/mL阿米卡星的培養液中,此時定為“0”點,分別于0、10、30和60 min加入預冷的細胞裂解液裂解細胞,做細菌CFU計數。
四、統計學方法
結果
一、 傷寒沙門菌質粒pR ST98對宿主細菌生物膜形成的影響
結晶紫染色實驗結果顯示,將傷寒沙門菌質粒pRST98接合導入到鼠傷寒沙門菌和大腸埃希菌后,宿主細菌形成生物膜的能力明顯增強。與接合前比較差異有統計學意義(P<0.05),見圖1。
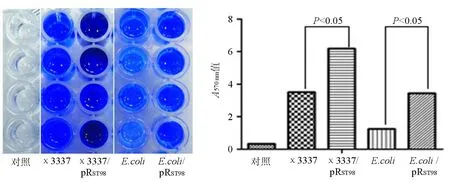
圖1 傷寒沙門菌質粒pR ST98對宿主細菌生物膜形成的影響
二、傷寒沙門菌質粒pR ST98對不同狀態下受試菌黏附CT26細胞的影響
分別將浮游狀態和生物膜狀態下的實驗菌株χ3306、χ3337、χ3337/pRST98、E.coli和E.coli/pRST98按MOI=100∶1與CT26細胞共培養,1 h后收集細胞用PBS洗滌,破膜后用平板菌落計數法檢測CFU,比較受試菌對細胞的黏附力。結果顯示在生物膜狀態和浮游狀態下,傷寒沙門菌質粒pRST98對宿主細菌的黏附力無明顯差異(P>0.05)。除E.coli外,其余幾種受試菌在生物膜狀態下對細胞的黏附力明顯增強,與浮游狀態比較差異有統計學意義(P<0.05)。與大腸埃希菌相比,鼠傷寒沙門菌對CT26細胞的黏附力更強,見圖2。
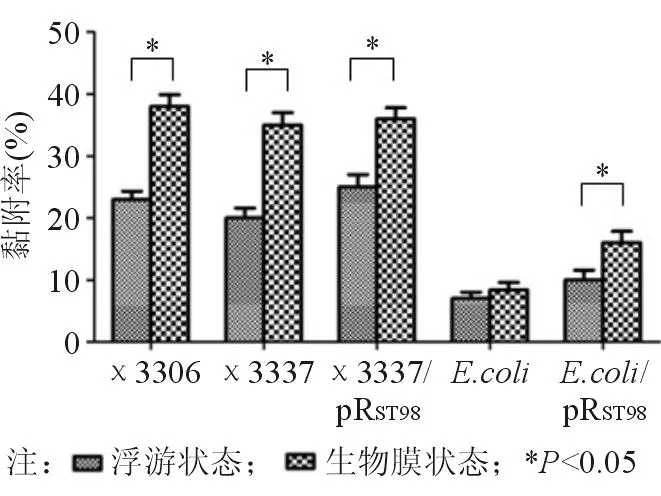
圖2 傷寒沙門菌質粒pR ST98對不同狀態下受試菌黏附CT26細胞的影響
三、傷寒沙門菌質粒pR ST98對不同狀態下受試菌侵襲CT26細胞的影響
傷寒沙門菌質粒pRST98在生物膜和浮游狀態下對宿主菌侵襲CT26細胞的能力均無明顯影響,生物膜的形成能抑制各受試菌對CT26細胞的侵襲能力。生物膜狀態的鼠傷寒沙門菌對細胞的侵襲力與浮游狀態相比明顯下降(P<0.01),大腸埃希菌在生物膜狀態下對細胞的侵襲力也低于浮游狀態(P<0.05)。見圖3。
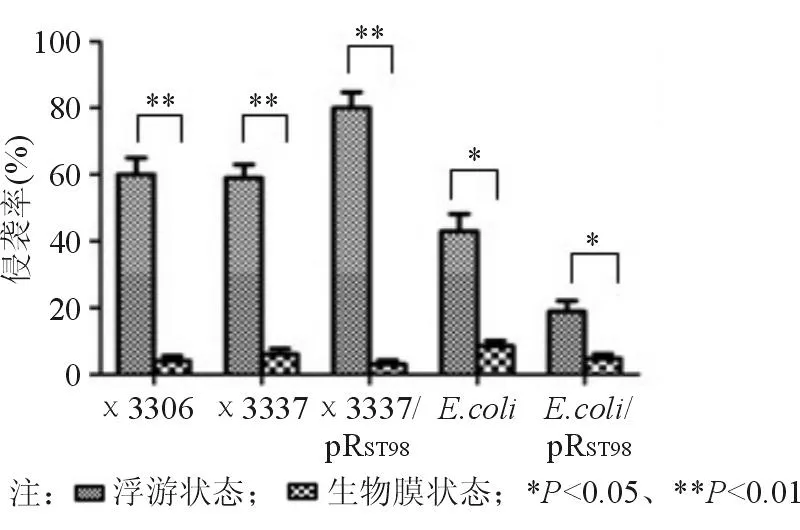
圖3 傷寒沙門菌質粒pR ST98對不同狀態下受試菌侵襲CT26細胞的影響
四、傷寒沙門菌質粒pR ST98對不同狀態下受試菌抗血清殺菌能力的影響
χ3337/pRST98無論是浮游狀態還是生物膜狀態,其抗兔血清和豚鼠血清殺菌能力均明顯高于χ3337(P均<0.05)。由此可見,傷寒沙門菌質粒pRST98能明顯提高宿主細菌不同狀態下的抗血清殺傷能力。生物膜狀態下的χ3306、χ3337和χ3337/pRST98在兔血清和豚鼠血清中的存活率均高于浮游狀態的細菌(P<0.05),見圖4、圖5。
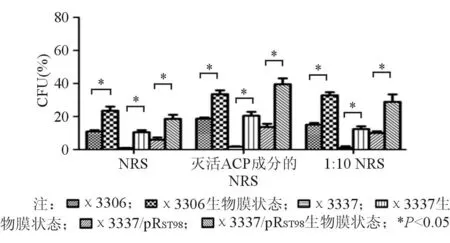
圖4 傷寒沙門菌質粒pR ST98對不同狀態下受試菌兔血清殺菌抵抗力的影響
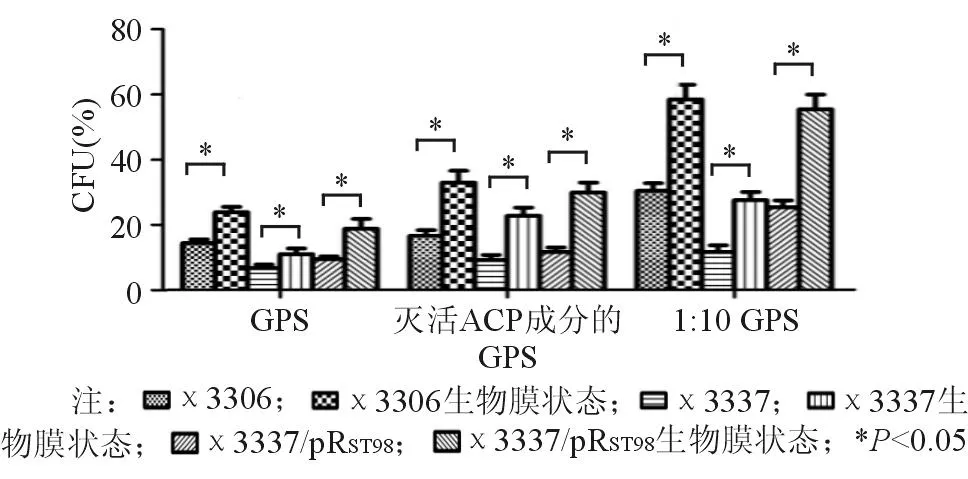
圖5 傷寒沙門菌質粒pR ST98對不同狀態下受試菌豚鼠血清殺菌抵抗力的影響
無論是在浮游狀態還是生物膜狀態下,E.coli/pRST98抗兔血清和豚鼠血清殺菌能力均明顯高于E.coli,說明傷寒沙門菌質粒pRST98能明顯提高大腸埃希菌抗血清殺傷能力。生物膜狀態的E.coli和E.coli/pRST98在兔血清和豚鼠血清中的存活率均高于浮游狀態(P<0.05),見圖6。
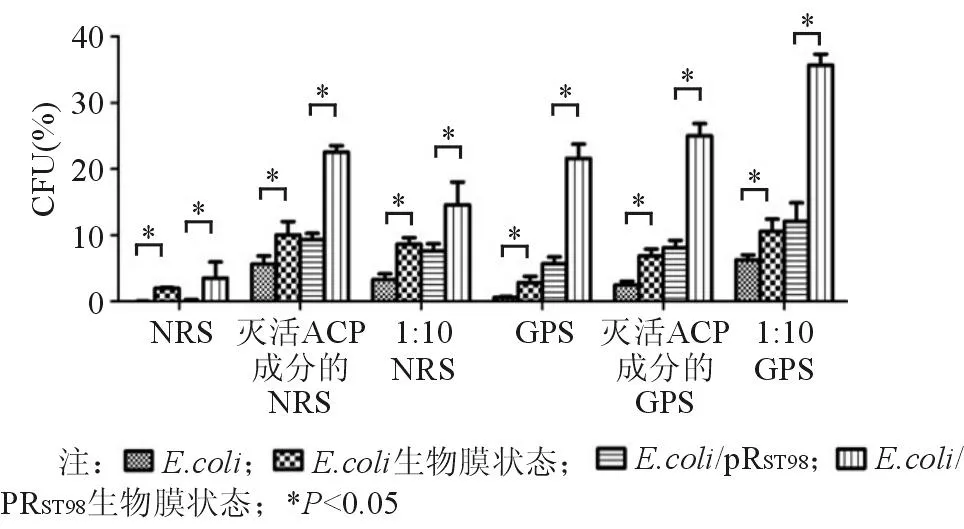
圖6 傷寒沙門菌質粒pR ST98對不同狀態下 E. coli抗血清殺菌能力的影響
五、傷寒沙門菌質粒pR ST98對不同狀態下的受試菌抗巨噬細胞吞噬作用的影響
在不同時間點,巨噬細胞內鼠傷寒沙門菌數量不一;且隨著時間延長,細胞內的活菌數量下降。生物膜狀態下的鼠傷寒沙門菌在巨噬細胞內的存活率明顯高于浮游狀態(P<0.05)。說明在生物膜狀態下,細菌抗巨噬細胞吞噬能力增強。在不同狀態下和各時間點,χ3337/pRST98在巨噬細胞內的存活率均高于χ3337(P<0.05)。說明傷寒沙門菌質粒pRST98在浮游狀態和生物膜狀態下均能促進宿主菌抵抗巨噬細胞吞噬的能力。見圖7。
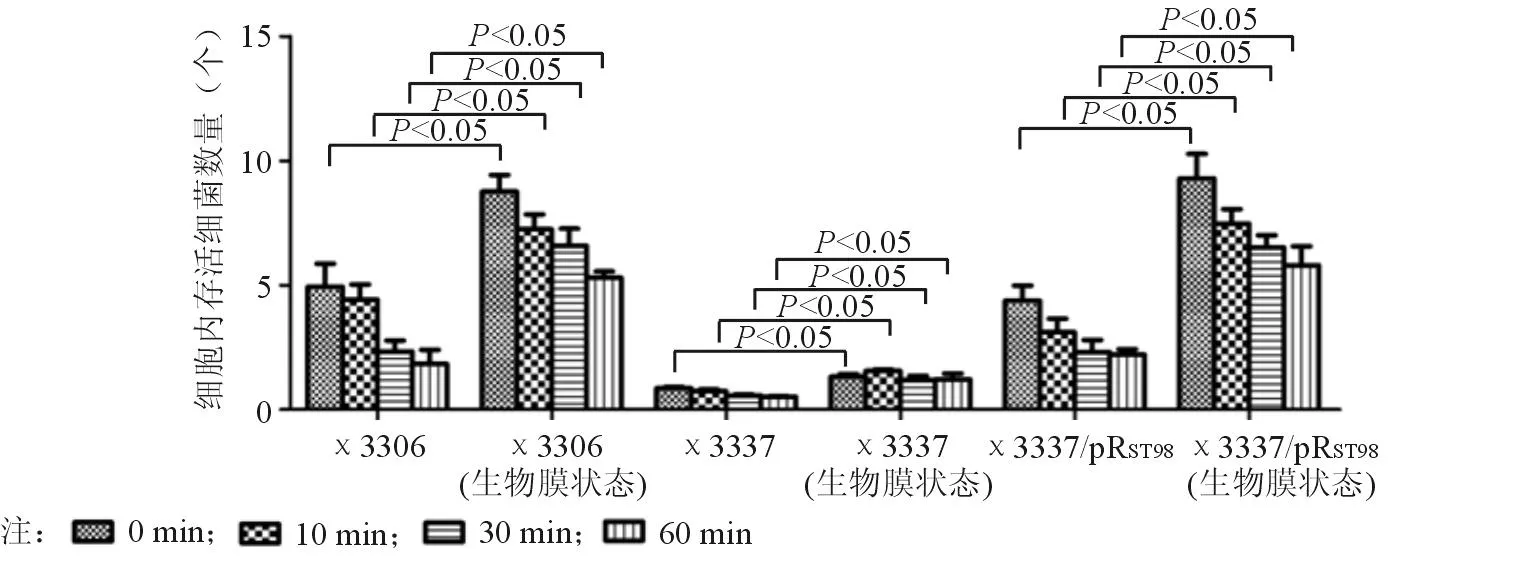
圖7 傷寒沙門菌質粒pR ST98對不同狀態下鼠傷寒沙門菌抵抗巨噬細胞吞噬殺傷的影響
討論
傷寒沙門菌質粒pRST98能明顯促進鼠傷寒沙門菌和大腸埃希菌在實驗室條件下形成生物膜。既往研究已經證實接合性質粒能促進多種細菌形成生物膜。本研究首次在鼠傷寒沙門菌中證實此聯系。另外與大腸埃希菌相比,鼠傷寒沙門菌形成生物膜的能力較強。宿主菌的遺傳背景影響了接合性質粒促進細菌形成生物膜的過程。
傷寒沙門菌質粒pRST98不僅能促進游離狀態宿主細菌的毒力,也能促進生物膜狀態下宿主細菌抗血清殺菌和抗巨噬細胞吞噬的能力。有文獻[9]報道,除傷寒沙門菌外所有致病沙門菌均有約8 Kb的與細菌血清抗性、黏附和定居有關的高度保守序列——沙門菌質粒毒力(Salmonellaplasmid virulence,spv)基因。傷寒沙門菌質粒pRST98上存在與spv基因中spvR和spvB同源性達99.6%的毒力基因片段。既往研究證實傷寒沙門菌質粒pRST98能促進宿主細菌形成生物膜,生物膜的形成有利于接合性質粒在不同宿主菌之間的接合轉移[10]。 這兩方面可以互相影響,彼此促進,加劇感染和疾病。
本研究結果顯示細菌生物膜的形成能明顯影響細菌的黏附侵襲、抗血清殺菌和抵抗巨噬細胞吞噬能力。菌毛是細菌生物膜的重要組分,這可能導致本研究中生物膜狀態下的鼠傷寒沙門菌χ3306、χ3337、χ3337/pRST98和E.coli/pRST98對CT26細胞的黏附力明顯增高。但是E.coli在兩種狀態下對細胞的黏附力無明顯差異,這可能與E.coli的弱毒性相關。
有研究報道,細菌csgD基因的表達能抑制沙門菌1型Ⅲ型分泌系統效應蛋白如SopE2 和 SipA的表達,而csgD基因是細菌生物膜形成的關鍵基因[11]。CRULL等[12]在小鼠模型中發現,生物膜的形成能抑制鼠傷寒沙門菌侵襲腫瘤細胞。本研究在體外細胞模型中也證實了鼠傷寒沙門菌和大腸埃希菌在生物膜狀態對細胞的侵襲力明顯降低。在兩種不同的狀態下,與大腸埃希菌相比,鼠傷寒沙門菌對CT26細胞的侵襲力更高。這是因為CT26細胞是小鼠結腸癌細胞,鼠傷寒沙門菌對其親和力較強。探討不同狀態下細菌對細胞黏附及侵襲性的差異在利用細菌作為工具開發抗腫瘤治療方案的領域具有重要的意義。
生物膜的形成可以誘導微生物某些重要基因的表達發生改變,以適應不利的環境壓力[13]。大腸埃希菌的基因表達分析顯示,生物膜能促進細菌中某些毒力基因的表達[14]。位于鼠傷寒沙門菌2型毒力島上的毒力基因sipA的表達隨著生物膜的形成而增加。而此基因突變會影響沙門菌生物膜的形成量。這說明了生物膜與細菌毒力之間有密切的聯系。銅綠假單胞菌作為研究生物膜的代表細菌,已有充分數據說明生物膜狀態和浮游狀態下的銅綠假單胞菌的表型有明顯差異[15]。
細菌生物膜形成導致毒力產生變化,使人體的免疫系統不能有效地清除相關病原菌,導致某些部位出現遷延難治的感染癥狀。基因水平的研究結果顯示,與浮游狀態相比,生物膜狀態下某些毒力基因的表達增加;而且在生物膜形成進程中可以發現,隨著生物膜的成熟,毒力基因的表達量呈上升趨勢[16]。另一種解釋是細菌生物膜的形成可能導致細菌某些病原相關抗體的隱藏,從而導致機體免疫系統不能及時發現病原菌并對其進行攻擊殺傷。研究從慢性生物膜感染患者體內分離到的細菌發現,這些細菌失去了鞭毛和菌毛等。在體外成熟的銅綠假單胞菌生物膜中分離到的銅綠假單胞菌也具有同樣的特征。細菌的這些變異是導致毒力差異的原因[17]。
參考文獻
[1]BROWNE SH,HASEGAWA P,OKAMOTO S,et al. Identification ofSalmonellaSPI-2 secretion system components required for SpvB-mediated cytotoxicity in macrophages and virulence in mice [J]. FEMS Immunol Med Microbiol,2008,52(2): 194-201.
[2]LI H,XU H,ZHOU Y,et al. The phosphothreonine lyase activity of a bacterial type Ⅲ effector family [J]. Science,2007,315(5814): 1000-1003.
[3]JANTSCH J,CHIKKABALLI D,HENSEL M. Cellular aspects of immunity to intracellularSalmonellaenterica[J]. Immunol Revi,2011,240(1):185-195.
[4]GONZALEZ-ESCOBEDO G,MARSHALL JM,GUNN JS. Chronic and acute infection of the gall bladder bySalmonellatyphi: understanding the carrier state [J]. Nat Rev Microbiol,2011,9(1):9-14.
[5]TOVAL F,K?HLER CD,VOGEL U,et al. Characterization ofEscherichiacoliisolates from hospital inpatients or outpatients with urinary tract infection [J]. J Clini Microbiol,2014,52(2):407-418.
[6]黃瑞, 吳淑燕,聞玉梅. 傷寒桿菌耐藥質粒pRST98介導細菌毒力的研究[J]. 中華微生物學與免疫學雜志,2001,21(3):302-305.
[7]ROE DE,WEINBERG A,ROBERTS MC. Mobile rRNA methylase genes coding for erythromycin resistance inActinobacillusactinomycetemcomitans[J]. J Antimicrob Chemother,1996,37(3): 457-464.
[8]PARK JM,GRETEN FR,LI ZW,et al. Macrophage apoptosis by anthrax lethal factor through p38 MAP kinase inhibition [J]. Science,2001,297(5589): 2048-2051.
[9]YGBERG SE,CLEMENTS MO,RYTK?NEN A,et al. Polynucleotide phosphorylase negatively controls spv virulence gene expression inSalmonellaenterica[J]. Infect Immun,2006,74(2): 1243-1254.
[10]MADSEN JS,BURM?LLE M,HANSEN LH,et al. The interconnection between biofilm formation and horizontal gene transfer [J]. FEMS Immunol Med Microbiol,2012,65(2):183-195.
[11]MIKA F,HENGGE R. Small regulatory RNAs in the control of motility and biofilm formation inE.coliandSalmonella[J]. Int J Mol Sci,2013,14(3):4560-4579.
[12]CRULL K,ROHDE M,WESTPHAL K,et al. Biofilm formation bySalmonellaentericaserovar Typhimurium colonizing solid tumours [J]. Cell Microbiol,2011,13(8):1223-1233.
[13]LIU Z,NIU H,WU S,et al. CsgD regulatory network in a bacterial trait-altering biofilm formation [J]. Emerg Microbes Infect,2014,3(1): e1.
[14]AL SAFADI R,ABU-ALI GS,SLOUP RE,et al. Correlation between in vivo biofilm formation and virulence gene expression inEscherichiacoliO104:H4 [J]. PLoS One,2012,7(7):e41628.
[15]JAIN R,BEHRENS AJ,KAEVER V,et al. Type Ⅳ pilus assembly inPseudomonasaeruginosaover a broad range of cyclic di-GMP concentrations [J]. J Bacteriol,2012,194(16):4285-4294.
[16]MONTEIRO C,FANG X,AHMAD I,et al. Regulation of biofilm components inSalmonellaentericaserovar Typhimurium by lytic transglycosylases involved in cell wall turnover [J]. J Bacteriol, 2011,193(23):6443-6451.
[17]SAUER K,CAMPER AK,EHRLICH GD,et al.Pseudomonasaeruginosadisplays multiple phenotypes during development as a biofilm [J]. J Bacteriol,2002,184(4):1140-1154.
(本文編輯:龔曉霖)

