Sensititre?結核藥敏板檢測結核分枝桿菌藥敏的方法學研究
王 浩,趙 青,陳妹紅(.河北省保定市傳染病醫院檢驗科,河北 保定 07000;.河北省保定市兒童醫院檢驗科,河北 保定 07000;3.河北省保定市第一中心醫院功能科,河北 保定 07000)
?
·論著·
病醫院主管技師,從事臨床病原微生物診斷研究。
Sensititre?結核藥敏板檢測結核分枝桿菌藥敏的方法學研究
王浩1,趙青2,陳妹紅3*(1.河北省保定市傳染病醫院檢驗科,河北 保定 071000;2.河北省保定市兒童醫院檢驗科,河北 保定 071000;3.河北省保定市第一中心醫院功能科,河北 保定 071000)
[摘要]目的評價使用Sensititre?結核藥敏板進行結核分枝桿菌藥敏試驗的價值。方法分別使用Sensititre?結核藥敏板和L-J比例法對124株結核分枝桿菌復合群的臨床分離株進行藥敏試驗(包括異煙肼、利福平、乙胺丁醇、鏈霉素、氧氟沙星、莫西沙星、阿米卡星、利福布汀、對氨基水楊酸、乙硫異煙肼、環絲氨酸、卡那霉素),并將兩法結果進行比較。結果使用Sensititre?結核藥敏板和L-J比例法對124株結核分枝桿菌復合群的臨床分離株進行異煙肼、利福平、乙胺丁醇、鏈霉素、氧氟沙星、莫西沙星、阿米卡星、利福布汀、對氨基水楊酸、乙硫異煙肼、環絲氨酸、卡那霉素等12種藥物的敏感性試驗。其敏感度、特異度均較好。各藥的符合率都達到了90.0%以上。結論使用Sensititre?結核藥敏板所得的藥敏結果與傳統的L-J比例法有較高的一致性,且其檢測時間較短、操作更為簡單,同時還能獲得抗結核藥物的最低抑菌濃度值。
[關鍵詞]結核分枝桿菌;微生物敏感性試驗;治療結果
doi:10.3969/j.issn.1007-3205.2016.02.016
近年來,結核分枝桿菌的耐藥性問題正在形成并呈上升態勢,已嚴重影響人們的健康。世界衛生組織估計每年新發的耐多藥結核(multi drug resistant tuberculosis,MDR-TB)病例約500 000起,而其中耐藥結核發生率較高的國家里就有中國。在我國,各地結核病實驗室一般都是采用絕對濃度法或者L-J比例法進行結核分枝桿菌的藥敏試驗,但世界衛生組織一直在倡導使用液體培養基去做細菌的藥物敏感性試驗[1]。在本研究中,我們使用了美國賽默飛世爾公司生產的Sensititre?結核藥敏板,這是一款專門用于測驗結核分枝桿菌復合群藥物敏感性試驗的藥敏板,采用的是微量肉湯稀釋法,通過一次檢測即可獲得12種一、二線抗結核藥物的藥敏結果,同時又可得到該細菌的最低抑菌濃度值(minimum inhibitory concentration,MIC),現報告如下。
1資料與方法
1.1標本來源本研究所涉及的124株結核分枝桿菌系河北省保定市傳染病醫院結核科2013年8月—2014年4月期間住院患者的痰標本培養物,經菌種鑒定的結核分枝桿菌復合群(本研究所有菌種均使用由杭州創新生物檢控技術有限公司生產的結核分枝桿菌抗原檢測試劑鑒定為結核分枝桿菌)。參照菌株系用標準菌株H37Rv(ATCC 27294),購于中國藥品生物制品檢定所。
1.2主要試劑與儀器
1.2.1L-J比例法相關試劑鏈霉素、異煙肼、利福平、乙胺丁醇、氧氟沙星、卡那霉素、阿米卡星、對氨基水楊酸、利福布汀、莫西沙星等含藥羅氏培養管以及對照用中性羅氏培養管均購自珠海貝索生物技術有限公司。環絲氨酸、乙硫異煙肼的含藥羅氏培養管為本室自配,原料購自Sigma公司[2]。
1.2.2Sensititre?結核藥敏板相關試劑Sensititre?結核藥敏板、含玻璃珠的吐溫80鹽水磨菌管、含油酸、白蛋白、葡聚糖、觸媒(OADC)的7H9肉湯管[3]等均購自美國賽默飛世爾科技有限公司。Sensititre?結核藥敏板的藥物排列和藥物濃度,見表1。
表1Sensititre?結核藥敏板的藥物排列和藥物濃度
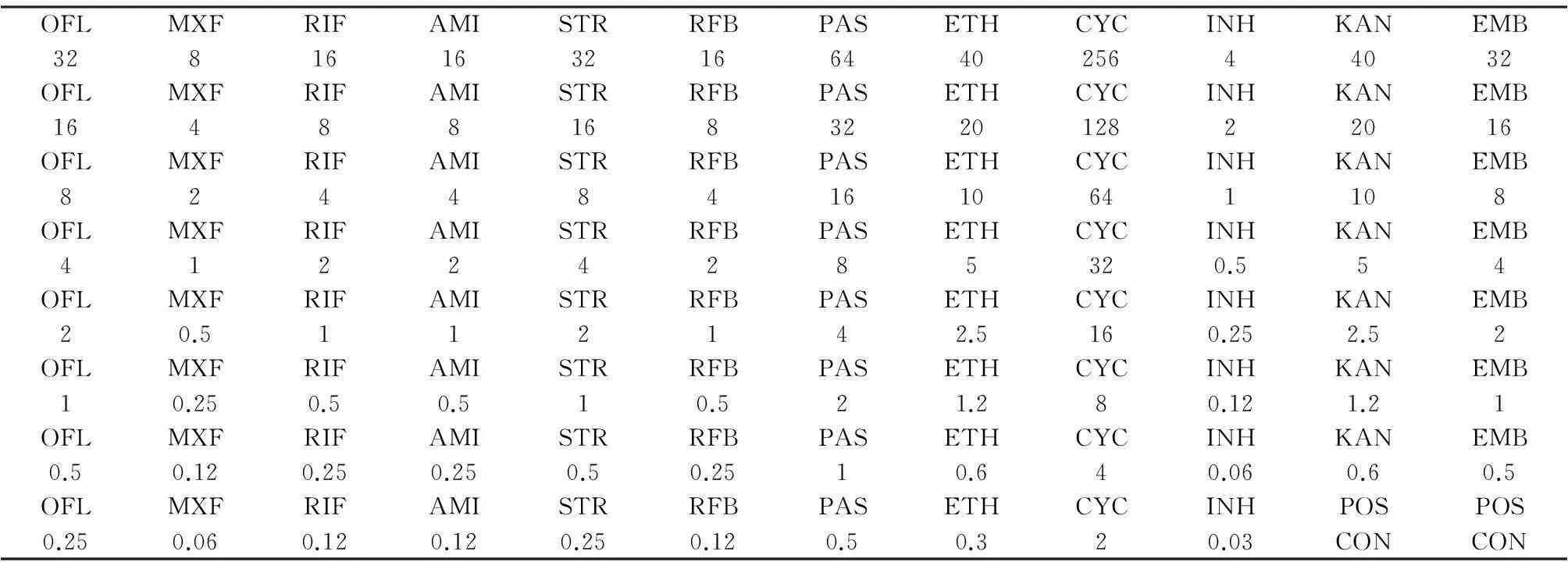
Table 1 Drug arrangement and drug concentration of Sensititre Mtb plate(mg/L)
OFL:氧氟沙星;MXF:莫西沙星;RIF:利福平;AMI:阿米卡星;STR:鏈霉素;RFB:利福布汀;PAS:對氨基水楊酸;ETH:乙硫異煙肼;CYC:環絲氨酸;INH:異煙肼;KAN:卡那霉素;EMB:乙胺丁醇;POS:陽性對照;CON:質控
1.2.3相關儀器漩渦振蕩器:型號MX-F,購自大龍興創實驗儀器(北京)有限公司;12道電子加樣槍、Sensititre?比濁儀以及Vizion藥敏判讀系統均購自美國賽默飛世爾科技有限公司
1.3藥敏試驗24株結核分枝桿菌臨床分離株分別用Sensititre?結核藥敏板和L-J比例法測試其藥物敏感性。將VERSATREK?自動細菌培養儀中報陽結核瓶取出,混勻后抽取瓶中全部菌液,經3 000 g離心15 min,取其沉淀物放入含玻璃珠的吐溫鹽水磨菌管中,之后在漩渦振蕩器上混勻60 s充分研磨后,使用Sensititre?比濁儀調整磨菌管中菌液濃度至1麥氏濁度。
1.3.1L-J比例法吸取1麥氏濁度的菌懸液100 μL,并用生理鹽水稀釋至10-2g/L和10-4g/L的菌懸液,取稀釋好的菌懸液分別接種于含藥培養基和對照培養基。35 ℃培養4周左右,待菌落長好時觀察結果,并計算耐藥百分比,耐藥百分比>1%為耐藥(R)、≤1%為敏感(S)。
1.3.2Sensititre?結核藥敏板將剩余1麥氏濁度的菌懸液用無菌生理鹽水調整至0.5麥氏濁度后,吸取100 μL加到11.5 mL的含OADC的7H9肉湯管中,漩渦振蕩混勻30 s,使接種液最終濃度在5×104~5×105cfu/mL范圍內。使用12道電子加樣槍接種菌液到藥敏板中,每孔100 μL,貼上封板膜后放入35 ℃培養箱培養。根據藥敏板2個生長對照孔(11H孔和12H孔)的生長情況,在10~21 d內使用Vizion藥敏判斷系統進行結果判讀。記錄生長明顯減少的最低抗生素濃度為MIC值,并依據各藥在瓊脂比例法中的關鍵濃度為其判定折點,如果MIC>關鍵濃度為耐藥(R),如果MIC≤關鍵濃度為敏感(S)。
1.4質量控制每周進行質控1次。質控菌株為結核分枝桿菌標準株H37Rv(ATCC 27294),該菌株對所有的抗結核藥均敏感。
1.5統計學方法應用SPSS 11.0軟件進行分析處理,Sensititre?結核藥敏板與L-J比例法藥敏試驗測定時間比較采用t檢驗。P<0.05為差異有統計學意義。
以L-J比例法檢測結果為判斷的標準,計算Sensititre?結核藥敏板的敏感度、特異度和準確度,2種方法檢測結果的一致性用Kappa檢驗,Kappa值≥0.75(阿米卡星除外),說明2種方法具有很好的一致性。阿米卡星的Kappa值略低的原因可能是在124個樣本中耐藥菌株的例數太少造成的。
2結果
2.1試驗時間比較應用Sensititre?結核藥敏板和L-J比例法對124株結核分枝桿菌復合群做藥敏試驗后,Sensititre?結核藥敏板所需試驗時間為10~18 d,平均(15.2±1.9) d,L-J比例法為20~31 d,平均(27.9±3.2) d,Sensititre?結核藥敏板比L-J比例法所需試驗時間短,差異有統計學意義(t=38.001,P<0.01)。
2.2藥敏結果比較使用2種方法對臨床分離到的124株結核分枝桿菌復合群進行異煙肼、利福平、乙胺丁醇、鏈霉素、氧氟沙星、莫西沙星、阿米卡星、利福布汀、對氨基水楊酸、乙硫異煙肼、環絲氨酸、卡那霉素等藥物敏感性試驗,其敏感度、特異度、準確度均在90.0%以上,見表2。
表22種藥敏試驗結果比較
Table 2The comparison of the results in two drug allergy testing experiments
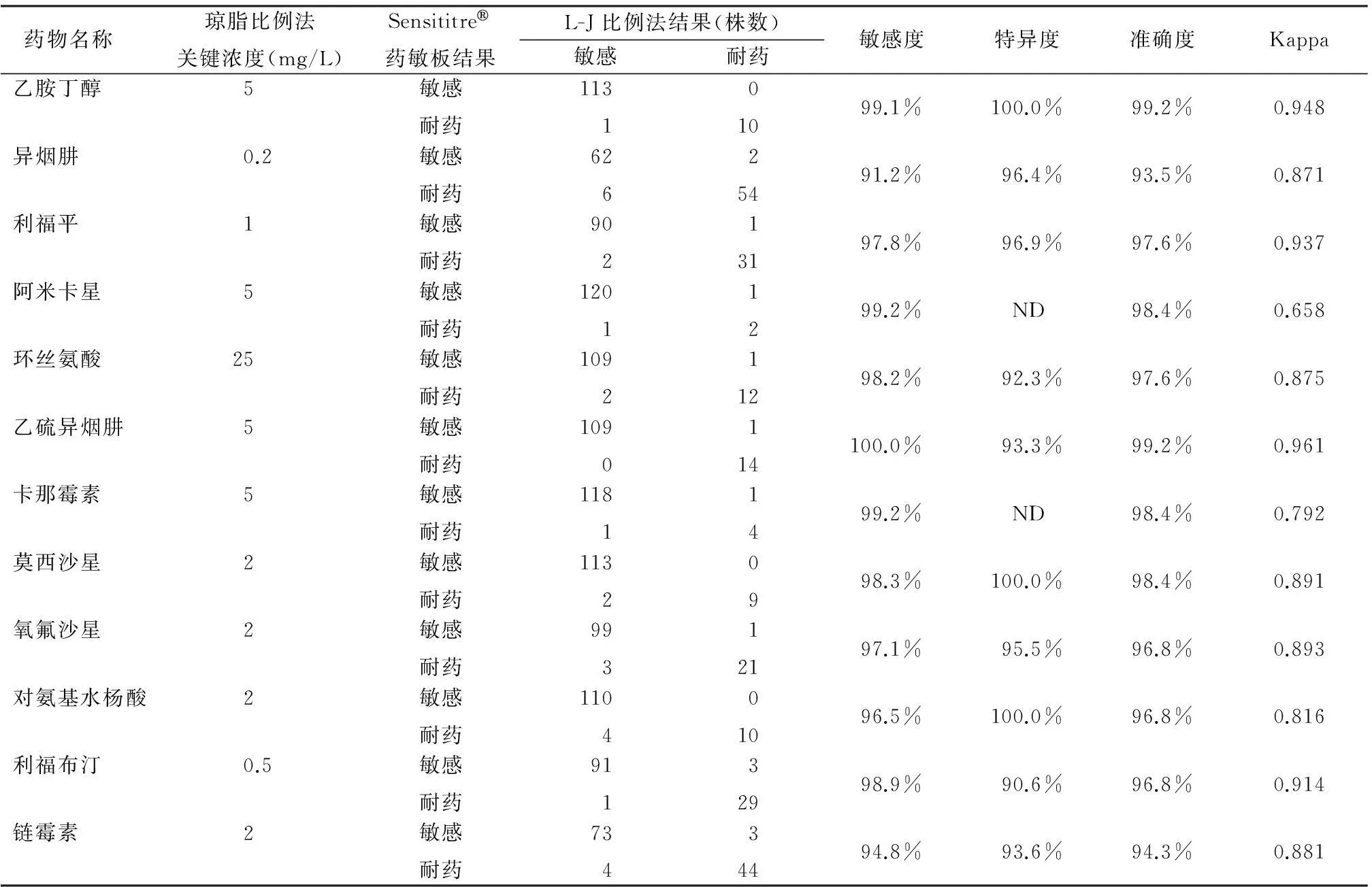
藥物名稱 瓊脂比例法關鍵濃度(mg/L)Sensititre藥敏板結果L-J比例法結果(株數)敏感耐藥敏感度特異度準確度Kappa乙胺丁醇5 敏感耐藥113 101099.1%100.0%99.2%0.948異煙肼0.2敏感耐藥62 625491.2%96.4%93.5%0.871利福平1敏感耐藥90 213197.8%96.9%97.6%0.937阿米卡星5敏感耐藥120 11299.2%ND98.4%0.658環絲氨酸25敏感耐藥109 211298.2%92.3%97.6%0.875乙硫異煙肼5敏感耐藥109 0114100.0%93.3%99.2%0.961卡那霉素5敏感耐藥118 11499.2%ND98.4%0.792莫西沙星2敏感耐藥113 20998.3%100.0%98.4%0.891氧氟沙星2敏感耐藥99 312197.1%95.5%96.8%0.893對氨基水楊酸2敏感耐藥110 401096.5%100.0%96.8%0.816利福布汀0.5敏感耐藥91 132998.9%90.6%96.8%0.914鏈霉素2敏感耐藥73 434494.8%93.6%94.3%0.881
注:ND為not determined的縮寫,由于在124株樣本中耐藥菌株低于10個可能會造成特異度的不準確性
3討論
目前我國結核病年發患者數約為130萬人,占全球發病的14.3%,居全球第2位,耐多藥結核病患者的估計人數居全球第1位。耐多藥/廣泛耐藥結核病的增長,給臨床治療帶來了極大的困難[4]。面對新的挑戰,需要用新的眼光或者說是新的技術來審視抗結核藥物的合理應用,尤其是要重視初治以及非耐多藥結核患者的規范用藥,阻斷耐藥的發生風險,才能最終達到控制耐藥結核病的流行[5]。而采取一種快速、準確、全面的結核菌藥敏試驗技術又是實現抗結核藥物合理使用的基石。
目前,多數醫院廣泛使用的仍然是L-J比例法,其局限性為試驗比較繁瑣,結果受多種因素影響,重復性較差,在得到純培養物后仍需4周時間才可報告結果;同時L-J比例法由于無法測定細菌的MIC值,只能間接推斷該測試藥物的敏感或耐藥,其對結核菌耐藥程度的高低無法作出判定,所以不能運用現在所提倡的藥動學/藥效學結合理論制定抗生素個體化給藥方案[6]。這種傳統藥敏方法的使用遠滯后于臨床診治的需要[7]。本研究中所用美國賽默飛世爾科技有限公司生產的Sensititre?結核藥敏板是一款使用微量肉湯稀釋法檢測MIC值的產品,該藥敏板對每種測試藥物由高到低做了8種或7種藥物濃度,能真實地檢測出MIC值[8]。在本研究中,Sensititre?結核藥敏板試驗平均報告時間為(15.2±1.9) d,明顯短于L-J比例法的(27.9±3.2) d。目前,臨床常用一線抗結核藥異煙肼的耐藥率最高,利福平次之,乙胺丁醇最低。因此,應格外關注復發以及經3個月治療痰檢抗酸桿菌仍陽性的患者是否已耐異煙肼和利福平,及時調整用藥。在目前耐單藥及耐多藥的結核分枝桿菌日益增多的環境下,應該使用肉湯稀釋法檢測MIC值并結合每個具體患者的血藥濃度監測來確定臨床治療方案。但不可否認的是,當前世界各國多數都沒有使用肉湯稀釋法檢測結核分枝桿菌的藥物敏感性,所以也就還未建立其MIC值的藥物敏感性判定界值。在本研究中,依據廠家的推薦,參考瓊脂比例法的關鍵濃度,并將其作為判定藥物敏感性的界值,經過與L-J比例法做對比,兩法具有很好的準確性。國內劉相等[9]也進行了類似的研究,得出了試驗組比傳統固體羅氏培養對照組藥敏試驗時間更短、結果更準確、更能及時服務于臨床的結論。
本研究中,我們也深刻體會到,采用Sensititre?結核藥敏板進行結核分枝桿菌藥敏試驗時需要注意幾個關鍵因素。①最終加入藥敏板微孔中細菌懸液的濃度一定要控制好。如果懸液濃度太高則無法區分孔底沉淀是細菌生長所致還是接種導致,幾個會影響MIC值的判定;如果濃度過低,會導致檢測時間延長。Sensititre?結核藥敏板推薦的濃度5×104~5×105cfu/mL范圍內。②因為要在7H9肉湯中培養較長時間,因此保持整個過程的無菌操作、防止環境菌的污染是非常重要的。如果環境菌污染了藥敏板則將無法正確判讀MIC值。③藥敏板需長時間在35 ℃培養箱中培養,可能會造成微孔內水分蒸發,因此除使用試劑盒中自帶的封板膜封板外,還應將藥敏板放入透明塑料袋內熱合機熱合后再放入培養箱開始培養。④為了防止試驗過程中氣溶膠外泄發生的生物危害以及無菌操作的需要,試驗全程一定要在B2級的生物安全柜中完成[10]。
[參考文獻]
[1]World Health Organization. Treatment of tuberculosis:guidelines for national programmes[S]. 4th ed.Geneva:World Health Organization,2009:420.
[2]王甦民,趙德福,王國治,等.結核病診斷實驗室檢驗規程[M].北京:中國教育文化出版社,2006:46-52.
[3]趙雁林,劉志敏,王海英,等.結核病實驗室標準化操作與網絡建設[M].北京:人民衛生出版社,2013:186-188.
[4]張賀秋,趙雁林,馮曉燕,等.現代結核病診斷技術[M].北京:人民衛生出版社,2013:4-5.
[5]肖和平.抗結核藥物的合理使用是控制耐藥結核病流行的基石[J].中華結核和呼吸雜志,2014,37(10):723-724.
[6]熊旭東.PK/PD參數與抗菌藥物的優化用藥[J].抗感染藥學,2012,9(1):11-13.
[7]孫自鏞,程黎明,管青,等.實驗診斷臨床指南[M].3版.北京:科學出版社,2013:413-414.
[8]Hall L,Jude Clark SL. Evaluation of the Sensititre MycoTB Plate for Susceptibility Testing of the Mycobacterium tuberculosis Complex against First-and Second-Line Agents[J]. J Clin Microbiol,2012,50(11):3732-3734.
[9]劉相,呂翠環,李玉靜,等.兩種不同結核菌藥物敏感試驗方法比較[J].河北醫藥,2012,34(7):1077-1078.
[10]王潔,陸俊梅,黃曉辰,等.微量MIC檢測判斷結核分枝桿菌藥敏的方法學研究[J].中華檢驗醫學雜志,2010,33(4):315-319.
(本文編輯:劉斯靜)
Methodological study of Sensititer tuberculosis drug sensitive plate in detecting mycobacterium tuberculosis
WANG Hao1,ZHAO Qing2,CHEN Mei-hong3*
(1.Depatment of Clinical Laboratory, Infectious Disease Hospital of Baoding City, Hebei Province,
Baoding 071000,China; 2.Depatment of Clinical Laboratory, Children's Hospital of Baoding
City, Hebei Province, Baoding 071000, China; 3.Depatment of Functional Section, the
First Central Hospital of Baoding City, Hebei Province, Baoding 071000, China)
[Abstract]ObjectiveThe present study is designed to evaluate Sensititre? tuberculosis drug sensitive plat in testing antituberculotics sensitivety to mycobacterium tuberculosis.MethodsTo assess the effectiveness of Sensititre? tuberculosis drug sensitive plat,the sensitivety of different antituberculotics(isoniazid, rifampicin, ethambutol, streptomycin, levofloxacin, moxifloxacin, Amikacin, rifabutin, para aminosalicylic acid, ethionamide, cycloserine, kanamycin) was tested on 124 strains of Mycobacterium tuberculosis complex from clinical isolates by Sensititre? tuberculosis drug sensitive plat or L-J propotion method.ResultsThe sensitivity and specifity of Sensititre? tuberculosis drug sensitive plat in testing the antituberculotics sensitivety were about 90.0% or more,which was compared with the L-J proportion method.ConclusionThe effectiveness of Sensititre? tuberculosis drug sensitive plat was consistent with that from the L-J proportion method,but it shortened the test duration and was more convenient.In addition,Sensititre? tuberculosis drug sensitive plat can get minimum inhibitory concentrations of the different antituberculotics.
[Key words]mycobacterium tuberculosis;microbial sensitivity tests;treatment outcome
[中圖分類號]R378.911
[文獻標志碼]A
[文章編號]1007-3205(2016)02-0187-04
通訊作者*。E-mail:bd7577637@sina.com
[作者簡介]王浩 (1977-),男,河北保定人,河北省保定市傳染
[收稿日期]2015-04-24;[修回日期]2015-06-25

