經導管去腎交感神經術治療高血壓性心臟病合并心衰患者的效果分析
夏大勝,盧成志,王麗
?
經導管去腎交感神經術治療高血壓性心臟病合并心衰患者的效果分析
夏大勝,盧成志,王麗
摘要:目的評估經導管去腎交感神經術(RDN)治療高血壓性心臟病合并收縮性心衰患者的有效性。方法對2例高血壓性心臟病合并心衰患者進行RDN,于術前及術后1年行心臟彩超、6分鐘步行試驗和腎功能、糖化血紅蛋白、N-末端腦鈉肽前體(NT-ProBNP)等檢查,評估治療效果。結果2例患者行RDN后,腎動脈造影顯示腎動脈無狹窄及夾層等并發癥。1年后隨訪,2例患者的6分鐘步行試驗結果、左室射血分數、NT-proBNP等心功能指標明顯改善,左心室明顯減小。結論RDN對高血壓性心臟病合并收縮性心衰患者的治療有效、可行。
關鍵詞:經導管去腎交感神經術;收縮性心衰;高血壓
高血壓是心衰發生、發展的重要病因。隨著高血壓的不斷進展,心室發生重構,心衰發生率不斷增加。高血壓與心衰具有共同的發病機制——交感神經過度激活,這就意味著阻斷交感神經活性可以同時改善高血壓性心臟病以及心衰的進程。近年來,經導管去腎交感神經術(renal sympathetic denerva?tion, RDN)用于治療頑固性高血壓及心衰的安全性及有效性已經得到證實。然而,用RDN治療高血壓性心臟病合并收縮性心衰的研究甚少。本研究近期采用RDN治療高血壓性心臟病合并收縮性心衰患者2例,效果較好,報告如下。
1 資料與方法
1.1病例資料例1男,33歲,主因“咳嗽、咳痰2個月余,活動后憋氣3 d”于2013年12月15日入院。2個月前患者無明顯誘因出現咳嗽、咳痰,為白黏痰,痰不易咳出,入院前3 d上三樓后出現胸悶、氣短,持續數分鐘,休息后緩解,就診于當地醫院,行胸X線片檢查提示:急性支氣管炎,心臟擴大,心尖左移,予以口服頭孢克洛抗感染治療后咳嗽、咳痰好轉,為進一步診治就診于我院。查體:體質指數(BMI)29.4 kg/m2,體溫36.5℃,脈搏頻率83次/min,呼吸頻率16次/min,血壓(BP)156/105 mmHg(1 mm Hg=0.133 kPa),心界擴大,心音低頓,心律齊,各瓣膜未及明顯雜音,雙下肢無水腫。既往高血壓病史15年,血壓最高180/120 mmHg,未規律服藥。入院實驗室檢查回報:N-末端腦鈉肽前體(NT-ProBNP)2 190 ng/L。糖耐量+胰島素激發試驗結果:糖耐量受損、高胰島素血癥。心電圖:竇性心律,左室高電壓,V4~V6導聯ST段壓低,廣泛導聯T波倒置。心臟彩超:左室射血分數(LVEF)= 0.38,全心增大,左心功能降低,左室壁增厚,二尖瓣關閉不全(輕~中度),主動脈關閉不全(輕度)。冠狀動脈+腎動脈造影均未見血管狹窄。入院診斷:(1)高血壓性心臟病、心功能不全、心功能Ⅲ級(NYHA)。(2)高血壓病3級、很高危。(3)糖耐量受損、高胰島素血癥。
例2男,37歲,主因“喘憋1周、加重2 d”于2014年4月21日入院。患者1周前活動后出現喘憋,休息后可緩解,伴咳嗽、無痰,予口服克拉霉素后癥狀未緩解。入院前2 d,患者上述癥狀加重,不能平臥,端坐時仍有憋氣、喘息出現,每天均有夜間陣發性呼吸困難,遂就診于我院。既往高血壓病史10余年,血壓最高180/120 mmHg,未規律服用降壓藥。入院查體:BMI 30.1 kg/m2,脈搏頻率93次/min,血壓150/120 mmHg,心肺查體未見明顯異常,雙下肢無水腫。實驗室檢查回報:肌酐(Cr)143.90 μmol/L,尿素氮(BUN)10.28 mmol/L, NT-proBNP 4 282 ng/L。糖耐量+胰島素激發試驗結果:糖尿病、高胰島素血癥。心電圖:竇性心律,W-P-W綜合征。心臟彩超: LVEF=0.31,全心增大,左心功能降低(重度),左室壁增厚,二尖瓣、肺動脈瓣關閉不全(輕度),心包積液(少量)。冠狀動脈造影:前降支中段狹窄50%,回旋支遠段狹窄90%。腎動脈造影:未見血管狹窄。入院診斷:(1)心功能不全、心功能Ⅳ級(NYHA)。(2)高血壓病3級、很高危。(3)心包積液。(4)2型糖尿病、高胰島素血癥。(5)腎功能不全。
1.2生化指標檢測入院后空腹12 h,次日清晨采血10 mL,使用日立H7600全自動生化分析儀測定肝腎功能、血脂等,試劑由北京利德曼生化技術有限公司提供。估算的腎小球濾過率(estimated glomerular filtration rate,eGFR)采用簡化的腎臟病飲食改良方程(MDRD): eGFR = 186×[Cr(μmol/L)/ 88.4]-1.154×年齡-0.203×(0.742女性)。
1.3其他相關檢查完善泌尿系超聲、腎上腺CT、立臥位實驗等檢查排除繼發性高血壓,并且完成糖耐量+胰島素激發試驗、6分鐘步行試驗、超聲心動圖等。
1.4RDN經入選患者簽署知情同意書、報備我院倫理委員會同意后,行RDN:患者平臥位,經右肱動脈穿刺,行雙側腎動脈造影。腎動脈造影排除解剖異常后行雙側腎動脈射頻消融術。將6F射頻導管(Celsius,Biosense Webster公司,美國)連接射頻消融儀(EP-SHUTTLE,Biosense Webster公司,美國),在患者背部貼上無透視標尺,如圖1所示,將導管頭端送至腎動脈遠段,由遠至近分別在上壁、下壁、前壁、后壁螺旋形點狀消融4~6個點,每個點至少距離5 mm以上,8~12 W消融2 min,在消融期間,監測導管尖端溫度和阻抗,消融過程中溫度波動于45~60℃。退出消融導管送至另一側腎動脈近段,行對側腎動脈點狀消融。經肱動脈入路的患者于穿刺處局部壓迫止血,彈力繃帶加壓包扎[1]。
2 結果
2.1RDN后造影結果腎動脈造影顯示,患者無腎動脈狹窄、夾層等并發癥出現,見圖1。
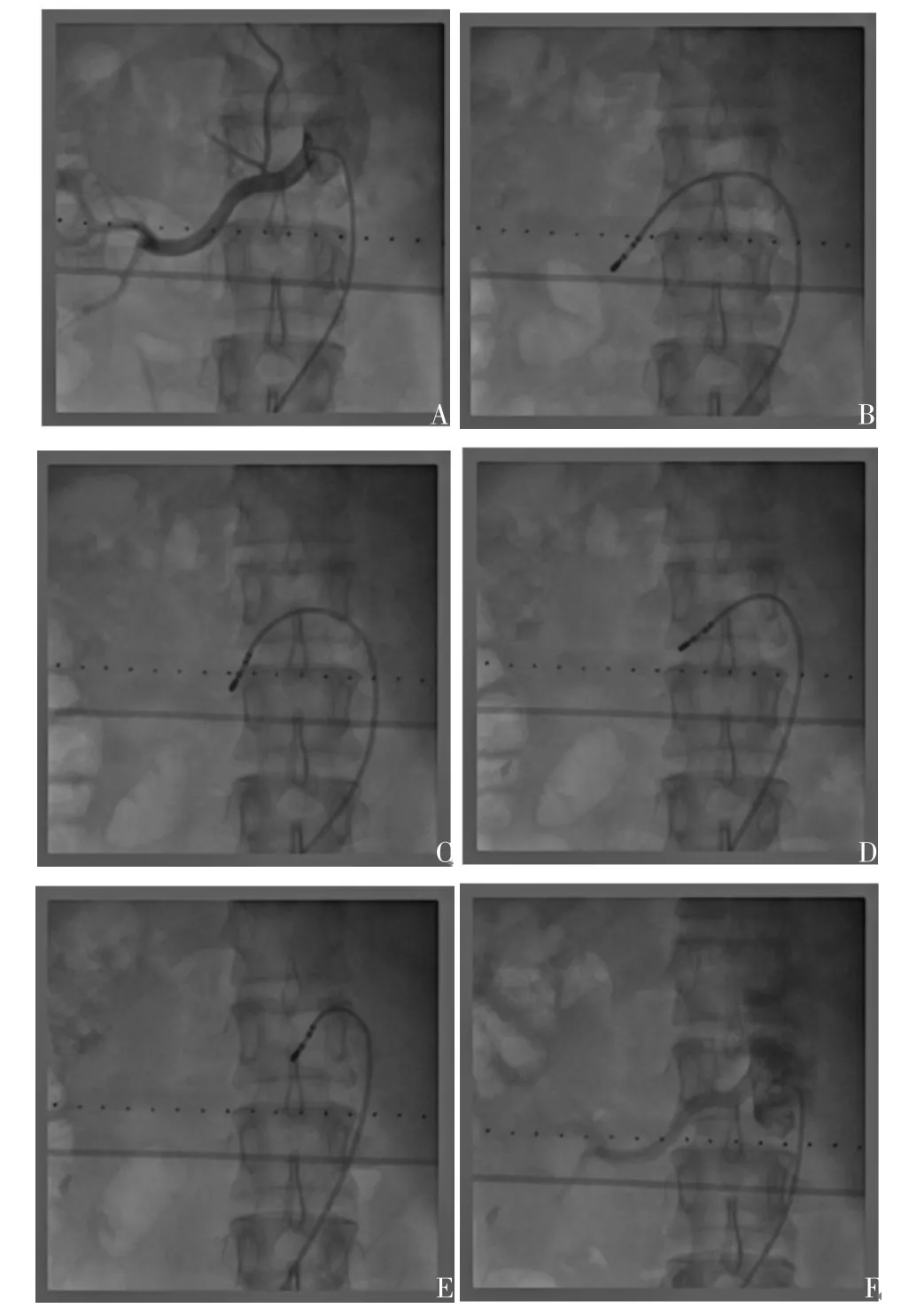
Fig. 1 The procedural of RDN [A:renal angiography before RDN showing no stenosis; B, C, D and E:renal artery abltion in different sites (superior wall,inferior wall, anterior wall and posterior wall);F:renal angiography after RDN showing no stenosis in renal artery]圖1 RDN過程[A:消融前腎動脈造影,顯示腎動脈無狹窄;B、C、D、E:不同位置(上壁、下壁、前壁、后壁)腎動脈消融;F:消融后腎動脈造影,腎動脈無狹窄]
2.2RDN前后彩超及腎功能結果經過1~1.5年的隨訪,2例患者心衰癥狀明顯改善,6分鐘步行試驗改善,LVEF明顯升高,心腔結構變小,血壓降低,腎功能改善,1年內未再因心衰或高血壓入院,見圖2,表1、2。

Fig. 2 Comparison of cardiac ultrasound before and after RDN圖2 例2患者RDN前后心臟彩超對比
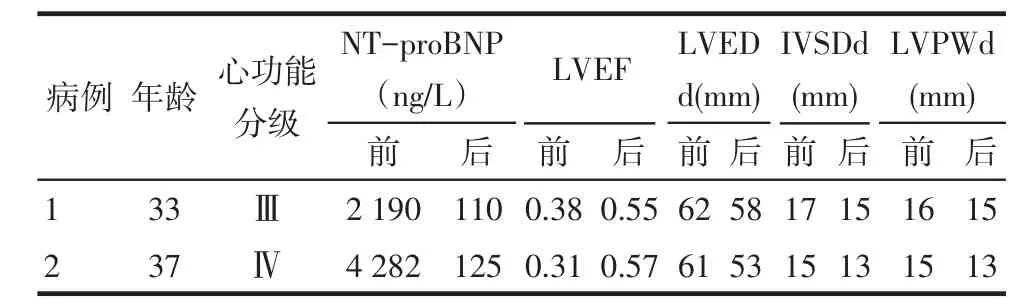
Tab. 1 Comparison of NT-proBNP and the data of cardiac ultrasound between pre- RDN and post-RDN表1 RDN前后NT-proBNP和心臟彩超參數比較

Tab. 2 Comparison of renal function between pre- and post-RDN表2 RDN前后腎功能參數比較
3 討論
高血壓和慢性心衰通常存在交感神經(SNS)過度激活,腎素-血管緊張素系統活性增加,多種炎性因子釋放[2]。在這些激活的神經內分泌系統中,SNS對心血管疾病預后起到了至關重要的作用,并且與NYHA心功能分級直接相關[3]。長期交感神經過度激活會加速心衰進展,其主要表現為血漿去甲腎上腺素(NE)水平增加、LVEF下降和高病死率。RDN可以降低腎和全身交感神經系統活性[4-5],降低循環中NE水平[6-7],降低血壓,減輕左室肥厚并改善心功能[8]。目前許多基礎研究結果顯示RDN對于心衰有一定的治療作用,臨床前期先導性研究(REACH-Pi?lot)結果已顯示了RDN治療慢性心衰患者的有效性及安全性[9]。
回顧本研究中的受試對象具有如下特點:(1)均為青年高血壓性心臟病患者。(2)心功能較差,LVEF<0.40,心衰癥狀明顯,NT-proBNP明顯升高。(3)高血壓病程長,血壓控制的較差。(4)合并糖代謝異常,高胰島素血癥。(5)例2患者合并慢性腎功能不全。(6)2例患者的體質指數較大,符合代謝綜合征診斷標準。
大量研究表明,心衰合并高血壓、糖代謝異常與交感神經活性亢進密切相關[10]。綜合患者如上的特點,以及既往大量的研究已證實RDN能夠降低血壓、改善心功能、糖代謝異常[9-10]。本研究選取年輕的心衰合并高血壓患者為研究對象,對其進行RDN,1年后隨訪,患者的癥狀明顯改善,NT-proBNP明顯降低,血壓明顯下降,LVEF明顯升高,左室重構改善,6分鐘步行試驗改善,腎功能可見好轉趨勢。分析其中原因可能與適應證選擇合理以及腎動脈消融效果較好有關,但仍需增加樣本量進一步證實。
參考文獻
[1] Wang L,Lu CZ,Zhang X,et al. The effect of catheter based renal symthetic denervation on renin angiotensin aldosterone system inpa?tients with resistant hypertension[J].Chin J Cardiol,2013, 41(1):3-7.[王麗,盧成志,張欣,等.經皮腎臟交感神經射頻消融術對難治性高血壓患者RAAS的影響[J].中華心血管病雜志,2013,41(1):3-7].
[2] Glezeva N, Baugh JA. Role of inflammation in the pathogenesis of heart failure with preserved ejection fraction and its potential as a therapeutic target[J]. Heart Fail Rev, 2014,19(5):681- 694. doi: 10.1007/s10741-013-9405-8.
[3] Ferguson DW, Berg WJ, Sanders JS. Clinical and hemodynamic cor?relates of sympathetic nerve activity in normal humans and patients with heart failure: evidence from direct microneurographic record?ings[J]. J Am Coll Cardiol, 1990,16(5):1125-1134.
[4] Hering D, Lambert EA, Marusic P, et al. Substantial reduction in single sympathetic nerve firing after renal denervation in patients with resistant hypertension[J]. Hypertension, 2013,61(2):457-464. doi: 10.1161/HYPERTENSIONAHA.111.00194.
[5] Schlaich MP, Bart B, Hering D, et al. Feasibility of catheter-based renal nerve ablation and effects on sympathetic nerve activity and blood pressure in patients with end-stage renal disease[J]. Int J Car?diol,2013,168(3):2214-2220. doi: 10.1016/j.ijcard.2013.01.218.
[6] Hou Y, Hu J, Po SS, et al. Catheter-based renal sympathetic dener?vation significantly inhibits atrial fibrillation induced by electrical stimulation of the left stellate ganglion and rapid atrial pacing[J]. PLoS One, 2013,8(11):e78218. doi: 10.1371/journal.pone.0078218.
[7] Hu J, Li Y, Cheng W, et al. A comparison of the efficacy of surgical renal denervation and pharmacologic therapies in post-myocardial infarction heart failure[J]. PLoS One, 2014,9(5): e96996. doi: 10.1371/journal.pone.0096996. eCollection 2014.
[8] Brandt MC, Mahfoud F, Reda S, et al. Renal sympathetic denerva?tion reduces left ventricular hypertrophy and improves cardiac func?tion in patients with resistant hypertension[J]. J Am Coll Cardiol, 2012,59(10):901-909. doi: 10.1016/j.jacc.2011.11.034.
[9] Davies JE, Manisty CH, Petraco R, et al. First-in-man safety evalu?ation of renal denervation for chronic systolic heart failure: Primary outcome from REACH-Pilot study[J]. Int J Cardiol, 2013, 162(3): 189-192. doi: 10.1016/j.ijcard.2012.09.019.
[10] McArdle MJ, deGoma EM, Cohen DL,et al. Beyond blood pressure: percutaneous renal denervation for the management of sympathetic hyperactivity and associated disease states[J]. Am Heart Assoc,2016,4(3). doi: 10.1161/JAHA.114.001415.
(2015-09-06收稿2015-10-20修回)
(本文編輯閆娟)
作者單位:天津市第一中心醫院心內科(郵編300192)
Renal sympathetic denervation for the treatment of hypertensive heart disease with systolic heart failure
XIA Dasheng, LU Chengzhi, WANG Li
Department of Cardiology of Tianjin First Center Hospital, Tianjin 300192,China
Abstract:Objective To evaluate the effectiveness of renal sympathetic denervation (RDN) for hypertensive heart dis?ease combined with systolic heart failure. Methods Two patients (mean age 35 years) with hypertensive heart disease com?bined with systolic heart failure on maximal tolerated heart failure therapy underwent bilateral renal denervation. Echocar?diography, the six minute walk distance, renal function, glycosylated hemoglobin and NT-proBNP were assessed at baseline and 1 year after renal denervation. Results Renal artery angiography showed that no stenosis and dissection. After 1 year follow up, the left ventricular ejection fraction (LVEF), six minute walk distance and NT-proBNP were significantly im?proved, and the size of left ventricular decreased. ConclusionRDN is effective and feasible for the treatment in patients with hypertensive heart disease and systolic heart failure.
Key words:renal sympathetic denervation; systolic heart failure; hypertension
中圖分類號:R541
文獻標志碼:B
DOI:10.11958/20150136
基金項目:天津市科技支撐項目(14JCYBJC26100);天津市衛生局科技基金面上項目(2014KY11)
作者簡介:夏大勝(1962),男,主任醫師,博士,主要從事冠心病、心衰、高血壓的臨床及基礎研究

