大蒜素治療白塞病的效果和安全性評價
鐘建橋,先德海
?
大蒜素治療白塞病的效果和安全性評價
鐘建橋1,先德海2
摘要:目的評價大蒜素對白塞病(BD)的治療效果和安全性的影響。方法將38例主要累及皮膚黏膜和關節的BD患者用隨機數字表法分為治療組(20例)和對照組(18例),分別予以大蒜素和安慰劑連續口服12周,隨訪至16周。觀察2組BD患者治療前后臨床癥狀和實驗室檢測值的變化,比較2組的治療效果和不良反應。結果共有31例患者完成試驗,治療組有效率為88.89%,明顯高于對照組(7.69%),差異有統計學意義;治療后治療組血中白細胞計數(WBC)與治療前及對照組比較均無明顯差異(P > 0.05),而紅細胞沉降率(ESR)和C反應蛋白(CRP)水平則較治療前及對照組顯著降低(P < 0.01);盡管大蒜素有一些不良反應,但大部分患者能耐受且停藥后可消退。結論大蒜素是治療BD的一種安全有效的藥物,療效明顯優于安慰劑,值得進一步研究和推廣。
關鍵詞:大蒜素;白塞病;隨機對照試驗
白塞病(Behcet′s disease, BD)是一種多系統炎癥性疾病,可累及皮膚黏膜、眼部、血管等多個系統,嚴重可導致視力損傷甚至危及生命,迄今為止仍無滿意的治療方法[1]。BD的確切發病機制尚不明確,大多認為主要與遺傳、感染、免疫及氧化應激有關。大蒜素是大蒜中的主要生物活性成分,具有抗感染、抗炎、抗氧化、調節免疫等作用,目前已被廣泛應用于感染性疾病、心血管疾病、腫瘤等疾病的治療[2-3],而關于大蒜素用于BD的治療目前尚鮮見報道。筆者前期研究發現大蒜素對實驗性BD有顯著療效[4]。本研究通過開展臨床研究觀察大蒜素對BD的有效性和安全性,以期為BD治療提供新途徑。
1 資料與方法
1.1患者資料選取2013年9月—2014年12月來我院皮膚科門診就診的BD患者38例,其中男22例,女16例;年齡20~69歲,平均(37.5±15.3)歲,病程2個月~7年,平均(46.3±38.9)個月。入選標準:(1)所有患者在入選前2個月沒有使用過激素、免疫抑制劑、生物制劑和抗氧化劑等藥物。(2)符合BD國際研究小組制定的診斷標準[5],即每年至少有3次復發性口腔潰瘍并且至少伴發2種下述表現:眼部損害、復發性生殖器潰瘍皮損(包括假性毛囊炎、結節性紅斑、痤瘡樣皮疹和丘疹性膿皰疹)和針刺反應陽性(用鈍針傾斜刺入皮膚48 h后,若針刺部位出現膿皰或毛囊炎樣皮損,為皮膚針刺反應試驗陽性)。(3)損害局限于皮膚黏膜或關節(關節炎/關節痛)。若伴有下述之一情況者須排除:近期曾攝入大蒜類制劑,對大蒜過敏,孕期或哺乳期,患有中、重度眼部損害、神經系統炎癥或累及其他內臟需接受免疫抑制劑治療者,伴有慢性病變或重癥疾病(包括精神病、全身感染、心肝腎呼吸系統疾病、血液病、紅斑狼瘡和腫瘤等)。在入選前,向患者詳細介紹本研究的目的、方案、持續時間以及大蒜素治療的優點和潛在的風險。所有患者已簽知情同意書,研究方案經倫理委員會審核同意。
1.2藥物大蒜素膠囊由江蘇正大清江制藥有限公司生產(批號:H32025683),每片含量為20 mg。安慰劑外觀、大小和顏色同大蒜素膠囊一致,內含乳糖、預膠化淀粉、羧甲淀粉鈉等成分。
1.3方法
1.3.1試驗設計和隨訪采用隨機對照開放安慰劑方法將38例BD患者分為治療組(20例)和對照組(18例)。治療組予以大蒜素口服,對照組予以安慰劑口服,均為每次1片,每日3次,連續12周。所有患者隨訪至16周。分別在治療前、治療開始后4周、12周和16周隨訪。每次隨訪時一旦有任何相關的系統癥狀出現,應立即行眼部、神經系統和內臟系統等方面的專業檢查。一旦發生下述情況應立即終止試驗:發生系統疾病需要其他治療,中、重度眼部損害,出現神經系統或內臟疾患,對治療無依從性或拒絕繼續進行試驗。
1.3.2實驗室檢查常規檢查2組治療前及治療16周后的血常規、紅細胞沉降率(ESR)和C反應蛋白(CRP)水平。
1.3.3療效評估根據患者臨床表現和實驗室檢查結果的變化對其治療效果進行評價。痊愈:臨床癥狀和體征消失,停藥后無復發,實驗室檢查未見異常。顯效:大部分癥狀和體征消失,實驗室檢查基本正常。好轉:部分癥狀和體征消失或改善,實驗室檢查結果有所改善。無效:臨床癥狀、體征及實驗室檢查無改善或加重。有效率=(痊愈例數+顯效例數)/總例數。
1.3.4安全性評價即在隨訪時對患者出現的藥物不良反應進行評價,主要包括皮疹、異味、惡心、嘔吐和腹痛以及其他可能出現的不良反應。
1.4統計學方法所有數據均用SPSS 15.0軟件進行統計分析,計量資料以±s表示,組間比較采用t檢驗,治療前后比較采用配對t檢驗;計數資料組間比較采用χ2檢驗。P < 0.05為差異有統計學意義。
2 結果
2.1一般資料比較2組BD患者的年齡、性別構成和病程比較均無明顯差異(P > 0.05),見表1。
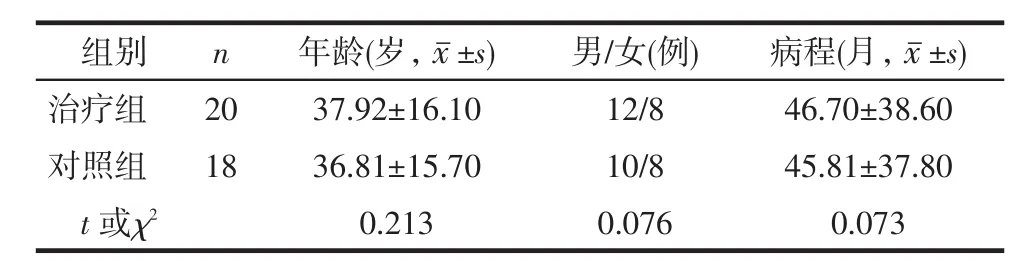
Tab. 1 Comparison of basic characteristics between two groups of patients表1 2組BD患者一般資料比較
2.2臨床療效評價至16周實驗結束時,共有31例患者完成本次臨床研究,治療組18例,對照組13例,其中治療組的有效率高于對照組(P < 0.01),見表2。
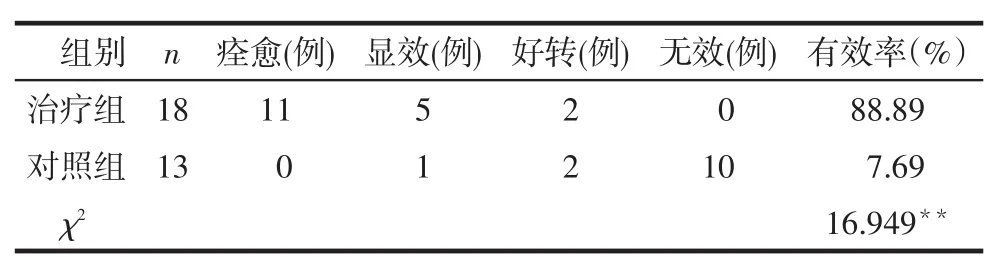
Tab. 2 Comparison of clinical efficacy between two groups of patients表2 2組臨床療效比較
2.3實驗室檢測結果2組BD患者治療后的白細胞計數(WBC)與治療前均無明顯差異(P > 0.05);治療前、后2組間WBC差異亦無統計學意義。治療組經大蒜素治療后ESR和CRP水平均明顯降低(P < 0.05),而對照組治療后的ESR和CRP水平與治療前無明顯差異(P > 0.05);治療前2組的ESR 和CRP水平無明顯差異,治療后治療組的ESR和CRP水平明顯低于對照組(P < 0.05),見表3。
Tab.3 Comparison of WBC, ESR and CRP levels before and after treatment between two groups表3 2組治療前后WBC、ESR及CRP水平比較 (±s)
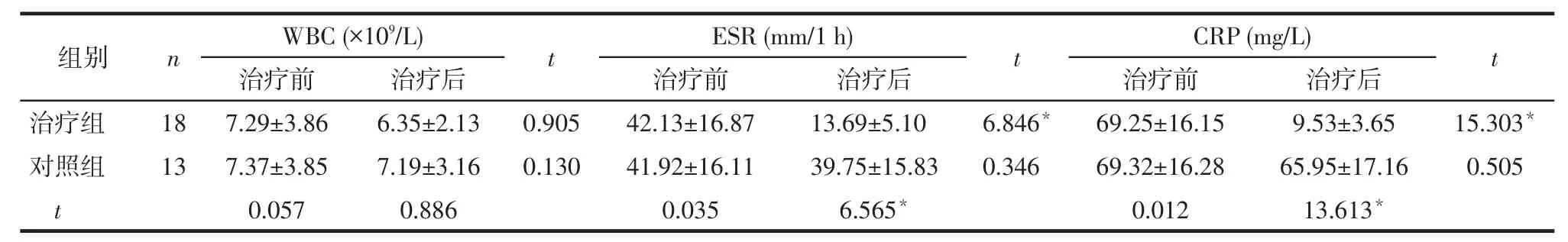
Tab.3 Comparison of WBC, ESR and CRP levels before and after treatment between two groups表3 2組治療前后WBC、ESR及CRP水平比較 (±s)
*P < 0.05
組別治療組對照組t n 18 13 WBC (×109/L)治療前7.29±3.86 7.37±3.85 0.057治療后6.35±2.13 7.19±3.16 0.886 t 0.905 0.130 ESR (mm/1 h)治療前42.13±16.87 41.92±16.11 0.035治療后13.69±5.10 39.75±15.83 6.565*t 6.846*0.346 CRP (mg/L)治療前69.25±16.15 69.32±16.28 0.012治療后9.53±3.65 65.95±17.16 13.613*t 15.303*0.505
2.4大蒜素的不良反應2組患者的不良反應均很少,但治療組更易出現不良反應。主要包括:特殊臭味(10例)、胃腸道不適(5例)、體質量減輕(2例)和過敏反應(1例)。治療組1例患者因過敏反應而中斷治療,1例因治療效果不明顯退出。其余患者均能耐受反應而完成整個研究,并且這些不良反應在藥物停止治療后消失,對工作和生活無明顯影響。
3 討論
目前關于BD的治療尚無有效的根治方法。雖然一些傳統藥物如激素、免疫抑制劑、細胞毒素劑等對BD有一定療效,但停藥后易復發,并且長期使用可能導致嚴重的不良反應,如嚴重感染或繼發性惡性腫瘤[6]。近年來也有報道采用β干擾素、腫瘤壞死因子抑制劑等生物制劑治療BD,但由于其潛在不良反應或昂貴的費用而限制其使用[7]。大蒜素來源于新鮮大蒜,為百合科植物大蒜鱗莖中所含的一種生物活性成分,其價額低廉、來源豐富,不良反應較少。同時具有抗炎、抗感染、抗氧化、降血壓、降血脂、預防心腦血管疾病等多種藥理作用,尤其在心血管損傷的防治研究較多[8-10]。作為嫡屬血管炎性疾病的BD,其病因可能與感染、氧化、免疫有關,故在大蒜素廣泛用于治療各種心血管疾病等安全有效的啟示下,筆者推測大蒜素可能具有治療BD的作用。本臨床試驗結果表明,大蒜素能較好治療BD患者的皮膚黏膜及關節部位損害,有效率明顯優于安慰劑(88.89% vs 7.69%),且能明顯降低BD患者血中的ESR和CRP水平,進而有效控制BD患者的現有癥狀,防止重要臟器的損傷,減緩疾病的發展。與筆者前期實驗結果[4]和國內謝曉莉等[11]研究結果一致。謝曉莉等[11]研究發現外用大蒜素軟膏能有效地緩解口腔潰瘍疼痛,促進口腔潰瘍愈合,減少復發,其作用機制可能與大蒜素抗菌、消炎、改善局部微循環和免疫調節有關。此外,本研究還發現大蒜素的不良反應不大,盡管有一些不良反應如特殊臭味、胃腸道不適、體質量減輕和過敏反應等,除1例因過敏反應中止試驗外,其余均能耐受,并且在停藥后其不良反應消失,對生活工作無不良影響。再次證實大蒜素是一種具有多種治療作用,不良反應較輕的中草藥替代物,值得進一步研究和推廣。
參考文獻
[1] Mat MC, Sevim A, Fresko I, et al. Beh?et′s disease as a systemic disease [J]. Clin Dermatol, 2014, 32(3):435- 442. doi: 10.1016/j. clindermatol.2013.11.012.
[2] Rahman MS. Allicin and other functional active components in gar?lic: Health benefits and bioavailability [J]. Int J Food Pro, 2007, 10 (2): 245-268. doi:10.1080/10942910601113327.
[3] Chan JY, Yuen AC, Chan RY, et al. A review of the cardiovascular benefits and antioxidant properties of allicin [J]. Phytother Res, 2013, 27(5):637-646. doi: 10.1002/ptr.4796.
[4] Zhong JQ, Xian DH, Liao YM. To investigate the treatment and mechanism of Allicin on Behcet′s disease [J]. Chongqing Medicine, 2014, 32(43): 4273-4276.[鐘建橋,先德海,廖勇梅.大蒜素對貝赫切特病的治療作用及機制探討[J].重慶醫學, 2014, 32(43): 4273-4276].
[5] Davatchi F, Sadeghi Abdollahi B, Chams-Davatchi C, et al. The sa?ga of diagnostic/classification criteria in Behcet′s disease[J]. Int J Rheum Dis,2015,18(6):594-605. doi: 10.1111/1756-185X.12520.
[6] Fresko I, Yazici H. Treatment strategies for Behcet′s disease [J]. Ex?pert Opin Pharmacother, 2008, 9: 3211- 3219. doi: 10.1517/ 14656560802457749.
[7] Saleh Z, Arayssi T. Update on the therapy of Beh?et disease [J]. Ther Adv Chronic Dis, 2014, 5(3):112- 134. doi: 10.1177/ 2040622314523062.
[8] Borlinghaus J, Albrecht F, Gruhlke MC, et al. Allicin: chemistry and biological properties [J]. Molecules, 2014, 19(8):12591-12618. doi: 10.3390/molecules190812591.
[9] Chan JY, Tsui HT, Chung IY, et al. Allicin protects rat cardiomyo?blasts (H9c2 cells) from hydrogen peroxide-induced oxidative inju?ry through inhibiting the generation of intracellular reactive oxygen species [J]. Int J Food Sci Nutr, 2014, 65(7):868-873. doi: 10.3109/ 09637486.2014.925428.
[10] Lin CH, Pan SY. The clinical study of allicin combined with aspirin in the treatment of angina pectoris [J]. World Health Digest, 2012, 9 (26): 449-450. [林創輝,潘少奕.大蒜素聯合拜阿司匹林治療冠心病心絞痛的臨床應用[J].中外健康文摘, 2012, 9(26): 449-450].
[11] Xie XL, Tang ZG, Yuan TH. The clinical study of garlic on recur?rent oral ulcer [J]. J Clin Stommol, 2004, 20 (2):113-114. [謝曉莉,唐瞻貴,袁濤洪.佳力克(大蒜素)治療口腔潰瘍的臨床研究[J].臨床口腔醫學雜志, 2004, 20 (2):113-114].
(2015-07-07收稿2015-09-10修回)
(本文編輯閆娟)
作者單位:1瀘州醫學院附屬醫院皮膚科(郵編646000);2瀘州醫學院解剖教研室
Efficacy and safety of allicin in Behcet′s disease
ZHONG Jianqiao1, XIAN Dehai2
1 Department of Dermatology, the Affiliated Hospital of Luzhou Medical College, Luzhou 646000, China;
2 Department of Human Anatomy, Luzhou Medical College
Abstract:Objective To evaluate the efficacy and safety of allicin in patients with Behcet′s disease (BD). Methods Thirty-eight patients with BD that was mainly involved skin, mucosa and joints were divided into treatment group (20 cases) and control group (18 cases) by randomized digital table method. Two groups of patients were respectively assigned to receive allicin tablets and identical placebo vehicles for 12 weeks, and were followed up to 16 weeks. The changes of clinical symp?toms and laboratory detection were observed in the time of pretreatment and post-treatment in two groups. Meanwhile, the ef?ficacy and side effects were compared between both groups. Results A total of 31 patients completed the experiment. The effective rate was 88.89% in treatment group, which was significantly higher than that of the control group (7.69%, P < 0.01). After administration of allicin or placebo, there was no significant difference in white blood cell (WBC) count between treat?ment group and control group(P > 0.05). The levels of ESR and CRP were significant lower in treatment group than those in pretreatment and control group (P < 0.01). Although allicin displayed some adverse reactions, most patients could tolerate them, and these side effects tended to dissipate once the drug ceased. ConclusionAllicin is a safe and effective drug in the treatment of BD, which is significantly better than placebo, and is worth to be further researched and promoted.
Key words:Allcin; Behcet′s disease (BD); randomized controlled trials
中圖分類號:R758.69
文獻標志碼:A
DOI:10.11958/59156
基金項目:四川省衛生廳科研課題(100283)
作者簡介:鐘建橋(1973),女,副主任醫師,博士,主要從事皮膚美容與炎癥性疾病研究

