右美托咪定、異丙酚對膿毒癥相關性腦病患者躁動及炎性反應的影響
王 璐,姚 蘭,鄒捍東,周晨亮,李 璐,周青山
(武漢大學人民醫院,湖北 武漢 430060)
?
麻醉
右美托咪定、異丙酚對膿毒癥相關性腦病患者躁動及炎性反應的影響
王璐,姚蘭,鄒捍東,周晨亮,李璐,周青山
(武漢大學人民醫院,湖北 武漢 430060)
[摘要]目的比較右美托咪定與異丙酚對膿毒癥相關性腦病患者躁動及炎性反應的影響。方法選取年齡18~80歲、格拉斯哥昏迷(GCS)評分6~13分的腦功能障礙并躁動的膿毒癥患者,采用隨機數字表法將其分為右美托咪定組(DEX組)和異丙酚組(PRO組)各28例。DEX組給予右美托咪定負荷劑量1.0 μg/kg,靜脈推注時間大于10 min,滴定維持劑量0.2~0.7 μg/(kg·h);PRO組給予異丙酚負荷量0.025~1.0 mg/kg,維持劑量0.5~4.0 mg/(kg·h)。分別于用藥后1 h(t1)、12 h(t2)、24 h(t3)、3 d(t4)抽取肘靜脈血樣,采用ELISA法測定血漿C反應蛋白(CRP)、TNF-α和IL-6的濃度,記錄患者鎮靜期間不良反應的發生情況。結果DEX組在t2~t4時血漿CRP、TNF-α濃度較PRO組均顯著降低(P均<0.05),在t3~t4時血漿IL-6濃度較PRO組顯著降低(P均<0.05);2組低血壓、心動過緩、呼吸抑制、惡心嘔吐、ICU留住時間和死亡率及并發癥比較差異均無統計學意義(P均>0.05)。結論右美托咪定用于膿毒癥相關性腦病躁動患者的鎮靜效果滿意,可有效減輕炎癥反應。
[關鍵詞]右美托咪定;異丙酚;膿毒癥相關性腦病;躁動;炎性反應
膿毒癥相關性腦病(sepsis-associated encephalopathy, SAE)是由感染引起的全身炎癥反應所導致的彌漫性腦功能障礙,表現為記憶力下降、無法集中注意力、有定向障礙、容易激惹、精神恍惚甚至昏迷等認知功能受損,其中躁動較常見[1]。右美托咪定(dexmedetomidine, DEX)是新型α2受體激動劑,有較好的鎮靜、鎮痛劑抗焦慮作用,因其對呼吸和腦循環沒有不良影響,近年來將其較多應用于重癥ICU的鎮靜治療,但目前右美托咪定應用于SAE的臨床研究資料非常有限。因此本研究觀察了右美托咪定對SAE患者躁動及炎性反應的影響,并評估其對患者遠期預后的影響,現將結果報道如下。
1臨床資料
1.1一般資料采用前瞻性隨機對照臨床研究。選擇2011年9月—2014年6月于武漢大學人民醫院重癥醫學科收治的全身感染患者,根據2012年膿毒癥診療指南[2]診斷為膿毒癥,排除合并血流動力學不穩定、肝腎功能衰竭、高鈉血癥、低血糖、顱內器質性病變、重度營養缺乏、腦出血、使用鎮靜藥物等影響中樞神經系統功能的患者,選取腦功能障礙并躁動患者,年齡18~80歲,格拉斯哥昏迷(GCS)評分6~13分。本研究符合醫學倫理學標準,經醫院倫理委員會批準,所有鎮靜給藥方案及治療獲得患者家屬的知情同意。入選56例SAE患者中,男34例,女22例;年齡19~76歲,GCS評分(10.71±1.951)分,APACHEⅡ評分(11.54±5.582)分,SOFA評分(11.04±5.134)分。肺部感染32例,腹腔感染11例,血流感染5例,泌尿系感染8例。采用隨機數字表法將患者分為右美托咪定(DEX)組和丙泊酚(PRO)組。2組性別、年齡、GCS、APACHEⅡ評分、SOFA評分比較差異無統計學意義(P均>0.05)。見表1。

表1 2組一般資料比較
1.2方法DEX組給予右美托咪定注射液(200 μg/支,江蘇恒瑞醫藥股份有限公司產品),負荷劑量1.0 μg/kg,靜脈推注時間大于10 min,滴定維持劑量0.2~0.7 μg/(kg·h);PRO組給予異丙酚注射液(1 g/支,Corden Pharma S.P.A.產品)負荷劑量0.025~1.0 mg/kg,維持劑量0.5~4.0 mg/(kg·h)。目標為患者鎮靜程度(Ramsay)評分3~4分,每隔1 h根據鎮靜鎮痛評分調整藥物劑量。治療指征:焦慮、躁動不安、疼痛,包括昏迷或肢體躁動不安,不耐受氣管插管者。
1.3監測指標于用藥后1 h(t1)、12 h(t2)、24 h(t3)、3 d(t4)記錄患者心率、血壓、呼吸、是否惡心嘔吐等。于t1、t2、t3、t4抽取肘靜脈血樣5 mL,離心取血漿,-70 ℃保存,采用ELISA法測定血漿CRP、TNF-α和IL-6的濃度,操作步驟嚴格按照試劑盒(R&D公司,美國)說明書進行。記錄患者鎮靜期間不良反應的發生情況,采用Ramsay評分評價鎮靜程度:1分,不安靜、煩躁;2分,安靜、合作;3分,嗜睡,能聽從指令;4分,睡眠狀態,可喚醒;5分,呼喚反應遲鈍;6分,深睡狀態,呼喚不醒。保持鎮靜程度3~4分。

2結果
2.1炎性因子比較DEX組在t2~t4時血漿CRP、TNF-α濃度較PRO組顯著降低(P均<0.05);在t3~t4時血漿IL-6濃度較PRO組顯著降低(P均<0.05)。見表2。
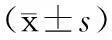
表2 2組血漿CRP、TNF-α、IL-6濃度比較
2.2不良反應比較2組低血壓、高血壓、心動過速、心動過緩、呼吸抑制、惡心嘔吐發生率比較差異均無統計學意義(P均>0.05)。見表3。

表3 2組不良反應比較 例(%)
2.3預后比較DEX組和PRO組ICU留住時間分別為(13.3±6.4)d和(12.0±4.2)d,病死率分別為11%(3/28)和18%(5/28),2組ICU留住時間、病死率比較差異均無統計學意義(P均>0.05)。
3討論
膿毒癥患者在一系列細胞因子作用下產生級聯反應,從而引起多器官功能障礙,其中最嚴重的腦功能障礙早期可表現為行為異常,注意力和定向力受損,隨著疾病進展可能出現譫妄、昏迷,稱之為SAE,其發病率可高達71%[3],是膿毒癥獨立死亡因素之一[4]。臨床上高APACHEⅡ、肝功能異常以及酸中毒的膿毒癥患者更易罹患腦功能障礙[5]。其發病機制可能與線粒體損傷、血管功能障礙、氧化應激損傷、神經傳導異常、感染、細胞程序性死亡等有關[6]。CRP、TNF-α、IL-6是在膿毒癥全身炎癥反應中起核心作用的炎癥因子。CRP是評估感染預后及嚴重程度的急性期蛋白,CRP濃度較高的患者更易合并譫妄、昏迷等腦功能障礙[7]。TNF-α在SAE炎癥反應中介導中性粒細胞在腦組織中浸潤、神經元細胞的凋亡和腦水腫過程[8]。IL-6通過局部及全身減輕炎癥損傷、阻止感染擴散并提供組織恢復的環境[9]。膿毒癥診斷治療過程中,需要使患者減輕應激反應,便于實施呼吸支持、血液凈化、腸內營養等治療[10],改善預后并降低病死率,因此如何控制患者躁動以及譫妄狀態成為臨床需要解決的問題之一。目前SAE患者較多采用丙泊酚、苯二氮卓類藥物等鎮靜藥物控制,但嚴重膿毒癥患者多合并休克,不適當應用上述藥物可能會產生休克加重、呼吸抑制等不利影響;除此之外苯二氮卓類藥物可能會引起譫妄。
右美托咪定是具有鎮靜、鎮痛、催眠、抑制交感神經的α2腎上腺素受體激動劑[11],特異作用于藍斑區的α2受體,抑制神經遞質由突觸末端釋放,從而抑制腦細胞信號通路并減輕炎癥損傷。右美托咪定的鎮靜鎮痛作用位點位于脊髓背角,因此可以有效鎮靜鎮痛并無呼吸抑制和藥物依賴等不良反應,且其作用接近生理狀態的睡眠-覺醒周期可降低譫妄發生[12],近年來被較多應用于綜合ICU的鎮靜鎮痛治療[13]。體外研究發現,右美托咪定在脂多糖誘導的膿毒癥模型中可以降低TNF-α和IL-6的表達,從而介導神經細胞炎癥反應過程[14],c-Jun氨基末端激酶(c-Jun N-terminal kinase, JNK)通路在此過程中發揮重要作用。在結腸結扎后腹腔感染膿毒癥大鼠模型中,右美托咪定通過調節TLR4/MyD88/NF-κB通路降低TNF-α和IL-6的表達,減輕臟器損傷[15]。而右美托咪定對CRP的作用尚未見報道。臨床研究中,膿毒癥患者體內試驗發現右美托咪定比咪唑安定腦功能障礙發生率低,機械通氣時間更短,且死亡率較低[16]。本研究發現,右美托咪定和異丙酚均可在一定程度上控制患者炎癥反應。在應用右美托咪定后,血漿CRP、TNF-α、IL-6均有明顯下降,考慮右美托咪定通過介導細胞炎性因子發揮鎮靜作用,促進患者腦功能恢復。2組患者不良反應、ICU留住時間及死亡率比較差異均無統計學意義,可能與入組患者數量較少有關,進行多中心大樣本研究可能得出更客觀的結果。
綜上所述,SAE患者體內存在復雜的炎癥反應過程,右美托咪定除通過對藍斑區的作用有效抑制去甲腎上腺素釋放,降低血漿兒茶酚胺濃度,從而有效鎮靜、無嚴重不良反應之外,CRP、TNF-α、IL-6等細胞因子可能也參與了炎癥反應的抑制。
[參考文獻]
[1]Iacobone E,Bailly-Salin J,Polito A,et al. Sepsis-associated encephalopathy and its differential diagnosis[J]. Crit Care Med,2009,37(10 Suppl):S331-S336
[2]Dellinger RP,Levy MM,Rhodes A,et al. Surviving sepsis campaign:international guidelines for management of severe sepsis and septic shock,2012[J]. Intensive Care Med,2013,39(2):165-228
[3]Bartynski WS,Boardman JF,Zeigler ZR,et al. Posterior reversible encephalopathy syndrome in infection,sepsis,and shock[J]. Am J Neuroradiol,2006,27(11):2179-2190
[4]Eidelman LA,Putterman D,Putterman C,et al. The spectrum of septic encephalopathy. Definitions,etiologies,and mortalities[J]. JAMA,1996,275(6):470-473
[5]馮麗芝,周青山,王常永. 影響膿毒癥相關性腦病發生的危險因素的Meta分析[J]. 藥物與臨床,2013,10(20):71-76
[6]Siami S,Annane D,Sharshar T. The encephalopathy in sepsis[J]. Crit Care Clin,2008,24(1):67-82
[7]McGrane S,Girard TD,Thompson JL,et al. Procalcitonin and C-reactive protein levels at admission as predictors of duration of acute brain dysfunction in critically ill patients[J]. Crit Care,2011,15(2):R78
[8]Pytel P,Alexander JJ. Pathogenesis of septic encephalopathy[J]. Curr Opin Neurol,2009,22(3):283-287
[9]Sheeran P,Hall GM. Cytokines in anesthesia[J]. BJA,1997,78(2):201-219
[10] Barr J,Fraser GL,Puntillo K,et al. Clinical practice guidelines for the management of pain,agitation,and delirium in adult patients in the intensive care unit[J]. Crit Care Med,2013,41(1):263-306
[11] Ma D,Hossain M,Rajakumaraswamy N,et al. Dexmedetomidine produces its neuroprotective effect via the alpha 2A-adrenoceptor subtype[J]. Eur J Pharmacol,2004,502(1/2):87-97
[12] Elbaradie S,El Mahalawy FH,Solyman AH. Dexmedetomidine vs. propofol for short-term sedation of postoperative mechanically ventilated patients[J]. J Egypt Natl Canc Inst,2004,16(3):153-158
[13] 黃青青. 右美托咪定在重癥監護病房中的應用[J]. 中國危重病急救醫學,2010,22(10):578-580
[14] Xiang H,Hu B,Li Z,et al. Dexmedetomidine Controls Systemic Cytokine Levels through the Cholinergic Anti-inflammatory Pathway[J]. Inflammation,2014,37(5):1763-1770
[15] Wu Y,Liu Y,Huang H,et al. Dexmedetomidine inhibits inflammatory reaction in lung tissues of septic rats by suppressing TLR4/NF-κB pathway[J]. Mediators Inflamm,2013,2013:562154
[16] Pandharipande PP,Sanders RD,Girard TD,et al. Effect of dexmedetomidine versus lorazepam on outcome in patients with sepsis:an a priori-designed analysis of the MENDS randomized controlled trial[J]. Crit Care,2010,14(2):R38
[收稿日期]2015-03-05
[中圖分類號]R614.2
[文獻標識碼]B
[文章編號]1008-8849(2016)05-0544-03
doi:10.3969/j.issn.1008-8849.2016.05.031

