低氧環境對大鼠骨髓間充質干細胞交感神經重構相關因子表達的影響
周智涓,伍 衛,黃穗花,劉 茂,陳 劍
中山大學附屬第五醫院(廣東珠海 519000)
?
低氧環境對大鼠骨髓間充質干細胞交感神經重構相關因子表達的影響
周智涓,伍衛,黃穗花,劉茂,陳劍
中山大學附屬第五醫院(廣東珠海 519000)
摘要:目的觀察低氧環境對大鼠骨髓間充質干細胞(BMSCs)三種交感神經重構相關因子內皮素-1(ET-1)、促紅細胞生成素(EPO)和粒細胞集落刺激因子(G-CSF)表達的影響。方法體外分離培養大鼠BMSCs至第三代,應用Western Blot技術檢測BMSCs各代細胞中ET-1、EPO和G-CSF蛋白表達水平。BMSCs培養至第三代后,更換無血清無糖培養基,將細胞培養皿置入缺氧培養箱分別培養2 h、6 h、12 h及24 h,分別檢測上述四組細胞ET-1、EPO、G-CSF蛋白表達水平。結果大鼠BMSCs在常氧狀態下具有分泌神經重構相關因子ET-1、EPO、G-CSF的功能。低氧環境可誘導大鼠BMSCs細胞ET-1、EPO、G-CSF蛋白表達水平上調,ET-1、EPO表達水平隨缺氧時間延長而進行性升高,差異有統計學意義(P<0.05)。結論低氧環境能顯著上調大鼠BMSCs交感神經重構相關因子的表達水平,促進心肌交感神經重構,可能與BMSCs移植治療后心律失常副反應的發生密切相關。
關鍵詞:骨髓間充質干細胞;交感神經重構;促紅細胞生成素;內皮素-1;粒細胞集落刺激因子
骨髓間充質干細胞(bone marrow-derived mesenchymal stem cells,BMSCs)是成體干細胞的一種,具有自我更新、自我維持以及多向分化的潛能,被認為是當前干細胞移植研究領域極具前景的種子細胞之一[1]。BMSCs可分化為血管內皮細胞和血管平滑肌細胞,自分泌或促進心肌細胞分泌促血管生長的細胞因子,從而直接和間接誘導新生血管形成,促進側支循環建立,挽救缺血心肌[2-3]。
然而,BMSCs移植治療心肌梗死的安全性尚不確切。BMSCs移植治療具有致心律失常的副反應,目前觀點認為其心律失常的發生可能與心肌交感神經結構和功能重構密切相關[4-5]。近年體外研究還發現,內皮素-1(endothelin-1,ET-1)、促紅細胞生成素(erythropoietin,EPO)和粒細胞集落刺激因子(granulocyte colony-stimulated factor,G-CSF)具有促進心肌梗死區神經生長因子(nerve growth factor,NGF)的表達、提高交感神經張力以及營養神經的作用,從而促進心肌交感神經重構的發生和發展[6-8]。那么,BMSCs移植治療的致心律失常作用是否與其分泌上述神經重構相關因子(ET-1、EPO、G-CSF)有關,以及低氧誘導環境下能否上調BMSCs細胞上述因子的表達水平呢?目前尚無相關文獻報道。本實驗通過體外分離培養大鼠BMSCs,觀察常氧條件下大鼠BMSCs能否分泌神經重構相關因子ET-1、EPO、G-CSF及其分泌特點;利用低氧誘導模擬心肌梗死缺氧環境,進一步觀察低氧環境對大鼠BMSCs交感神經重構相關因子表達的影響,從而為探索BMSCs移植治療致心律失常的原因提高實驗依據。
1材料與方法
1.1實驗動物清潔級雄性Sprague-Dawley(SD)大鼠,體質量80 g~120 g,3周~4周齡,共6只,由中山大學實驗動物中心提供(實驗動物質量合格證號:SCXK粵2012-0029)。實驗過程中對動物的處置符合動物倫理學標準。
1.2主要試劑和儀器胎牛血清(美國Hyclone公司);DMEM-F12培養基(美國Hyclone公司);甘油醛-3-磷酸脫氫酶兔抗鼠多克隆抗體(Anti-GAPDH antibody,美國Abcam公司);兔抗鼠內皮素-1單克隆抗體(Anti-ET-1 antibody,美國Abcam公司);重組促紅細胞生成素多克隆抗體(Anti-EPO antibody,美國CST公司);兔抗鼠粒細胞集落刺激因子單克隆抗體(Anti-G-CSF antibody,美國PeproTech 公司);超凈工作臺(美國Thermo Forma公司);缺氧細胞培養箱(美國Thermo Forma公司);熒光倒置顯微鏡(德國Leica公司);超低溫冰箱(美國Thermo公司)等。
1.3BMSCs分離、培養及鑒定取3周~4周齡SD大鼠,無菌條件下分離中雙側股骨及脛骨,采取全骨髓貼壁分離和消化控制相結合分離純化BMSCs。顯微鏡下觀察原代(P0)BMSCs生長情況及形態變化,細胞增殖至培養皿80%~90%時,處于對數生長期,用0.25%胰蛋白酶-EDTA消化,離心機離心、重懸,傳代培養。首次傳代為P1,其后依次為P2、P3等,每天觀察細胞生長情況。采用流式細胞儀檢測P3期BMSCs細胞表面抗原CD44H、CD45、CD29、CD11b/c和CD90.1的表達情況。
1.4實驗分組為分析常氧環境BMSCs細胞分泌神經重構相關因子ET-1、EPO、G-CSF特點,按照細胞培養周期將細胞分為3組:P1期(第一代BMSCs細胞)、P2期(第二代BMSCs細胞)、P3期(第三代BMSCs細胞)。分別檢測三代細胞ET-1、EPO、G-CSF蛋白表達水平。為分析低氧環境對大鼠BMSCs細胞分泌神經重構相關因子的影響,取第三代BMSCs細胞進行試驗。BMSCs培養至第三代(P3期)后,更換無血清無糖培養基,將細胞培養皿置入94%N2、5%CO2、1%O2缺氧培養箱分別培養2 h、6 h、12 h及24 h,分別檢測上述4組細胞ET-1、EPO、G-CSF蛋白表達水平。
1.5蛋白印跡每瓶細胞加入裂解液后,用槍吹打數下,置于冰上并用水平搖床搖晃使裂解液和細胞充分接觸。充分裂解后,于4 ℃,12 000 r/min離心10 min,取上清。提取總蛋白后,立即測定蛋白濃度。采用BCA法進行蛋白定量試劑盒進行定量。按說明書稀釋標準品以及配制BCA工作液。將提取的總蛋白加入5×SDS蛋白緩沖液,100 ℃煮沸5 min,置于超低溫冰箱保存備用。將蛋白用Bradford法定量后,選擇不同濃度的聚丙烯酰胺凝膠(G-CSF15%,ET-1 12%,EPO12%),經SDS-PAGE電泳后將蛋白轉至PVDF膜上。5%脫脂牛奶封閉后,加入相應的一抗,室溫下孵育1 h~2 h或者4 ℃過夜。用TBST每次5 min洗3次后,用相應的稀釋好的二抗,室溫下孵育1 h~2 h后,用TBST沖洗3次,每次10 min,然后進行化學發光顯影。用Gel-Proanalyzer4.0分析目標條帶的光密度值。本實驗采用GAPDH作為內參照,比較不同處理后上述蛋白表達的差異。
2結果
2.1BMSCs細胞鑒定顯微鏡下形態學觀察可見BMSCs為長梭形或纖維狀細胞,形態均一,排列密集,呈放射狀或漩渦狀生長(圖1A)。利用流式細胞儀檢測干細胞表面標志物,結果提示細胞CD29、CD90.1表達呈陽性,CD34、CD45和CD11b/c呈陰性,符合BMSCs細胞表面標志物特點(圖1B)。
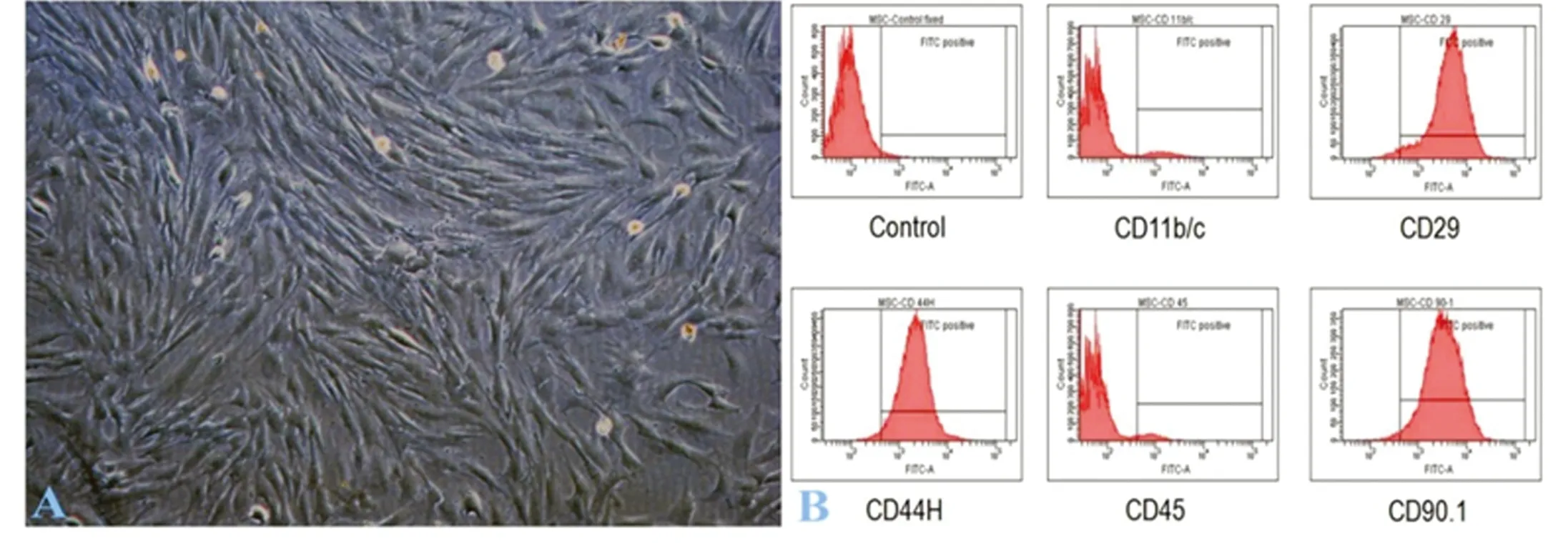
圖1 BMSCs細胞形態學及流式細胞儀鑒定
2.2常氧環境BMSCs細胞ET-1、EPO和G-CSF蛋白表達應用Western Blot技術檢測BMSCs細胞 P1、P2及P3三個培養周期中ET-1、EPO和G-CSF蛋白表達水平。結果發現,常氧環境中BMSCs細胞P1、P2、P3三個培養周期均可檢測到ET-1、EPO和G-CSF蛋白表達,提示BMSCs細胞能夠自分泌上述三種蛋白。P3期BMSCs細胞ET-1蛋白表達較P1、P2期顯著增高,差異有統計學意義(P<0.05)。P2期與P1期BMSCs細胞比較,ET-1蛋白表達差異無統計學意義(P>0.05)。詳見圖2。P2期BMSCs細胞EPO蛋白表達水平較P1、P3期增高(P<0.05),而P3期與P1期BMSCs細胞比較發現前者EPO蛋白表達水平明顯升高,差異有統計學意義(P<0.05)。詳見圖3。P2和P3期BMSCs細胞G-CSF蛋白水平較P1期增高(P<0.05),而P2和P3 期之間G-CSF蛋白表達水平差異無統計學意義(P>0.05)。詳見圖4。
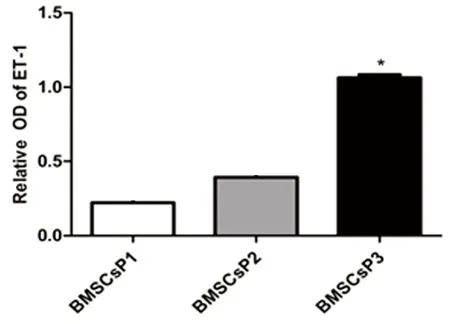
注:與BMSCs P1、P2期比較,* P<0.05。
圖2常氧環境BMSCs細胞ET-1蛋白表達
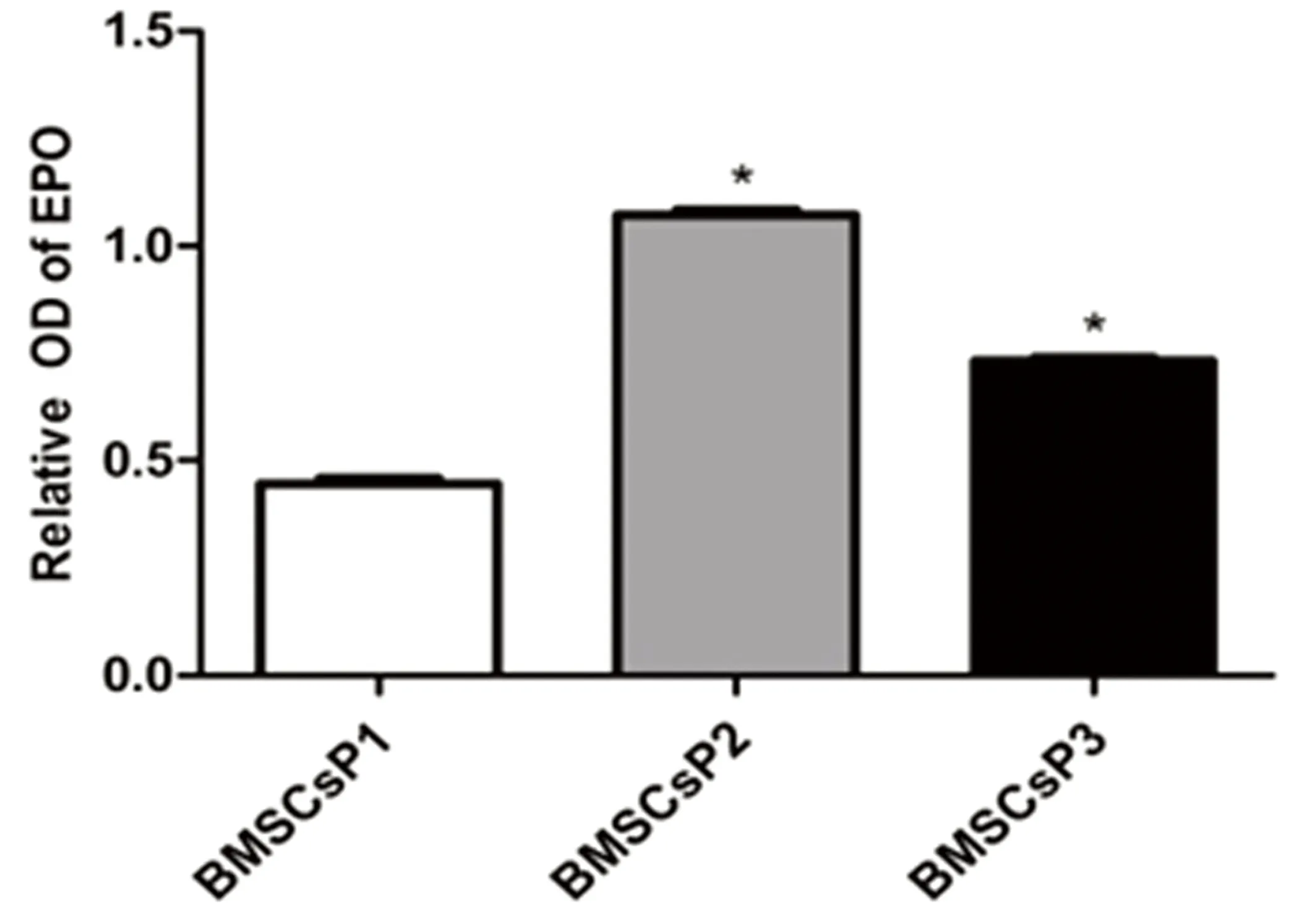
注:與BMSCs P1期比較,*P<0.05。
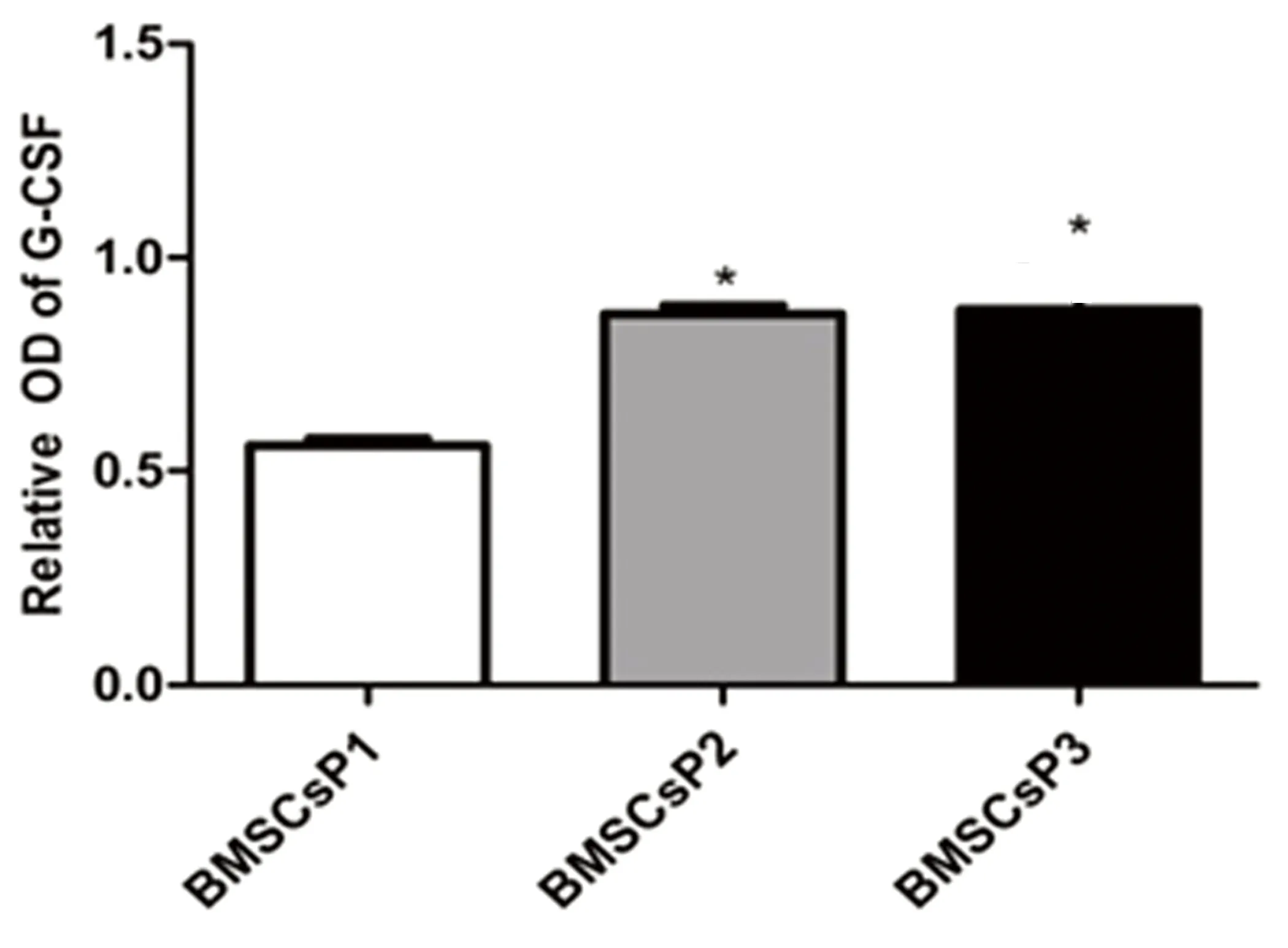
注:與BMSCs P1期比較,*P<0.05。
2.3低氧環境BMSCs細胞ET-1蛋白表達低氧誘導環境下BMSCs細胞ET-1蛋白表達量較常氧對照組顯著增加(P<0.05),且隨缺氧時間延長而逐漸增高,在缺氧24 h達到高峰(P<0.05),提示低氧環境可誘導BMSCs細胞ET-1蛋白表達水平上調。詳見圖5。
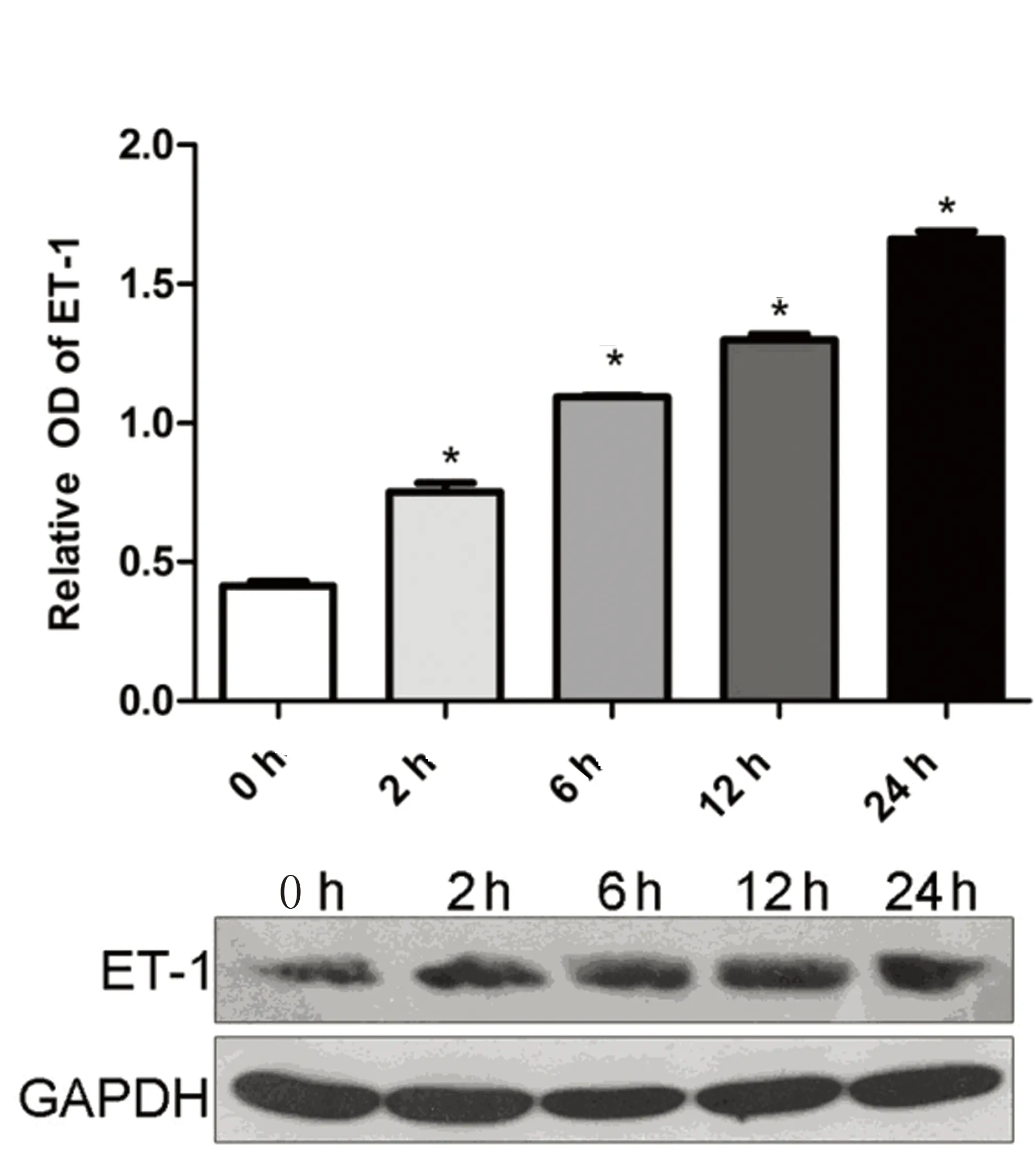
注:與對照組比較,*P<0.05。
2.4低氧環境BMSCs細胞EPO蛋白表達低氧誘導環境下BMSCs細胞EPO蛋白分泌量較常氧對照組明顯升高(P<0.05),并隨缺氧時間延長而進行性升高,在缺氧24 h達到高峰(P<0.05),提示低氧環境可誘導BMSCs細胞EPO蛋白表達水平上調。詳見圖6。
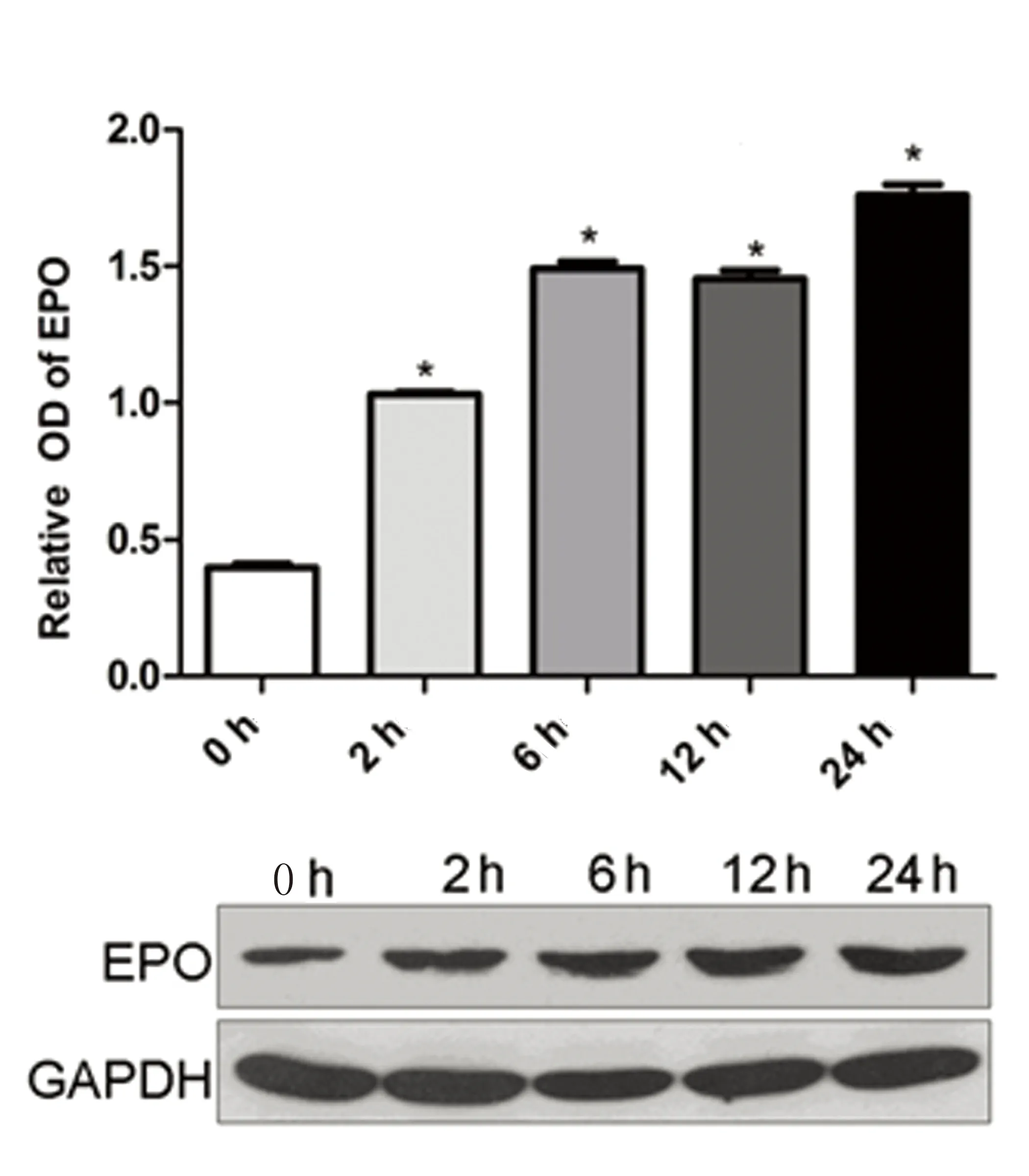
注:與對照組比較,* P<0.05。
圖6低氧環境BMSCs細胞EPO蛋白表達
2.5低氧環境BMSCs細胞G-CSF蛋白表達低氧誘導環境下BMSCs細胞G-CSF蛋白分泌量較常氧對照組顯著增加(P<0.05),但G-CSF蛋白表達量未隨缺氧時間延長而進一步增加。詳見圖7。
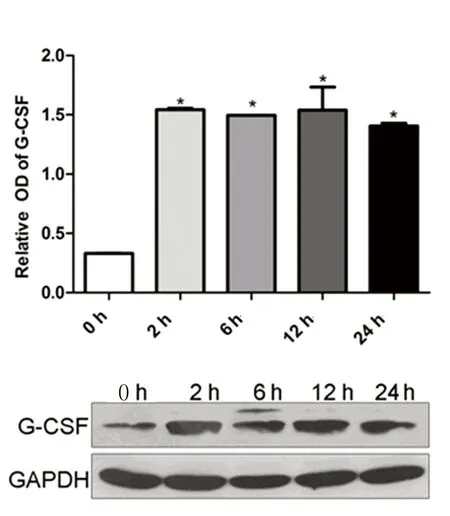
注:與對照組比較,* P<0.05。
3討論
干細胞是一類具有自我更新、自我維持和多向分化潛能的細胞,能表達、合成或分泌生長因子、細胞因子、調節肽及氣體信號分子等多種生物活性因子。而這些生物活性因子又具有調節組織細胞代謝、分化、增殖、遷移、凋亡等功能[9]。植入干細胞的分泌功能不僅直接影響植入干細胞自身的存活和分化,而且是干細胞移植發揮其他生物學效應的重要機制[10]。本研究通過體外分離培養大鼠BMSCs發現,常氧條件下大鼠BMSCs具有分泌神經重構相關因子ET-1、EPO、G-CSF的作用,低氧環境能夠顯著增加上述因子的表達水平,加劇心肌交感神經重構,從而促使BMSCs移植治療后心律失常的發生。
ET-1是目前所知最強大的血管收縮因子,最早從豬主動脈內皮細胞上清液中分離發現。ET-1主要來源于內皮細胞,可通過旁分泌的形式激活內皮素受體并參與心血管系統多種生理病理過程[11]。研究發現,ET-1與ET-1受體結合后,可激活P38MAPK、ERK等信號通路,誘導心肌細胞表達與分泌NGF,從而促進交感神經重構[12]。在干細胞相關研究中發現,脂肪源性MSCs可表達ET-1,但骨髓源性MSCs是否同樣表達ET-1,尚未見文獻報道。本研究觀察到BMSCs在P1、P2、P3三代細胞均可表達ET-1,且在純化的P3中,ET-1表達量最高。通過體外單一細胞培養,排除了造血干細胞、造血細胞如單核細胞、淋巴細胞、成纖維細胞、巨噬細胞等干擾后,本研究首次發現骨髓來源的干細胞BMSCs同樣具有分泌ET-1的作用。本研究還觀察低氧處理對BMSCs細胞 24 h內ET-1表達量的影響。首次發現低氧可增強BMSCsET-1的表達,并發現在一定缺氧時程內,ET-1表達量隨缺氧時程延長而增高,繼續延長缺氧時間,ET-1表達量逐漸回降。這一結果提示低氧可調節BMSCs自分泌功能并可能在缺氧早期即發揮這一作用,提示這種機制可能與BMSCs移植治療的致心律失常副反應相關。
另外,BMSCs由中胚層分化而成,可分泌多種支持造血因子,為BMSCs的存活提供營養支持及支架作用。既往研究發現,BMSCs可分泌和表達EPO和G-CSF[13-15]。EPO作為強大的神經營養因子,具有促進軸突再生的作用,還可促進腦和脊髓的星形膠質細胞分泌NGF,從而發揮神經保護作用[16]。G-CSF是一種促進粒細胞生長的細胞因子,前期研究證實G-CSF可通過與粒細胞集落刺激因子受體結合,促進干細胞遷移及定位[14,17]。Lee等[8]研究發現G-CSF可促進心肌梗死后大鼠梗死區域NGF表達及交感神經重分布。而Kuhlmann和Baldo等學者則持相反觀點,認為G-CSF或可通過增加Connexin43表達而減少心肌梗死室性心律失常的發生[1,14]。在本研究中,通過蛋白印跡法檢測未分化的BMSCs細胞EPO和G-CSF蛋白表達水平,也發現BMSCs可分泌上述細胞因子,且晚期成熟的BMSCs中更為明顯,與國內外研究結論一致[15,18]。同時,本研究還發現,缺氧環境可誘導EPO和G-CSF蛋白表達增加,前者隨缺氧時間增加而增加,后者則不隨缺氧作用時間變化而進一步變化。該現象說明缺氧可影響BMSCs細胞EPO表達,或可通過持續分泌EPO而促進NGF表達,促進交感神經重構,從而誘發室性心律失常。另外,缺氧也可促進BMSCs細胞G-CSF蛋白表達,但是否能夠通過G-CSF表達水平變化這一途徑而影響心肌交感神經重構尚有待后續研究探索。
低氧環境可能通過以下途徑影響BMSCs細胞交感神經重構相關因子的表達:低氧可增加抗凋亡蛋白Bcl-2的表達,抑制P53信號表達,抑制白介素1β轉化酶生成,減少氧化應激損傷和氧自由基生成,穩定線粒體電位,從而保持移植入宿主的干細胞存活率[19];低氧可增強了干細胞的分化能力[20];低氧還可調節干細胞某些基因和受體表達并影響多個細胞信號通路,如ERK1/2、P38 MAPK、JNK通路等,參與其下游多種功能的調節,促進多種生物活性因子的合成與分泌[19,21]。
本研究具有一些不足之處。首先,本研究僅為初期體外實驗,暫未進行在體實驗或人體研究。其次,既往研究提示外源性ET-1可誘導BMSCs分化成心肌樣細胞,本研究采用第1代~第3代BMSCs細胞進行研究,結果發現早期BMSCs可表達ET-1,而BMSCs自分泌的ET-1又能否促進其自身分化并影響其他細胞因子的分泌,本研究未進一步探討。再次,本研究僅報告了上述三種細胞因子的蛋白表達水平,關注的細胞因子種類有限,且未報告低氧對BMSCs轉錄水平的影響;本研究未能縱向探討BMSCs細胞分泌上述細胞因子后如何通過旁分泌影響周圍心肌細胞NGF表達,如何進一步誘導心律失常發生。為此,本課題組正在進行后續研究。最后,本研究未進一步觀察不同氧濃度下BMSCs分泌各細胞因子水平是否存在差異,且觀察時間僅限于24 h內,未能橫向多層次比較,有待更多同行的進一步合作與研究。
綜上所述,大鼠BMSCs細胞具有分泌神經重構相關因子ET-1、EPO、G-CSF的功能,低氧環境能顯著上調其上述細胞因子的表達水平,促進心肌交感神經重構,可能與BMSCs移植治療后心律失常副反應的發生密切相關。
參考文獻:
[1]Baldo MP,Davel AP,Nicoletti-Carvalho JE,et al.Granulocyte colony-stimulating factor reduces mortality by suppressing ventricular arrhythmias in acute phase of myocardial infarction in rats.[J].J Cardiovasc Pharmacol,2008,52(4):375-380.
[2]Gnecchi M,Melo LG.Bone marrow-derived mesenchymal stem cells: isolation,expansion,characterization,viral transduction,and production of conditioned medium[J].Methods Mol Biol,2009,482:281-294.
[3]Wen Z,Zheng S,Zhou C,et al.Repair mechanisms of bone marrow mesenchymal stem cells in myocardial infarction[J].J Cell Mol Med,2011,15(5):1032-1043.
[4]Zhang J,Wang LL,Du W,et al.Hepatocyte growth factor modification enhances the anti-arrhythmic properties of human bone marrow-derived mesenchymal stem cells[J].PLoS One,2014,9(10):e111246.
[5]Macia E,Boyden PA.Stem cell therapy is proarrhythmic[J].Circulation,2009,119(13):1814-1823.
[6]Lee JH,Kemp DM.Human adipose-derived stem cells display myogenic potential and perturbed function in hypoxic conditions[J].Biochem Biophys Res Commun,2006,341(3):882-888.
[7]Kolettis TM.Ventricular tachyarrhythmias during acute myocardial infarction:the role of endothelin-1[J].Life Sci,2014,118(2):136-140.
[8]Lee TM,Chen CC,Chang NC.Granulocyte colony-stimulating factor increases sympathetic reinnervation and the arrhythmogenic response to programmed electrical stimulation after myocardial infarction in rats[J].Am J Physiol Heart Circ Physiol,2009,297(2):H512-H522.
[9]Burdon TJ,Paul A,Noiseux N,et al.Bone marrow stem cell derived paracrine factors for regenerative medicine: current perspectives and therapeutic potential[J].Bone Marrow Res,2011,2011:207326.
[10]Maldonado-Soto AR,Oakley DH,Wichterle H,et al.Stem cells in the nervous system[J].Am J Phys Med Rehabil,2014,93(11 Suppl 3):S132-S144.
[11]Barton M,Yanagisawa M.Endothelin: 20 years from discovery to therapy[J].Can J Physiol Pharmacol,2008,86(8):485-498.
[12]Ieda M,Fukuda K,Hisaka Y,et al.Endothelin-1 regulates cardiac sympathetic innervation in the rodent heart by controlling nerve growth factor expression[J].J Clin Invest,2004,113(6):876-884.
[13]Bunn HF.Erythropoietin[J].Cold Spring Harb Perspect Med,2013,3(3):a11619.
[14]Kuhlmann MT,Kirchhof P,Klocke R,et al.G-CSF/SCF reduces inducible arrhythmias in the infarcted heart potentially via increased connexin43 expression and arteriogenesis[J].J Exp Med,2006,203(1):87-97.
[15]Wei L,Fraser JL,Lu ZY,et al.Transplantation of hypoxia preconditioned bone marrow mesenchymal stem cells enhances angiogenesis and neurogenesis after cerebral ischemia in rats[J].Neurobiol Dis,2012,46(3):635-645.
[16]Tan H,Zhong Y,Shen X,et al.Erythropoietin promotes axonal regeneration after optic nerve crush in vivo by inhibition of RhoA/ROCK signaling pathway[J].Neuropharmacology,2012,63(6):1182-1190.
[17]Shim W,Mehta A,Lim SY,et al.G-CSF for stem cell therapy in acute myocardial infarction: friend or foe?[J].Cardiovasc Res,2011,89(1):20-30.
[18]Liu SP,Lee SD,Lee HT,et al.Granulocyte colony-stimulating factor activating HIF-1alpha acts synergistically with erythropoietin to promote tissue plasticity.[J].PLoS One,2010,5(4):e10093.
[19]Peterson KM,Aly A,Lerman A,et al.Improved survival of mesenchymal stromal cell after hypoxia preconditioning: role of oxidative stress[J].Life Sci,2011,88(1-2):65-73.
[20]Ren H,Cao Y,Zhao Q,et al.Proliferation and differentiation of bone marrow stromal cells under hypoxic conditions[J].Biochem Biophys Res Commun,2006,347(1):12-21.
[21]Zhou Y,Guan X,Wang H,et al.Hypoxia induces osteogenic/angiogenic responses of bone marrow-derived mesenchymal stromal cells seeded on bone-derived scaffolds via ERK1/2 and p38 pathways[J].Biotechnol Bioeng,2013,110(6):1794-1804.
(本文編輯郭懷印)
(收稿日期:2015-10-21)
中圖分類號:R329
文獻標識碼:A
doi:10.3969/j.issn.1672-1349.2016.06.013
文章編號:1672-1349(2016)06-0599-05
通訊作者:伍衛,E-mail:wuwei9@mail.sysu.edu.cn
基金項目:廣東省醫學科研基金資助項目(No.B2013155)

