LSD1與冬凌草提取物相互作用的電化學研究
葛蓓蕾 陳艷 左菲菲 姚珂 徐少博 徐霞
(1.鄭州大學 實驗動物中心 河南 鄭州 450052; 2.鄭州大學 藥學院 河南 鄭州 450001)
?
LSD1與冬凌草提取物相互作用的電化學研究
葛蓓蕾1陳艷2左菲菲2姚珂2徐少博2徐霞2
(1.鄭州大學 實驗動物中心河南 鄭州450052; 2.鄭州大學 藥學院河南 鄭州450001)
【摘要】目的研究LSD1與冬凌草提取物的相互作用。方法在PH 7.40的緩沖液中,采用循環伏安法研究LSD1與冬凌草提取物(JD160和JD284)在不同條件下的相互作用。結果 在分別改變提取物濃度和掃描速率的條件下,提取物峰電流與提取物濃度和掃描速率均呈現良好的線性關系。在pH 7.40的緩沖液中,LSD1無峰電流出現,提取物有峰電流出現,且其電化學行為具有典型的不可逆特征。當LSD1逐漸加入到提取物中,二者發生作用,峰電流減小,峰電位負移。結論JD160和JD284均可與LSD1結合生成非電活性化合物,使電解液中游離化合物濃度降低。LSD1的加入使冬凌草提取物的氧化峰峰值電流減小。LSD1與JD160的相互作用可逆,與JD284不可逆。
【關鍵詞】LSD1;冬凌草提取物;循環伏安法;峰值電流
組蛋白的表觀遺傳共價修飾主要包括甲基化、乙酰化、磷酸化等。其中,組蛋白的甲基化是研究較多的修飾方式。賴氨酸特異性組蛋白去甲基化酶(lysine specific demethylase 1,LSD1) 是2004年被發現的第1個可以催化組蛋白h1K4和h1K9去甲基化的特異性去甲基化酶[1]。近幾年的研究發現,LSD1的活化過程與腫瘤細胞發生和發展相關,在前列腺癌、結腸癌、肺癌等腫瘤細胞中均發現了LSD1的高表達[2-4]。因此,LSD1一直被視為一個重要的和有前途的抗癌目標,新型LSD1抑制劑的研發也成了科研的熱點。
冬凌草是一種多年生草本植物,主產地在河南省濟源王屋山和太行山一帶。當地人用于治療食道癌已有30多年的歷史[5]。冬凌草提取物已經廣泛應用于治療腸炎、關節炎、黃疸、蛔蟲病、肝炎等病,先前的研究發現冬凌草中的二萜類化合物(如冬凌草甲素,冬凌草乙素)對人癌細胞有明顯的抑制作用[6]。本研究選擇新的冬凌草提取物JD160(圖1A)和JD284(圖1B),通過循環伏安法研究冬凌草提取物JD160和JD284與LSD1的相互作用。LSD1可以影響基因轉錄的激活和抑制,JD160和JD284與LSD1之間的相互作用可能會為LSD1抑制劑的研發提供一些重要的信息。
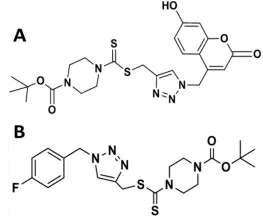
圖1 JD160(A)和JD284(B)的分子結構
1實驗部分
1.1試劑與儀器CHI-650A型電化學工作站(上海辰華儀器公司),電化學實驗用三電極系統:碳電極為工作電極,飽和甘汞電極和鉑電極分別作為參比電極和輔助電極。PHS-3C型酸度計(上海精密科學儀器有限公司),KQ-100型超聲波清洗器(昆山市超聲波儀器廠),LSD1(美國Sigma公司)用二次重蒸水配制成0.125×10-6mol/L儲備液,-20 ℃冰箱保存。冬凌草提取物JD160和JD284(均為鄭州大學藥學院自制)溶于二甲基亞砜(DMSO,天津恒興化學試劑有限公司)配成濃度為0.5×10-3mol/L的儲備液,4 ℃冰箱保存。磷酸鹽緩沖溶液(PBS,pH 4.0~6.86)備用,根據實際需要再稀釋到所需的pH值,在pH計上校準。其它試劑均為分析純或優級純。實驗用水為二次石英重蒸水。
1.2試驗方法將碳電極在濕潤的金相砂紙上磨光,然后用0.05 μm的Al2O3懸浮液拋光成鏡面,并依次用無水乙醇、二次重蒸水超聲波清洗,之后浸入到pH 7.4磷酸鹽電解液中備用。實驗在室溫(25℃)下進行。
在2個10 ml容量瓶中以pH 7.40的PBS緩沖液為底液,分別加入一定量的JD160和JD284溶液,在改變提取物濃度和掃描速率的條件下分別測定相應的循環伏安曲線。在3個10 ml容量瓶中以pH 7.40的PBS緩沖液為底液,分別加入一定量的JD160和JD284溶液及LSD1溶液,然后在前兩者中加入一定量的LSD1溶液,測定相應的循環伏安曲線。掃描速率100 mV/s,掃描范圍1.0~2.0 V。
2結果
2.1提取物濃度對峰值電流的影響用循環伏安法測定提取物濃度與峰值電流的關系如圖2所示。JD160和JD284濃度在1~8 μmol/L范圍逐漸增加時,與峰電流之間呈現線性關系。JD160濃度與峰電流的關系式為y=0.077x+0.085,相關系數R2=0.998;JD284濃度與峰電流的關系式為y=0.025x+0.136,R2=0.999。根據測定結果,選取4 μmol/L的提取物用于下一步分析。


圖2 JD160(左)和JD284(右)濃度與峰值電流的關系
2.2掃描速率對峰值電流的影響在pH 7.4的PBS電解液中,JD160和JD284在玻璃碳電極的CV圖顯示,峰值電流在第二周期減小,說明峰電流有吸附行為[7]。當掃描速率分別為20、50、100、150、200和250 mV/s,掃描范圍為1~2 V時,得到的速率與電流的關系如圖3所示。隨著掃描速率增加,JD160和JD284的氧化電流增大,并呈現良好的線性關系。JD160的峰電流與掃速的關系式為y=31.06x+2.368,R2=0.999;JD284的峰電流與掃速的關系式為y=32.00x+0.789,R2=0.998。二者關系說明在一定的掃描速率區間內,提取物JD160和JD284在電極表面上的反應受吸附控制[8]。


圖3 不同掃描速率對6.0 μmol/l的JD160(左)和JD284(右)峰值電流的影響
2.3提取物與LSD1的相互作用循環伏安法測定結果如圖4所示。0.125×10-6mol/L的LSD1溶液在pH 7.4的PBS緩沖液中1.0~2.0 V的掃描范圍內無峰電流出現。JD160和JD1284在pH 7.4的PBS緩沖液中有峰電流出現,且其電化學行為具有典型的不可逆特征[9]。當LSD1逐漸加入到JD160和JD1284中,二者相互作用,峰電流減小,峰電位負移,說明JD160和JD1284與LSD1發生了較強的作用。


a:0.125×10-6mol/L LSD1;b:4 μmol/L JD160 (JD284);c:4 μmol/L JD160 (JD284) +0.125×10-6mol/L LSD1;d:4 μmol/L JD160 (JD284) +0.25×10-6mol/L LSD1。
圖4提取物JD160(左)和JD284(右)與LSD1的相互作用
2.4相互作用時間對峰值電流的影響反應時間與峰值電流變化的關系見圖5。由左圖可見,隨著JD160與LSD1相互作用時間的增加,氧化電流開始下降,但二者作用到一定時間后,氧化電流逐漸增大。從電流減少轉向增大發生在相互作用30 min到40 min之間。由此初步推斷,LSD1與JD160可以結合生成非電活性化合物,且LSD1對JD160的抑制作用是可逆的。由右圖可見,隨著JD284與LSD1相互作用時間的增加,氧化電流開始下降,但二者作用15 min后,氧化電流基本保持穩定。由此推斷LSD1對JD284的抑制作用可能是不可逆的。


圖5 相互作用時間對JD160(左)和JD284(右)峰值電流的影響
2.5電化學參數的計算JD160和JD1284與LSD1相互作用前后的電子轉移系數可以按照下列公式計算:
|Ep-Ep/2|= 0.056 5/n
Ep/2是半峰電位,n是電子轉移常數。JD160和JD284的n值計算結果均為1。電子轉移系數α是用來描述電極電勢對陰陽極反應影響的程度,也是最動力學參數之一。根據Laviron理論[10]來估算α。
Ep=Eo-(RT/αnF)ln(αnF/RTK)-(RT/αnF)lnυ.
其中R是通用氣體常數[8.314 J/(K·mol)],T是298K,F是法拉第常數(96487 C/mol),υ是掃描速率。JD160的Epa和lnυ的線性關系為Epa= 0.073 6lnυ +1.27,R2= 0. 990,結合以上公式計算出α值為0.348。JD284的Epa和lnυ的線性關系為Epa= 0.064lnυ +1.23,R2= 0.990, 得出α值為0.40。
3討論
本文利用循環伏安法研究LSD1和冬凌草提取物之間的相互作用。結果表明,當LSD1逐漸加入到JD160和JD1284中時,二者相互作用,峰電流減小,峰電位負移,但隨著作用時間的增加,氧化電流開始下降,繼續作用到一定時間后,JD160氧化電流逐漸增大,JD1284氧化電流基本不變。這表明JD160和JD284可以與LSD1結合,生成非電化合物。LSD1對JD160的抑制是可逆的,對JD284的抑制不可逆。據此推測,LSD1與兩種提取物作用的結果不同可能與提取物的結構和相互作用的機制有關。化學參數計算結果示,JD160和JD284的電子轉移常數n為1,JD160和JD284電子轉移系數α分別為0.348和0.40。
綜上所述,我們成功地采用循環伏安法對LSD1與提取物的作用進行了測定,實驗結果證實該方法具有良好的靈敏度及選擇性,有良好的應用前景。本實驗也為新型LSD1抑制劑的研發提供了思路。
參考文獻
[1]Shi Y,Lan F,Matson C,et al.Histone demethylation mediated by the nuclear amine oxidase homolog LSD1[J].Cell,2004,119(7):941-953.
[2]Cai C,He H H,Chen S,et al.Androgen receptor gene expression in prostate cancer is directly suppressed by the androgen receptor through recruitment of lysine-specific demethylase 1[J].Cancer Cell,2011,20(4):457-471.
[3]Pollock J A,Larrea M D,Jasper J S,et al.Lysine-specific histone demethylase 1 inhibitors control breast cancer proliferation in ERα-dependent and -independent manners[J].ACS Chem Biol,2012,7(7):1221-1231.
[4]Lim S,Janzer A,Becker A,et al.Lysine-specific demethylase 1 (LSD1) is highly expressed in ER-negative breast cancers and a biomarker predicting aggressive biology[J].Carcinogenesis,2010,31(3):512-520.
[5]Tang J,Zhao M,Wang Y,et al.One single HPLC-PDA/(-)ESI-MS/MS analysis to simultaneously determine 30 components of the aqueous extract of Rabdosia rubescens[J].J Chromatogr B Analyt Technol Biomed Life Sci,2011,879(26):2783-2793.
[6]劉靜,梁敬鈺,謝韜.冬凌草研究進展[J].海峽藥學,2004,16(2):1-7.
[7]王辰,付艷麗,王振.環境激素雙酚A與蛋白質相互作用的電化學研究[J].云南民族大學學報(自然科學版),2011,20(2):92-95.
[8]廖天錄,趙強.紅霉素與DNA相互作用的電化學研究[J].大慶師范學院學報,2011,31(6):45-47.
[9]劉德龍,吳彥環,郭慧芳.鈣調素與重金屬Pb2+結合反應的方波極譜與循環伏安法研究[J].高等學校化學學報,2009,30(11):2154-2158.
[10]Dai H,Yang C,Tong Y,et al.Label-free electrochemiluminescent immunosensor for α-fetoprotein: performance of Nafion-carbon nanodots nanocomposite films as antibody carriers[J].Chem Commun(Camb),2012,48(25):3055-3057.
Electrochemical detection of lysine specific demethylase 1(LSD1) and Rabdosia extracts
Ge Beilei1, Chen Yan2, Zuo Feifei2, Yao Ke2, Xu Shaobo2, Xu Xia2
(1.TheLaboratoryAnimalCenter,ZhengzhouUniversity,Zhengzhou450052,China;2.SchoolofPharmaceuticalSciences,ZhengzhouUniversity,Zhengzhou450001,China)
【Abstract】ObjectiveTo screen the interaction of lysine specific demethylase 1(LSD1) and Rabdosia extracts. MethodsIn pH 7.4 buffer, the interaction of LSD1 and Rabdosia extracts (JD160 and JD284) was detected by cyclic voltammetry under different conditions. ResultsWhen changing extract concentration and scan rate respectively, the peak current of extract showed good linear relationship with the extract concentration and scan rate. In pH 7.40 buffer, no peak current of LSD1 appeared, while the peak current of extract appeared, and the electrochemical behavior was typically irreversible. When adding LSD1 into the extract gradually, the peak current obviously decreased, and there was a negative shift in the oxidation peak of extracts. ConclusionBoth JD160 and JD284 can be combined with LSD1 to generate non-electric complexes, which led to a decrease in the free drug concentration in the solutions. From changes to the reduction and oxidation currents, it can be concluded that the inhibition of JD160 against LSD1 is reversible, whereas JD284 is irreversible.
【Key words】lysine specific demethylase 1; Rabdosia extracts; cyclic voltammetry; peak current
(收稿日期:2015-10-27)
【中圖分類號】R 915
doi:10.3969/j.issn.1004-437X.2016.04.004
基金項目:河南省教育廳科學技術研究重點項目(13A350598)。

