抗HPV11病毒樣顆粒單克隆抗體的性質(zhì)鑒定及初步應(yīng)用
李敏,林知捷,魏希,李少偉,4,夏寧邵,4,趙勤儉Δ
(1.廈門大學(xué) 分子疫苗學(xué)和分子診斷學(xué)國(guó)家重點(diǎn)實(shí)驗(yàn)室,福建 廈門 361102;2.廈門大學(xué) 公共衛(wèi)生學(xué)院,福建 廈門 361102;3.廈門萬(wàn)泰滄海生物技術(shù)有限公司,福建 廈門 361000;4.廈門大學(xué) 生命科學(xué)學(xué)院,福建 廈門 361102)
抗HPV11病毒樣顆粒單克隆抗體的性質(zhì)鑒定及初步應(yīng)用
李敏1,2,林知捷3,魏希3,李少偉1,2,4,夏寧邵1,2,4,趙勤儉1,2Δ
(1.廈門大學(xué) 分子疫苗學(xué)和分子診斷學(xué)國(guó)家重點(diǎn)實(shí)驗(yàn)室,福建 廈門 361102;2.廈門大學(xué) 公共衛(wèi)生學(xué)院,福建 廈門 361102;3.廈門萬(wàn)泰滄海生物技術(shù)有限公司,福建 廈門 361000;4.廈門大學(xué) 生命科學(xué)學(xué)院,福建 廈門 361102)
目的 分析和鑒定抗HPV11病毒樣顆粒(virus-like particle,VLP)鼠源單克隆抗體的性質(zhì),篩選性質(zhì)和生物學(xué)活性較優(yōu)的抗體,并初步應(yīng)用于抗原或疫苗的質(zhì)量分析。方法 分別利用間接ELISA法和Western blot對(duì)HPV11的22株單克隆抗體的亞類、與HPV11 VLP的結(jié)合能力和構(gòu)象敏感性進(jìn)行檢測(cè);采用血凝抑制實(shí)驗(yàn)對(duì)單克隆抗體的血凝抑制活性進(jìn)行分析;運(yùn)用基于假病毒的抗體中和實(shí)驗(yàn)對(duì)單克隆抗體的中和活性進(jìn)行鑒定,選出中和活性高的單抗進(jìn)行兩兩配對(duì),采用雙抗夾心ELISA法捕獲單抗并篩選合適的配對(duì)雙抗。結(jié)果 對(duì)22株單抗的性質(zhì)進(jìn)行了詳細(xì)和完整的鑒定,并根據(jù)構(gòu)象敏感性進(jìn)行排序,篩選出6株型別特異、結(jié)合活性強(qiáng)且中和活性高的單抗(2A2、4A1-3、16G7、14A6、9C12和19C7);成功建立了基于單抗的雙抗夾心(14A6:Ag:9C12-HRP)ELISA定量分析方法。結(jié)論 獲得了較全面的HPV11 VLP單抗性質(zhì)信息,建立了重組HPV11抗原質(zhì)量分析的雙抗夾心ELISA法,為HPV11抗原的生命周期管理或尖銳濕疣疫苗的研發(fā)、工藝優(yōu)化、產(chǎn)品放行和穩(wěn)定性研究等提供了技術(shù)支持。
人乳頭瘤病毒;單克隆抗體;假病毒;中和活性;質(zhì)量分析
人乳頭瘤病毒(human papillomavirus,HPV)是一類無(wú)包膜的正二十面體對(duì)稱的DNA病毒,主要侵害皮膚和粘膜組織,持續(xù)感染可引起上皮細(xì)胞增生甚至癌變[1]。目前,已鑒定出200多種亞型,約40種HPV可侵犯人體粘膜組織[2]。研究表明,多種HPV類型都可引起生殖器和肛周部位的疣狀病變,即尖銳濕疣,其中近90%是由低危型HPV6/11引起[3-6]。迄今,市場(chǎng)上僅有2種基于重組病毒樣顆粒(virus-like particle,VLP)研發(fā)的對(duì)HPV6/11有保護(hù)作用的疫苗,分別是Gardasil?-4四價(jià)疫苗(HPV6/11/16/18)和Gardasil?-9九價(jià)疫苗(HPV6/11/16/18/31/33/45/52/58)[7]。目前,由本實(shí)驗(yàn)室研發(fā)的HPV6/11尖銳濕疣疫苗已進(jìn)入臨床實(shí)驗(yàn)I期。
與傳統(tǒng)的減毒或滅活疫苗相比,重組VLP疫苗不含有病毒基因,相對(duì)較安全,其功能對(duì)完整結(jié)構(gòu)的依賴性更強(qiáng),且不同病毒的重組VLP疫苗的質(zhì)量分析方法具有共性。在宮頸癌疫苗的研究中,有兩家公司已經(jīng)建立了基于特異性中和單抗的較為完善的質(zhì)量分析體系,其中較為重要的單抗分別為HPV16.V5和HPV18.J4[8]。目前,有關(guān)HPV6/11單抗的研究很少,尚未有優(yōu)勢(shì)單抗用于尖銳濕疣疫苗質(zhì)量分析的報(bào)道。所以,本研究主要是對(duì)本實(shí)驗(yàn)室研發(fā)HPV11 VLP(尖銳濕疣疫苗的有效成分之一)的單抗盤進(jìn)行詳細(xì)地性質(zhì)分析和鑒定,篩選型別特異、構(gòu)象敏感、中和活性高的單抗,并將其初步用于建立HPV11 VLP的質(zhì)控方法(雙抗夾心ELISA法),為尖銳濕疣疫苗的周期管理、生產(chǎn)放行和工藝改進(jìn)等提供技術(shù)支持。
1 材料與方法
1.1 材料
1.1.1 病毒及細(xì)胞:實(shí)驗(yàn)所用HPV6/11 VLP抗原、22株鼠源單克隆抗體及HPV11假病毒均為實(shí)驗(yàn)室生產(chǎn)純化并保存[8-10];293FT細(xì)胞購(gòu)自Invitrogen公司。
1.1.2 實(shí)驗(yàn)動(dòng)物:Balb/C小鼠購(gòu)自上海萊斯克實(shí)驗(yàn)動(dòng)物有限責(zé)任公司,飼養(yǎng)于廈門大學(xué)分子疫苗學(xué)與分子診斷學(xué)國(guó)家重點(diǎn)實(shí)驗(yàn)室 SPF 級(jí)動(dòng)物房?jī)?nèi)。本實(shí)驗(yàn)遵循《實(shí)驗(yàn)動(dòng)物保護(hù)條例》,得到本校實(shí)驗(yàn)動(dòng)物倫理委員會(huì)批準(zhǔn),廈門大學(xué)實(shí)驗(yàn)動(dòng)物許可證號(hào): SCXK(閩) 2013-0001。
1.1.3 試劑:羊抗鼠多抗GAM購(gòu)自萬(wàn)域美藍(lán)公司;單抗分型試劑盒購(gòu)自英國(guó)Serotec公司;胎牛血清(南美血源)購(gòu)自PAN Biotech;Bradford蛋白濃度測(cè)定試劑盒購(gòu)自碧云天生物技術(shù)研究所;硝酸纖維素膜為德國(guó)Schleicher&Schuell公司產(chǎn)品;Western blot ECL試劑盒購(gòu)自美國(guó)Advansta公司;辣根過(guò)氧化物酶(HRP)購(gòu)自Sigma公司;ELISA實(shí)驗(yàn)中的封閉液、樣品稀釋液和標(biāo)酶稀釋液均為實(shí)驗(yàn)室配制,命名為ED;ELISA實(shí)驗(yàn)終止液和顯色液購(gòu)自北京萬(wàn)泰生物公司;其余生化藥品均為分析純。
1.1.4 儀器:熒光斑點(diǎn)分析儀(ImmunSpot@S5 UV Analyzer)購(gòu)自美國(guó)CTL公司;蛋白電泳儀(Basic)及轉(zhuǎn)移裝置(TE77)購(gòu)自美國(guó)Bio-Rad公司;酶標(biāo)儀(PHOMO)購(gòu)自安圖實(shí)驗(yàn)儀器(鄭州)有限公司;自動(dòng)洗板機(jī)(DEM-3)購(gòu)自北京拓普分析儀器有限責(zé)任公司。
1.2 方法
1.2.1 基于間接ELISA法的單抗性質(zhì)檢測(cè)
① 單抗與抗原結(jié)合活性檢測(cè):重組蛋白HPV11 VLP(1 μg/mL)包被96孔板,每孔100 μL,用ED封閉(200 μL/孔);將22株抗HPV11 VLP單抗分別用ED稀釋至1 μg/mL,加入首孔,2倍系列稀釋11個(gè)梯度,雙孔重復(fù),室溫放置1 h;酶標(biāo)二抗GAM-HRP(1:5000)100 μL/孔,室溫放置1 h;室溫顯色10 min,終止,酶標(biāo)儀450 nm波長(zhǎng)處檢測(cè);使用GraphPad Prism 5(GraphPad, USA)軟件進(jìn)行數(shù)據(jù)分析,以四參數(shù)模型進(jìn)行曲線的擬合,計(jì)算EC50數(shù)值。
② 單抗構(gòu)象敏感性檢測(cè):重組蛋白HPV11 VLP進(jìn)行變性處理:用含有20 mM二硫蘇糖醇(DTT)的20 mM碳酸鹽緩沖液(pH 9.6)將蛋白稀釋至2 μg/mL,50 μL/孔加入96孔板內(nèi),37 ℃處理過(guò)夜烘干,獲得構(gòu)象破壞的抗原,并用ED室溫封閉2 h;同時(shí),使用未處理的HPV11 VLP 以100 ng/孔包被96孔板。實(shí)驗(yàn)過(guò)程中,單抗分別與完整HPV11 VLP和變性的HPV11抗原反應(yīng),進(jìn)行四參數(shù)擬合,分別得到EC50, Native和EC50, Denatured。單抗對(duì)所識(shí)別抗原表位的構(gòu)象敏感性由rEC50(rEC50= EC50,Native/EC50,Denatured)表示,rEC50值越大說(shuō)明單抗構(gòu)象敏感性越強(qiáng)。
③ 單抗亞類鑒定:采用Serotec公司抗體分型試劑盒通過(guò)間接ELISA法對(duì)單抗亞類進(jìn)行鑒定。
④ 單抗與HPV6 VLP的交叉反應(yīng)性檢測(cè)(型別特異性):將固定濃度的HPV11單抗(1 μg/mL)分別與包被在96孔板中的HPV6/11抗原反應(yīng)。HPV11型單抗與HPV6 VLP交叉反應(yīng)率為:OD450,HPV6/ OD450,HPV11×100%。
1.2.2 Western blot檢測(cè)單抗性質(zhì):將HPV11 VLP 進(jìn)行SDS-PAGE凝膠電泳,轉(zhuǎn)膜,封閉;將膜裁剪為0.5 cm寬的矩形條,分別與22株單抗(1 μg/mL)反應(yīng)1 h,清洗3次,與酶標(biāo)二抗GAM-HRP(1:5000)反應(yīng)1 h,清洗3次,曝光顯色。
1.2.3 基于細(xì)胞水平的單抗性質(zhì)檢測(cè)
① 小鼠紅細(xì)胞凝集與凝集抑制實(shí)驗(yàn):Balb/C小鼠眼球后取血,阿氏液抗凝;將采集到的小鼠血用PBS清洗,2500 r/min離心5 min,清洗3次,再與PBS按體積比1:99配制成1%的紅細(xì)胞懸液;取96孔U型板,在第1-11孔中加入40 μL 用PBS 1.5倍稀釋的HPV11抗原,在第12孔中加入40 μL PBS(陰性對(duì)照),雙孔重復(fù);每孔加入40 μL 1%的紅細(xì)胞懸液,室溫靜置4 h,觀察抗原使小鼠紅細(xì)胞凝集現(xiàn)象;以引起血凝現(xiàn)象的抗原最低濃度的4倍作為凝集抑制實(shí)驗(yàn)的抗原濃度。
取96孔U型板,用PBS將抗體(首孔45 μg/mL)進(jìn)行1.5倍系列稀釋到第10孔,每孔終體積40 μL,在第12孔中加入80 μL PBS;將稀釋好的抗原加入板中1-11孔,每孔40 μL;將1%的紅細(xì)胞懸液緩慢加入板中,每孔40 μL,雙孔重復(fù);室溫靜置4 h,觀察小鼠紅細(xì)胞凝集抑制現(xiàn)象。以抗體抑制血凝現(xiàn)象最低濃度的4倍作為抗體的血凝抑制滴度。
② 假病毒中和試驗(yàn)測(cè)定單抗的中和活性:基于假病毒的中和試驗(yàn)參考已有報(bào)道[8,11-12],簡(jiǎn)介如下:將100 μL 293FT細(xì)胞鋪于96孔細(xì)胞培養(yǎng)板中(1.5×104個(gè)細(xì)胞/孔)培養(yǎng)至貼壁;單抗用10%DMEM培養(yǎng)基2倍系列稀釋,雙孔重復(fù),每個(gè)梯度取60 μL與同樣體積稀釋于10%DMEM培養(yǎng)基的假病毒液(MOI=0.2)混合;取100 μL抗體-假病毒混合液加入細(xì)胞板,37 ℃孵育72 h;熒光斑點(diǎn)分析儀讀取熒光點(diǎn)數(shù),單抗的感染抑制率=[1-(樣品孔計(jì)數(shù)點(diǎn)-陰性對(duì)照孔計(jì)數(shù)點(diǎn))/(陽(yáng)性孔計(jì)數(shù)點(diǎn)-陰性對(duì)照孔計(jì)數(shù)點(diǎn))]×100%,以單抗感染抑制率和單抗?jié)舛葦M合中和曲線。抗體中和活性為抑制50%假病毒感染細(xì)胞的濃度。
1.2.4 基于非重疊雙表位的雙抗夾心ELISA方法建立:基于以上單抗性質(zhì),篩選型別特異、結(jié)合活性強(qiáng)、構(gòu)象敏感、中和活性高的單抗,分別進(jìn)行HRP標(biāo)記,兩兩配對(duì)(排除自身配對(duì));其中捕獲抗體濃度為1 μg/mL,每孔100 μL包板;抗原首孔為1 μg/mL,2倍系列稀釋11個(gè)梯度,室溫靜置1 h;酶標(biāo)二抗X-HRP(1:4000)100 μL/孔,室溫靜置1 h;顯色,終止,酶標(biāo)儀(450 nm)檢測(cè)。
數(shù)據(jù)分析采用平行線分析法:得到的雙孔重復(fù)ELISA數(shù)據(jù)偏差不超過(guò)20%時(shí)認(rèn)為重復(fù)性良好,去除偏差超過(guò)20%的數(shù)據(jù)后,用 “GraphPad Prism 5” 四參數(shù)模型進(jìn)行第一次擬合,得到4個(gè)Hillslope,樣品的Hillslope與對(duì)照樣品的Hillslope偏差不超過(guò)20%時(shí)樣品曲線有效,否則不能參與下一步擬合;排除不可用曲線后,數(shù)據(jù)進(jìn)行第二次擬合,用四參數(shù)模型進(jìn)行等底、等高和等斜率擬合,得到EC50值;樣品的相對(duì)效價(jià)rEC50=(EC50, Reference)/(EC50, Sample)×100%。
2 結(jié)果
2.1 基于免疫化學(xué)檢測(cè)方法(間接ELISA)的單抗性質(zhì)檢測(cè)
2.1.1 單抗與抗原的結(jié)合活性測(cè)定:通過(guò)單抗?jié)舛扰c顯色效應(yīng)值擬合結(jié)合曲線,計(jì)算得到EC50,EC50值越小說(shuō)明單抗與抗原的結(jié)合活性越強(qiáng),見(jiàn)圖1。單抗盤中2A2、4A1-3、16G7、10D6、14A6、9C12、19C7、18D3、1H8和17B9 10株單抗的EC50均<20 ng/mL,與抗原的結(jié)合活性較高,且均為IgG1亞型(見(jiàn)表1)。
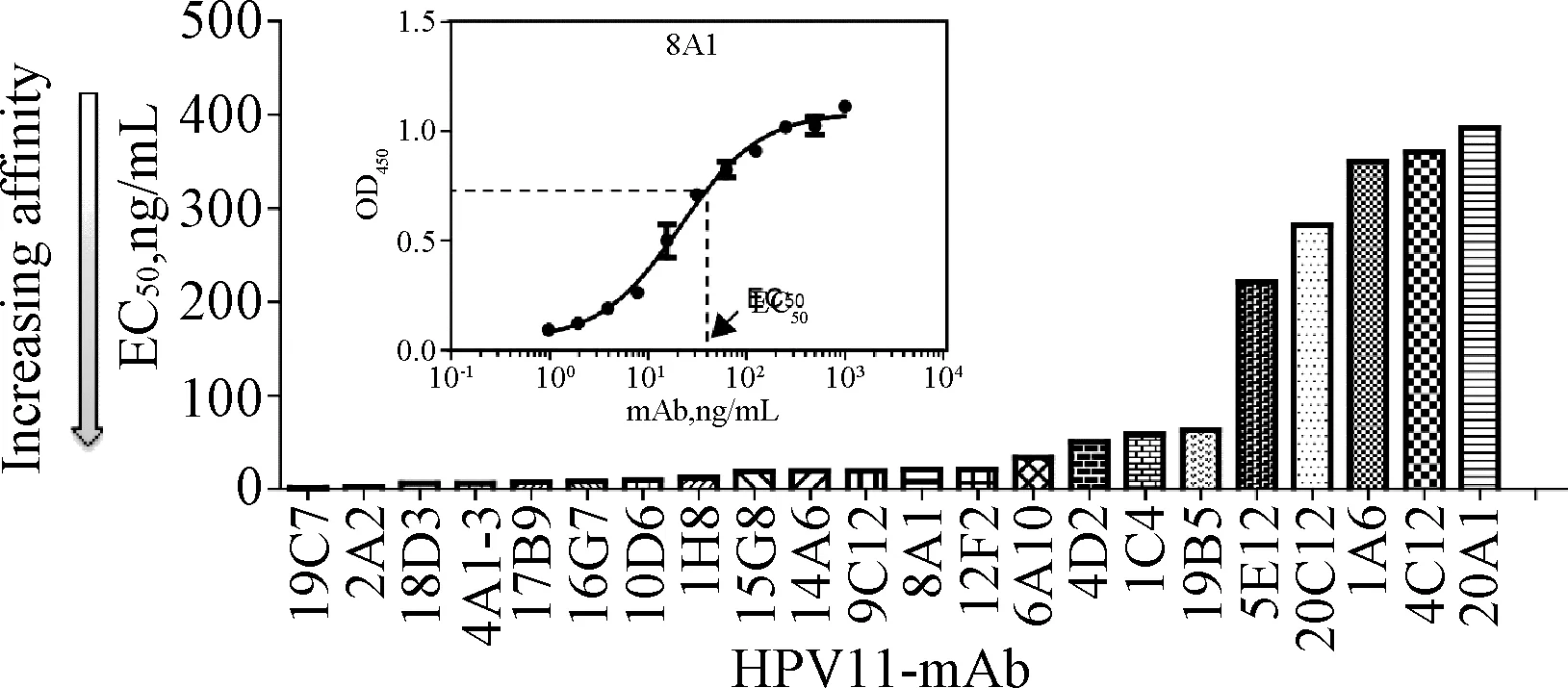
圖1 基于EC50排序的單抗與抗原結(jié)合活性(插圖:以8A1為例說(shuō)明抗體與抗原的結(jié)合反應(yīng)曲線)Fig.1 Affinity ranking based on EC50 derived from a direct ELISA assay (Inset: Binding profiles for one mAb(8A1)with strong affinity to native HPV11 antigen in a direct binding ELISA)

抗體分型結(jié)合滴度(完整VLP)EC50,ng/mL結(jié)合活性(變性VLP)EC50,ng/mL構(gòu)象敏感性(rEC50)中和活性NT50,ng/mL血凝抑制滴度μg/mL與HPV6VLP交叉反應(yīng)(%)Ⅰ.構(gòu)象非常敏感組(rEC50>15)2A2IgG12.7>1000>36022.0>45—4A1-3IgG16.4>1000>1502.05.93—16G7IgG18.3>1000>1204.045—10D6IgG110.2>1000>98.2>1000309514A6IgG119.3>1000>51.81.945—9C12IgG119.4>1000>51.73.9>45—12F2IgG2b21.4>1000>46.722.03023Ⅱ.構(gòu)象敏感組(rEC50,2.0~15)19C7IgG11.31310.31.7305418D3IgG16.328.54.62.230185E12IgG1220.8>1000>4.550.545—20C12IgM282.3>1000>3.5<1301008A1IgG121.372.13.419.230394C12IgG2a359.8>1000>2.8344.5>45271A6IgG3349.8775.32.2212.330—Ⅲ.構(gòu)象不敏感組(rEC50,0.5~2.0)19B5IgG163.6791.2>1000>45744D2IgG150.661.21.2>100020—6A10IgG2a3433.31>100020—1C4IgG158.645.90.8>100013.339115G8IgG118.7130.7>10008.8910020A1IgG1386212.60.6>100020100Ⅳ.與變性抗原反應(yīng)增強(qiáng)組(rEC50<0.5)1H8IgG112.34.50.4>100030-17B9IgG17.30.90.1>10008.89100
2.1.2 單抗構(gòu)象敏感性檢測(cè):以9C12、17B9和19C7 3株單抗為例展示擬合曲線,根據(jù)擬合曲線計(jì)算抗體與抗原的結(jié)合活性EC50,進(jìn)而求得rEC50,見(jiàn)圖2A。根據(jù)rEC50值的大小將22株單抗分為4組:構(gòu)象非常敏感組、構(gòu)象敏感組、構(gòu)象不敏感組和與變性抗原反應(yīng)增強(qiáng)組。2A2、4A1-3、16G7、10D6、14A6、9C12、12F2和19C7 8株單抗的rEC50比值均在10以上,具有較強(qiáng)構(gòu)象敏感性,可用于抗原結(jié)構(gòu)完整性的檢測(cè)。見(jiàn)表1。

圖2 ELISA檢測(cè)HPV11單抗的構(gòu)象敏感性A:9C12、17B9和19C7 的ELISA檢測(cè)曲線;B:?jiǎn)慰沟臉?gòu)象敏感性排序Fig.2 Conformational sensitivity of a panel of murine anti-HPV11 VLP mAbs based on their binding activity using native vs.denatured antigen in a direct ELISA assayA: The primary ELISA binding profiles to denatured HPV11 VLP (black curve) as compared to native HPV11 VLP (red curve), using three representative mAbs, 9C12, 17B9 and 19C7; B: Conformational sensitive priority of mAbs according to rEC50
2.1.3 單抗型別特異性鑒定:間接ELISA法檢測(cè)結(jié)果顯示:2A2、4A1-3、16G7、14A6、9C12、5E12、1A6、4D2、6A10和1H8共10株單抗與HPV6 VLP均無(wú)反應(yīng),為HPV11型別特異的單抗;其余12株單抗與HPV6 VLP均有不同程度的交叉反應(yīng)(見(jiàn)表1)。
2.2 Western blot檢測(cè)單抗的效價(jià) Western blot檢測(cè)結(jié)果顯示:?jiǎn)慰古cHPV11 VLP作用后在55 kDa 左右有明顯條帶;6A10、15G8、17B9、20A1、4D2、1C4、1H8、1A6和8A1等單抗與變性HPV11抗原反應(yīng)較明顯,為識(shí)別線性表位單抗;其余單抗反應(yīng)不明顯,為識(shí)別構(gòu)象表位單抗;該結(jié)果與圖2中ELISA檢測(cè)結(jié)果一致,見(jiàn)圖3。

圖3 Western blot檢測(cè)HPV11單抗的構(gòu)象敏感性Fig.3 Conformational sensitivity of a panel of murine anti-HPV6 VLP mAbs based on Western blot assay
2.3 小鼠紅細(xì)胞凝集與凝集抑制實(shí)驗(yàn) 在小鼠紅細(xì)胞凝集實(shí)驗(yàn)中,HPV11 VLP濃度為3.94 μg/mL時(shí)可引起小鼠紅細(xì)胞凝集,以4倍該濃度即15.76 μg/mL為凝集抑制實(shí)驗(yàn)抗原的濃度;以4A1-3為例展示單抗抑制小鼠紅細(xì)胞凝集現(xiàn)象,隨著單抗?jié)舛鹊慕档停溲种颇芰χ饾u減弱,見(jiàn)圖4。除2A2、9C12、4C12和19B5 4株單抗在濃度45 μg/mL時(shí)未觀察到凝集抑制現(xiàn)象,其余18株單抗均可以產(chǎn)生凝集抑制現(xiàn)象,但其效力不同(見(jiàn)表1)。表明HPV11 VLP具有完整的生物活性,且部分抗體可抑制由HPV11 VLP引起的細(xì)胞凝集反應(yīng)。

圖4 HPV11單抗的血凝抑制活性Fig.4 Cell-based hemagglutination inhibition activity of anti-HPV11 mAbs
2.4 基于假病毒中和試驗(yàn)的單抗中和活性 以抗體濃度與假病毒感染抑制率擬合曲線,結(jié)果見(jiàn)圖5。通過(guò)抑制曲線計(jì)算抗體的中和滴度NT50(ng/mL),結(jié)果見(jiàn)表1。NT50越小說(shuō)明抗體的中和活性越高,綜合表1數(shù)據(jù)可發(fā)現(xiàn):中和活性越高的單抗與抗原的結(jié)合活性越高,構(gòu)象敏感性越強(qiáng)。

圖5 基于假病毒(L1+L2)中和模型的HPV11單抗中和活性擬合曲線(以4A1-3,5E12和8A1為例)Fig.5 Profiles of viral neutralizing activity of anti-HPV11 mAbs (taking 4A1-3,5E12 and 8A1 for examples) in a HPV PsV-based assay
2.5 基于非重疊雙表位的雙抗夾心ELISA方法建立 根據(jù)以上對(duì)HPV11 VLP單抗的性質(zhì)鑒定,篩選出型別特異、結(jié)合活性強(qiáng)、構(gòu)象敏感、中和活性高的6株單抗(2A2、4A1-3、9C12、10D6、16G7、19C7和14A6)。以上6株抗體與結(jié)合活性較高、構(gòu)象較敏感的單抗10D6共同用于雙抗夾心ELISA法的建立。如圖6A所示:以19C7:Ag:X-HRP為例,每種配對(duì)均可得到完整的擬合曲線并求得EC50,EC50值越小說(shuō)明該配對(duì)的靈敏度越高。通過(guò)初步篩選(圖6B),確定14A6、19C7和9C12作為候選捕獲單抗,9C12、10D6和19C7作為候選檢測(cè)單抗,進(jìn)行重現(xiàn)性考察。
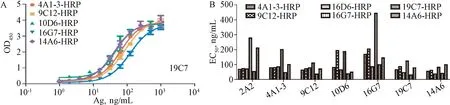
圖6 基于非重疊雙表位的雙抗夾心方法的初步篩選A:以19C7為捕獲抗體的配對(duì)擬合曲線;B:雙抗夾心ELISA配對(duì)初步結(jié)果Fig.6 Screening of two none-overlapping epitopes based sandwich ELISA assay in detecting the elative antigenicity determination of HPV11 antigenA: Profiles of 19C7:Ag:X-HRP in a sandwich ELISA; B: Preliminarily screening of the capture mAb and detection mAb in a sandwich ELISA assay


圖7 基于非重疊雙表位的雙抗夾心ELISA方法的建立A:候選雙抗夾心ELISA法單抗配對(duì)重現(xiàn)性考察;B:雙抗夾心ELISA方法14A6:Ag:9C12-HRP的確立Fig.7 Establishing of two none-overlapping epitopes based sandwich ELISA assay in detecting the elative antigenicity determination of HPV11 antigenA: Reproducibility study of 7 candidates in the sandwich ELISA; B: Profiles used to show the relative antigenicity(rEC50)of HPV11 using 14A6:Ag:9C12-HRP
3 討論
重組VLP疫苗的質(zhì)量分析是運(yùn)用定性或定量的方法對(duì)可誘發(fā)保護(hù)性中和抗體表位進(jìn)行分析的過(guò)程。HPV型別特異的中和單抗可特異性的識(shí)別VLP上的表位,間接反映VLP的結(jié)構(gòu)特點(diǎn)和活性成分,因此,可利用特異性的單抗建立疫苗的質(zhì)量分析方法[13-15]。本研究對(duì)HPV11 VLP的單抗盤進(jìn)行了詳細(xì)的性質(zhì)分析,獲得了22株單抗的亞類、與抗原的結(jié)合活性、構(gòu)象敏感性、血凝抑制活性及中和活性等性質(zhì),并根據(jù)單抗的構(gòu)象敏感性將其分為4組:構(gòu)象非常敏感組、構(gòu)象敏感組、構(gòu)象不敏感組和與變性后抗原結(jié)合活性增強(qiáng)組。根據(jù)單抗性質(zhì),篩選出型別特異、構(gòu)象敏感、中和活性高的抗體6株(2A2、4A1-3、9C12、16G7、19C7和14A6),與結(jié)合活性高、構(gòu)象較敏感的10D6共同用于建立HPV11抗原及疫苗的質(zhì)量分析方法;利用14A6和9C12 2株單抗建立了靈敏度高、重現(xiàn)性較好的雙抗夾心ELISA法,可用于疫苗抗原的生產(chǎn)周期管理,疫苗的放行、工藝改進(jìn)及穩(wěn)定性研究。
雙抗夾心ELISA方法可作為疫苗的體外效力評(píng)價(jià)實(shí)驗(yàn)(in vitro relative potency assay,IVRP)。有公司已通過(guò)長(zhǎng)期的數(shù)據(jù)積累確立了IVRP與動(dòng)物實(shí)驗(yàn)之間的相關(guān)性,并將其取代動(dòng)物實(shí)驗(yàn)用于HPV疫苗的常規(guī)生產(chǎn)監(jiān)測(cè)和放行實(shí)驗(yàn)中[16]。本課題組亦將積累IVRP與動(dòng)物實(shí)驗(yàn)的相關(guān)數(shù)據(jù),并分析2者的相關(guān)性,為IVRP代替動(dòng)物實(shí)驗(yàn)應(yīng)用于疫苗生產(chǎn)和放行中提供數(shù)據(jù)支持。
型別特異、構(gòu)象敏感、中和活性高的單抗作為分子探針可以用于疫苗的免疫效果評(píng)價(jià)[17-19],從而更好的認(rèn)識(shí)和理解抗原表位信息,有利于進(jìn)一步研究HPV11抗原與機(jī)體的作用機(jī)制[20-22]。為獲得更加詳細(xì)的抗原表位信息,后期課題組將嘗試通過(guò)X-射線晶體衍射技術(shù)或低溫電鏡三維立體重建技術(shù)確定關(guān)鍵中和抗體識(shí)別的表位,這將有助于新的治療手段或新型疫苗的研發(fā)[23-25]。
綜上,本研究獲得了較為詳細(xì)的HPV11 VLP單抗盤的信息,為建立基于抗原抗體特異反應(yīng)的多角度全方位的疫苗抗原分析方法奠定了工作基礎(chǔ);利用篩選出的單抗建立了HPV11抗原質(zhì)量分析的雙抗夾心ELISA法,為基因工程重組尖銳濕疣疫苗的研發(fā)、工藝優(yōu)化、產(chǎn)品放行和穩(wěn)定性研究等提供了技術(shù)支持。
[1] De Villiers EM.Cross-roads in the classification of papillomaviruses[J].Virology,2013,445(1-2): 2-10.
[2] Chesson HW,Dunne EF,Hariri S,et al.The estimated lifetime probability of acquiring human papillomavirus in the United States[J].Sex Transm Dis,2014,41(11):660-664.
[3] Aubin F,PRETET JL,Jacquard AC,et al.Human papillomavirus genotype distribution in external acuminata condylomata: A large French national study (EDiTH IV)[J].Clin Infect Dis,2008,47(5): 610-615.
[4] Bosch FX,Burchell AN,Schiffman M,et al.Epidemiology and natural history of human papillomavirus infections and type-specific implications in cervical neoplasia[J].Vaccine,2008,26 Suppl 10(K1-16).
[5] Garland SM,Steben M,Sings HL,et al.Natural history of genital warts: analysis of the placebo arm of 2 randomized phase III trials of a quadrivalent human papillomavirus (types 6,11,16,and 18) vaccine[J].J Infect Dis,2009,199(6): 805-814.
[6] Gissmannl L,Wolnik L,Ikenbenrg H,et al.Human papillomavirus types 6 and 11 DNA sequences in genital and laryngeal papillomas and in some cervical cancers[J].Proc Natl Acad Sci U S A,1983,80(2): 560-563.
[7] Dochez C,Bogers JJ,Verhelst R,et al.HPV vaccines to prevent cervical cancer and genital warts: an update[J].Vaccine,2014,32(14): 1595-1601.
[8] Smith JF,Kowalski R,Esser MT,et al.Evolution of type-specific immunoassays to evaluate the functional immune response to Gardasil: a vaccine for human papillomavirus types 16,18,6 and 11[J].Hum Vaccin,2008,4(2): 134-142.
[9] 楊春燕,李少偉,王晉,等.大腸桿菌來(lái)源的人乳頭瘤病毒11型病毒樣顆粒的制備及其免疫原性[J].微生物學(xué)報(bào),2009,49(11):1527-1533.
[10] 潘暉榕,李少偉,劉波,等.人乳頭狀瘤病毒6型類病毒顆粒的制備及其中和抗體的檢測(cè)[J].腫瘤免疫,2009,29(1):71-76.
[11] 盧五迅,程通,李少偉,等.人乳頭瘤病毒16型假病毒中和實(shí)驗(yàn)的建立和初步應(yīng)用[J].生物工程學(xué)報(bào),2006,22(6):990-995.
[12] 趙慧,李娟,潘暉榕,等.HPV16/18假病毒中和抗體檢測(cè)方法的驗(yàn)證[J].微生物學(xué)免疫學(xué)進(jìn)展,2012,40(6):20-24.
[13] Culp TD,Spatz CM,Reed CA,et al.Binding and neutralization efficiencies of monoclonal antibodies,Fab fragments,and scFv specific for L1 epitopes on the capsid of infectious HPV particles[J].Virology,2007,361(2):435-446.
[14] Guan J,Bywaters SM,Brendle SA,et al.Structural comparison of four different antibodies interacting with human papillomavirus 16 and mechanisms of neutralization[J].Virology,2015,483:253-263.
[15] Rizk RZ,Christesen ND,Michael KM,et al.Reactivity pattern of 92 monoclonal antibodies with 15 human papillomavirus types[J].J Gen Virol,2008,89(Pt 1):117-129.
[16] Shank-retzlaff M,Wang F,Morley T,et al.Correlation between mouse potency and In Vitro relative potency for human papillomavirus vype 16 virus-like particles and gardasil(R)vaccine samples[J].Hum Vaccines,2005,1(5):191-197.
[17] Wang ZH,Christensen N,Schiller JT,et al.A monoclonal antibody against intact human papillomavirus type 16 capsids blocks the serological reactivity of most human sera[J].J Gen Virol,1997,78:2209-2215.
[18] Roberts C,Green T,Hess E,et al.Development of a human papillomavirus competitive luminex immunoassay for 9 HPV types[J].Hum Vacc Immunother,2014,10(8):2168-2174.
[19] Zhao QJ,Potter CS,Carragher B,et al.Characterization of virus-like particles in GARDASIL(R)by cryo transmission electron microscopy[J].Hum Vacc Immunother,2014,10(3):734-739.
[20] Combita AL,Touze A,Bousarghin L,et al.Identification of two cross-neutralizing linear epitopes within the L1 major capsid protein of human papillomaviruses[J].J Virol,2002,76(13):6480-6486.
[21] Vidyasagar P,Sridevi VN,Rajan S,et al.Generation and characterization of neutralizing monoclonal antibodies against baculo-expressed HPV 16 VLPs[J].Eur J Microbiol Immunol (Bp).,2014,4(1):56-64.
[22] Zhang X,Xin L,Li S,et al.Lessons learned from successful human vaccines: Delineating key epitopes by dissecting the capsid proteins[J].Hum Vaccin Immunother,2015,11(5):1277-1292.
[23] Fleury MJJ,Touze A,Coursaget P.Human papillomavirus type 16 pseudovirions with few point mutations in L1 major capsid protein FG loop could escape actual or future vaccination for potential use in gene therapy[J].Mol Biotechnol,2014,56(5):479-486.
[24] Schellenbacher C,Kwak K,Fink D,et al.Efficacy of RG1-VLP vaccination against infections with genital and cutaneous human papillomaviruses[J].J Invest Dermatol,2013,133(12):2706-2013.
[25] Huber B,Schellenbacher C,Jindra C,et al.A chimeric 18L1-45RG1 virus-like particle vaccine cross-protects against oncogenic alpha-7 human papillomavirus types[J].PloS one,2015,10(3): e0120152.
(編校:吳茜)
Monoclonal antibodies against HPV11 virus-like particles: functional characteristics and application on quality assessment
LI Min1,2, LIN Zhi-jie3, WEI Min-xi3, LI Shao-wei1,2,4, XIA Ning-shao1,2,4, ZHAO Qin-jian1,2 Δ
(1.State Key Laboratory of Molecular Vaccinology and Molecular Diagnostics, Xiamen University, Xiamen 361102, China;2.School of Public Health, Xiamen University, Xiamen 361102, China; 3.Innovax Corporation, Xiamen 361000, China;4.School of Life Science, Xiamen University, Xiamen 361102, China)
ObjectiveTo quantitatively analyze the characteristics of a panel of murine anti-human papillomavirus(HPV)11 L1-derived virus-like particle(VLP)monoclonal antibodies(mAbs)and establish the mAb-based methods for antigen quality analysis.MethodsA panel of 22 murine anti-HPV11 mAbs were characterized in details with their isotype, and binding affinity, conformational sensitivity were examined quantitatively in the direct binding ELISA and Western blot.The hemagglutination inhibition activity of mAbs were identified using the hemagglutination inhibition assay and the pseudovirus(PsV)neutralization efficiency were examined quantitatively using the PsV-based neutralization assay.The type-specific, highly conformational sensitive and neutralizing mAbs were selected to be used in the sandwich ELISA assay.ResultsBased on the quantitative and semi-quantitative results, six type-specific, highly conformational sensitive and neutralizing mAbs (2A2, 4A1-3, 16G7, 14A6, 9C1 and 19C7) were identified.These mAbs, along with 10D6 were screened as the capture mAb or as the detection mAb in the sandwich ELISA.ConclusionThe binding affinity, conformational sensitivity and neutralization efficiency of anti-HPV11 mAbs were characterized in details.A mAb-based sandwich ELISA assay (14A6:Ag:9C12-HRP) were developed, which could be used in the in vitro potency analysis of HPV11 VLP-based vaccine.
human papillomavirus; monoclonal antibody; pseudovirion; neutralization; quality analysis
重大新藥創(chuàng)制(2015ZX09101034)
李敏,女,碩士在讀,研究方向:生物大分子質(zhì)量分析,E-mail:km123ll@163.com;趙勤儉,通信作者,男,博士,教授、博士生導(dǎo)師,研究方向:大分子藥物研發(fā),E-mail:qinjian_zhao@xmu.edu.cn。
R373
A
10.3969/j.issn.1005-1678.2016.04.03

