隱丹參酮抑制惡性神經膠質瘤細胞C6增殖及對JAK2-STAT3信號通路的影響
唐煥煥,沈曉燕,段小群,徐 慶,苑 博,張嫦麗,呂 良
隱丹參酮抑制惡性神經膠質瘤細胞C6增殖及對JAK2-STAT3信號通路的影響
唐煥煥1,沈曉燕2,段小群1,徐慶1,苑博1,張嫦麗1,呂良1
目的 評估隱丹參酮對惡性神經膠質瘤細胞C6的增殖作用及對JAK2-STAT3信號通路的影響。方法 使用MTT法評價隱丹參酮對C6細胞存活率的影響,使用hochest染色和BrdU插入法檢測隱丹參酮對C6細胞凋亡和增殖的影響,使用Western blot法檢測隱丹參酮對C6細胞p-JAK2和p-STAT3(Tyr705)的影響。結果 隱丹參酮顯著抑制C6的生長和增殖(P<0.05),但不促進凋亡。隱丹參酮顯著抑制p-STAT3(Tyr705)蛋白表達,但不影響p-JAK2。結論 隱丹參酮是惡性神經膠質瘤C6的抗增殖劑,其作用機制與抑制STAT3信號有關。
惡性神經膠質瘤;增殖;JAK2-STAT3信號通路
網絡出版時間:2016-5-9 15:43:10 網絡出版地址:http://www.cnki.net/kcms/detail/34.1065.R.20160509.1543.004.html
惡性神經膠質瘤是原發性腦腫瘤中最常見的惡性腫瘤,并具有高死亡率[1]。惡性神經膠質瘤的經典治療方法包括手術切除、術后放射治療和化療(通常用替莫唑胺)。但是,基于這些療法,患者平均存活時間僅為14.6個月,并且,在過去的二十年中,患者的存活率并沒有顯著改善[2]。因此,為了提高神經膠質瘤的治療的效果,探索更有效的治療方法很有必要。隱丹參酮(cryptotanshinone),從丹參中提取分離得到的主要活性成分之一,已經報道具有廣泛的藥理作用。研究[3]顯示隱丹參酮可以減輕氧化低密度脂蛋白誘導的動脈粥樣硬化病灶的事件,并減輕大鼠心肌缺血再灌注損傷。隱丹參酮通過抑制RAW264.7細胞NF-κB和絲裂原活化蛋白激酶(MAPK)信號傳導途徑抑制炎性細胞因子的分泌[4]。同時,隱丹參酮通過調節淀粉樣前體蛋白的代謝產生神經保護和抗阿爾茨海默病的作用[5]。研究[6-9]顯示,隱丹參酮具有抗腫瘤的活性。該研究旨在研究隱丹參酮對惡性神經膠質瘤細胞C6的抗腫瘤作用,并探索其作用機制。
1 材料與方法
1.1主要儀器與試劑 熒光倒置顯微鏡購自日本NIKON公司產品;CO2培養箱購自美國Thermo公司產品;酶標儀購自美國Bio-Tech公司;C6細胞購自中國科學院上海生命科學研究院細胞資源中心;DMEM、青霉素鏈霉素雙抗(PS)、胎牛血清(FBS)購自美國Gibco公司;隱丹參酮、MTT、DMSO購自美國Sigma Aldrich公司;BrdU細胞增殖試驗盒購自美國Exalpha Biologicals公司;抗p-STAT3(Tyr705)和抗p-JAK2抗體購自美國Cell Signaling Technology公司;抗GAPDH抗體、hochest33258購自蘇州碧云天公司。
1.2方法
1.2.1細胞培養 C6細胞用高葡萄糖DMEM培養基,含10%FBS、100 μg/ml鏈霉素和100 U/ml的青霉素,在37℃、5%CO2培養箱中培養。每周1次的間隔,以1∶5的比例進行傳代培養。
1.2.2MTT法 為了測量細胞生長,進行MTT測定法。細胞鋪在100 μl 96孔板的培養基中。培養過夜后,將細胞用各種濃度的CTS的處理24~48 h,然后用MTT(5 mg/ml)孵育和DMSO(100 μl/孔)溶解。用酶標儀測定570 nm處的吸光度值。
1.2.3hochest33258法染色細胞 細胞接種于培養板,不同濃度隱丹參酮處理24 h后,棄去培養液,用PBS洗3次,4%多聚甲醛常溫下固定30 min,PBS洗3次,5 mg/L Hoechst 33258常規染色10 min,PBS洗3次,倒置熒光顯微鏡下觀察。
1.2.4BrdU細胞增殖試驗 參考文獻[10]報道和BrdU細胞增殖測定試劑盒說明,對細胞增殖進行測定。簡言之,將細胞懸浮在生長培養基中接種在96孔板中,密度為每個孔10 000個細胞,并在5%的CO2培養箱37℃培養過夜。第2天加入0~20 μmol/L濃度的隱丹參酮。隱丹參酮處理48 h后,20 μl的BrdU加入到每個孔,孵育12 h。然后加入固定液在室溫中培養30 min。洗滌后,細胞與一個預稀釋的檢測抗體在室溫下孵育1 h。加入HRP偶聯的二抗在室溫下孵育1 h后,加入終止液。然后用酶標儀在450 nm測定光密度值。
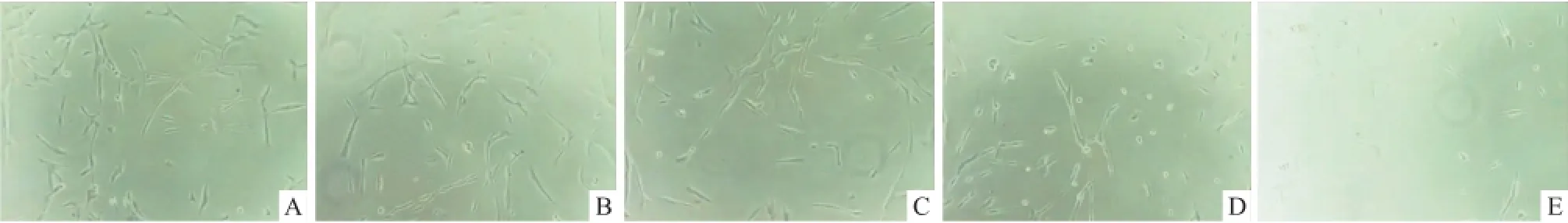
圖1 不同濃度隱丹參酮對C6細胞形態的影響 ×100A:隱丹參酮(0 μmol/L)處理組;B:隱丹參酮(2.5 μmol/L)處理組;C:隱丹參酮(5 μmol/L)處理組;D:隱丹參酮(10 μmol/L)處理組;E:隱丹參酮(20 μmol/L)處理組
1.2.5Western blot法檢測 各組細胞用預冷的PBS洗滌2次,用RIPA緩沖液[含50 mmol/L的Tris,pH 7.4,150 mmol/L NaCl,1 mmol/L的PMSF,1 mmol/L的EDTA,1%的Triton X-100,0.1%十二烷基硫酸鈉(SDS),1 mmol/L的Na3VO4,1 mmol/L的NaF和蛋白酶抑制劑混合物(羅氏公司)]收集蛋白樣品。含等量蛋白的樣品通過SDS-PAGE凝膠電泳分離,并轉移至硝酸纖維素膜上。膜在含0.05% Tween-20的PBS中用5%脫脂牛奶封閉1 h,然后在4℃中用一抗孵育過夜。然后將膜用PBS洗滌后,用辣根過氧化物酶連接的二抗在室溫孵育1 h。條帶通過增強型化學發光液進行免疫發光并進行檢測,用化學發光成像儀觀察。
2 結果
2.1從細胞形態角度觀察隱丹參酮對C6細胞生長的影響 加不同濃度隱丹參酮后,在顯微鏡下觀察細胞的密度、形態,見圖1,隨著隱丹參酮濃度的增加,細胞密度減少。
2.2采用MTT法檢測隱丹參酮對C6細胞生長的影響 各組間差異有統計學意義(F=100.87,P<0.05),隱丹參酮呈濃度依賴性抑制C6細胞生長。見圖2。
2.3使用BrdU摻入測定法確認CTS對細胞增殖的效果 各組間差異有統計學意義(F=48.08,P<0.05),隱丹參酮劑量依賴性抑制C6細胞增殖。見圖3。
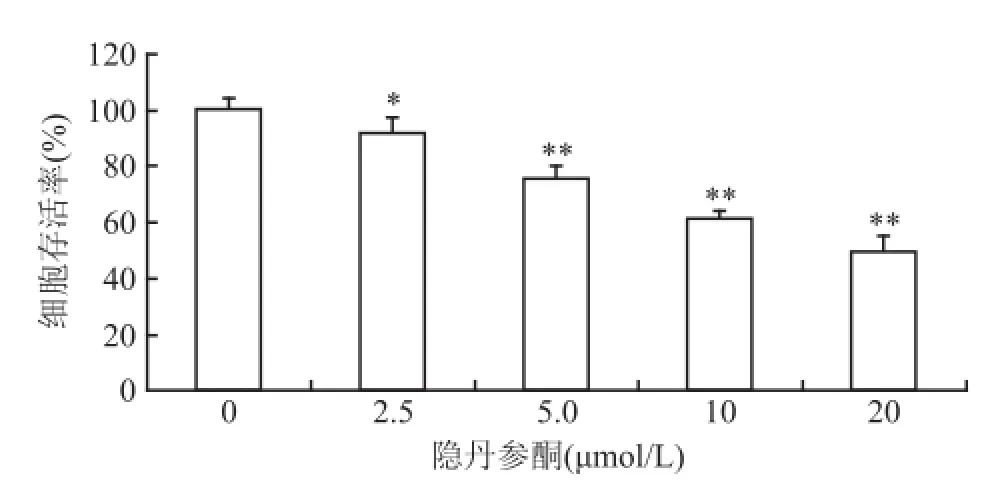
圖2 隱丹參酮對C6細胞存活率的影響與隱丹參酮0 μmol/L組比較:*P<0.05,**P<0.01
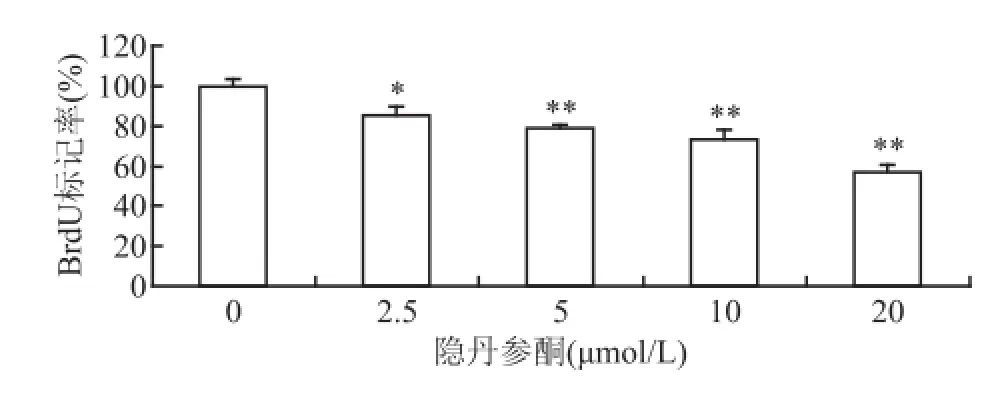
圖3 隱丹參酮對C6細胞增殖率的影響與隱丹參酮0 μmol/L組比較:*P<0.05,**P<0.01
2.4采用hochest33258法檢測隱丹參酮對C6細胞凋亡的影響 不同劑量隱丹參酮(0~20 μmol/ L)處理24 h后細胞核呈現彌漫均勻的低強度熒光,呈淺染核大形態,均未出現核碎裂、核固縮等典型細胞凋亡形態。見圖4。
2.5Western blot法檢測隱丹參酮對激活狀態的STAT3的作用 STAT3信號通路在腫瘤生長中有關鍵作用,STAT3信號通路在人腦膠質瘤細胞呈持續激活狀態。本實驗研究隱丹參酮是否對激活狀態的STAT3具有作用。隱丹參酮(5、10 μmol/L)對C6細胞Tyr705位點磷酸化具有抑制作用。為了探索隱丹參酮是否通過抑制STAT3上游信號通路引起的其磷酸化水平的變化,本研究檢測STAT3的上游激酶JAK2的磷酸化水平。隱丹參酮(5、10 μmol/L)處理1 h后,使用Western blot法檢測p-JAK2、p-STAT3(Tyr705)和GAPDH蛋白表達水平,結果顯示隱丹參酮并不影響上游激酶JAK2的磷酸化水平,見圖5。

圖4 不同濃度隱丹參酮對C6細胞核hochest33258染色的影響 ×100A:隱丹參酮(0 μmol/L)處理組;B:隱丹參酮(2.5 μmol/L)處理組;C:隱丹參酮(5 μmol/L)處理組;D:隱丹參酮(10 μmol/L)處理組;E:隱丹參酮(20 μmol/L)處理組
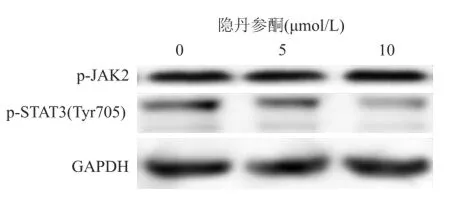
圖5 不同濃度隱丹參酮對C6細胞p-JAK2和p-STAT3(Tyr705)的影響
3 討論
本實驗研究了隱丹參酮對神經膠質瘤細胞株C6的增殖作用,并探討其可能機制。結果表明:①隱丹參酮具有抑制神經膠質瘤細胞株C6生長的作用;②隱丹參酮抑制神經膠質瘤細胞株C6的生長是通過抑制細胞增殖途徑,而不是凋亡;③隱丹參酮抑制p-STAT3(Tyr705),但不抑制其上游激酶JAK2。
前期研究[11]中用隱丹參酮處理正常大鼠腦細胞(原代皮層神經元和星形膠質細胞)顯示,在2.5~20 μmol/L濃度范圍內隱丹參酮對正常細胞沒有毒性。因此本研究使用了上述濃度進行大鼠來源的惡性膠質瘤細胞株C6的抗腫瘤實驗。隱丹參酮對其它類型腫瘤的作用已有部分報道[6-9],在HepG2和MCF7腫瘤細胞,隱丹參酮通過誘導細胞凋亡抑制細胞生長。在前列腺癌、白血病和宮頸癌細胞株,隱丹參酮既誘導細胞凋亡,又抑制其增殖,從而抑制腫瘤細胞生長[6-9]。研究顯示隱丹參酮抑制神經膠質瘤細胞的生長作用是通過增殖途徑,且沒有證據表明隱丹參酮會誘導神經膠質瘤細胞凋亡。而在惡性神經膠質瘤細胞STAT3是持續性激活的,這與正常細胞不同[12]。因此,特異性靶向STAT3信號的被認為是治療惡性神經膠質瘤的具有潛在開發價值的靶點[13]。
已經有文獻[14]報道,隱丹參酮不會影響上游激酶的磷酸化水平,如EGFR和Src。因此,本研究選擇檢測這些生長因子和細胞因子受體的下游激酶(JAK2),而這些激酶在膠質瘤中是異常激活的。遺憾的是,并沒有顯示隱丹參酮對p-JAK2具有改變作用。雖然最近的研究[10]表明,CTS通過抑制mTOR信號抑制Rh30和DU145細胞的增殖。并且,在C5a誘導的RAW264.7細胞的遷移實驗中,隱丹參酮抑制p-Akt[15]。因此在不同細胞類型中隱丹參酮可能具有不同的作用和機制。可以確認CTS選擇性阻斷STAT3的酪氨酸磷酸化。
綜上所述,當前的研究表明,CTS可能是一個潛在的神經膠質瘤抗增殖劑,其機制可能與STAT3信號有關。
[1] Ohgaki H,Kleihues P.Population-based studies on incidence,survival rates,and genetic alterations in astrocytic and oligodendroglial gliomas[J].J Neuropathol Exp Neurol,2005,64(6):479-89.
[2] Stupp R,Mason W P,van den Bent M J,et al.Radiotherapy plus concomitantand adjuvant temozolomide for glioblastoma[J].N Engl J Med,2005,352(10):987-96.
[3] Ang K P,Tan H K,Selvaraja M,et al.Cryptotanshinone attenuates in vitro oxLDL-induced prelesional atherosclerotic events[J].Planta Med,2011,77(16):1782-7.
[4] Tang S,Shen X Y,Huang H Q,et al.Cryptotanshinone suppressed inflammatory cytokines secretion in RAW264.7 macrophages through inhibition of the NF-kappaB and MAPK signaling pathways[J].Inflammation,2011,34(2):111-8.
[5] Mei Z,Zhang F,Tao L,et al.Cryptotanshinone,a compound from Salvia miltiorrhiza modulates amyloid precursor protein metabolism and attenuates beta-amyloid deposition through upregulating alpha-secretase in vivo and in vitro[J].Neurosci Lett,2009,452(2):90-5.
[6] Park I J,Kim M J,Park O J,et al.Cryptotanshinone induces ER stress-mediated apoptosis in HepG2 and MCF7 cells[J].Apopto-sis,2012,17(3):248-57.
[7] Li H,Zhang Q,Chu T,et al.Growth-inhibitory and apoptosis-inducing effects of tanshinones on hematological malignancy cells and their structure activity relation-ship[J].Anticancer Drugs,2012,23(8):846-55.
[8] 葉因濤,徐文清,仲 巍.隱丹參酮對宮頸癌Hela細胞增殖及細胞凋亡的影響[J].中國中藥雜志,2010,35(1):118-21.
[9] Chen W,Luo Y,Liu L,et al.Cryptotanshinone inhibits cancer cell proliferation by suppressing Mammalian target of rapamycinmediated cyclin D1 expression and Rb phosphorylation[J].Cancer Prev Res(Phila),2010,3(8):1015-25.
[10]Park S J,Kong H K,Kim Y S,et al.Inhibition of S-adenosylhomocysteine hydrolase decreases cell mobility and cell proliferation through cell cycle arrest[J].Am J Cancer Res,2015,5(7):2127-38.
[11]Lu L,Li C,Li D,et al.Cryptotanshinone inhibits human glioma cell proliferation by suppressing STAT3 signaling[J].Mol Cell Biochem,2013,381(1-2):273-82.
[12]Heimberger A B,Priebe W.Small molecular inhibitors of p-STAT3:novel agents for treatment of primary and metastatic CNS cancers[J].Recent Patent CNS Drug Discov,2008,3(3):179 -88.
[13]Doucette T A,Kon g L Y,Yang Y,et al.Signal transducer and activator of transcription 3 promotes angiogenesis and drives malignant progression in glioma[J].Neuro Oncol,2012,14(9):1136-45.
[14]Shin D S,Kim H N,Shin K D,et al.Cryptotanshinone inhibits constitutive signal transducer and activator of transcription 3 function through blocking the dimerization in DU145 prostate cancer cells[J].Cancer Res,2009,69(1):193-202.
[15]Don M J,Liao J F,Lin L Y,et al.Cryptotanshinone inhibits chemotactic migration in macrophages through negative regulation of the PI3K signaling pathway[J].Br J Pharmacol,2007,151(5):638-46.
Cryptotanshinone inhibits proliferation of malignant glioma C6 cells and its influence on JAK2-STAT3 signal pathway
Tang Huanhuan1,Shen Xiaoyan2,Duan Xiaoqun1,et al
(1Dept of Pharmacology,Guilin Medical University of Pharmacy,Guangxi 541001;2Dept of Pharmacology and Biochemistry,Fudan University of Pharmacy,Shanghai 200120)
Objective To evaluate the effect of cryptotanshinone(CTS)on the proliferation of malignant glioma C6 cells and its influence on JAK2-STAT3 signal pathway.Methods MTT was used to evaluate the survival rate of CTS on C6 cells.Hochest staining and BrdU assay was used to detect the cell apoptosis and proliferation.Western blot was used to detect the expressions of p-JAK2 and p-STAT3(Tyr705).Results CTS inhibited C6 cells growth and proliferation significantly(P<0.05),but not induced apoptosis.CTS decreased phosphorylation of p-STAT3(Tyr705),but not p-JAK2.Conclusion CTS may be a potential anti-proliferation agent of malignant glioma C6 cells and that its mechanism may be related to the inhibition of STAT3 signaling.
malignant glioma;proliferation;JAK2-STAT3 signaling pathway
R 966
A
1000-1492(2016)06-0769-04
2016-03-04接收
國家自然科學基金(編號:81460619);廣西自然科學基金青年項目(編號:2015GXNSFBA139178)
1桂林醫學院藥學院藥理學教研室,桂林 5410012復旦大學藥學院藥理學與生物化學教研室,上海200120
唐煥煥,女,碩士研究生;呂 良,男,講師,碩士生導師,責任作者,E-mail:luliang998@163.com

