siRNA抑制HMGA1基因表達對甲狀腺乳頭狀癌K1細胞增殖的影響
周大新,周 銳,李德群,董慧明,張 暉,朱金海,馬小開,陳春春,馬桂凱,陳海龍,王志軍
siRNA抑制HMGA1基因表達對甲狀腺乳頭狀癌K1細胞增殖的影響
周大新1,2,周銳1,李德群1,董慧明1,張暉1,朱金海1,馬小開1,陳春春1,馬桂凱1,陳海龍1,王志軍1
目的 研究HMGA1-siRNA基因對甲狀腺乳頭狀癌K1細胞增殖的影響。方法 HMGA1-siRNA組轉染HMGA1的小干擾RNA(siRNA);陰性對照組轉染HMGA1的無關序列,并轉染甲狀腺乳頭狀癌K1細胞。采用CCK-8法檢測轉染HMGA1-siRNA基因后對K1細胞增殖的影響;RT-PCR法檢測正常組、HMGA1-siRNA組和陰性對照組的HMGA1-mRNA表達;Western blot法檢測三組的HMGA1蛋白表達;Transwell侵襲實驗檢測三組HMGA1-siRNA基因轉染后K1細胞的侵襲能力。結果 HMGA1-siRNA基因對K1細胞的抑制增殖作用明顯,呈現時間-劑量依賴關系;HMGA1-siRNA基因在K1細胞中mRNA和蛋白的表達顯著低于正常組和陰性對照組;HMGA1-siRNA組K1細胞侵襲能力顯著低于正常組和陰性對照組。結論 siRNA可以沉默HMGA1基因,減緩甲狀腺乳頭狀癌K1細胞增殖。
HMGA1-siRNA基因;甲狀腺乳頭狀癌;K1細胞;干擾技術RNA
網絡出版時間:2016-5-9 15:43:10 網絡出版地址:http://www.cnki.net/kcms/detail/34.1065.R.20160509.1543.010.html
高遷移率族蛋白A1(high mobility group A1,HMGA1)是一組非組蛋白染色質相關蛋白,屬于高遷移率族蛋白(HMG)的成員,可作為真核生物轉錄因子的輔助因子參與轉錄過程。在正常情況下,HMGA1主要存在于胚胎發育階段,而迅速增殖的細胞內和分化成熟的組織內幾乎沒有表達,已有國內外文獻[1-3]報道HMGA1基因參與了不同胚胎起源的腫瘤相關基因的轉錄調控。目前,在甲狀腺癌組織中HMGA1基因及其具體作用機制仍知之甚少,在K1細胞內運用HMGA1-siRNA研究HMGA1基因功能的應用尚未見報道。該研究構建HMGA1-siRNA基因并轉染甲狀腺乳頭狀癌K1細胞株,研究其對K1細胞抑制及侵襲力的影響。
1 材料與方法
1.1實驗材料
1.1.1試劑及來源 兔抗人HMGA1單克隆抗體購自美國Santa Cruz生物公司;胎牛血清(FBS)購自杭州四季青公司;DMEM/F12培養液購自美國Gibco公司;CCK-8細胞計數試劑盒購自美國Sigma公司;RT-PCR AMV試劑盒購自立陶宛Fermentas公司。
1.1.2細胞株來源 人甲狀腺乳頭狀癌K1細胞株購自上海美軒公司產品。
1.2實驗方法
1.2.1HMGA1-siRNA基因的轉染 本實驗共分為3組:HMGA1-siRNA組;不加任何干預設為正常組;siRNA陰性對照進行干預設為陰性對照組。各組引物序列由上海美軒公司設計并合成,序列如下,HMGA1-siRNA上游引物:5′-GCCGGGGCAGGCCGCGCAATT-3′;下游引物:5′-UUGCGCGGCCUGCCCCGGCTT-3′;陰性對照上游引物:5′-UUCACUCCAAGUCUCUUCCTT-3′;下游引物:5′-GGAAGAGACUUGGAGUGAATT-3′,根據LipofectaminTM2000說明書進行轉染。
1.2.2細胞培養 采用DMEM/F12培養基分組培養人甲狀腺乳頭狀癌K1細胞至對數生長期,各組用0.25%胰蛋白酶消化,制成單細胞懸液,稀釋至5 ×103細胞懸液,逐步分別接種于新的培養瓶繼續傳代培養,建立人甲狀腺乳頭狀癌K1細胞株。
1.2.3測定細胞生長曲線 細胞懸液接種到細胞板,該板為96孔板,每孔置入1 000個細胞數,每組設3個復孔,每天定時加入10 μl的CCK-8試劑,連續3 d,待細胞貼壁后,培養板置入37℃條件下孵育4 h后,測定各孔在450 nm處的吸光度(optical density,OD)值。并計算KI細胞抑制率。細胞抑制率(%)=(1-實驗組平均OD值/對照組平均OD值)×100%。
1.2.4RT-PCR定量分析 細胞培養建立人甲狀腺乳頭狀癌K1細胞株。引物由上海生物工程公司合成,序列如下,HMGA1上游引物:5′-GAAGGTGAAGGTCGGAGTC-3′;下游引物:5′-GAAGATGGTGATGGGATTTC-3′;GAPDH上游引物:5′-GGCACTGAGAAGCGGGGCCG-3′;下游引物:5′-CCCTTGTTTTTTGCTTCCCTT-3′。總RNA的提取和反轉錄嚴格按照說明書進行操作;PCR反應體系為20 μl,反應條件:預變性4 min,94℃變性30 s,55℃退火30 s,72℃延伸30 s,30個循環。在瓊脂糖凝膠中觀察PCR產物。并計算mRNA表達抑制率。mRNA表達抑制率:抑制率(%)=(1-對照組平均相對灰度值/正常組平均相對灰度值)×100%。
1.2.5Western blot法檢測 同上,建立人甲狀腺乳頭狀癌K1細胞株。測定各樣品蛋白濃度使用BCA法,將漂洗后的凝膠轉移到NC膜上(4℃、1 h)。將膜置于5%的脫脂奶粉封閉液,設置37℃恒溫封閉2 h,β-actin抗體(1∶1 000)/HMGA1抗體(1∶400)加入,4℃搖床上一抗孵育過夜,加入5%脫脂奶粉稀釋的辣根過氧化物酶標記的第二抗體(1∶4 000),設置37℃恒溫搖床上溫育1.5 h二抗孵育。將膜置于ECL顯色液中1~5 min曝光,顯影,清洗后放入定影液中定影,最后用凝膠成像系統分析結果。根據以下公式計算蛋白表達抑制率:抑制率(%)=(1-實驗組平均相對灰度值/對照組平均相對灰度值)×100%。
1.2.6Transwell侵襲實驗 實驗同上,建立人甲狀腺乳頭狀癌K1細胞株。Transwell小室底部為8 μm孔徑乙烯濾膜,預先鋪上Matrigel凝膠(1 mg/ml)100 μl。細胞轉染24 h后,常規收集細胞,5組均以無血清DMEM/F12制成1×105/ml細胞液,各取100 μl移入小室,小室外加入各200 μl的條件培養和完全培養液。置37℃的培養箱內孵育48 h后取出。侵襲并黏附至下室面的細胞以10%甲醛固定、HE染色。在400倍高倍鏡下細胞計數。細胞侵襲力抑制率(%)=(1-實驗組細胞數/對照組細胞數)×100%。
1.3統計學處理 采用SPSS 17.0軟件進行分析,數據以±s表示。各組間比較用單因素方差分析法,數據間的兩兩比較采用LSD檢驗。
2 結果
2.1HMGA1-siRNA基因對K1細胞增殖的影響
各組細胞在處于對數生長期時細胞分裂增殖旺盛,形態正常,生長狀態良好,均出現增殖,在干預后24 h開始出現差異,且作用時間增長,轉染后K1細胞增殖的抑制率越明顯,呈現時間-劑量依賴關系(72 h作用最明顯),在各時間點HMGA1-siRNA組與陰性對照組比較差異均有統計學意義(F= 168.23,P<0.05);正常組與陰性對照組比較差異均無統計學意義。見圖1。
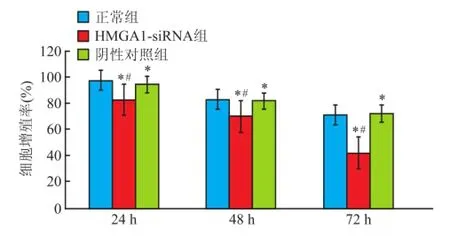
圖1 轉染后HMGA1基因對K1細胞增殖的影響與正常組比較:*P<0.05;與陰性對照組比較:#P<0.05
2.2HMGA1-siRNA基因在K1細胞中mRNA的表達 HMGA1-siRNA處理72 h后,HMGA1-siRNA組mRNA表達水平、陰性對照組分別與正常組比較,均明顯降低(正常組:1.000±0.00;HMGA1-siRNA組:0.247±0.02;陰性對照組:0.931±0.05)(F =388.72,P<0.05),抑制率分別為75.28%、6.90%。HMGA1基因的mRNA表達水平在正常組、陰性對照組之間差異無統計學意義。
2.3HMGA1-siRNA基因在K1細胞中蛋白的表達 Western blot檢測轉染72 h后,與正常組比較,HMGA1-siRNA組和陰性對照組K1細胞的抑制率分別為41.68%和2.1%,見圖2。正常組和陰性對照組之間差異無統計學意義。
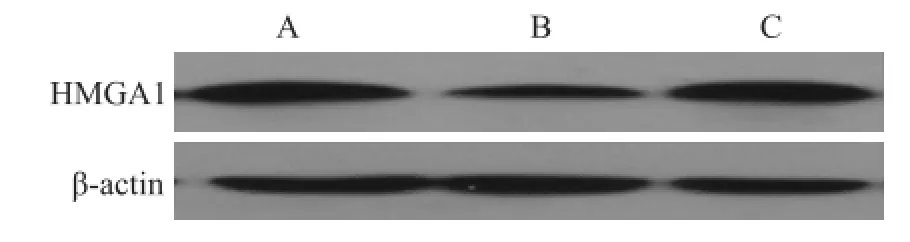
圖2 轉染后HMGA1基因在K1細胞中蛋白的表達A:正常組;B:HMGA1-siRNA組;C:陰性對照組
2.4Transwell侵襲實驗 通過檢測轉染72 h后,HMGA1組的K1細胞,穿膜細胞數低于正常組、陰性對照組的細胞,侵襲力抑制率分別為36.32%、1.23%,差異有統計學意義(F=263.85,P<0.05)。見圖3。正常組與陰性對照組比較,細胞侵襲數的差異無統計學意義。
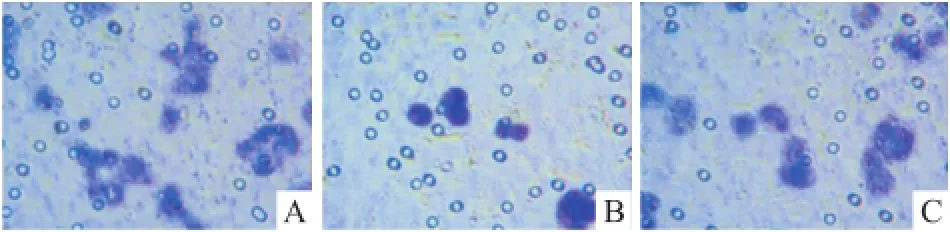
圖3 Transwell侵襲實驗 ×300A:正常組;B:HMGA1-siRNA組;C:陰性對照組
3 討論
目前,基因沉默主要通過干擾RNA(siRNA)、反義寡脫氧核苷酸和核酶等技術手段來實現[4]。研究[5-8]表明,由于siRNA失去了抑制基因表達的活性,其誘導的特定基因阻斷技術具有高度的序列特異性。siRNA抑制基因表達的效率高,且具備高度的序列特異性,可以特異性抑制mRNA序列,達到阻斷目的蛋白的表達作用,同時又具備防止長鏈dsRNA引發的非特異性基因降解和細胞死亡的功能。故siRNA已成為RNAi施展重要作用的中間效應分子。
臨床研究[7]證明,HMGA1與腫瘤的侵襲轉移能力密切相關,HMGA1基因在甲狀腺癌、肺癌、宮頸癌、前列腺癌、大腸癌、乳腺癌等許多腫瘤中呈高水平表達,而癌旁正常組織不表達或微弱表達,推測其可能與腫瘤的發生、發展密切相關。正常細胞若轉染HMGA1基因可導致正常細胞的惡化,腫瘤細胞轉HMGA1基因,可導致細胞惡性程度的增加。研究[9]表明,不管在轉基因動物身上的惡性腫瘤或應用致癌誘導劑導致的正常細胞惡變都可以檢測到細胞內HMGA1水平迅速升高;可以設想,若抑制HMGA1的高表達,是否可以阻止細胞的惡化,HMGA1有望成為腫瘤治療的新靶點。
本研究表明人甲狀腺乳頭狀癌組織中有HMGA1蛋白異常表達,但還有許多關鍵性問題沒有搞清楚,本課題通過設計并合成HMGA1 siRNA,然后轉染甲狀腺乳頭狀癌K1細胞,對照組以等量陰性對照siRNA轉染K1細胞,實時熒光定量RT-PCR技術檢測轉染后K1細胞中HMGA1 mRNA的表達,HMGA1 mRNA的表達以PGR循環數閾值(Ct值)表示;Western blot法測定K1細胞中HMGA1蛋白的表達;顯微鏡觀察并計數轉染后存活的K1細胞數,篩選出有效的siRNA。用有效的siRNA重新轉染K1細胞,選取穩定轉染HMGA1 siRNA的甲狀腺乳頭狀癌K1細胞,實時熒光定量PCR、Western blot法檢測穩定轉染HMGA1 siRNA的甲狀腺乳頭狀癌K1細胞株中HMGA1 mRNA和蛋白的表達;CCK8、Transwell法分別檢測轉染后細胞的增殖、凋亡及遷移力。觀察穩定轉染HMGA1 siRNA對甲狀腺乳頭狀癌細胞的生物學行為的影響,從而進一步了解HMGA1基因在甲狀腺乳頭狀癌發生、發展中的作用,以期為甲狀腺乳頭狀癌的治療開辟新的途徑。
本研究利用RNA干擾技術,制備HMGA1-siRNA基因,并植入甲狀腺乳頭狀癌K1細胞,觀察siRNA對HMGA1基因表達的影響。研究顯示siRNA可以沉默HMGA1基因,減緩甲狀腺乳頭狀癌K1細胞增殖。該研究結果對甲狀腺乳頭狀癌的診斷、治療具有一定的啟示意義,有待進一步研究。
[1] Fusco A M,Fedele M.Roles of HMGA proteins in cancer[J].Nat Rev Cancer,2007,7(12):899-910.
[2] Chang Z G,Yang L Y,Wang W,et al.Determination of high mobility group A1 HMGA1 expression in hepatocellular carcinoma a potential prognostic marker[J].Dig Dis Sci,2005,50(10):1764 -70.
[3] Flohr A M,Rogalla P,Bonk U,et al.High mobility group protein HMGA1 expression in breast cancer reveals a positive correlation with tumour grade[J].Histol Histopathol,2003,18(4):999-1004.
[4] Matsui K,Sasaki Y,Komatsu T,et al.RNAi gene silencing using cerasome as a viral-size siRNA-carrier free from fusion and crosslinking[J].Bioorg Med Chem Lett,2007,17(14):3935-8.
[5] 尋慶英,王玲玲,周懷君.siRNA抑制RRM2表達對子宮內膜癌Ishikawa細胞增殖影響的研究[J].東南大學學報(醫學版),2015,34(6):890-6.
[6] 盧燕軍,付陸軍,楊家進,等.siRNA介導BMP7基因沉默對人肝癌HepG2細胞增殖和遷移的影響[J].世界華人消化雜志,2016,24(1):10-8.
[7] 農晰婷,楊 光,張 昱.siRNA靶向抑制MACC1對結直腸癌細胞增殖和侵襲能力的影響[J].陜西醫學雜志,2016,45(1):9-11.
[8] 張英芝,勞佩維,白延青.HMGA1在卵巢上皮性癌組織中的表達及臨床意義[J].腫瘤學雜志,2014,20(1):51-4.
[9] 江振洲,劉曉昕,周 旺,等.我國疾病靶點研究最新進展[J].前沿與進展,2015,39(5):335-50.
Impact on proliferation of K1 cells in papillary thyroid carcinoma under the inhibition of siRNA on HMGA1 gene
Zhou Daxin1,2,Zhou Rui1,Li Dequn1,et al
(1Dept of Oncology,The First Affiliated Hospital of Bengbu Medical College,Hefei 233004;2Huaibei Clinical Institute of Anhui Medical University,Dept of General Surgery,Huaibei People's Hospital,Huaibei 235100)
Objective To study the effect of HMGA1-siRNA gene on proliferation of K1 cells in papillary thyroid carcinoma.Methods Experimental group was transfected with HMGA1 by small interfering RNA(siRNA);the negative contrast group was transfected with HMGA1 nonrelevant sequence,and transfected with K1 cells of thyroid papillary carcinoma.The impact on the proliferation of K1 cells after the transfection of HMGA1-siRNA was tested by CCK-8.The HMGA1-mRNA expression in the normal group was tested by RT-PCR.The HMGA1 protein expression in the three groups was tested by Western blot.The invasion of K1 cells transfected with HMGA1-siRNA gene was detected by Transwell invasion assay in three groups.Results The effect of HMGA1-siRNA gene on the proliferation of K1 cells was obvious,which was relevant to time and dosage.The expression of mRNA and protein in K1 cells was significantly lower than that in normal in HMGA1-siRNA cells.The expression of mRNA and protein in K1 cells was significantly lower than that in the normal group and the negative control group.The invasion ability of K1 cells in HMGA1-siRNA group was significantly lower than that in the normal group and the negative control group.Conclusion siRNA can silence HMGA1 gene,and slow down the proliferation of papillary thyroid carcinoma K1 cells.
HMGA1-siRNA gene;papillary thyroid carcinoma;K1 cell;RNA interference technology
R 739.91
A
1000-1492(2016)06-0783-04
2016-04-13接收
安徽省高等學校自然科學基金(編號:KJ2015B106by)
1蚌埠醫學院第一附屬醫院腫瘤外科,蚌埠 2330042安徽醫科大學淮北臨床學院、淮北市人民醫院普外科,淮北 235100
周大新,男,碩士研究生;周 銳,男,主治醫師,碩士,責任作者,E-mail:zhourui19810120@126.com;李德群,男,教授,主任醫師,碩士生導師,責任作者,E-mail:lidequn8888@163.com

