腎臟去交感神經對肥胖型高血壓家兔血壓及相關神經體液因子的影響
王 彬, 王海昌, 薛玉生, 范博淵, 尚福軍
(第四軍醫大學唐都醫院心內科,西安 710038; *通訊作者,E-mail:shangfujun4@163.com)
?
腎臟去交感神經對肥胖型高血壓家兔血壓及相關神經體液因子的影響
王彬, 王海昌, 薛玉生, 范博淵, 尚福軍*
(第四軍醫大學唐都醫院心內科,西安710038;*通訊作者,E-mail:shangfujun4@163.com)
目的觀察腎臟去交感神經支配術(renal sympathetic denervation,RSD)對肥胖型高血壓家兔的血壓及相關神經體液因子的影響。方法大耳白兔40 只,隨機分為對照組、對照+射頻組、肥胖組、肥胖+射頻組,對照組和對照+射頻組動物給予普通飼料飼養,肥胖組和肥胖+射頻組動物給予高能飼料飼養。飼養8周后,通過經腹腎動脈外膜射頻消融進行RSD,術后繼續飼養8周,測定血壓,采用酶聯免疫吸附試驗(ELISA)檢測血漿中去甲腎上腺素(NE)、精氨酸血管加壓素(AVP)、血管緊張素Ⅱ(AngⅡ)、醛固酮(Ald)的變化。結果與對照組比較,肥胖+射頻組的血壓無顯著差異(P>0.05);與肥胖組比較,肥胖+射頻組的血壓顯著降低(P<0.05)。肥胖組NE、AVP、AngⅡ和Ald 較對照組明顯升高(P<0.05),RSD后肥胖+射頻組NE、AVP、AngⅡ和Ald 較肥胖組明顯下降(P<0.05)。結論RSD可以降低肥胖型高血壓動物的血壓,降低血漿NE、AVP、AngⅡ和Ald 水平。
肥胖型高血壓;腎臟去交感神經支配術;神經體液因子;兔
高血壓病是心腦血管事件主要危險因素之一。然而,5%-10%的高血壓患者存在降壓藥物抵抗現象,稱為頑固性高血壓[1]。Krum等[2]2009年首次報道了腎臟去交感神經支配術(renal sympathetic denervation,RSD)治療難治性高血壓的方法,顯示了良好的降壓效果,為頑固性高血壓的治療提供了新的選擇。然而,新近的研究結果顯示RSD未能起到明顯的降壓作用,對RSD臨床應用提出了質疑和挑戰[3]。但對此全盤否定也為時尚早。引起高血壓的原因較多,如何選擇不同病因引起的頑固性高血壓患者進行RSD成為研究重點。肥胖是高血壓病的重要危險因素,也是導致頑固性高血壓的主要原因之一,但RSD能否降低肥胖型高血壓的血壓水平,目前尚不明確。因此,本文以肥胖型高血壓動物為研究對象,研究RSD對肥胖型高血壓的影響,并探討相關神經體液因子水平的變化及其與降壓作用的關系,為RSD的臨床應用提供新的實驗依據。
1 材料和方法
1.1實驗動物
5-6月齡大耳白兔,體質量2-3 kg,標準飼料及高能飼料均由第四軍醫大學動物實驗中心提供。
1.2主要試劑及儀器
去甲腎上腺素(NE)、精氨酸血管加壓素(AVP)、血管緊張素Ⅱ(AngⅡ)、醛固酮(Ald)、酶聯免疫吸附試驗(enzyme linked immunosorbent assay,ELISA)試劑盒(北京奇松生物有限公司),戊巴比妥鈉(北京百奧萊博科技有限公司),肝素鈉注射液(上海第一生化藥業有限公司)。動脈壓力傳感器(荷蘭飛利浦),GY 6328多導電生理儀(華南醫電),射頻消融儀(美國圣猶達),射頻消融導管(強生),酶標儀(美國Bio-Tek)。
1.3肥胖型高血壓兔模型的建立及分組
大耳白兔40 只,隨機分為對照組、對照+射頻組、肥胖組、肥胖+射頻組。每組10只。參照文獻[4]通過高能飲食建立肥胖型高血壓模型。對照組給予普通飼料喂養8周,肥胖組給予高能飼料(苜蓿草粉31%、玉米36%、麩皮15%、豆餅12%、魚粉3%、骨粉2%、食鹽0.5%、多維0.4%和微量元素0.1%),連續喂養8周。
1.4經腹雙側腎動脈外膜射頻消融
連續喂養8周,大耳白兔稱重,術前2 h給予肌注青霉素(10萬U/kg)。耳緣靜脈注射戊巴比妥鈉(30 mg/kg)麻醉,背外側手術切口,暴露并分離雙側腎動脈后行腹動脈穿刺并連接多導生理記錄儀測定血壓,并抽取血液測定神經體液因子水平,分別圍繞雙側腎動脈外膜沿軸向旋轉分割的6個區域行溫控射頻消融(4-6 W,43-46 ℃),每個消融部位消融2 min。術后逐層縫合腹壁,肌注青霉素(10萬U/kg)。對照組+射頻組和肥胖+射頻組進行雙側腎動脈消融,其余兩組除不進行腎動脈消融外,其他處理相同。
1.5血壓測定
繼續飼養8周后,大耳白兔稱重,戊巴比妥鈉(30 mg/kg)耳緣靜脈注射麻醉,頸外側切開,分離頸總動脈,插入鞘管,連接多導生理記錄儀的壓力轉換器,測定血壓。
1.6血液神經體液因子的測定
采用ELISA方法測定兔血漿NE、AVP、AngⅡ和Ald濃度。血管鞘內抽取動脈血,室溫靜止3 min 后,1 000×g離心,取上清液,ELISA方法測定各組神經體液因子濃度。
1.7統計學分析
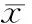
2 結果
2.1動物一般狀況
整個實驗過程中無動物死亡,4只家兔RSD后出現食欲不振和活動量減少,但均不嚴重,3 d內恢復正常。
2.2實驗后實驗兔的體重、心率及血壓情況
實驗前各組實驗兔體重無明顯差異,實驗后,分別與對照組及對照+射頻組比較,肥胖組和肥胖+射頻組的體質量均明顯增加(P<0.05); 4組兔子的心率無顯著差異(P>0.05)。與對照組和對照+射頻組比較,肥胖+射頻組的血壓無顯著差異(P>0.05);與肥胖組比較,肥胖+射頻組的血壓顯著降低(P<0.05,見表1)。
表1實驗后各組實驗兔體重、心率及血壓的比較
Table 1Comparison of rabbit body weight,heart rate and blood pressure among four groups

組別體質量(kg)心率(次/min)收縮壓(mmHg)對照組3.36±0.31228±3194±7對照+射頻組3.12±0.28231±3392±6肥胖組4.64±0.37*241±36133±9肥胖+射頻組4.52±0.33#238±35105±7△
與對照組比較,*P<0.05;與對照+射頻組比較,#P<0.05;與肥胖組比較,△P<0.05
2.3各組血漿神經體液因子濃度比較
肥胖組兔的血漿NE、AVP、AngⅡ和ALD濃度均較對照組顯著升高,差異有統計學意義(均P<0.05);與肥胖組比較,肥胖+射頻組兔的血漿NE、AVP、AngⅡ和ALD濃度均顯著下降,差異有統計學意義(均P<0.05,見表2)。
3 討論
肥胖型高血壓發病率極高,是導致頑固性高血壓的主要原因之一,這類人群有較高的患病率和死亡率,包括冠心病、充血性心力衰竭、心源性猝死、慢性腎病、腎終末期疾病和中風[5]。交感神經系統激活在高血壓病發展過程中起著重要作用,近年來,多項臨床研究證實腎臟去交感神經支配術作為一種新的手段治療頑固性高血壓,可明顯降低難治性高血壓患者的血壓,為難治性高血壓的治療提供了新的希望[2,6,7]。
表2消融對各組實驗兔的神經體液因子的影響(ng/L)
Table 2Effects of RSD on neurohormonal factors in experimental rabbits(ng/L)
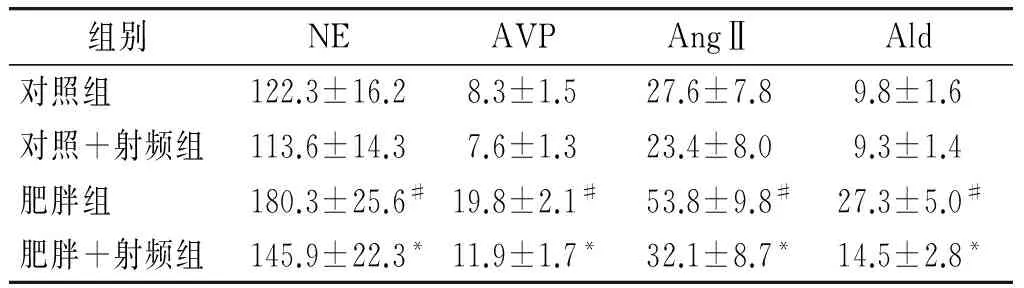
組別NEAVPAngⅡAld對照組122.3±16.28.3±1.527.6±7.89.8±1.6對照+射頻組113.6±14.37.6±1.323.4±8.09.3±1.4肥胖組180.3±25.6#19.8±2.1#53.8±9.8#27.3±5.0#肥胖+射頻組145.9±22.3*11.9±1.7*32.1±8.7*14.5±2.8*
與肥胖組比較,*P<0.05;與對照組比較,#P<0.05
肥胖型高血壓發病機制復雜多樣,交感神經活性異常增高可能是其發病的關鍵因素之一[8]。腎交感神經激活可以通過以下機制影響血壓:①腎素的分泌,激活腎素-血管緊張素-醛固酮;②腎交感神經的傳入;③容量性負荷的增加;④其他,如內分泌紊亂、腎動脈的管壁增厚等[9,10]。本實驗通過高能飼料喂養建立肥胖型高血壓模型,為了得到客觀的實驗結果,同時設立了對照組、對照+射頻組,通過進行雙側腎交感神經射頻消融觀察其對血壓的影響,實驗結果顯示:肥胖+射頻組實驗兔的血壓較肥胖組顯著下降,證實了RSD可降低肥胖型高血壓的血壓水平,其降壓機制可能是通過降低腎動脈交感神經節傳入纖維活性,達到降低血壓的治療效果。
高血壓患者由于交感神經過度激活可引起相關神經體液因子進一步升高,包括血漿中NE、AVP、AngⅡ和Ald等,在過度激活的交感神經及神經體液因子的共同作用下,傳至中樞系統,進一步激活交感神經系統,最終導致血壓異常升高[11]。為了進一步探討RSD降壓和改善心臟重構的機制,本研究測定了血漿中NE、AVP、AngⅡ和Ald的變化,實驗結果顯示:雙側腎交感神經射頻消融后實驗兔血漿中NE、AVP、AngⅡ和Ald 水平也顯著下降,這與其他相關研究的實驗結果一致[7,12,13],表明RSD可降低肥胖型高血壓的血壓水平,并可降低血漿中NE、AVP、AngⅡ和Ald水平,進一步說明RDS可通過降低交感神經活性及調節神經體液因子水平,最終達到降壓效果。
綜上所述,本實驗證明RSD可降低肥胖型高血壓模型動物的血壓水平,其可能是通過降低交感神經活性及調節神經體液因子水平發揮降壓作用,血漿中的NE、AVP、AngⅡ和Ald濃度可作為RSD治療效果的預測指標。然而,頑固性高血壓成因復雜,不同類型的高血壓發病機制不盡相同,需要進一步研究頑固性高血壓的病因,并進行相關治療方案研究,以及RSD在不同類型高血壓中的治療作用。
[1]ESH/ESC Task Force for the Management of Arterial Hypertension.2013 Practice guidelines for the management of arterial hypertension of the European Society of Hypertension(ESH)/the European Society of Cardiology(ESC):ESH/ESC Task Force the Management of Arterial Hypertension(ESC):ESH/ESC Task Force the Management of Arterial Hypertension[J].J Hypertension,2013,31(10):1925-1938.
[2]Krum H,Schlaich M,Whitbourn R,etal.Catheter-based renal sympathetic denervation for resistant hypertension:a multicentre safety and proof-of-principle cohort study[J].Lancet,2009,373(9671):1275-1281.
[3]Bhatt DL,Kandzari DE,O’Neill WW,etal.A controlled trial of renal denervation for resistant hypertension[J].N Engl J Med,2014,370(15):1393-1340.
[4]馬利芹,耿光瑞,孫秀梅.大黃減肥復方對家兔脂肪代謝的影響[J].黑龍江畜牧獸醫,2009,(3):107-108.
[5]Vongpatanasin W.Resistant hypertension:a review of diagnosis and management[J].JAMA,2014,311(21):2216-2224.
[6]Papademetriou V,Tsioufis CP,Sinhal A,etal.Catheter-based renal denervation for Resistant hypertension:12-month results of the enlightn Ⅰfirst-in-human study using a multielectrode ablation system[J].Hypertension,2014,64(3):565-572.
[7]Lu J,Ling Z,Chen W,etal.Effects of renal sympathetic denervation using saline-irrigated radiofrequency ablation catheter on the activity of the renin-angiotensin system andendothelin-1[J].J Renin Angiotensin Aldosterone Syst,2014,15(4):532-539.
[8]White WB,Galis ZS,Enegar J,etal.Renal denervation therapy for hypertension: pathways for moving development forward[J].Am Soc Hypertens,2015,9(5):341-350.
[9]Van Vark LC,Bertrand M,Akkerhuis KM,etal.Angiotensin-converting enzyme inhibitors reduce mortality in hypertension:a meta analysis of randomized clinical trials of renin-angiotensin-aldosterone system inhibitors involving 158,998 patients[J].Eur Heart J,2012,33(16):2088-2097.
[10]Kotchen TA.Obesity-related hypertension:epidemiology,pathophysiology and clinical management[J].Am J Hypertens,2010,23(11):1170-1178.
[11]Tsioufis C,Dimitriadis K,Thomopoulos C,etal.Renal and cardiac effects of renal sympathetic denervation and carotid baroreceptor stimulation[J].Curr Vasc Pharmacol,2014,12(1):55-62.
[12]尚福軍,王捷頻,于亮,等.腎臟去交感神經對腎性高血壓的影響及預測指標的篩選[J].嶺南心血管病雜志,2015,21(6):858-861.
[13]Streitparth F,Walter A,Stolzenburg N,etal.MR-guided periarterial ethanol injection for renal sympathetic denervation:a feasibility study in pigs[J].Cardiovasc Intervent Radiol,2013,36(3):791-796.
Effects of renal sympathetic denervation on obesity-associated hypertension and related neurohormonal factors in rabbits
WANG Bin, WANG Haichang, XUE Yusheng, FAN Boyuan,SHANG Fujun*
(DepartmentofCardiology,TangduHospital,FourthMilitaryMedicalUniversity,Xi’an710038,China;*Correspondingauthor,E-mail:shangfujun4@163.com)
ObjectiveTo investigate the effects of renal sympathetic denervation on obesity-associated hypertension and related neurohormonal factors in rabbits.MethodsForty rabbits were randomly divided into four groups: control group, control+ablation group, obesity group and obesity+ablation group. Rabbits in control group and control+ablation group were fed by common diet, and rabbits in obesity group and obesity+ablation group were fed by high energy diet. After feeding for eight weeks, RSD was carried out by transabdominal radiofrequency ablation of renal arterial adventitia. Then rabbits were continuously fed for eight weeks, and then blood pressure was measured. Plasma concentrations of norepinephrine(NE), arginine vasopressin(AVP), angiotensin Ⅱ(Ang Ⅱ) and aldosterone(ALD) were determined by enzyme-linked immunosorbent assay(ELISA).ResultsCompared with control group, the systolic blood pressure(SBP) showed no significant change in obesity+ablation group(P>0.05).After RSD,the SBP in obesity+ablation group was significantly lower than in obesity group(P<0.05). Compared with control group, plasma concentrations of NE, AVP, Ang II and Ald were significantly decreased in obesity group(P<0.05). Compared with obesity group, plasma concentrations of NE, AVP, Ang II and Ald in obesity+ablation group were declined significantly after RSD(P<0.05).ConclusionRSD can reduce the blood pressure of obesity-associated hypertension, and reduce the levels of NE, Ang II, AVP and Ald.
obesity-associated hypertension;renal sympathetic denervation;neurohormonal factor;rabbits
陜西省衛生廳科研基金項目資助(2012D72)
王彬,男,1981-05生,碩士,主治醫師,E-mail:binwang800@163.com
2016-04-25
R544.1
A
1007-6611(2016)08-0703-03
10.13753/j.issn.1007-6611.2016.08.006

