鮑曼不動桿菌臨床分離株外排泵分布水平與碳氫酶烯類抗生素耐藥研究*
李卓成,張彥鵬,吳偉清,李延武,丁芳林
(廣東省深圳市第二人民醫院檢驗科 518000)
?
鮑曼不動桿菌臨床分離株外排泵分布水平與碳氫酶烯類抗生素耐藥研究*
李卓成,張彥鵬,吳偉清,李延武,丁芳林
(廣東省深圳市第二人民醫院檢驗科518000)
目的研究鮑曼不動桿菌臨床分離株中外排泵分布水平與碳氫酶烯類抗生素耐藥相關情況。方法選擇2015~2016年度深圳地區臨床分離的182株鮑曼不動桿菌,同時進行外排泵抑制試驗和肉湯稀釋法藥敏試驗,并對結果按照藥敏和外排泵表型兩種因素分組進行統計學分析。結果鮑曼不動桿菌182株臨床分離株中,外排泵表型陽性54株(29.7%);結合碳氫酶烯類抗生素藥敏分組統計,陽性組中耐藥和敏感分別為31.9%和13.9%,差異有統計學意義(χ2=4.46,P<0.05)。結論鮑曼不動桿菌外排泵耐藥機制在臨床分離株的碳氫酶烯類抗生素耐藥中起作用。
鮑曼不動桿菌;外排泵;耐藥
鮑曼不動桿菌是一類重要的革蘭染色陰性的非發酵醫院內感染病原菌,常引起醫院內免疫功能低下患者嚴重的呼吸機相關性肺炎、手術傷口部位感染、泌尿道感染、血流感染及繼發性腦膜炎等[1]。隨著近年來廣譜抗生素普遍使用等原因,臨床上鮑曼不動桿菌的多重耐藥株和泛耐藥株在世界范圍內不斷涌現[2]。碳青霉烯類抗生素是目前臨床治療鮑曼不動桿菌感染最有效的抗菌藥物之一[3]。常見的有亞胺培南(IPM)和美羅培南(MEO)等,能夠抵抗大多數超廣譜β-內酰胺酶(ESBL)和AmpC的水解。近年來,耐碳青霉烯類抗生素的鮑曼不動桿菌耐藥比例也逐年增高,而其耐藥一旦突破碳青霉烯類,人類將面臨無藥可選的窘境[4]。鮑曼不動桿菌針對碳氫酶烯類抗生素的耐藥機制主要有4類:(1)表達碳氫酶烯酶。主要是Ambler分類中的D類酶,即苯唑西林酶(OXA),包括OXA-23、OXA-24、OXA-51和OXA-58[5]。(2)產生構象改變的青霉素結合蛋白降低碳氫酶烯類抗生素的結合量。(3)下調外膜通道蛋白的表達或缺如,如Car類、OPM類,從而減少抗生素進入細菌[5]。(4)多種外排泵基因的過量表達,將進入細菌的抗生素主動排出。鮑曼不動桿菌的外排泵主要有5大家族,其中最重要的為RND家族,包括均由3部分構成的AdeABC、AdeFGH和AdeIJK等外排泵[6]。細菌外排泵對藥物的外排作用是主動耗能過程,其能力源于質子的濃度梯度,而羰基氰氯苯腙(carbonyl cyanide-m-chlorophenyl hydrazone,CCCP)可以抑制質子轉運的解偶聯劑,通過破壞質子濃度梯度,抑制主動外排系統的外排作用[7]。本研究擬使用CCCP作為泵抑制劑,研究鮑曼不動桿菌臨床分離株外排泵的分布水平,并分析外排泵表型與碳氫酶烯類抗生素耐藥的相關性。
1 資料與方法
1.1菌株來源2015~2016年分離自深圳市第二人民醫院的182株鮑曼不動桿菌臨床分離株。細菌分離培養按《全國臨床檢驗操作規程進行》進行[8],所有菌株均經過鑒定,剔除分離自同一患者相同部位標本的重復菌株。
1.2儀器與試劑全自動微生物分析儀(VITEK-2 COMPACT)購自法國生物梅里埃公司;泵抑制劑CCCP來源于Sigma公司;MH平板和MH肉湯來源于鄭州貝瑞特公司,無菌聚苯乙烯96孔板來源于美國CORNING公司;IPM標準品來源于中國藥品生物制品檢定研究院,IPM溶劑選擇pH8.0的磷酸鹽緩沖液(PBS),濃度為1 280 μg/mL,分裝后貯存于-70 ℃保存備用;恒溫振蕩培養箱為太倉實驗設備廠生產。
1.3質控菌株鮑曼不動桿菌ATCC17978,大腸埃希菌ATCC25922,金黃色葡萄球菌ATCC25923。質控菌株源于衛生部臨床檢驗中心。
1.4鮑曼不動桿菌外排泵抑制實驗復蘇凍存于-70 ℃超低溫冰箱的菌株,接種于MH平板37 ℃培養10~16 h后,選擇鮑曼不動桿菌典型單菌落接種于MH肉湯培養基;37 ℃ 180 r/min恒溫振蕩過夜培養16~18 h后,配置菌液濃度0.5個麥氏單位,用MH肉湯1∶1 000稀釋后每孔中100 μL接種以下2種96孔板。(1)泵抑制實驗板:各孔含終濃度10 μg/mL的CCCP,且每行第1~12孔從左到右含終濃度為128、64、32、16、8、4、2、1、0.5、0.25、0.125、0 μg/mL的IPM,每行最后1孔均為僅含相同濃度CCCP的MH肉湯做生長對照孔;(2)最小抑菌濃度(MIC)測定板:不含CCCP,且每行各孔從左到右含終濃度為128、64、32、16、8、4、2、1、0.5、0.25、0.125、0 μg/mL的IPM;將各96孔板置于37 ℃普通空氣孵箱中,孵育16~20 h判斷結果[9]。
1.5結果判斷各菌株MIC結果判讀按2010 版美國臨床實驗室標準化委員會(CLSI) 標準進行,且96孔板相應最后一列生長對照孔內細菌明顯生長外排泵抑制實驗才成立[9]。如微量肉湯稀釋法測定各菌株MIC值出現跳孔現象,則選擇抑制細菌生長的較高藥物濃度為其MIC值。如出現多處跳孔,則需重復試驗進行測定。各菌株外排泵陽性表型的判斷標準:存在泵抑制劑CCCP時的菌株MIC測定結果比不存在CCCP的MIC值下降4倍及以上。
1.6統計學處理采用SPSS16.0軟件進行數據處理,使用χ2檢驗,以P<0.05為差異有統計學意義。
2 結 果
2.1鮑曼不動桿菌臨床分離株的科室分布鮑曼不動桿菌臨床分離株共計182株,其中重癥監護室(ICU)病區分離株最多,共78株(42.8%);呼吸內科和神經外科的分離株也均超過10%(分別為15.3%和13.4%)。見表1。

表1 182株鮑曼不動桿菌的科室分布
2.2鮑曼不動桿菌外排泵抑制實驗結果將鮑曼不動桿菌臨床分離株按標本類型可分為痰液(48.2%)、肺泡灌洗液(8.9%)、分泌物(10.7%)、尿液(14.3%)、血液(7.1%)和其他(10.7%)。182株鮑曼不動桿菌中,根據肉湯稀釋法測定各菌株MIC結果,其中IPM敏感(S)36株(19.8%),中介(I)31株(17.0%),耐藥(R)116株(63.7%)。182株鮑曼不動桿菌中外排泵表型陽性54株(29.7%),外排泵陰性表型128株(70.3%)。陽性組中S與R比較差異有統計學意義(χ2=4.46,P<0.05)。見表2。
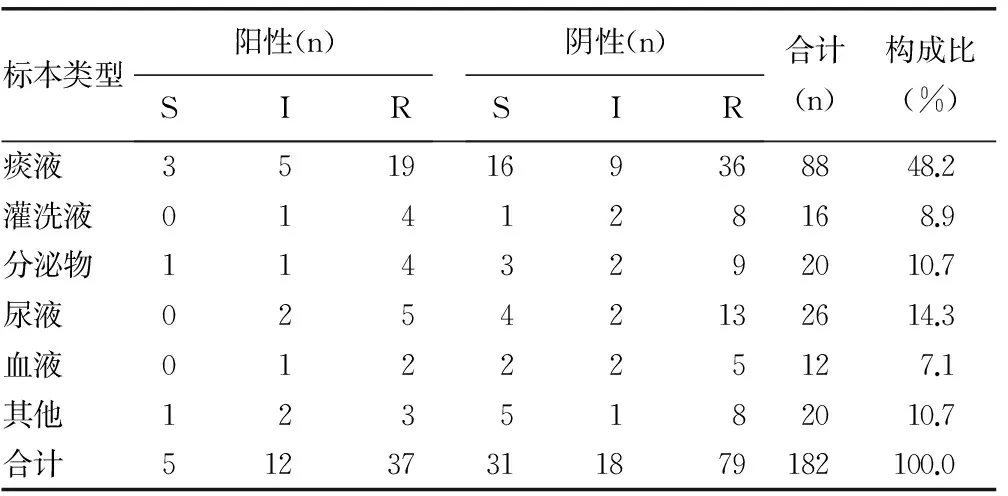
表2 182株鮑曼不動桿菌外排泵表型與耐藥表型分布
3 討 論
鮑曼不動桿菌為條件致病的革蘭陰性非發酵菌。臨床分離株多源于ICU病房、呼吸科、神經外科、康復科等病區的痰液、肺泡灌洗液、分泌物等組織標本。該菌可在住院患者及醫院環境中定植,且抗逆性強,是醫院感染最常見的致病菌[10]。長期廣譜抗生素的使用對菌株產生持續的抗生素選擇壓力,造成該菌耐藥性逐年提高,多重耐藥和泛耐藥鮑曼不動桿菌不斷產生[11]。全國耐藥監測網監測數據(2014年)顯示該菌對于青霉素類、頭孢菌素類、碳青霉烯類、喹諾酮類、氨基糖苷類抗生素的耐藥水平均超過60%[12];鮑曼不動桿菌多重耐藥,甚至泛耐藥菌株的出現,成為醫院感染控制和臨床治療的重大威脅,被喻為革蘭陰性菌中的“耐甲氧西林金黃色葡萄球菌(MRSA)”[7]。本研究所用的182株鮑曼不動桿菌對碳氫酶烯類抗生素IPM耐藥率為63.7%,且有17%為中介,對其敏感的菌株僅占19.8%,菌株耐藥控制的境況不容樂觀。
藥物外排泵機制是鮑曼不動桿菌重要的耐藥機制,迄今為止已發現20余種外排泵[12],可以大致分為5大外排泵家族,其中最重要的為RND家族,包括均由3個蛋白質部分構成的AdeABC、AdeFGH和AdeIJK等外排泵[13]。這些外排泵多為能量依賴型外排泵,利用質子或Na+離子偶聯交換提供動力,能夠將多種抗生素、金屬離子、表面活性劑和多種消毒劑排出細胞外[14]。2013年西班牙學者 Rumbo等[4]研究了鮑曼不動桿菌5大外排泵家族近20種外排泵在臨床菌株中的大致分布情況,以及外排泵機制對于菌株耐藥水平影響;有研究發現主動外排泵機制是細菌抵御外界抗生素壓力等不良環境和因素的重要手段,成為細菌獲得性多重耐藥的重要原因[7,15]。
本研究中,臨床分離的182株鮑曼不動桿菌中,約有54株(29.7%)有外排泵機制,陽性組中S與R比較差異有統計學意義(χ2=4.46,P<0.05)。提示鮑曼不動桿菌主動外排泵的耐藥機制在本研究臨床分離株對碳青霉烯類抗生素的耐藥機制中起作用,通過抑制外排泵的對碳氫酶烯類抗生素主動泵出,提高了菌體內抗生素有效水平從而降低了MIC值。可以認為,較低的毒副作用和較高外排抑制活性,成為開發前景良好的外排泵抑制劑類新型抗生素的必要條件。
[1]王輝,郭萍,孫宏莉,等.碳青霉烯類耐藥的不動桿菌分子流行病學及其泛耐藥的分子機制[J].中國檢驗醫學雜志,2006,29(12):1066-1073.
[2]Jia W,Li C,Zhang H,et al.Prevalence of Genes of OXA-23 Carbapenemase and AdeABC Efflux Pump Associated with Multidrug Resistance of Acinetobacter baumannii Isolates in the ICU of a Comprehensive Hospital of Northwestern China[J].Int J Environ Res Public Health,2015,12(8):10079-10092.
[3]朱德妹,汪復,胡付品,等.2010年中國CHINET細菌耐藥性監測[J].中國感染與化療雜志,2011,11(5):321-329.
[4]Rumbo C,Gate E,López M,et al.Contribution of efflux pumps,porins,and beta-lactamases to multidrug resistance in clinical isolates of Acinetobacter baumannii[J].Antimicrob Agents Chemother,2013,57(11):5247-5257.
[5]沈繼錄,朱德妹,吳衛紅,等.革蘭陰性桿菌碳青霉烯酶產生與細菌耐藥性關系的研究[J].中華檢驗醫學雜志,2008,31(4):408-414.
[6]侯天文,尹曉琳,李瑋,等.多重耐藥鮑曼不動桿菌相關耐藥基因檢測分析[J].中華微生物學和免疫學雜志,2007,27(4):379-383.
[7]Yoon EJ,Courvalin P,Grillot-Courvalin C.RND-type efflux pumps in multidrug-resistant clinical isolates of Acinetobacter baumannii:major role for AdeABC overexpression and AdeRS mutations[J].Antimicrob Agents Chemother,2013,57(7):2989-2995.
[8]葉應嫵,王毓三,申子瑜.全國臨床檢驗操作規程[M].3版.南京:東南大學出版社,2006.
[9]Richmond GE,Chua KL,Piddock LJ.Efflux in Acinetobacter baumannii can be determined by measuring accumulation of H33342 (bis-benzamide)[J].J Antimicrob Chemother,2013,68(7):1594-1600.
[10]王輝,劉穎梅,陳民鈞,等.鮑曼不動桿菌對碳青霉烯類耐藥機制的研究[J].中國醫學科學院學報,2003,25(5):567-571.
[11]Hornsey M,Loman N,Warcham DW,et al.Whole-genome comparison of two Acinetobacter baumannii isolates from a single patient,where resistance developed during tigecycline therapy[J].J Antimicrob Chemother,2011,66(7):1499-1503.
[12]Coldham NG,Webber M,Woodward MJ,et al.A 96-well plate fluorescence assay for assessment of cellular permeability and active efflux in Salmonella enterica serovar Typhimurium and Escherichia coli[J].J Antimicrob Chemother,2010,65(8):1655-1663.
[13]Tiwari V,Tiwari M.Quantitative proteomics to study carbapenem resistance in Acinetobacter baumannii[J].Front Microbiol,2014,5:512.
[14]Hornsey M,Ellington MJ,Doumith M,et al.AdeABC-mediated efflux and tigecycline MICs for epidemic clones of Acinetobacter baumannii[J].J Antimicrob Chemother,2010,65(8):1589-1593.
[15]Seifert H,Dolzani L,Bressan R,et al.Standardization and interlaboratory reproducibility assessment of pulsed-field gel electrophoresis-generated fingerprints of Acinetobacter baumannii[J].J Clin Microbiol,2005,43(9):4328-4335.
Study on the distribution of efflux pump and the antibiotic resistance of carbapenems in clinical isolates of Acinetobacter Bauman*
Li Zhuocheng,Zhang Yanpeng,Wu Weiqing,Li Yanwu ,Ding Fanglin
(Department of Clinical Laboratory,the Second People′s Hospital of Shenzhen City,Shenzhen,Guangdong 518000,China)
ObjectiveTo study the distribution of efflux pump and the antibiotic resistance of carbapenems in clinical isolates of 182 strains of Bauman Acinetobacter,and to understand the correlation between distribution of efflux pump and the drug resistance of hydrocarbon.MethodsTotally 182 clinical isolates of Acinetobacter Baumannii were selected to detect the efffux phenotype,which were separated between 2015 to 2016 isolated from Shenzhen district,Guangdong province.Efflux pump inhibition test and broth dilution method drug sensitivity test were used.According to the results of the drug sensitivity and the phenotype of efflux pump,Acinetobacter Baumannii were divided into groups(carbapenems resistance group,carbapenems sensitive group,efflux pump positive group and efflux pump negative group),then the results were made statistically analysis.ResultsIn all the 182 isolates,there were 54 strains with positive efflux pump phenotype,and the positive rate was 29.7%.And the efflux phenotype positive rate was 31.9% in carbapenems resistance group,comparing to 13.9% positive rate in carbapenems sensitive group(χ2=4.46,P<0.05).ConclusionThe efflux pumps paly an important role in the resistant mechanism of Acinetobacter Baumannii clinical isolates to carbapenems.
acinetobacter baumannii;efflux pump;resistance
深圳市科技創新委員會“知識創新計劃”項目(JCYJ20140414170821183)。作者簡介:李卓成(1959-),主任技師,碩士,主要從事臨床微生物與免疫研究。
論著·臨床研究10.3969/j.issn.1671-8348.2016.22.012
R378
A
1671-8348(2016)22-3057-03
2016-02-21
2016-04-09)

