不同實驗室ELISA檢測系統(tǒng)對HCV抗體測定的可比性研究*
曾艷華,盧香云,張 麗,張朝霞△,程 江
(1.新疆醫(yī)科大學(xué)第一附屬醫(yī)院醫(yī)學(xué)檢驗中心,烏魯木齊 830054;2.石河子大學(xué)第一附屬醫(yī)院檢驗科,新疆石河子 832000)
?
不同實驗室ELISA檢測系統(tǒng)對HCV抗體測定的可比性研究*
曾艷華1,盧香云2#,張麗1,張朝霞1△,程江2▲
(1.新疆醫(yī)科大學(xué)第一附屬醫(yī)院醫(yī)學(xué)檢驗中心,烏魯木齊 830054;2.石河子大學(xué)第一附屬醫(yī)院檢驗科,新疆石河子 832000)
目的探討不同實驗室酶聯(lián)免疫吸附試驗(ELISA)對丙型肝炎病毒抗體(HCV抗體)測定結(jié)果的可比性,為不同實驗室之間檢驗結(jié)果的互認提供實驗依據(jù)。 方法參照美國臨床實驗室標準化協(xié)會(CLSI) EP12-A2文件,收集100例新鮮血清標本,其中50例HCV抗體初篩陽性,50例HCV抗體初篩陰性,兩家醫(yī)院均采用國產(chǎn)addcare ELISA 1100全自動酶免分析系統(tǒng)(簡稱addcare ELISA 1100)隨機盲法檢測HCV抗體,同時用重組免疫印跡試驗(RIBA)和聚合酶鏈反應(yīng)(PCR)進行確認,通過比較兩家醫(yī)院的符合率,判斷測定結(jié)果的可比性。 結(jié)果兩家醫(yī)院實驗室間檢測臨床標本HCV抗體的敏感度和特異度均相同,分別為100%和96%;陽性符合率100%,陰性符合率100%,總符合率100%,差異無統(tǒng)計學(xué)意義(P>0.05)。 結(jié)論不同醫(yī)院實驗室采用不同檢測系統(tǒng)檢測HCV抗體,在儀器性能良好的情況下,根據(jù)自建Cut-off值判斷檢測結(jié)果,其測定結(jié)果具有可比性,達到檢驗結(jié)果的互認。
丙型肝炎抗體;酶聯(lián)免疫吸附測定;重組免疫印跡法;聚合酶鏈反應(yīng);符合率
丙型肝炎病毒(hepatitis C virus,HCV)感染被認為是全球公共衛(wèi)生安全的主要威脅之一,并可以導(dǎo)致急、慢性肝臟疾病[1]。前瞻性研究結(jié)果顯示,80%的急性丙型肝炎患者將發(fā)展為慢性感染,10%~20%的感染者將出現(xiàn)慢性肝臟疾病并發(fā)癥,且在20~30年內(nèi)出現(xiàn)臨床癥狀如肝硬化,1%~5%的患者將發(fā)展為肝細胞癌[2]。HCV感染所致的病死率將在未來20年呈持續(xù)上升趨勢[3]。因此,準確、及時地對丙型肝炎患者進行早期診斷、治療,是防止疾病慢性化,從而控制并治愈疾病的關(guān)鍵。
隨著檢驗醫(yī)學(xué)的發(fā)展,檢測系統(tǒng)逐漸多樣化、規(guī)模化,不同實驗室擁有多種品牌或同一品牌多臺儀器的情況十分普遍。由于不同檢測系統(tǒng)的檢測結(jié)果可能存在不可比性,因此,醫(yī)學(xué)實驗室認可的兩個國際標準ISO/IEC 17025(檢測和校準實驗室能力的通用要求)和ISO/15189(醫(yī)學(xué)實驗室質(zhì)量和能力的專用要求)都對檢驗結(jié)果的溯源性和可比性提出了明確要求,強調(diào)方法學(xué)比較試驗(比對試驗)是實現(xiàn)準確度溯源和患者標本檢驗結(jié)果可比性的重要途徑[4]。本研究參考美國臨床實驗室標準化協(xié)會(CLSI)的EP12-A2文件,對不同醫(yī)院實驗室HCV抗體測定結(jié)果進行分析,通過比較符合率,判斷結(jié)果的可比性。
1 材料與方法
1.1標本收集2014年6月至2014年7月新疆醫(yī)科大學(xué)第一附屬醫(yī)院醫(yī)學(xué)檢驗中心門診和住院患者血清標本共100例,其中酶聯(lián)免疫吸附試驗(ELISA)初篩HCV抗體 50例陽性,50例陰性,各分離兩份血清置于-80 ℃冰箱保存待測。
1.2儀器與試劑醫(yī)院1(新疆醫(yī)科大學(xué)第一附屬醫(yī)院)使用儀器:國產(chǎn)addcare ELISA 1100全自動酶免分析系統(tǒng)(簡稱addcare ELISA 1100,煙臺生物科技有限公司);BIO-RAD iCycler 擴增儀;使用試劑:抗HCV診斷試劑盒ELISA,由北京萬泰生物藥業(yè)股份有限公司提供(批號C20140408);HCV抗體確證試劑盒重組免疫印跡法(recombinant immunoblot assay,RIBA)由北京萬泰生物藥業(yè)股份有限公司提供(批號RC20130101);HCV-RNA檢測采用中山大學(xué)達安基因股份有限公司生產(chǎn)的HCV基因分型檢測試劑盒(批號2014003)。醫(yī)院2(石河子大學(xué)第一附屬醫(yī)院)所用酶免儀及型號與醫(yī)院1相同,試劑由上海科華生物工程股份有限公司提供(批號201404011)。所有試劑均在有效期內(nèi)使用,并嚴格按照試劑盒說明書進行實驗操作。
1.3方法
1.3.1儀器準備2臺儀器在實驗前均進行日常維護保養(yǎng),確定其處于良好狀態(tài)。
1.3.2精密度驗證批內(nèi)精密度:分別取高、中、低3個濃度的樣本,在一批檢測內(nèi),重復(fù)檢測20次(孔),計算所得吸光度(A)值的均值和標準差,計算批內(nèi)變異系數(shù)(CV)。批間精密度:在10 d以上時間內(nèi)單次(孔或管)重復(fù)進行20批檢測,計算所得A值的均值和標準差,計算批間CV。批內(nèi)精密度可接受范圍為CV≤10%,批間精密度可接受范圍為CV≤15%。
1.3.3臨界值(Cut-off值)驗證準備具有Cut-off值濃度和濃度在Cut-off值±20%的樣本,重復(fù)測定每個樣本20次,計算出樣本的陰性和陽性百分比。Cut-off值濃度的樣本重復(fù)測定應(yīng)有50%陽性和50%陰性結(jié)果,Cut-off值+20%濃度的標本檢測陽性率大于或等于95%,且Cut-off值-20%濃度的標本檢測陰性率大于或等于95%,此時,標本濃度在Cut-off值±20%濃度范圍之外就能得到穩(wěn)定的檢測結(jié)果。
1.3.4灰區(qū)的確定方法:CO±2S,其中CO是檢測儀器的Cut-off值,S為實驗室做室內(nèi)質(zhì)控ROC的S。
1.3.5標本檢測對-80 ℃保存待測的100份(初篩50例陽性,50例陰性)血清標本根據(jù)隨機數(shù)字表進行隨機編號,用HCV抗體診斷試劑ELISA盲法分10 d進行檢測,同時用RIBA進行確認,RIBA檢測不確定的標本用聚合酶鏈反應(yīng)(PCR)檢測,記錄A值及確認結(jié)果。
1.3.6PCR及RIBA結(jié)果判斷標準PCR判斷標準:當(dāng)樣本的HCV-RNA濃度小于1×103IU/mL為陰性,≥1×103IU/mL為陽性。對于RIBA檢測為陽性及陰性的樣本,直接報告為HCV抗體陽性或陰性;對于RIBA檢測不確定的標本,用PCR進行檢測,當(dāng)PCR檢測為陽性時,報告為陽性,當(dāng)PCR檢測為陰性時,報告為不確定。
1.3.7質(zhì)量控制HCV抗體診斷試劑盒每一批分別設(shè)定1個空白對照、2個陰性對照、2個陽性對照和一個質(zhì)控孔,其中陰性對照孔A≤0.08,陽性對照孔A≥0.50,否則實驗無效;質(zhì)控孔S/CO值為2.39~4.96。HCV抗體確證試劑盒每一批分別設(shè)定1個陰性對照和1個陽性對照,其中陰性對照出現(xiàn)對照線-1和對照線-2,陽性對照出現(xiàn)Core、NS3、NS4-1、NS4-2、NS5、對照線-1和對照線-2,且每條試驗結(jié)果中對照線-1和對照線-2均必須出現(xiàn),如果對照線-1和對照線-2均不出現(xiàn)或僅出現(xiàn)1條,則此條的檢測結(jié)果無效。該試驗的整個過程均有良好的質(zhì)量控制。
1.4統(tǒng)計學(xué)處理采用SPSS16.0軟件進行統(tǒng)計分析,用配對四格表χ2檢驗,P<0.05為差異有統(tǒng)計學(xué)意義。
2 結(jié) 果
2.1精密度驗證結(jié)果見表1。
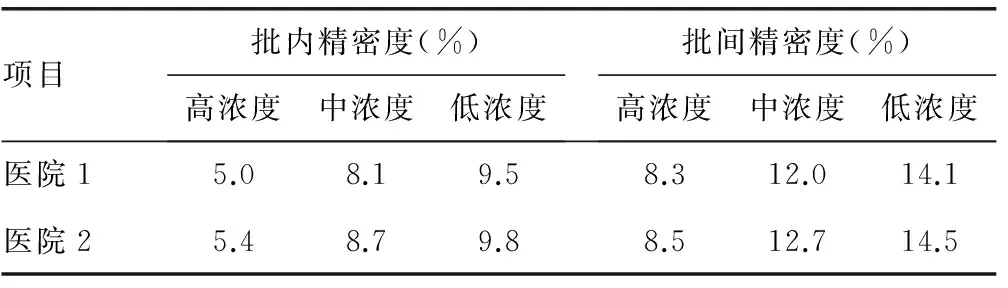
表1 兩家醫(yī)院精密度驗證結(jié)果
2.2Cut-off值驗證醫(yī)院1的自建Cut-off值為0.448,該濃度與其上下20%濃度的標本經(jīng)驗證后與唐婧等[5]研究結(jié)果相符,醫(yī)院2的自建Cut-off值為0.550,經(jīng)驗證后與之相符。
2.3灰區(qū)范圍及結(jié)果醫(yī)院1的灰區(qū)范圍是0.317~0.579,醫(yī)院2的灰區(qū)范圍是0.406~0.694。研究100例標本中共收集10例初篩濃度在0.361~0.683的灰區(qū)標本,結(jié)果顯示,兩家醫(yī)院ELISA對10例灰區(qū)標本均檢測出陽性7例,陰性3例,RIBA及PCR聯(lián)合檢出陽性5例,陰性5例。
2.4ELISA檢測結(jié)果兩家醫(yī)院實驗室各自按照驗證后的Cut-off值判斷HCV抗體檢測結(jié)果,醫(yī)院1及醫(yī)院2均檢測出陽性47例,陰性53例。
2.5RIBA及PCR確證結(jié)果RIBA及PCR聯(lián)合檢出陽性45例,陰性55例。其中RIBA檢測不確定的標本HCV抗體特異條帶的分布情況分別是:Core蛋白強度為2+的有5例(5/9),強度為1+的有2例(2/9);NS3蛋白強度為1+的有2例(2/9)。
2.6靈敏度和特異度根據(jù)ELISA檢測HCV抗體結(jié)果及RIBA和PCR確證結(jié)果分析,醫(yī)院1及醫(yī)院2的靈敏度和特異度相同,分別為100%、96%。見表2。

表2 兩家醫(yī)院檢測HCV抗體的結(jié)果
2.7符合率兩家醫(yī)院實驗室間檢測臨床標本HCV抗體的陽性符合率100%,陰性符合率100%,總符合率100%,差異無統(tǒng)計學(xué)意義(P=1.000),見表3。
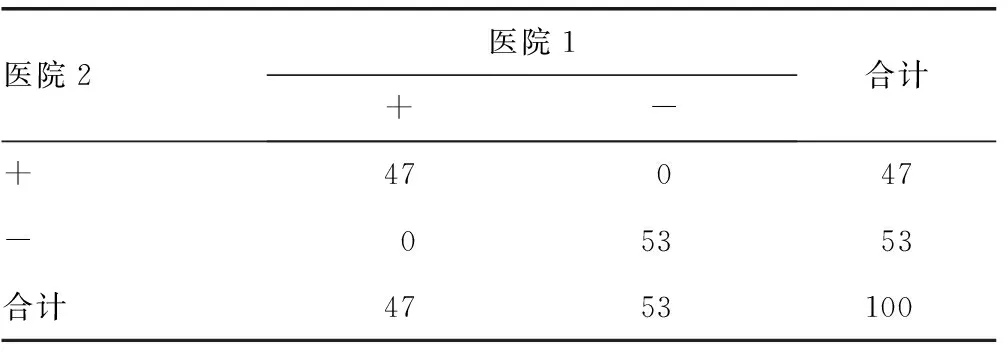
表3 兩家醫(yī)院實驗室間檢測HCV抗體的符合率結(jié)果
3 討 論
本研究中兩家醫(yī)院實驗室所用儀器型號相同,均為國產(chǎn)addcare ELISA 1100全自動酶免分析系統(tǒng),但試劑不同。研究目的在于分析不同國產(chǎn)儀器和試劑在不同環(huán)境下檢測HCV抗體結(jié)果的可比性,從而為不同實驗室之間檢驗結(jié)果的互認提供實驗依據(jù)。
精密度是檢驗方法評估中最基本的評價指標,主要評價測定結(jié)果的重復(fù)性,一般采用CV來反映精密度的好壞,本研究精密度結(jié)果顯示,兩家醫(yī)院的批內(nèi)CV<10%,批間CV<15%,符合比對實驗的要求,說明這兩家醫(yī)院的檢測系統(tǒng)均穩(wěn)定可靠且重復(fù)性較好。
對定性試驗來講,Cut-off值是惟一的醫(yī)學(xué)決定水平,而Cut-off值的確定缺乏統(tǒng)一的標準,使得在測定中對同一份標本的檢測結(jié)果有可能出現(xiàn)很大的差異,尤其是對弱陽性標本及僅出現(xiàn)針對HCV單個蛋白成分抗體的標本[6],因此定性試驗Cut-off值的高低,直接關(guān)系到試驗結(jié)果的正確與否,而驗證Cut-off值是否正確對試驗結(jié)果的確定顯得尤為重要。本研究經(jīng)驗證后結(jié)果顯示與醫(yī)院1和醫(yī)院2的自建Cut-off值相符,但彼此略有不同,分別是0.448和0.550,經(jīng)分析后可能存在的原因是兩家醫(yī)院使用的試劑不同,不同的試劑盒其抗原的來源及包被量有所差異,因此可能出現(xiàn)檢測結(jié)果的差異而導(dǎo)致Cut-off值設(shè)定結(jié)果不同。
此外,ELISA測定技術(shù)本身在Cut-off值的設(shè)置上具有一定模糊性,即所謂的灰區(qū),也就是說在Cut-off值周圍一定區(qū)域內(nèi),測定結(jié)果難以明確判斷是陰性還是陽性,但是目前國內(nèi)所應(yīng)用的傳染性病原體抗原或抗體檢測的ELISA試劑盒基本上都沒有涉及灰區(qū)問題,而僅僅是以Cut-off值來判斷陰陽性結(jié)果,這就會造成處于Cut-off值附近的樣品易檢測為假陽性或假陰性[7],而檢測系統(tǒng)對灰區(qū)標本的檢出能力更能反映其性能。因此,灰區(qū)的設(shè)置對提高HCV抗體的檢出率,最大限度地降低誤檢,防止漏檢同樣具有重要的意義。本研究中灰區(qū)標本的HCV抗體檢測結(jié)果顯示兩家醫(yī)院均有兩份血清標本ELISA檢測為HCV抗體陽性,但金標準確認結(jié)果為HCV抗體陰性,即出現(xiàn)假陽性結(jié)果。在排除標本溶血、脂血及黃疸的情況下,分析其可能的原因有:(1)高免疫球蛋白G血癥、類風(fēng)濕因子、超氧化物歧化酶、異嗜性抗體及某些自身抗體等[8];(2)用于試劑固相包被的基因工程抗原不純[9];(3)操作過程中洗板不徹底而導(dǎo)致結(jié)果偏高。由于灰區(qū)標本易出現(xiàn)假陽性和假陰性結(jié)果,建議對灰區(qū)標本經(jīng)金標準確認后再發(fā)檢驗報告。
由于定性試驗的結(jié)果不同于生化試驗的比對,需要用臨床資料或確診試驗所證實,所以通常用靈敏度和特異度來評價定性試驗的性能[10]。若根據(jù)試劑說明書給定的Cut-off值(醫(yī)院1為0.14,醫(yī)院2為0.25)判斷檢測結(jié)果,醫(yī)院1的靈敏度和特異度分別為100%和80%,醫(yī)院2的靈敏度和特異度分別為100%和89%,雖然靈敏度都很高,但其特異度均較低,更容易出現(xiàn)假陽性結(jié)果而導(dǎo)致誤診率較高。本研究中兩家實驗室根據(jù)各自建立的Cut-off值判斷檢測結(jié)果,研究顯示兩臺儀器的靈敏度和特異度相同且均較高,分別為100%和96%,表明不同實驗室以自建Cut-off值為判斷標準,可以在不降低靈敏度的情況下顯著提高其特異度,不僅對HCV敏感且檢出率高、漏檢率低,為實現(xiàn)丙型肝炎患者的早發(fā)現(xiàn)、早診斷、早治療從而控制并治愈疾病發(fā)揮重要作用,同時也減少了因誤診而帶來的不便和血液資源的浪費。
對于定性試驗,在診斷未知的情況下,比較不同醫(yī)院間檢測結(jié)果的準確性及可比性,可以選用陰性、陽性符合率指標。本研究結(jié)果顯示,兩家醫(yī)院的陽性符合率100%,陰性符合率100%,總符合率100%,差異無統(tǒng)計學(xué)意義(P=1.000),表明兩家醫(yī)院實驗室的檢測結(jié)果互認可比。
綜上所述,定期對實驗室同一項目不同檢測系統(tǒng)進行比對分析,是保證測定結(jié)果準確可比的重要手段,也是實驗室內(nèi)質(zhì)量控制的一個良好補充,為實現(xiàn)實驗室間檢測結(jié)果的互認打下基礎(chǔ)。
[1]Williams R.Global challenges in liver disease[J].Hepatology,2006,44(3):521-526.
[2]Global burden of Hepatitis C working Group.Global burden of disease (GBD) for hepatitis C[J].J Clin Pharmacol,2004,44(1):20-29.
[3]Deuffic-Burban S,Poynard T,Sulkowski MS,et al.Estimating the future health burden of chronic hepatitis C and human immunodeficiency virus infections in the United States[J].J Viral Hepat,2007,14(2):107-115.
[4]魏昊,叢玉隆.醫(yī)學(xué)實驗室質(zhì)量管理與認可指南[M].北京:中國計量出版社,2004:72-74.
[5]唐婧,包建玲,孟存仁,等.ROC曲線對ELISA檢測丙型肝炎抗體陽性判斷值的確定和分析[J].檢驗醫(yī)學(xué),2014,29(8):826-830.
[6]江濤,李軍,王昌富,等.基于ISO15189要求的免疫學(xué)定性試驗性能驗證方法的探討[J].國際檢驗醫(yī)學(xué)雜志,2014,35(3):332-333.
[7]鄧巍,王露楠,李金明.丙型肝炎病毒抗體酶聯(lián)免疫吸附試驗陽性判斷值在獻血員血液篩檢中的意義[J].中華檢驗醫(yī)學(xué)雜志,2004,27(10):39-41.
[8]Mimms L,Vallari D,Ducharme L,et al.Specificity of anti-HCV ELISA assessed by reactivity to three immunodominant HCV regions[J].Lancet,1991,336(8730):1590-1591.
[9]黃秀琳,李維,程穎,等.HIV酶免試劑在獻血標本中檢測效果評價[J].國際檢驗醫(yī)學(xué)雜志,2013,34(10):1297-1298.
[10]國家藥典委員會.中華人民共和國藥典-三部[M].北京:化學(xué)工業(yè)出版社,2005:335.
The comparative study of the determination of hepatitis C antibody by ELISA detection system in different laboratories*
Zeng Yanhua1,Lu Xiangyun2#,Zhang Li1,Zhang Zhaoxia1△,Cheng Jiang2▲
(1.Laboratory Medicine Center,the First Affiliated Hospital of Xinjiang Medical University, Urumqi,Xinjiang 830054,China;2.Department of Clinical Laboratory,the First Affiliated Hospital of Shihezi University,Shihezi,Xinjiang 832000,China)
ObjectiveTo investigate the comparability of the determination of hepatitis C antibody(anti-HCV) by ELISA detection system in different laboratories,in order to provide the experimental basis for the mutual recognition of test results between different laboratories.MethodsIn accordance with EP12-A2 files from the American association of Clinical Laboratory Standards Institute (CLSI),a total of 100 patients were recruited,including 50 cases of anti-HCV screening positive and 50 negative.The domestic addcare ELISA 1100 full autokinetic enzyme analysis system(addcare ELISA 1100) was used to test HCV antibody under randomized blind method in different labs,and recombinant immunoblot assay (RIBA) and polymerase chain reaction (PCR) were also carried out to provide a evidence of true positive for HCV antibody tests.Further,we compared the coincidence rate of HCV antibody tests,estimated the comparability of test results.ResultsThe sensitivity and specificity of the two laboratories were 100% and 96% respectively.The positive coincidence rate was 100%,negative coincidence rate was 100% and total coincidence rate was 100%,the difference was not statistically significant(P>0.05).ConclusionThe test results has a better comparability and recognition between the two laboratories when use the self-built cut-off value under the good condition of the instruments,the determination results are comparable.
hepatitis C antibody;enzyme linked immunosorbent assay;recombinant immunoblotting;polymerase chain reaction;coincidence rate
衛(wèi)生部醫(yī)藥衛(wèi)生科技發(fā)展研究中心專項課題(28-1-13)。作者簡介:曾艷華(1988-),在讀碩士,主要從事丙型肝炎的免疫學(xué)新進展研究。#并列第一作者。△
,E-mail:285715300@qq.com。▲通訊作者,E-mail:jyk6857@vip.163.com。
·技術(shù)與方法·10.3969/j.issn.1671-8348.2016.22.027
R392
A
1671-8348(2016)22-3104-03
2016-03-18
2016-05-06)

