拉米夫定阻斷HBV宮內感染療效及安全性的薈萃分析
劉江英 劉亦赤 李北萍
拉米夫定阻斷HBV宮內感染療效及安全性的薈萃分析
劉江英1劉亦赤2李北萍3
目的 系統評價拉米夫定(lamivudine LMV)在孕晚期阻斷HBV母嬰傳播的療效及安全性。方法 計算機檢索中英文數據庫中2014年6月前發表的關于在孕晚期應用LMV的隨機對照試驗的文獻,并應用Stata 12.0軟件對符合納入標準的文獻進行統計學分析。結果 本研究共納入7篇文獻,LMV組共計納入病例383例,對照組共計納入病例370例,所有病例HBV-DNA均≥106copies/ml。新生兒和6月齡時血清HBsAg陽性的風險較對照組分別減少56%[RR=0.441,95% CI(0.316,0.615)]、83%[RR=0.172,95% CI(0.085,0.346)];新生兒和6月齡時血清HBV-DNA陽性的風險較對照組分別減少69%[RR=0.312,95% CI(0.198,0.491)]、76%[RR=0.243,95% CI(0.122,0.485)]。結論 對于高病毒載量的孕婦,孕晚期口服LMV可有效地阻斷HBV母嬰傳播。
乙型肝炎病毒;宮內感染;母嬰傳播;垂直傳播;Meta分析
【Abstract】
ObjectiveEvaluation on the efficacy and safety of lamivudine in late pregnancy to block mother-to-child transmission of HBV. Methods Computer database retrieval English and Chinese before June 2014 on lamivudine in late pregnancy application literatures of of LMV group randomized controlled trials. Using Stata 12.0 software for statistical analysis. Results 7 articles were included in this study,a total of cases in 383 cases,the blank group total cases in 370 cases,all cases of HBV - DNA were ≥106copies / ml. The risk of neonatal HBsAg positive 56% less than the control group[RR = 0.441,95% CI (0.316,0.615)],Was born six months HBsAg positive risk 83% less than the control group[RR = 0.172,95% CI (0.085,0.346)]. The risk of neonatal serum HBV - DNA positive 69% less than the control group[RR = 0.312,95% CI (0.198,0.491)],Was born six months serum HBV - DNA positive risk is 76% less than the control group[RR = 0.243,95% CI (0.122,0.485)]. Conclusion Oral lamivudine in late pregnancy can effectively block mother-to-child transmission of HBV when high viral load in these patients
【Key words】Hepatitis B virus,Intrauterine infection,Mother to child transmission,Vertical transmission,Meta analysis
母嬰垂直傳播是我國慢性乙型肝炎病毒(hepattitis B virus,HBV)感染的主要傳播途徑,目前采取的新生兒主動免疫及被動免疫主要是減少圍產期及哺乳期感染,難以阻斷子宮內感染,有研究表明孕婦血清中HBV-DNA水平與子宮內感染呈正相關性,若母親血清HBV-DNA≥108copies/ml,新生兒出生后即使采用標準主動及被動免疫預防,母嬰垂直傳播率仍高達8.5%[1-4]。為進一步從循證醫學的角度對拉米夫定(lamivudine,LMV)阻斷HBV母嬰傳播的臨床試驗進行系統評價,本研對2014年6月以前國內外發表的相關文獻進行Meta分析,以評價LMV阻斷HBV母嬰傳播療效及安全性。
1 材料與方法
1.1檢索策略
計算機檢索PubMed、Cochrane Library、CNKI全文數據庫、維普中文科技期刊數據庫及中文生物醫學文獻數據庫(CBM),并追查了所有納入文獻的參考文獻。檢索年限均為從建庫到2014 年6月。檢索詞包括:lamivudine、HBV(or hepatitis B virus)、intrauterine(or pregnant or pregnancy or mother or maternity or children or uterus )、拉米夫定、乙型肝炎病毒、妊娠、懷孕、孕婦、垂直傳播、母嬰傳播等。
1.2納入和排除標準
納入標準:(1)研究設計:隨機對照試驗(RCT);(2)研究對象:年齡20~40歲,孕24~32周,HBsAg陽性超過6個月,肝功正常,HBV-DNA≥106copies/ml,既往未使用抗病毒治療,孕早期無先兆流產、保胎等病史,未合并甲、丙、丁、戊肝炎病毒、HIV等感染,三維B型超聲排除胎兒畸形,孕期未使用其他藥物如免疫調節劑、細胞毒性藥物或糖皮質激素等,丈夫無HBV感染,符合倫理學要求;(3)兩組在年齡、生化等方面具有均衡可比性;(4)國內外公開發表的文獻且均為全文;(5)干預措施:治療組為孕母孕期單用LMV(100 mg),對照組為空白(模擬劑或安慰劑或空白)。
排除標準:(1)合并有藥物性肝損害、自身免疫性肝病、酒精性肝病、遺傳代謝性肝病等;(2)伴有惡性腫瘤、嚴重血液系統疾病等;(3)僅報道了不良反應或描述性研究;(4)文獻提供的數據在分析時無法轉化或應用;(5)重復發表的文獻。
1.3療效判定指標
(1)主要指標:新生兒出生后即刻及6月齡嬰兒血清HBsAg、HBV-DNA陽性率;(2)次要指標:孕婦對藥物的不良反應、血常規和肝腎功能變化、妊娠及分娩并發癥、新生兒生長發育指標(身長、體重)、新生兒窒息率、新生兒畸形等。宮內感染的判定指標:6月齡時嬰兒血清HBsAg或HBV-DNA陽性為宮內感染的判斷標準[5]。
1.4質量評價和資料提取
根據納入和排除標準,至少由2名評價員分別獨立篩選文獻,對納入文獻獨立進行質量評價和資料提取,然后交叉核對,如有分歧,通過第三者協商解決。隨機對照試驗質量評價按Jadad量表[6]。
1.5統計分析
用Stata 12.0軟件進行統計學分析。本研究中計數資料采用相對危險度(relative risk RR)及95%可信區間(95% CI)作為系統評價指標。
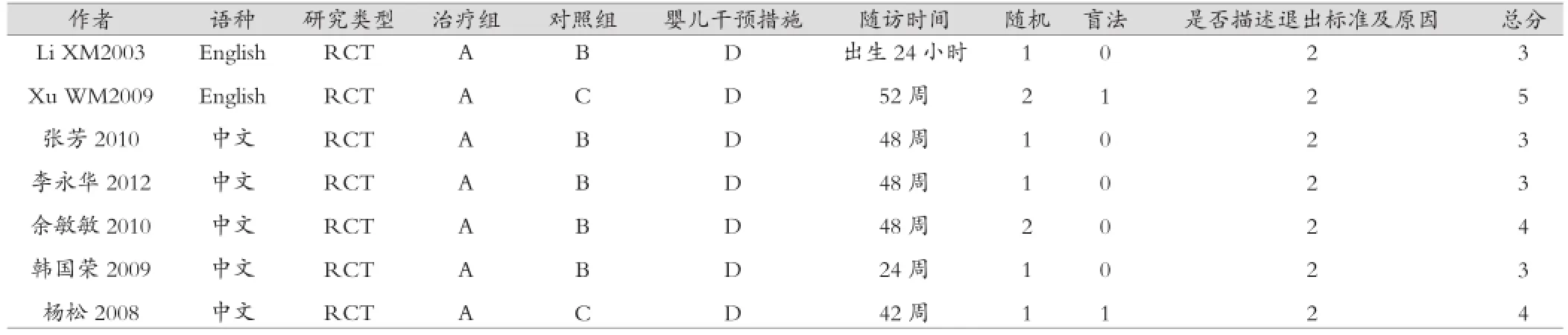
表1 納入文獻基本特征
2 結果
2.1納入文獻的基本情況
共檢索到相關文獻96篇(英文25篇、中文71篇),經初篩納入37篇,進一步閱讀全文后最終納入7篇[7-13],其中英文文獻2篇,中文文獻5篇(詳見表1)。LMV組共計納入病例383例,對照組共計納入病例370例。
2.2LMV的治療效果
2.2.1LMV對新生兒及嬰兒HBsAg的影響 納入的文獻中有5篇[7,8,10-12]將新生兒(出生時免疫預防接種前)HBsAg陽性率作為療效判定的指標,其中拉米夫定組納入311例病例,對照組納入300例病例。Meta分析結果顯示,拉米夫定治療組新生兒HBsAg陽性率低于對照組 [RR=0.441,95%CI(0.316,0.615)];納入的文獻中有6篇[8-13]將嬰兒(6個月)HBsAg陽性率作為療效判定的指標,其中拉米夫定組納入340例病例,對照組納入319例病例。Meta分析結果顯示,拉米夫定治療組嬰兒6個月時HBsAg陽性率低于對照組 [RR=0.172,95% CI (0.085,0.346)]。
2.2.2LMV對新生兒及嬰兒HBV-DNA的影響 納入的文獻中有4篇[8,10-12]將新生兒(出生時免疫預防接種前)HBV-DNA陽性率作為療效判定的指標,其中拉米夫定組納入268例病例,對照組納入248例病例。Meta分析結果顯示,拉米夫定治療組新生兒HBV DNA陽性率低于對照組 [RR=0.312,95% CI(0.198,0.491)];納入的文獻中有4篇[8,10-12]將嬰兒(6個月)HBVDNA陽性率作為療效判定的指標,其中拉米夫定組納入270例病例,對照組納入248例病例。Meta分析結果顯示,拉米夫定治療組嬰兒6個月時HBV DNA陽性率低于對照組 [RR=0.243,95%CI(0.122,0.485)]。
2.3不良反應
1篇文獻[8]報道了LMV組孕婦1例羊水過多,經治療后好轉,1例因先天發育不全導致死胎,LMV組孕婦分娩的新生兒1例出現新生兒黃疸,對照組孕婦分娩的新生兒有1例出現新生兒黃疸;1篇文獻報道[11]LMV組孕婦1例發生肌痛伴CK輕度升高,對照組孕婦分娩的新生兒1例出現唇、腭裂。
3 討論
垂直傳播仍是乙型肝炎最主要的傳播途徑。而目前采取的新生兒出生后盡早注射乙肝疫苗和聯合使用HBIG的主動免疫及被動免疫主要是盡可能減少圍產期感染及哺乳期感染[14,15],但難以阻斷子宮內的感染。
研究表明,在妊娠后期,由于胎盤的通透性升高,且損害胎盤屏障的因素增多,HBV可以通過損傷的胎盤直接進入胎兒的體內循環使胎兒感染HBV或者HBV感染胎盤后可穿透胎盤屏障感染胎兒,而且隨著孕婦血清HBV-DNA水平增高,胎兒發生宮內感染的危險性也呈增高趨勢[17]。而且越來越多的指南[2]均建議高病毒載量的HBV感染母親在妊娠晚期使用LMV、替諾福韋或替比夫定,并將其作為預防HBV母嬰傳播的一種有效措施。本研究顯示,在出生時,與空白對照組相比,LMV組新生兒血清HBsAg、HBV-DNA陽性的風險較對照組分別減少56%和69%,差異有統計學意義;在6個月齡時,與對照組相比,LMV組嬰兒血清HBsAg、HBV-DNA的陽性的風險較對照組分別減少83%和76%,差異亦有統計學意義,提示孕晚期應用LMV可以有效保護胎兒,預防宮內感染的發生。
本研究同時將孕婦對藥物的不良反應、血妊娠及分娩并發癥、新生兒生長發育指標(身長、體重)、新生兒窒息率、新生兒畸形戀等作為次要觀察指標,納入的文獻中,1篇文獻[8]報道了LMV組孕婦1例羊水過多,經治療后好轉,1例因先天發育不全導致死胎,LMV組孕婦分娩的新生兒1例出現新生兒黃疸,對照組孕婦分娩的新生兒1例出現新生兒黃疸;1篇文獻報道[11]LMV組孕婦1例發生肌痛伴CK輕度升高,對照組孕婦分娩的新生兒1例出現唇、腭裂。但均與LMV無關,提示LMV對母嬰的安全性良好。
雖然我們盡可能全面的檢索文獻,并通過多種方法對發表性偏倚進行分析,但由于部分陰性結果可能未進行報道,這在一定程度上限制了資料的全面性,故上述結論還有待納入更多高質量隨機對照試驗加以證實。
[1] Jonas MM. Hepatitis B and pregnancy:an underestimated issue[J]. Liver International,2009,29(s1):133-139.
[2] 中華醫學會肝病學分會,中華醫學會感染病學分會. 慢性乙型肝炎防治指南(2015更新版)[J]. 中華肝臟病雜志,2015,23(12):888-905.
[3] Zhang H,Pan CQ,Pang Q,et al. Telbivudine or lamivudine use in late pregnancy safely reduces perinatal transmission of hepatitis B virus in real-life practice[J]. Hepatology,2014,60(2):498-476.
[4] Sarkar M,Terrault NA. Ending vertical transmission of hepatitis B:the third trimester intervention[J]. Hepatology,2014,60(2):448-451.
[5] 楊淑麗,劉繼明,王宇明. 乙型肝炎病毒宮內感染研究現狀[J].傳染病信息,2007,20(4):217-220.
[6] Jadad AR,Moore RA,Carroll D,et al. Assessing the quality of reports of randomized clinical trials:is blinding necessary? [J]. Controlled Clin Trials,1996,17(1):1-12.
[7] Li XM,Yang YB,Hou HY,et al. Interruption of HBV intrauterine transmission:a clinical study[J]. World J Gastroenterol,2003,9(7):1501-1503.
[8] Xu WM,Cui YT,Wang L,et al. Lamivudine in late pregnancy to prevent perinatal transmission of hepatitis B virus infection:a multicentre,randomized,double-blind,placebo-controlled study [J]. Journal of viral Hepatits,2009,16(2):94-103.
[9] 張彥芳. 拉米夫定阻斷慢性 HBV感染孕婦母嬰傳播 50例臨床效果觀察[J]. 實用婦產科雜志,2010,26(5):367-368.
[10] 李永華,莫慧瓊,王文鳳,等. 拉米夫定阻斷乙型肝炎病毒在母嬰傳播的臨床研究[J]. 齊齊哈爾醫學院學報,2012,33(2):207-208.
[11] 余敏敏,江紅秀,吳凱華,等. 妊娠中晚期拉米夫定抗病毒治療阻斷乙型肝炎病毒母嬰垂直傳播的研究[A]. 第二屆慢性乙型肝炎抗病毒治療難點和熱點學術會議匯編[C].2010:35-39.
[12] 韓國榮,方之勛,趙偉,等. 拉米夫定對乙型肝炎病毒母嬰傳播的影響及安全性[J]. 中華傳染病雜志,2009,27(11):673-676.
[13] 楊松,劉敏,王玲. 拉米夫定對乙型肝炎病毒陽性孕婦母嬰垂直傳播的影響[J]. 中華婦產科雜志,2008,43(5):329-331.
[14] Lee C,Gong Y,Brok J,et al. Effect of hepatitis B immunisation in newborn infants of mothers positive for hepatitis B surface antigen:systematic review and meta-analysis[J]. BMJ,2006,332(7537):328-336.
[15] Tran TT,Keeffe EB. Management of the pregnant hepatitis B patient[J]. Current Hepatitis Reports,2008,7(7):12-17.
[16] Burk RD,Hwang LY,Ho GY,et al. Outcome of perinatal hepatitis B virus exposure is dependent on maternal virus load[J]. J Infect Dis,1994,170(6):1418-1423.
[17] Wiseman E,Fraser MA,Hoden S,et al. Pernatal transmission of hepatitis B virus:an Australian experience[J]. Med Aust,2009,190:489-492.
A Meta-analysis of Efficacy and Safety of Lamivudine in Blocking HBV Intrauterine Infection
LIU Jiangying1LIU Yichi2LI Beiping31 Department of Obstetrics and Gynecology,Quanzhou Guangqian Hospital,Quanzhou Fujian 362000,China,2 Department of Clinical Laboratory,Quanzhou Guangqian Hospital,Quanzhou Fujian 362000,China,3 Department of Obstetrics and Gynecology,The People's Hospital of Changji City,Changji Xinjiang 831110,China
R512.62
A
1674-9316(2016)14-0087-03
10.3969/j.issn.1674-9316.2016.14.058
1 泉州市光前醫院婦產科,福建 泉州 362000;
2泉州市光前醫院檢驗科,福建 泉州 362000;
3新疆醫科大學第一附屬醫院昌吉分院產科,新疆 昌吉831100

