新輔助化療方案聯合手術治療晚期宮頸癌的效果及安全性探討
杜魯豫 陳懷博
1聊城市中心醫院婦產科,山東 聊城 252000
2陽谷縣疾病預防控制中心檢驗科,山東 聊城 252300
新輔助化療方案聯合手術治療晚期宮頸癌的效果及安全性探討
杜魯豫1#陳懷博2
1聊城市中心醫院婦產科,山東聊城252000
2陽谷縣疾病預防控制中心檢驗科,山東聊城252300
目的探討新輔助化療(NACT)紫杉醇聯合順鉑(TP)治療晚期宮頸癌的臨床效果及安全性。方法收集晚期宮頸癌患者67例作為研究對象,根據手術前新輔助化療方案分為化療組37例和對照組30例,化療組給予1~2個療程的TP化療方案治療后實施廣泛子宮切除+盆腔淋巴結清掃術,對照組給予順鉑60 mg+氟脲苷500 mg+亞葉酸鈣300 mg+多柔比星30 mg化療及上述手術治療。比較兩組療效及生存時間。結果兩組患者在經過1~2個周期的化療方案治療后(手術前),化療組的有效率為54.05%,對照組的有效率為43.33%,兩組比較,差異無統計學意義(P>0.05);化療組的盆腔淋巴結轉移率13.51%、宮旁累及率2.70%、脈管浸潤率5.41%、切緣陽性率2.70%均低于對照組,差異有統計學意義(P<0.05);兩組患者的化療不良反應比較,差異無統計學意義(P>0.05);化療組的3年生存率64.86%(24/37)與對照組的43.33%(13/40)比較,差異無統計學意義(P>0.05);化療組的3年中位生存期為33.8個月,高于對照組的28.6個月,差異有統計學意義(P<0.05)。結論晚期宮頸癌患者手術前采用TP化療方案治療能夠降低淋巴結轉移率,縮小病灶范圍,延長患者的遠期生存時間。
新輔助化療;紫杉醇;順鉑;晚期宮頸癌;臨床效果;安全性
Oncol Prog,2016,14(3)
宮頸癌為女性人群中發病率僅次于乳腺癌的第二大生殖系統惡性腫瘤,其發病高危因素包括過早進行性生活、早孕、多產以及性生活紊亂,臨床上主要表現為宮頸接觸性出血。雖然近年來宮頸篩查已成為已婚女性常規檢查項目,但宮頸癌的檢出率以及發病例數仍均維持在較高水平[1]。晚期宮頸癌的治療方式以廣泛全子宮切除聯合盆腔淋巴結清掃為主,部分學者認為,術前聯合新型輔助化療方案紫杉醇+順鉑能顯著改善患者術后宮頸癌臨床緩解率,并有助于改善術后五年生存時間[2-3]。本研究分析術前聯合使用新型輔助化療方案的臨床應用價值,具體研究報道如下。
1 對象與方法
1.1研究對象
收集晚期宮頸癌患者67例作為研究對象,根據是否行手術前新輔助化療方案分為化療組37例和對照組30例。納入標準:①宮頸癌的診斷主要依據術前病理活檢及手術后標本病理檢查證實;②入選患者的Kamofsky(KPS)評分>70分;③術前相關檢查未發現遠處臟器轉移;④患者知情同意并獲得聊城市中心醫院醫學倫理委員會的批準。排除標準:①合并嚴重的肝腎功能障礙;②合并血液性疾病或已經發生遠處轉移;③對化療方案嚴重不耐受;④同期參與其他臨床研究;⑤入組本研究前采用其他化療并放棄治療。化療組37例患者,年齡36~67歲,平均年齡(48.27±8.05)歲;入組時KPS評分(74.6±2.8)分;根據國際婦產聯盟(FIGO)分期:Ⅰb2期9例,Ⅱa期14例,Ⅱb期14例;術后病理分化程度:高分化8例,中分化11例,低分化18例;入組時局部腫瘤直徑(5.6±2.0)cm,盆腔淋巴結轉移3例。對照組30例患者,年齡33~62歲,平均年齡(46.39±7.78)歲;KPS評分(75.1±2.4)分;FIGO分期:Ⅰb2期11例,Ⅱa期12例,Ⅱb期7例;術后病理分化程度:高分化6例,中分化11例,低分化13例;入組時局部腫瘤直徑(5.4±1.8)cm,盆腔淋巴結轉移2例。兩組基本情況比較,差異均無統計學意義(P>0.05),具有可比性。
1.2化療方法
化療組術前化療方案:新輔助化療(NACT)為TP方案,采用紫杉醇175 mg/m2聯合順鉑(TP)75 mg/m2,采用Seldinger置管技術從一側股動脈插管至對側髂內動脈,造影顯示盆腔血供后插入對側子宮動脈,在半小時內緩慢注射化療藥物,并使用明膠海綿栓塞,再次將導管退回至髂內動脈分支處,注射剩余的化療劑量。對照組采用順鉑60 mg+氟脲苷500 mg+亞葉酸鈣300 mg+多柔比星30 mg方案行全身靜脈化療1~2個療程。兩組患者術后均予以水化、抗感染、止吐等對癥處理。
1.3臨床療效觀察
①近期療效評價標準參照RECIST實體瘤療效評價標準:完全緩解(CR):可見病灶完全消失;部分緩解(PR):腫瘤病灶的最大直徑×最大垂直直徑減少>50%;疾病穩定(SD):腫瘤最大直徑×最大垂直直徑減少<50%或增大<25%;疾病進展(PD):患者出現一個或多個病灶的腫瘤最大直徑×最大垂直直徑增大>25%。總有效率=(CR+PR)例數/本組樣本量×100%。②比較兩組患者術后的病理檢查結果差異。③對兩組在化療中出現的不良反應進行評價,采用WHO不良反應5級分級標準:0級:無不良反應;Ⅰ級:輕度反應;Ⅱ級:中度不良反應;Ⅲ級:重度不良反應;Ⅳ級:有嚴重的并發癥。④觀察比較化療組和對照組患者的3年生存率、中位生存時間的差異。
1.4統計學方法
所有數據分析及統計采用SAS 9.0統計軟件,計量資料采用均數±標準差(±s)表示;計數資料以百分率(%)表示,組間比較采用χ2檢驗;生存分析采用Kaplan-Meier法,組間比較采用Log-rank檢驗。P<0.05為差異有統計學意義。
2 結果
2.1兩組化療后療效比較
兩組患者在經過1~2個周期的化療方案治療后(手術前)。化療組有效率為54.05%(20/37),對照組有效率為43.33%(13/30),兩組比較差異無統計學意義(χ2=0.762,P=0.386)。(表1)

表1 兩組化療后療效[n(%)]
2.2兩組患者術后病理結果比較
化療組的盆腔淋巴結轉移率、宮旁累及率、脈管浸潤率、切緣陽性率均低于對照組,差異有統計學意義(P<0.05)。(表2)

表2 兩組患者術后病理結果比較[n(%)]
2.3兩組患者化療不良反應比較
兩組患者血紅蛋白減少、血紅蛋白減少、血小板減少、惡心、嘔吐、周圍神經炎、脫發、關節肌肉疼痛、肌酐升高的化療不良作用發生率比較,差異均無統計學意義(P>0.05)。(表3)
2.4兩組患者3年生存率及中位生存期比較
兩組3年隨訪中,各有一例患者失訪,化療組的3年生存率64.86%(24/37)與對照組的43.33% (13/40)比較,差異無統計學意義(χ2=2.650,P= 0.104)。化療組的3年中位生存期為33.8個月,高于對照組的28.6個月,差異有統計學意義(χ2= 4.221,P=0.041)。生存曲線見圖1。
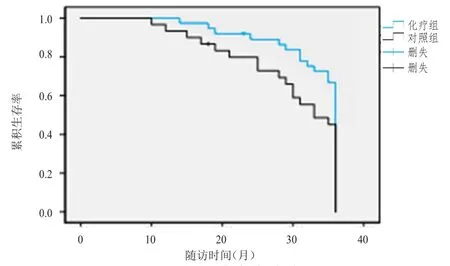
圖1 兩組的生存曲線圖
3 討論
宮頸癌為近年來臨床上常見的婦科惡性腫瘤,隨著婦科宮頸篩查模式的規范化,宮頸癌的臨床檢出率顯著增加。相關臨床研究報道每年宮頸癌新發病例為50萬左右,約占婦科惡性腫瘤發病的15%[4]。宮頸癌早期臨床表現較為隱匿,典型表現為宮頸接觸性出血,部分患者僅表現為白帶帶血、陰道分泌物腥臭味等非特異性表現,宮頸癌晚期可表現為大出血、惡病質、惡臭以及貧血等晚期腫瘤表現,侵犯周圍組織時可產生較為嚴重的局部壓迫癥狀,主要表現為坐骨神經痛、尿頻尿急、腰痛以及肛門墜脹感,嚴重威脅女性的生命健康[5]。現階段如何采取合理有效的治療應對晚期宮頸癌已成為婦科腫瘤領域專家共同關注的課題。Ma等[6]和Saito等[7]臨床研究者在回顧性分析了美國中晚期宮頸癌手術后聯合放化療的臨床資料后發現,對于中晚期宮頸癌,術后放療的同時聯合TP方案化療,能改善患者術后半年內的惡性腫瘤臨床緩解水平,但對于患者術后五年生存時間并無顯著影響。Lissoni等[8]研究了國內278例晚期宮頸癌臨床治療方案后發現,對于宮頸癌分期Ⅱb期及以上晚期臨床病例,放療的同時聯合使用TP化療方案能顯著改善患者淋巴結侵襲癥狀、遠處轉移癥狀,但對于患者生存時間并無顯著性影響[5,9]。
部分學者認為,對于部分中晚期宮頸癌手術治療的患者,術前聯合新型輔助化療方案能顯著緩解手術后臨床癥狀,延長術后五年生存時間[10],但相關臨床研究較少。本研究通過收集晚期宮頸癌患者67例,化療組給予1~2個療程的TP化療方案治療后實施廣泛子宮切除+盆腔淋巴結清掃術,對照組給予順鉑+氟脲苷+亞葉酸鈣+多柔比星并聯合上述手術治療,結果發現化療組在經過1~2個周期的TP化療方案治療后,有6例患者達到CR,14例患者達到PR,同時化療組的疾病進展率僅為13.51%,較對照組16.67%的疾病進展率有所下降,另外化療組的有效率為54.05%,對照組的有效率為43.33%,提示術前聯合TP化療方案能顯著緩解術后臨床癥狀。王路芳等[10]和Huang等[11]研究了相關新型輔助化療方案后認為,術前聯合TP化療不僅能通過抑制宮頸鱗狀細胞癌增殖、促進凋亡進而有利于腫瘤病灶的縮小,且化療效果有利于廣泛全子宮切除術中對于相關病灶的切除,腫瘤病灶縮小后手術中視野的探查更為清晰,避免術中對于周邊正常組織如膀胱以及直腸的損傷。劉弘揚等[12]也認為,術前聯合新型TP化療能顯著改善廣泛全子宮切除術后生存時間,這與本次研究結論較為一致,此外劉弘揚等還認為,術前TP方案化療能顯著降低盆腔淋巴結轉移率、宮旁累及率以及脈管浸潤率,進而有利于緩解術后晚期宮頸癌患者惡性腫瘤負荷效應,有助于延長術后生存時間。本研究發現化療組的3年中位生存期為33.8個月,高于對照組的28.6個月。一項匯集了3項研究共計280例宮頸癌不同化療方案的分析研究顯示,紫杉醇聯合鉑類化療相比于多柔比星或者氟脲苷可以延長術后(3±0.2)個月生存時間,并提高5%~10%的術后五年無瘤生存率,進一步提示了術前聯合新型TP化療的重要臨床意義,但是新型化療存在一定的并發癥,主要表現為造血系統抑制以及免疫抑制等不良反應,臨床上對于部分化療反應較為嚴重的病例應及時處理,減少患者因化療并發癥導致腫瘤病灶出現進展期表現。
綜上所述,對于晚期宮頸癌廣泛全子宮切除+盆腔淋巴結清掃的病例,術前聯合新型輔助TP化療,能顯著增加臨床緩解率,有利于改善宮頸癌局部浸潤以及遠處轉移,從而延長術后生存時間,但對于部分患者出現的較為嚴重的化療不良反應應尤為重視,積極采取相關措施對癥處理,從而有利于改善患者臨床預后。
[1]朱怡,吳旭,楊蓉,等.上海市育齡婦女HPV感染情況調查及感染因素分析[J].現代儀器與醫療,2015,21(3):119-120.
[2]陳林龍.TP方案聯合放療治療中晚期宮頸癌48例療效觀察[J].廣東醫學院學報,2011,32(6):661-662.
[3]劉少曉,程曉燕,鄭紅楓,等.紫杉醇聯合順鉑新輔助治療局部晚期宮頸癌的臨床療效及安全性評價[J].中國臨床藥理學雜志,2015,31(6):432-434.
[4]覃小敏,李琳,黃艷麗,等.中老年宮頸癌患者預后相關影響因素的分析[J].癌癥進展,2015,13(3):346-349.
[5]劉彥章,李娟,羅福申.三維適形放療同步TP方案治療中晚期宮頸癌的臨床觀察[J].現代預防醫學,2012,39(7):1639-1641.
[6]Ma K,Yang YH,Yang X,et al.Efficacy of postoperative simple chemotherapy and concurrent chemoradiotherapy in FIGO stage IB2-IIB cervical cancer[J].Beijing Da Xue Xue Bao,2013,45(6):910-915.
[7]Saito I,Kitagawa R,Fukuda H,et al.A phase III trial of paclitaxel plus carboplatin versus paclitaxel plus cisplatin in stage IVB,persistent or recurrent cervical cancer:Gynecologic Cancer Study Group/Japan Clinical Oncology Group Study(JCOG0505)[J].Jpn J Clin Oncol,2010,40(1):90-93.
[8]Lissoni AA,Colombo N,Pellegrino A,et al.Aphase II,randomized trial of neo-adjuvant chemotherapy comparing a three-drug combination of paclitaxel,ifosfamide,and cisplatin(TIP)versus paclitaxel and cisplatin(TP)followed by radical surgery in patients with locally advanced squamous cell cervical carcinoma:the Snap-02 Italian Collaborative Study[J].Ann Oncol,2009,20(4):660-665.
[9]王美清,程小珍,毛山山,等.洛鉑聯合多西他賽對宮頸癌的臨床療效觀察[J].中國現代醫學雜志,2014,24(23):84-87.
[10]王路芳,韓娜娜,茹明芳,等.TP與PVB兩種同步放化療方案在維吾爾族中晚期宮頸癌的近期療效比較[J].實用醫學雜志,2014,30(18):2928-2930.
[11]Huang L,Liao LM,Liu AW,et al.Analysis of the impact of platinum-based combination chemotherapy in small cell cervical carcinoma:a multicenter retrospective study in Chinese patients[J].BMC Cancer,2014,14:140.
[12]劉弘揚,奈嫚嫚,封全靈.局部晚期宮頸癌術前新輔助化療效果分析[J].廣東醫學,2014,35(4):556-558.
The efficacy and safety of combined therapy of NACT and surgery in the treatment of advanced cervical cancer
DU Lu-yu1#CHEN Huai-bo2
1Department of Obstetrics andGynecology,Liaocheng City Central Hospital,Liaocheng 252000,Shandong,China
2Department of Clinical Laboratory,Yanggu Shandong County Center for Disease Control and Prevention,Liaocheng 252300,Shandong,China
ObjectiveTo study the efficacy and safety of the combined therapy of NACT in the treatment of advanced cervical cancer.Method67 cases of advanced cervical cancer were included in this study,and were grouped according to the preoperative neoadjuvant chemotherapy regimen as Chemo group(n=37)and control group(n=30),1-2 cycles of NACT chemotherapy and radical hysterectomy+pelvic lymph node dissection were administered for the Chemo group,while the control group was given a chemotherapy of cisplatin 60 mg+FUDR 500 mg+leucovorin calcium 300 mg+doxorubicin 30 mg and a same surgical procedure.The survival of both groups were compared.ResultAfter 1 or 2 cycles of preoperative chemotherapy,the response rate(RR)for Chemo and control group was 54.05%vs 43.33%,with no significant difference observed(P>0.05).The pelvic lymph node metastasis was 13.51%,the parametrial involvement rate of 2.70%,with a vascular infiltration rate of 5.41%,and a positive margin rate 2.70%in the Chemo group,all were significantly lower than that of the control group(P<0.05).The toxicities of chemotherapy of the two groups were similar.The 3-year survival rate was 64.86%(24/37)vs 43.33%(13/40)in the Chemo and the control group,with no statistically significant difference observed(P>0.05).The 3-year median survival in the Chemo group was 33.8 months,significantly longer than that in the control group at 28.6 months(P<0.05).ConclusionThe use of preoperative NACT chemotherapy in patients with advanced cervical cancer is effective in reducing lymphatic metastases,narrowing the lesion,and may prolong the long-term survival.
Neoadjuvant chemotherapy;paclitaxel;cisplatin;advanced cervical cancer;clinical effect;safety
R737.33
A
10.11877/j.issn.1672-1535.2016.14.03.14
2015-06-29)
(corresponding author),郵箱:yuanshangdu1008@126.com

