乙烯齊聚催化體系中的Friedel-Crafts烷基化反應(yīng)研究進(jìn)展
王俊,侯爽,宋磊,王斯晗,李翠勤
?
乙烯齊聚催化體系中的Friedel-Crafts烷基化反應(yīng)研究進(jìn)展
王俊1,侯爽1,宋磊2,王斯晗2,李翠勤1
(1東北石油大學(xué)化學(xué)化工學(xué)院,石油與天然氣化工省重點(diǎn)實(shí)驗(yàn)室,黑龍江大慶 163318;2中國(guó)石油化工研究院大慶化工中心,黑龍江大慶 163318)
采用過渡金屬配合物催化乙烯齊聚是制備-烯烴的一條重要工藝路線,部分催化體系已進(jìn)入了中試和工業(yè)化生產(chǎn)階段,但近年來的研究工作表明,一些過渡金屬催化劑在甲苯溶劑中的齊聚產(chǎn)物可直接與甲苯發(fā)生Friedel-Crafts烷基化反應(yīng),這將為烷基苯的生產(chǎn)開辟一條新的途徑。綜述了近年來乙烯齊聚過程中發(fā)生Friedel-Crafts烷基化反應(yīng)的研究進(jìn)展,詳細(xì)闡述了催化劑的結(jié)構(gòu)、催化體系、工藝條件等對(duì)烷基化反應(yīng)及烷基化產(chǎn)物分布的影響。同時(shí),給出了乙烯齊聚中Friedel-Crafts烷基化反應(yīng)的反應(yīng)過程,對(duì)設(shè)計(jì)可催化乙烯齊聚制備混合烷基苯的催化劑具有重要的意義。
催化;乙烯齊聚;催化劑;Friedel-Crafts烷基化;烷基苯;反應(yīng)
引 言
烷基苯是生產(chǎn)表面活性劑的重要中間體,工業(yè)上主要是采用苯與長(zhǎng)鏈烯烴為原料,在酸性催化劑存在的條件下進(jìn)行烷基化反應(yīng)來制備。早在1973年,Olechowski[1]在研究中發(fā)現(xiàn),乙烯與苯在催化劑MoCl5/EtAlCl2/ROH體系中可發(fā)生烷基化反應(yīng)得到乙苯,同時(shí)得到了乙烯二聚的烷基化產(chǎn)物丁苯及其異構(gòu)化產(chǎn)物。由這一研究發(fā)現(xiàn)可以判定,由乙烯和苯反應(yīng)生成丁苯的過程中發(fā)生了齊聚反應(yīng)和Friedel-Crafts烷基化反應(yīng)。
近年來,在乙烯齊聚制備-烯烴的過程中研究者意外發(fā)現(xiàn)了產(chǎn)物中存在烷基苯,烷基苯的生成符合Olechowski報(bào)道的串聯(lián)反應(yīng)機(jī)理。許多研究者通過改變催化劑結(jié)構(gòu)、改變助催化劑及各種反應(yīng)條件對(duì)這兩個(gè)串聯(lián)反應(yīng)進(jìn)行了深入的研究。本文根據(jù)文獻(xiàn),闡述了不同催化體系對(duì)乙烯齊聚與Friedel-Crafts烷基化反應(yīng)的影響,為實(shí)現(xiàn)乙烯齊聚制備烷基苯催化劑的設(shè)計(jì)提供參考。
1 吡唑基配體金屬配合物催化體系
目前研究的吡唑基配體金屬配合物主要包括含吡啶基吡唑類、含苯環(huán)吡唑類及氨基吡唑類,主要通過改變五元環(huán)上的取代基或是吡唑環(huán)之間的橋聯(lián)基來改變配體空間結(jié)構(gòu)、配位齒數(shù)來調(diào)變催化劑的性能。
2009年,Ojwach等[2]合成了吡唑-甲基吡啶鎳配合物催化劑1(圖1),在助催化劑二氯乙基鋁(EtAlCl2)活化下,以甲苯為溶劑,經(jīng)分析8種催化劑催化乙烯齊聚所得產(chǎn)物均全部為相應(yīng)的丁烯、己烯、辛烯的烷基化產(chǎn)物及其異構(gòu)化產(chǎn)物,對(duì)于烷基化異構(gòu)物可認(rèn)為是產(chǎn)物的鄰、間、對(duì)位烷基苯,也可能是預(yù)先生成的-烯烴經(jīng)異構(gòu)化得到的內(nèi)烯烴或是帶有取代基的烯烴與甲苯發(fā)生烷基化得到的。在產(chǎn)物中沒有檢測(cè)到乙基甲苯的存在,表明在烷基化之前乙烯首先發(fā)生齊聚反應(yīng)得到烯烴。另外,在該催化體系下催化劑結(jié)構(gòu)的變化對(duì)產(chǎn)物分布并沒有產(chǎn)生較大的影響,含三齒配體的1a~1d催化劑得到48%~53%稍高含量的丁基甲苯,而含雙齒配體的1e~1h催化劑中最終得到了41%~44%的丁基甲苯,對(duì)于這種細(xì)微的含量差別,可認(rèn)為是配位氮原子的供電子效應(yīng)影響了鎳活性中心的電子云密度,使得乙烯插入較為困難。不同于其他催化劑取代基的空間位阻效應(yīng)對(duì)乙烯齊聚產(chǎn)物分布產(chǎn)生的較大影響[3],催化劑1a~1h其吡唑環(huán)上取代基空間位阻雖也有不同,但因配體上所連的取代基與鎳活性中心相距較遠(yuǎn),位阻的變化并未對(duì)產(chǎn)物分布造成明顯影響。
針對(duì)催化劑1a體系,考察了反應(yīng)時(shí)間和壓力對(duì)烷基化產(chǎn)物分布的影響(表1),結(jié)果表明,產(chǎn)物中丁基甲苯與辛基甲苯的含量發(fā)生了明顯的變化,而己基甲苯的含量則基本不變。時(shí)間由15 min增加到180 min,辛基甲苯含量由11%增加到33%,這與Brookhart等[4]與Small等[5]的報(bào)道是一致的。隨時(shí)間增加烯烴有重新插入的趨勢(shì),因而會(huì)得到較高組分的高碳烯烴;乙烯壓力由1 MPa增加到4 MPa,辛基甲苯含量由11%增加到24%,盡管壓力的增加會(huì)使齊聚反應(yīng)更傾向于鏈終止[4,6],但在該催化過程中,乙烯的重新插入及其與低聚物的共聚反應(yīng)占據(jù)了催化過程的主導(dǎo)從而得到了較高含量的辛烯。將體系中的溶劑改為正己烷,同時(shí)減少甲苯的用量,所得產(chǎn)物以-烯烴為主,僅得到了少量的烷基苯,表明甲苯同時(shí)作為一種原料參與了烷基化反應(yīng)。
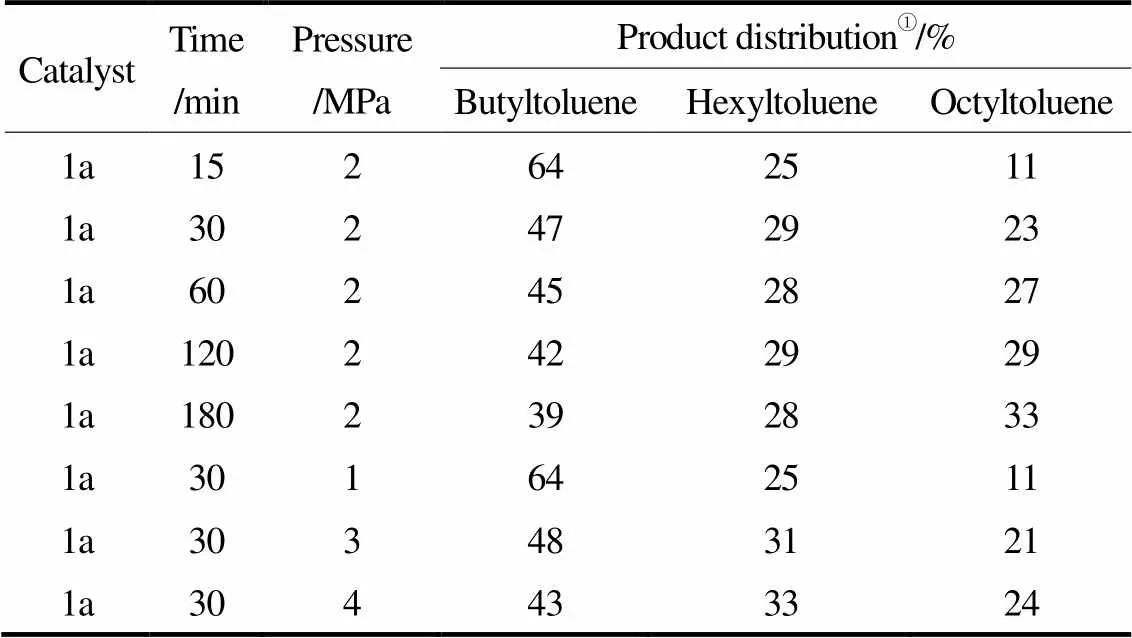
表1 反應(yīng)條件對(duì)乙烯齊聚的影響
① Determined by GC.
改變吡唑基配合物催化劑上的配位原子可很大程度上影響乙烯齊聚產(chǎn)物分布。2011年,Michael等[7]將羥基引入配體吡唑環(huán)上,合成了一種新型的N, O配位的吡唑基鎳配合物催化劑2(圖2),以EtAlCl2為助催化劑,甲苯為溶劑,催化劑2a所得產(chǎn)物為丁烯、己烯及少量烷基苯(表2)。在催化劑2a體系中,Al/Ni比及反應(yīng)時(shí)間是影響烷基苯含量的主要因素,較高的Al/Ni比傾向于得到更多的烷基苯,在Al/Ni比為1700時(shí),體系中的烷基苯含量最高可達(dá)到40%;延長(zhǎng)反應(yīng)時(shí)間也可增加該體系中的烷基苯含量,時(shí)間增加1.5 h,烷基苯含量可提高17%。而催化劑2b體系中的烯烴則全部轉(zhuǎn)化為烷基化物質(zhì),其中90%為丁基甲苯,表明催化劑2b可選擇性催化乙烯二聚。兩種催化體系中產(chǎn)物分布的顯著差異是由催化劑配體上取代基不同導(dǎo)致的,催化劑2a為典型的N, O配位螯合結(jié)構(gòu)[8],而OH 官能團(tuán)與EtAlCl2會(huì)發(fā)生鍵合,減弱了EtAlCl2對(duì)Friedel-Crafts烷基化反應(yīng)的催化作用,最大程度地降低了甲苯溶劑與齊聚產(chǎn)物的烷基化反應(yīng),因而得到了更多的齊聚產(chǎn)物。
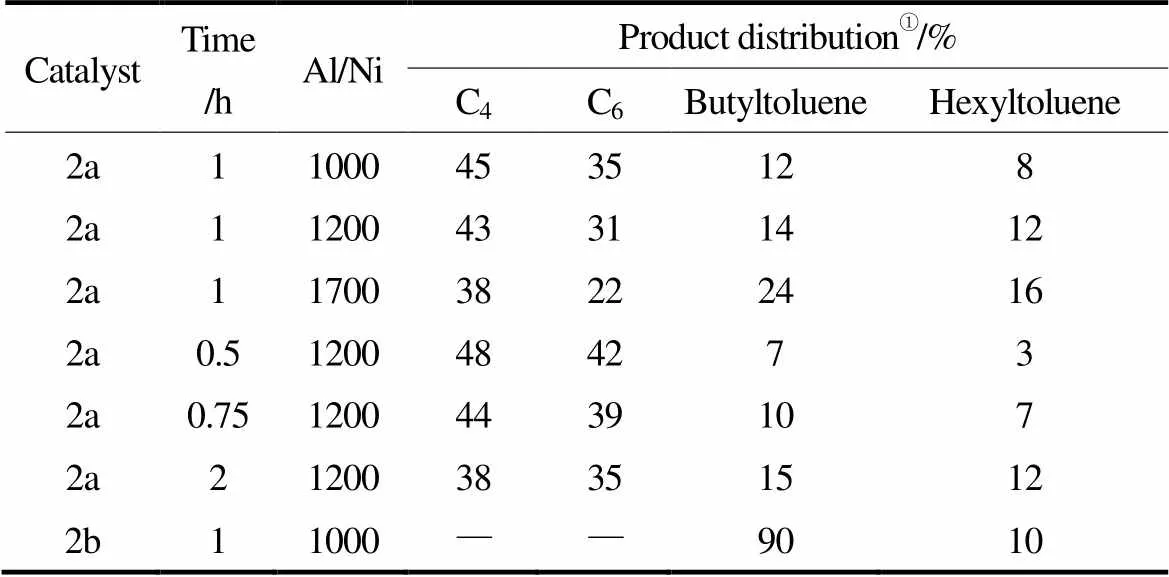
表2 催化劑2a和2b的齊聚產(chǎn)物分布
① Determined by GC.
對(duì)于含N, O配位的催化劑,其催化乙烯齊聚所得產(chǎn)物以烯烴為主,而以吡唑環(huán)上的氮原子配位的催化劑催化乙烯齊聚時(shí)則對(duì)烷基苯有著較高的選擇性。2013年,Budhai等[9]在吡唑-苯鎳配合物催化劑3(圖3)催化體系中提出了乙烯齊聚與甲苯Friedel-Crafts烷基化的串聯(lián)反應(yīng),結(jié)果得到了7種含不同取代基的烷基苯混合物及少量的烯烴,其中烷基化產(chǎn)物主要是單取代、雙取代、三取代丁基甲苯及少量的乙基甲苯(表3),而乙基甲苯的出現(xiàn)則表明了在該催化體系中乙烯齊聚與烷基化反應(yīng)存在一種競(jìng)爭(zhēng)關(guān)系,但4種催化劑催化乙烯齊聚最終均只得到了少量的乙基甲苯,說明乙烯發(fā)生齊聚的速度要大于其與甲苯烷基化的反應(yīng)速度。對(duì)比4種不同催化劑,在催化劑3b和3c體系中,產(chǎn)物中烷基化程度很完全,而在催化劑3a和3d體系中,烷基化程度為79.75%,產(chǎn)物中還存在一定量的烯烴。
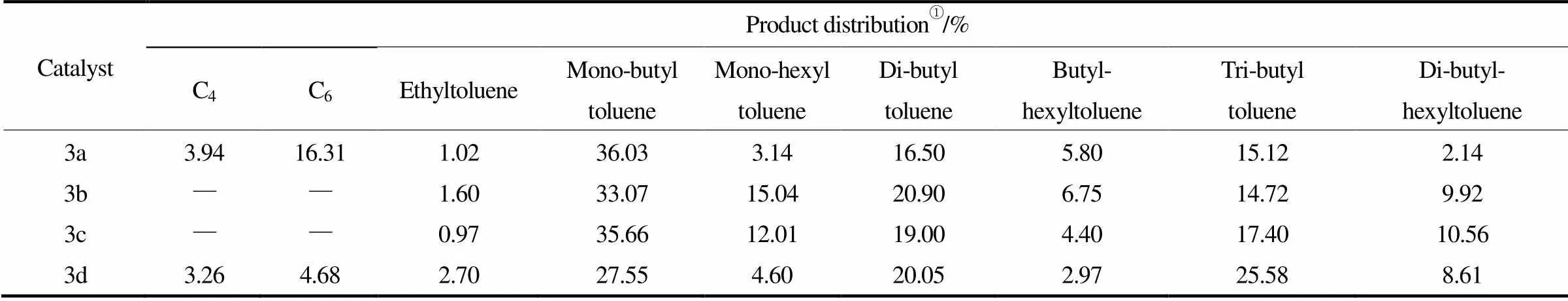
表3 催化劑3a~3d的乙烯齊聚/Friedel-Crafts烷基化產(chǎn)物分布
① Determined by GC.
在催化劑3a體系中考察了不同反應(yīng)條件對(duì)產(chǎn)物烷基化程度的影響(表4),Al/Ni比、反應(yīng)時(shí)間及反應(yīng)壓力對(duì)產(chǎn)物烷基化程度均有不同程度的影響,其中以Al/Ni比的影響最為突出。隨著Al/Ni比的增加,產(chǎn)物烷基化程度先增大再減小,當(dāng)Al/Ni比為350時(shí),產(chǎn)物均為烷基苯。較高的Al/Ni比可為體系提供更多的活性中心來催化甲苯的烷基化反應(yīng),在Braunstein等[10-17]的報(bào)道中,使用較低Al/Ni比,避免了助催化劑EtAlCl2的過量,則沒有發(fā)生烷基化反應(yīng)。反應(yīng)時(shí)間及反應(yīng)壓力對(duì)烷基化程度的影響則是相反的,增加時(shí)間,產(chǎn)物烷基化程度由57.58%增加到85.55%;增加反應(yīng)壓力,產(chǎn)物烷基化程度會(huì)由70.49%降低到57.93%。
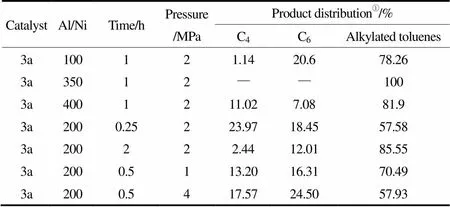
表4 不同反應(yīng)條件對(duì)產(chǎn)物分布的影響
① Determined by GC.
2014年,Obuah等[18]合成了吡唑基胺類鎳配合物催化劑4(圖4),以EtAlCl2為助催化劑,甲苯為溶劑,4種催化劑均可催化乙烯齊聚得到丁烯、己烯和烷基苯產(chǎn)物。經(jīng)分析,所有的烷基化產(chǎn)物均為丁基甲苯,其中二丁基甲苯存在異構(gòu)化產(chǎn)物,在苯環(huán)的鄰對(duì)位上丁基出現(xiàn)支化現(xiàn)象,而三丁基甲苯則不存在異構(gòu)化產(chǎn)物。在該體系中,時(shí)間對(duì)產(chǎn)物分布有一定的影響,如在催化劑4b體系中,反應(yīng)時(shí)間增加1.5 h,混合物中烷基苯組分的含量增加11%(表5),這表明隨時(shí)間增加,丁烯含量增加進(jìn)而得到了更多的丁基甲苯。不同溶劑得到的產(chǎn)物也有很大的差別,在催化劑4b和4c體系中,當(dāng)用氯苯作為溶劑時(shí),所得產(chǎn)物為丁烯、己烯及支化聚乙烯,并沒有烷基苯生成,這可能是因?yàn)槁缺街械穆仍訛閺?qiáng)吸電子基,其誘導(dǎo)效應(yīng)使得苯環(huán)電子云密度降低,使其鈍化很難進(jìn)行親電取代反應(yīng)。因此,若想在產(chǎn)物中得到烷基苯,在選擇溶劑時(shí)需考慮苯環(huán)上取代基的電子效應(yīng)。
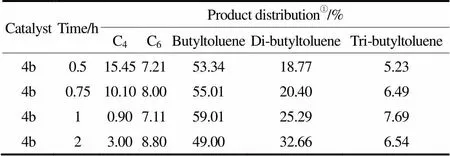
表5 催化劑4b催化乙烯齊聚和Friedel-Crafts烷基化產(chǎn)物分布
① Determined by GC.
2014年,Nyamato等[19]合成了具有不對(duì)稱結(jié)構(gòu)的含吡唑基吡啶金屬配合物催化劑5(圖5)。在此催化體系中,EtAlCl2為助催化劑,甲苯為溶劑,乙烯同時(shí)進(jìn)行了齊聚反應(yīng)和烷基化反應(yīng),主產(chǎn)物為乙烯及乙烯齊聚所得烯烴與甲苯的烷基化產(chǎn)物(表6)。5d及5f催化劑對(duì)乙烯與甲苯的烷基化反應(yīng)有著非常高的選擇性,如5d催化體系得到了83%的乙烯-甲苯,表明乙烯與甲苯的烷基化反應(yīng)要優(yōu)先于乙烯齊聚反應(yīng),這可能是因?yàn)镕eCl3本身就是一個(gè)良好的烷基化反應(yīng)催化劑,可直接催化乙烯與甲苯發(fā)生烷基化反應(yīng)[20]。反應(yīng)時(shí)間及反應(yīng)壓力對(duì)產(chǎn)物分布有著很大的影響,在短時(shí)間內(nèi)可以得到較多的乙基甲苯和丁基甲苯,增加反應(yīng)時(shí)間則會(huì)得到更多的己基甲苯和二取代丁基甲苯;另外增加乙烯壓力也會(huì)導(dǎo)致丁基甲苯含量的增加。
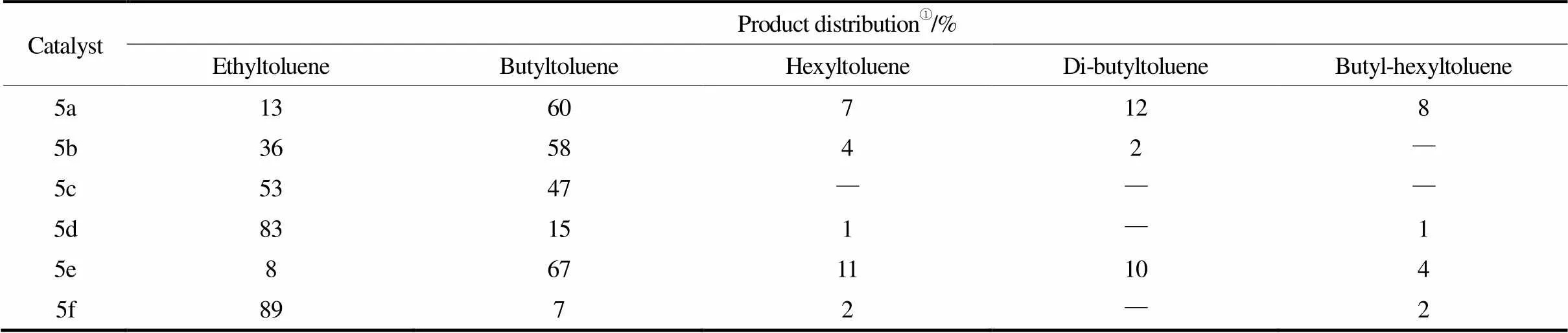
表6 二氯乙基鋁為助催化劑甲苯中催化劑5a~5f的乙烯齊聚產(chǎn)物分布
① Determined by GC.
大量研究表明,在以EtAlCl2為助催化劑時(shí),有利于烷基苯的生成,而對(duì)采用其他助催化劑也有一些報(bào)道。2015年,Nyamato等[21]在前期工作的基礎(chǔ)上合成了一種新的吡唑基吡啶類鎳配合物催化劑6(圖6),以甲基鋁氧烷(MAO)為助催化劑,在甲苯為溶劑的條件下,得到的產(chǎn)物以丁烯為主,同時(shí)含少量的己烯和辛烯,并伴有2%左右的二乙基甲苯(表7)。對(duì)催化劑6b體系,改用EtAlCl2為助催化劑,產(chǎn)物分布發(fā)生了很大的改變,其中46%為烷基苯。然而,不同于其之前的報(bào)道[19],本次所合成的催化劑6b催化乙烯齊聚僅有部分烯烴發(fā)生了烷基化反應(yīng),而在催化劑5體系中則發(fā)生了徹底的烷基化反應(yīng),這可能與吡啶環(huán)上取代基的不同以及其與吡唑環(huán)間橋聯(lián)基的不同有關(guān),即催化劑的結(jié)構(gòu)影響了烷基化程度。在催化劑5體系中,以MAO為助催化劑時(shí),6種催化劑催化乙烯齊聚最終均得到了丁烯作為主產(chǎn)物以及己烯和辛烯并伴隨很少量的二乙基甲苯。通過對(duì)兩種催化體系的分析,EtAlCl2和MAO分別作為助催化劑時(shí),EtAlCl2具有更高的Lewis酸強(qiáng)度,可以使乙烯齊聚反應(yīng)中發(fā)生更加徹底的Friedel-Crafts烷基化反應(yīng)。
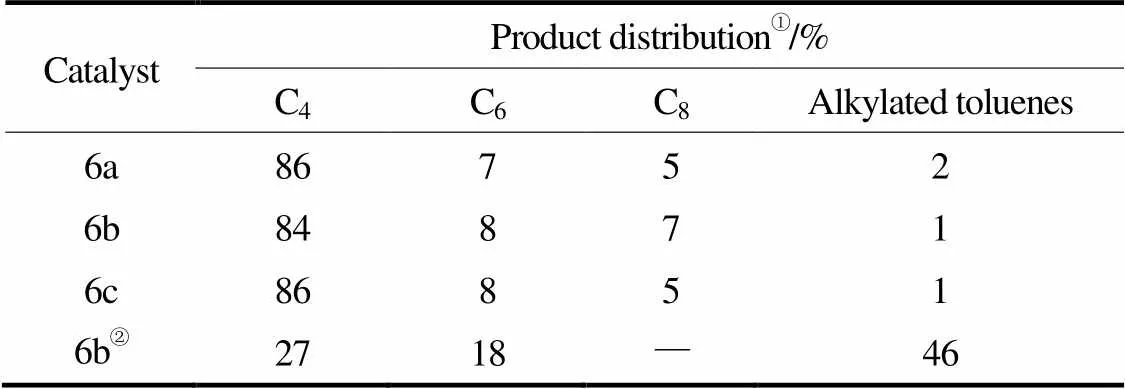
表7 甲基鋁氧烷為助催化劑甲苯中催化劑6a~6c的乙烯齊聚產(chǎn)物分布
① Determined by GC; ② Cocatalyst: EtAlCl2.
在吡唑基金屬配合物催化體系中,使用EtAlCl2為助催化劑,所有催化劑催化乙烯齊聚均可得到不同含量的烷基苯,并且吡唑環(huán)上帶有甲基吡啶基團(tuán)及苯環(huán)類的催化劑更容易得到較高含量的烷基苯。在這一過程中,反應(yīng)時(shí)間及乙烯壓力均對(duì)產(chǎn)物分布有著不同程度的影響,可通過控制反應(yīng)條件來調(diào)控產(chǎn)物中烯烴與烷基苯的相對(duì)含量。
事實(shí)上,也有很多文獻(xiàn)報(bào)道在甲苯溶劑中使用EtAlCl2作為助催化劑時(shí)只產(chǎn)生丁烯、己烯和辛烯等烯烴產(chǎn)物[22-25]。然而,在這些沒有產(chǎn)生烷基化產(chǎn)物的文獻(xiàn)報(bào)道中,一般采用了較低的Al/Ni比,避免了助催化劑的過量來催化甲苯的烷基化。如Braunstein等[22]在吡啶-三唑類鎳配合物催化劑催化乙烯齊聚反應(yīng)中使用的Al/Ni比為10和20,結(jié)果并沒有得到甲苯的烷基化產(chǎn)物,因此,高的Al/Ni比也是導(dǎo)致發(fā)生甲苯烷基化的原因。在一些非吡唑基的過渡金屬配合物催化體系中[26-27],相同實(shí)驗(yàn)條件下并沒有發(fā)生烷基化反應(yīng),表明催化劑的結(jié)構(gòu)對(duì)于乙烯齊聚過程中烷基化反應(yīng)的發(fā)生具有一定的影響。
2 金屬樹枝狀配合物催化體系
將金屬催化活性中心嵌入樹枝狀大分子的骨架中得到的催化劑稱為金屬樹枝狀催化劑,由于樹枝狀大分子的特殊結(jié)構(gòu),金屬催化活性中心可在樹枝狀大分子的端基、分枝點(diǎn)或是核心。將催化劑樹枝化的一個(gè)明顯優(yōu)勢(shì)是其可在一個(gè)體系中結(jié)合均相與非均相催化劑的優(yōu)點(diǎn),催化效率高并且易于從反應(yīng)體系中分離出來。樹枝狀催化劑的研究幾乎涉及到所有的有機(jī)合成反應(yīng)[28-29],同樣包括乙烯齊聚制備-烯烴的反應(yīng)。在乙烯齊聚過程中同時(shí)能夠得到烷基苯的樹枝狀催化劑主要包括樹枝狀水楊醛亞胺類金屬催化劑以及吡啶亞胺類金屬催化劑。
Malgas等[30-31]將一種以聚丙烯亞胺樹枝狀大分子為骨架的多核金屬配合物催化劑應(yīng)用于降冰片烯的聚合反應(yīng)并得到了較高的催化活性。2013年,Malgas等[32]又用這種聚丙烯亞胺樹枝狀大分子合成了1.0代、2.0代和3.0代的樹枝狀水楊醛亞胺鎳系催化劑及吡啶亞胺鎳系催化劑,圖7為1.0代樹枝狀類鎳系催化劑。以EtAlCl2為助催化劑,甲苯為溶劑,評(píng)價(jià)了這幾種催化劑在乙烯齊聚反應(yīng)中的性能。經(jīng)分析,產(chǎn)物中既存在烯烴齊聚物也含有大量的烷基苯。在樹枝狀水楊醛亞胺鎳配合物催化體系中,產(chǎn)物中均得到了大量的烷基苯,如3.0代催化劑的產(chǎn)物中得到了46%的丁基甲苯和3.5%的己基甲苯,從1.0代到3.0代催化劑,其烷基化產(chǎn)物含量由31.6%增加到49.5%。而在樹枝狀吡啶亞胺鎳配合物催化體系中,產(chǎn)物烷基化程度較低,如在2.0代催化體系中僅得到了17.3%的丁基甲苯,大部分產(chǎn)物為長(zhǎng)碳鏈的齊聚物,從1.0代到3.0代催化劑,產(chǎn)物烷基苯含量由18.05%增加到21.5%。由此可推斷產(chǎn)物烷基化程度可能與催化劑的代數(shù)有關(guān),高代數(shù)的催化劑體系中更易于發(fā)生烷基化反應(yīng),這可能是因?yàn)檫^渡金屬在烷基化的過程中起到了促進(jìn)的作用。并且根據(jù)比較分析可知樹枝狀水楊醛亞胺類鎳催化劑比吡啶亞胺類鎳催化劑更易于使乙烯齊聚過程中發(fā)生烷基化反應(yīng)。
考察了3.0代樹枝狀水楊醛亞胺鎳催化劑在不同Al/Ni比下產(chǎn)物的選擇性(表8),在Al/Ni比為1000時(shí),得到了10.1%的丁烯,增加Al/Ni比,烷基化程度增大。產(chǎn)物中多為丁烯和己烯與甲苯的單烷基化產(chǎn)物,含量可達(dá)60%,在Al/Ni比達(dá)到7000時(shí)產(chǎn)物中會(huì)出現(xiàn)11%的二丁基甲苯。相同條件下的空白實(shí)驗(yàn)表明,僅使用EtAlCl2作為催化劑,結(jié)果不會(huì)得到任何產(chǎn)物。表明在該催化體系下,如不加入樹枝狀催化劑,乙烯既不會(huì)發(fā)生齊聚反應(yīng)也不會(huì)與甲苯發(fā)生烷基化反應(yīng),同時(shí)也說明了烷基化反應(yīng)發(fā)生在烯烴的形成之后,因此,這兩種反應(yīng)過程是串聯(lián)進(jìn)行的。
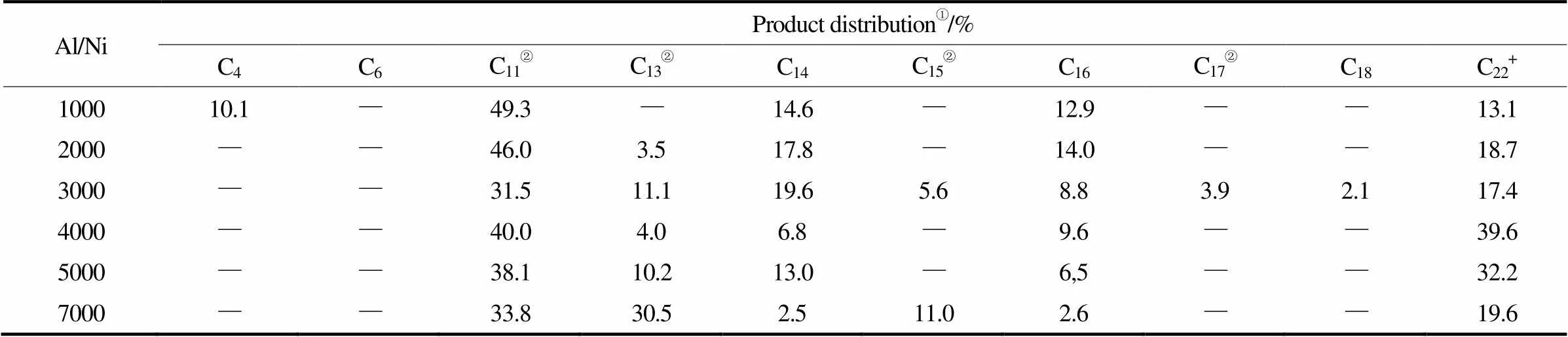
表8 不同Al/Ni比下的產(chǎn)物分布
① Determined by GC. ② Friedel-Crafts alkylation products.
在此金屬樹枝狀催化體系中,Malgas[33]推斷了串聯(lián)體系中Frieded-Crafts烷基化反應(yīng)的可能機(jī)理(圖8),例如在乙烯齊聚形成1-丁烯后,丁烯上的雙鍵會(huì)去進(jìn)攻EtAlCl2從而形成一個(gè)仲碳正離子,它作為親核試劑向苯環(huán)進(jìn)攻,形成新的碳正離子,然后失去一個(gè)質(zhì)子生成烷基苯,并釋放了EtAlCl2。
王海琛[34]合成了同樣的1.0代樹枝狀水楊醛亞胺鎳系催化劑并應(yīng)用于乙烯齊聚反應(yīng)的研究,產(chǎn)物中僅得到了少量的丁烯、己烯、辛烯等烯烴,大部分為其與甲苯反應(yīng)生成的烷基化產(chǎn)物,反應(yīng)過程如圖9所示。考察了反應(yīng)條件對(duì)產(chǎn)物碳數(shù)分布的影響:增加Al/Ni比,產(chǎn)物向高碳數(shù)移動(dòng),其多為C15和C17;升高溫度產(chǎn)物向低碳移動(dòng),增加了丁烯的含量即增加了丁基甲苯的含量;隨著反應(yīng)時(shí)間的增加,烯烴產(chǎn)物向高碳數(shù)移動(dòng),因此烷基化產(chǎn)物也向高碳數(shù)移動(dòng);聚合壓力的增加也使產(chǎn)物傾向于高碳烷基化物質(zhì)的生成。
在金屬樹枝狀配合物催化體系中,乙烯齊聚速度要大于烷基化反應(yīng)速度,因而產(chǎn)物為烯烴與烷基苯的混合物。此類催化體系的報(bào)道很少,但就現(xiàn)有的工作基礎(chǔ)可以推測(cè)[32-33],樹枝狀大分子的代數(shù)對(duì)于烷基化反應(yīng)的程度有很大的影響,代數(shù)越高所含過渡金屬越多,而相應(yīng)的烷基化程度可能越高。因此,如果想靈活控制產(chǎn)物中烷基苯的含量,在設(shè)計(jì)此類樹枝狀催化劑時(shí)需考慮其代數(shù)的影響。
3 其他催化體系
近些年,在不斷開發(fā)新的乙烯齊聚催化劑的過程中,仍有許多研究者發(fā)現(xiàn)在乙烯齊聚體系中會(huì)發(fā)生Friedel-Crafts烷基化反應(yīng)。
在發(fā)現(xiàn)的烷基化體系中,催化劑多為N, N配位,2008年,Dyer等[35]設(shè)計(jì)合成了一種N, P配位的鎳系催化劑8(圖10),以EtAlCl2為助催化劑,甲苯為溶劑,結(jié)果表明,催化劑8b~8d催化乙烯齊聚最終得到C4、C6、C8以及它們的異構(gòu)物,而在相同條件下,催化劑8a得到了完全不同的產(chǎn)物,只有1%左右的烯烴,主要是C4、C6、C8和C10等烯烴與甲苯的烷基化產(chǎn)物(表9)。在催化劑8a體系下,改用二氯甲烷或是氯苯作為溶劑,產(chǎn)物中僅有少量的丁烯和己烯,但是如果在二氯甲烷中加入一定量的甲苯則會(huì)導(dǎo)致產(chǎn)物的完全烷基化。相同催化體系,以苯為溶劑,得到的主產(chǎn)物為二乙基苯與丁苯,對(duì)于異構(gòu)化產(chǎn)物的出現(xiàn)可認(rèn)為是由碳正離子重排形成的。為了說明烷基苯中乙基甲苯的出現(xiàn),在催化劑8a體系中分別使用甲苯和苯作為溶劑,二氯甲基鋁(MeAlCl2)為助催化劑,得到的產(chǎn)物與使用EtAlCl2作為助催化劑時(shí)是相同的,因此,排除了產(chǎn)物由烷基鋁直接烷基化得到的可能。主要原因可能是在催化反應(yīng)開始時(shí)催化活性較高生成了大量的短鏈烯烴,隨后催化活性中心逐漸失活,這些不飽和烯烴與甲苯發(fā)生了烷基化反應(yīng)。

表9 催化劑8a體系下乙烯與甲苯反應(yīng)中的Friedel-Crafts烷基化產(chǎn)物分布
①Determined by GC.
秦一超等[36]合成了一系列具有Zr(OAr)Cl4-n·ArOH(=1~4,=0~7)結(jié)構(gòu)的芳香基鋯系催化劑9(圖11),這類催化劑可催化乙烯齊聚與Friedel-Crafts烷基化的串聯(lián)反應(yīng)。在該體系中,乙烯壓力是影響產(chǎn)物分布的重要因素。在常壓條件下(0.1 MPa),催化劑9a體系中,以甲苯為溶劑、EtAlCl2為助催化劑,所得產(chǎn)物全部為C4~C18的-烯烴。當(dāng)壓力增加到0.2 MPa時(shí),產(chǎn)物中出現(xiàn)大量烷基苯,-烯烴含量降低到13.1%,并且隨著壓力的增加,烷基化程度升高,其中甲苯的一取代物含量降低,雙取代和三取代物逐漸增加(表10)。
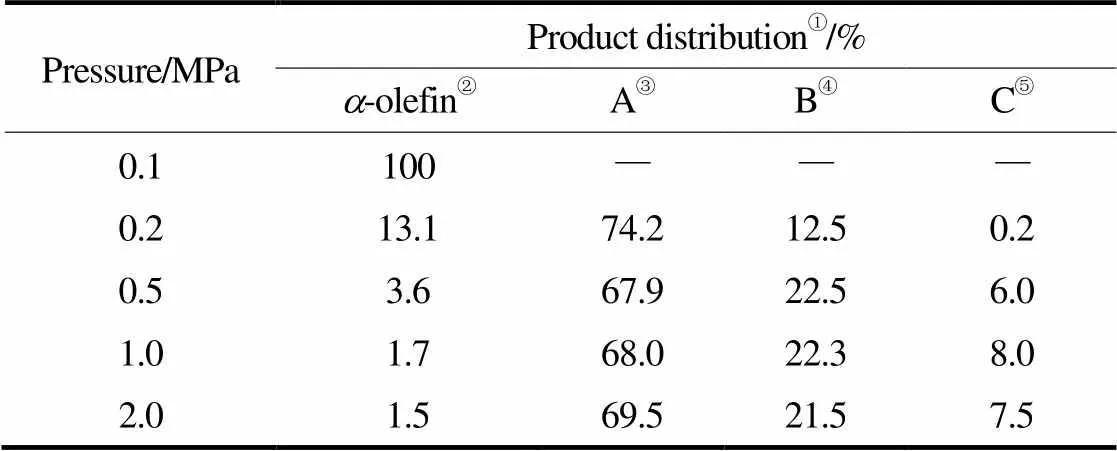
表10 不同壓力下產(chǎn)物的分布
① Determined by GC. ② C4—C18. ③ Mono-substituted alkylation of toluene. ④ Bis-substituted alkylation of toluene. ⑤ Tri-substituted alkylation of toluene.
在該催化體系中,催化劑的結(jié)構(gòu)也是影響烷基化反應(yīng)的一個(gè)重要因素,主要表現(xiàn)為酚取代基的電子效應(yīng)。在常壓下對(duì)不同催化劑進(jìn)行了對(duì)比實(shí)驗(yàn)(表11),催化劑9a在常壓下發(fā)生了穩(wěn)定的齊聚反應(yīng);催化劑9b與9d均含有吸電子基團(tuán),產(chǎn)物中90%以上為烷基苯,烷基化程度較高;而催化劑9c與9e均含有推電子基團(tuán),產(chǎn)物中存在30%~40%的-烯烴,其烷基化程度較低。
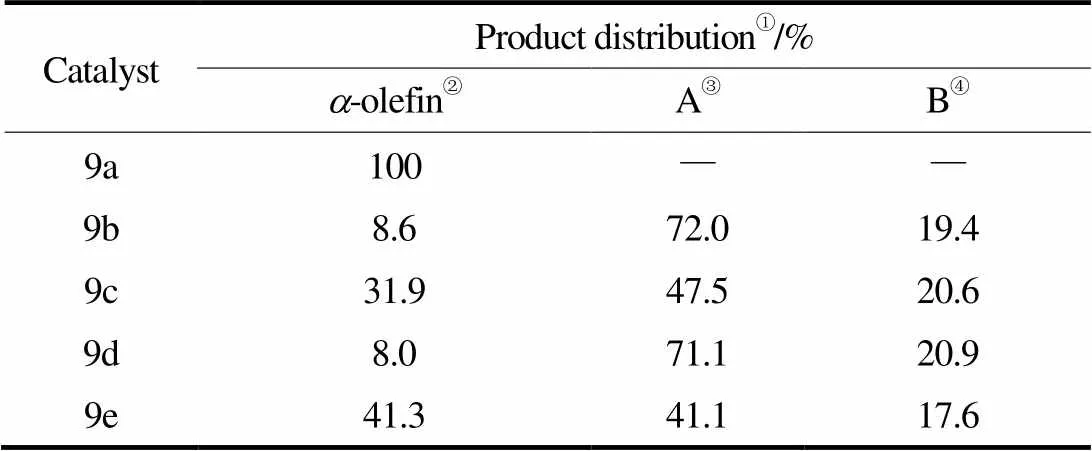
表11 常壓下不同催化劑的產(chǎn)物分布
① Determined by GC. ② C4—C22. ③ Mono-substituted alkylation of toluene. ④ Bis-substituted alkylation of toluene.
2010年,Zaidman等[37]合成了一種甲臜為配體的鎳配合物催化劑,可催化乙烯齊聚生成丁烯和己烯。在此工作基礎(chǔ)上,Zaidman等[38]又合成了一種以甲瓚衍生物為配體的鎳系催化劑10(圖12),當(dāng)以EtAlCl2為助催化劑、甲苯為溶劑時(shí),得到烯烴與烷基苯的混合物。在單核催化劑10a催化體系中,烷基化程度較高,產(chǎn)物中含96%的烷基苯;而在雙核催化劑10b催化體系中,烷基苯的含量降為69%,由此可推斷催化劑活性中心的增加可增加目標(biāo)產(chǎn)物烯烴的產(chǎn)率。2013年,Pavlova等[39]研究了類似的甲臜為配體的鐵系配合物催化劑催化乙烯齊聚的性能,結(jié)果表明,以MAO為助催化劑時(shí)主要促進(jìn)-烯烴的生成,而以EtAlCl2為助催化劑時(shí)則增加了體系對(duì)烷基苯產(chǎn)物的選擇性。
乙烯齊聚過程中Friedel-Crafts烷基化反應(yīng)的發(fā)生與助催化劑的選擇密不可分,在多數(shù)催化體系中,均是使用了EtAlCl2作為助催化劑,而在Song等[40]合成的雙膦氨基鎳系催化劑11(圖13)體系中,以MAO為助催化劑,5種催化劑均表現(xiàn)出了良好的乙烯齊聚活性。在低溫條件下可得到丁烯與己烯,但當(dāng)體系反應(yīng)溫度達(dá)到50℃時(shí),產(chǎn)物主要為烷基苯混合物。烷基化產(chǎn)物由乙烯及其齊聚物與溶劑甲苯的烷基化反應(yīng)[41-43]所得。推測(cè)可能是由于溫度的升高導(dǎo)致了催化活性中心較快地分解進(jìn)而形成了一種新的強(qiáng)Lewis酸使得乙烯或烯烴產(chǎn)物發(fā)生了質(zhì)子化,碳正離子再與甲苯發(fā)生烷基化反應(yīng)。
為了進(jìn)一步研究該體系的烷基化反應(yīng),分別單獨(dú)使用催化劑10a、10d、MAO、AlCl3和NiBr2/MAO在相同條件下進(jìn)行實(shí)驗(yàn)并將結(jié)果與催化體系10a/MAO和10d/MAO所得結(jié)果對(duì)比(表12)。結(jié)果表明,當(dāng)單獨(dú)使用MAO或是催化劑10a時(shí),既沒有發(fā)生乙烯齊聚反應(yīng)也沒有發(fā)生烷基化反應(yīng);在催化體系10d中,最終只得到了2.7%的三取代乙基甲苯。當(dāng)體系僅存在AlCl3時(shí),反應(yīng)得到86.3%的乙基甲苯和11.0%的二乙基甲苯,這可能是因?yàn)锳lCl3作為一種典型的Lewis酸,催化了乙烯與甲苯的烷基化反應(yīng)[44-45]。另外,在NiBr2/MAO體系中既沒有乙烯的消耗也沒有烷基化的發(fā)生,說明了配體對(duì)于發(fā)生烷基化反應(yīng)有重要的影響。

表12 甲苯中烷基化反應(yīng)數(shù)據(jù)
① Determined by GC.
4 結(jié) 語
直到現(xiàn)在,有關(guān)乙烯齊聚體系中發(fā)生甲苯的Friedel-Crafts烷基化反應(yīng)活性中心形成機(jī)理的報(bào)道并不多見,但是這一意外發(fā)現(xiàn)在乙烯齊聚領(lǐng)域仍然是一個(gè)很大的突破,吸引著研究人員不斷地研究與探索。從目前的文獻(xiàn)報(bào)道來看,含吡唑基配體的金屬配合物催化劑對(duì)乙烯齊聚過程中Friedel-Crafts烷基化反應(yīng)有很好的選擇性,通過調(diào)整催化劑配體的結(jié)構(gòu)及控制不同反應(yīng)條件可將產(chǎn)物烯烴全部轉(zhuǎn)變?yōu)橄鄳?yīng)的烷基苯,對(duì)混合烷基苯的制備有很好的應(yīng)用前景,但所得烷基苯烷基鏈較短。相較于吡唑基金屬催化體系,金屬樹枝狀催化劑催化乙烯齊聚所得產(chǎn)物分布較寬,它的代數(shù)以及外圍取代基的空間位阻效應(yīng)對(duì)于烷基化反應(yīng)的程度有很大的影響,且甲苯上可接入較長(zhǎng)碳鏈的烯烴,所得長(zhǎng)鏈烷基苯應(yīng)用較為廣泛,但卻不能控制體系中發(fā)生完全的烷基化。由于催化體系的不同,對(duì)于催化Friedel-Crafts烷基化反應(yīng)的活性中心尚不明確,這也有待研究者們進(jìn)一步的探索,最終實(shí)現(xiàn)對(duì)烷基化產(chǎn)物分布的控制。
References
[1] Olechowski J. Alkylation process: US 3720725[P]. 1973-3-13.
[2] Ojwach S O, Guzei I A, Benade L L,. (Pyrazol-1-ylmethyl)pyridine nickel complexes: ethylene oligomerization and unusual Friedel-Crafts alkylation catalysts[J]. Organometallics, 2009, 28(7): 2127-2133.
[3] Zhang Y, Cao Y, Leng X,. Cationic palladium (Ⅱ) complexes of phosphine-sulfonamide ligands: synthesis, characterization, and catalytic ethylene oligomerization[J]. Organometallics, 2014, 33(14): 3738-3745.
[4] Doherty M D, Trudeau S, White P S,. Ethylene oligomerization catalyzed by a unique phosphine-oxazoline palladium (Ⅱ) complex. Propagation and chain transfer mechanisms[J]. Organometallics, 2007, 26(5): 1261-1269.
[5] Small B L, Rios R, Fernandez E R,. Oligomerization of ethylene using new iron catalysts bearing pendant donor modified-diimine ligands[J]. Organometallics, 2007, 26(7): 1744-1749.
[6] Ittel S D, Johnson L K, Brookhart M. Late-metal catalysts for ethylene homo- and copolymerization[J]. Chemical Reviews, 2000, 100(4): 1169-1204.
[7] Ainooson M K, Ojwach S O, Guzei I A,. Pyrazolyl iron, cobalt, nickel, and palladium complexes: synthesis, molecular structures, and evaluation as ethylene oligomerization catalysts[J]. Journal of Organometallic Chemistry, 2011, 696(8): 1528-1535.
[8] Keim W, Hoffmann B, Lodewick R,. Linear oligomerization of olefinsnickel chelate complexes and mechanistic considerations based on semi-empirical calculations[J]. Journal of Molecular Catalysis, 1979, 6(2): 79-97.
[9] Budhai A, Omondi B, Ojwach S O,. Tandem ethylene oligomerisation and Friedel-Crafts alkylation of toluene catalysed by bis-(3,5-dimethylpyrazol-1-ylmethyl) benzene nickel(Ⅱ) complexes and ethylaluminium dichloride[J]. Catalysis Science &Technology, 2013, 3(12): 3130-3135.
[10] Kermagoret A, Braunstein P. Mono- and dinuclear nickel complexes with phosphino-, phosphinito-, and phosphonitopyridine ligands: synthesis, structures, and catalytic oligomerization of ethylene[J]. Organometallics, 2007, 27(1): 88-99.
[11] Kermagoret A, Tomicki F, Braunstein P. Nickel and iron complexes with N, P, N-type ligands: synthesis, structure and catalytic oligomerization of ethylene[J]. Dalton Transactions, 2008, 252(22): 2945-2955.
[12] Speiser F, Braunstein P, Saussine L. Nickel and iron complexes with oxazoline- or pyridine-phosphonite ligands; synthesis, structure and application for the catalytic oligomerisation of ethylene[J]. Dalton Transactions, 2004, 10(10): 1539-1545.
[13] Kermagoret A, Braunstein P. Contrasting bonding modes of a tridentate bis(oxazoline)phosphine ligand in cobalt and ironpalladium complexes: unprecedented N, N-coordination for a N, P, N ligand[J]. Dalton Transactions, 2008, 2008(5): 585-587.
[14] Speiser F, Braunstein P, Saussine L. New nickel ethylene oligomerization catalysts bearing bidentate P, N-phosphinopyridine ligands with different substituents α to phosphorus[J]. Organometallics, 2004, 23(11): 2625-2632.
[15] Speiser F, Braunstein P, Saussine L. Nickel complexes bearing new P, N-phosphinopyridine ligands for the catalytic oligomerization of ethylene[J]. Organometallics, 2004, 23(11): 2633-2640.
[16] Speiser F, Braunstein P, Saussine L. Nickel complexes bearing new P, N-phosphinopyridine ligands for the catalytic oligomerization of ethylene [J]. Accounts of Chemical Research, 2005, 38(10): 784-793.
[17] Speiser F, Braunstein P, Saussine L,. Nickel complexes with oxazoline-based P, N-chelate ligands: synthesis, structures, and catalytic ethylene oligomerization behavior[J]. Organometallics, 2004, 23(11): 2613-2624.
[18] Obuah C, Omondi B, Nozaki K,Solvent and co-catalyst dependent pyrazolylpyridinamine and pyrazolylpyrroleamine nickel(Ⅱ) catalyzed oligomerization and polymerization of ethylene[J]. Journal of Molecular Catalysis A Chemical, 2014, 382(382): 31-40.
[19] Nyamato G S, Ojwach S O, Akerman M P,Unsymmetrical (pyrazolylmethyl)pyridine metal complexes as catalysts for ethylene oligomerization reactions: role of solvent and co-catalyst in product distribution[J]. Journal of Molecular Catalysis A Chemical, 2014, 394(10): 274-282.
[20] Rueping M, Nachtsheim B J. A review of new developments in the Friedel-Crafts alkylation—from green chemistry to asymmetric catalysis[J]. Beilstein Journal of Organic Chemistry, 2010, 6(4): 1007-1013.
[21] Nyamato G S, Alam M, Ojwach S O,. Nickel (Ⅱ) complexes bearing pyrazolylpyridines: synthesis, structures and ethylene oligomerization reactions[J]. Applied Organometallic Chemistry, 2016, 30(2): 89-94.
[22] Schweinfurth D, Su C Y, Wei S C,Nickel complexes with “click”-derived pyridyl-triazole ligands: weak intermolecular interactions and catalytic ethylene oligomerisation[J]. Dalton Transactions, 2012, 41(41): 12984-12990.
[23] Boudier A, Breuil P A R, Magna L,. Ethylene oligomerization using iron complexes: beyond the discovery of bis(imino) pyridine ligands[J]. Chemical Communications, 2014, 50(12): 1398-1407.
[24] He F, Hao X, Cao X,. Nickel halide complexes bearing 2-benzimidazolyl--arylquinoline-8-carboxamide derived ligands: synthesis, characterization and catalytic behavior towards ethylene oligomerization and the vinyl polymerization of norbornene[J]. Journal of Organometallic Chemistry, 2012, 712(5): 46-51.
[25] Boudier A, Breuil P A R, Magna L,. Nickel(Ⅱ) complexes with imino-imidazole chelating ligands bearing pendant donor groups (SR, OR, NR2, PR2) as precatalysts in ethylene oligomerization[J]. Journal of Organometallic Chemistry, 2012, 718: 31-37.
[26] Chandran D, Lee K M, Chang H C,. Ni(Ⅱ) complexes with ligands derived from phenylpyridine, active for selective dimerization and trimerization of ethylene[J]. Journal of Organometallic Chemistry, 2012, 718(718): 8-13.
[27] Ma J, Feng C, Wang S,. Bi- and tri-dentate imino-based iron and cobalt pre-catalysts for ethylene oligo-/polymerization[J]. Inorganic Chemistry Frontiers, 2014, 1(1): 14-34.
[28] Astruc D, Chardac F. Dendritic catalysts and dendrimers in catalysis.[J]. Chemical Reviews, 2001, 101(9): 2991-3024.
[29] Andres R, Jesus E D, Flores J C. Catalysts based on palladium dendrimers[J]. New Journal of Chemistry, 2007, 31(7): 1161-1191.
[30] Malgas-Enus R, Mapolie S F, Smith G S. Norbornene polymerization using multinuclear nickel catalysts based on a polypropyleneimine dendrimer scaffold[J]. Journal of Organometallic Chemistry, 2008, 693(13): 2279-2286.
[31] Malgas-Enus R, Mapolie S F. A novel nickel (Ⅱ) complex based on a cyclam-cored generation-one dendrimeric salicylaldimine ligand and its application as a catalyst precursor in norbornene polymerization: comparative study with some other first generation DAB-polypropyleneimine metallodendrimers[J]. Polyhedron, 2012, 47(1): 87-93.
[32] Malgas-Enus R, Mapolie S F. Nickel metallodendrimers as catalyst precursors in the tandem oligomerization of ethylene and Friedel-Crafts alkylation of its olefinic products[J]. Inorganica Chimica Acta, 2014, 409(1): 96-105.
[33] Malgas-Enus R. The preparation and characterization of multinuclear catalysts based on novel dendrimers: application in the oligomerization and polymerization of unsaturated hydrocarbons[D]. Stellenbosch: University of Stellenbosch, 2011: 163.
[34] 王海琛. 樹枝狀亞胺水楊醛鎳配合物的合成及催化性能研究[D]. 大慶:東北石油大學(xué), 2013. WANG H C. Study on the synthesis and catalysis of dendritic imine salicylad nickel complexes [D].Daqing:Northeast Petroleum University, 2013.
[35] Dyer P W, Fawcett J, Hanton M J.. Rigid N-phosphino guanidine P, N ligands and their use in nickel-catalyzed ethylene oligomerization[J]. Organometallics, 2008, 27(19): 5082-5087.
[36] 秦一超, 葉健, 蔣斌波, 等. 芳氧基鋯系催化劑催化乙烯齊聚與Friedel-Crafts烷基化的串聯(lián)反應(yīng)[J]. 高等學(xué)校化學(xué)學(xué)報(bào), 2015, 36(9): 1825-1831. QIN Y C, YE J, JIANG B B,. Ethylene oligomerization and Friedel-Crafts alkylation tandem action catalyzed by aryloxy zirconium catalyst[J]. Chemical Journal of Chinese Universities, 2015, 36(9): 1825-1831.
[37] Zaidman A V, Kayumov R R, Belov G P,. Ethylene oligomerization in the presence of catalytic systems based on nickel(Ⅱ) formazanates[J]. Petroleum Chemistry, 2010, 50(6): 450-454.
[38] Zaidman A V, Pervova I G, Vilms A I,. Synthesis, characterization and ethylene oligomerization studies of nickel (Ⅱ) based new formazane derivatives[J]. Inorganica Chimica Acta, 2011, 367(1): 29-34.
[39] Pavlova I S, Pervova I G, Belov G P,. Ethylene oligomerization mediated by iron formazanates and organoaluminum compounds[J]. Petroleum Chemistry, 2013, 53(2): 127-133.
[40] Song K, Gao H, Liu F,. Syntheses, structures, and catalytic ethylene oligomerization behaviors of bis (phosphanyl) aminenickel (Ⅱ) complexes containing N-functionalized pendant groups[J]. European Journal of Inorganic Chemistry, 2009, 2009(20): 3016-3024.
[41] Perego C, Ingallina P. Recent advances in the industrial alkylation of aromatics: new catalysts and new processes[J]. Catalysis Today, 2002, 73(1): 3-22.
[42] Xiao L, Johnson K E, Treble R G. Alkane cracking, alkene polymerization, and Friedel-Crafts alkylation in liquids containing the acidic anions HX2?, XH (AlX4)?, XH (Al2X7)?, and Al2X7?(X= chlorine, bromine)[J]. Journal of Molecular Catalysis A: Chemical, 2004, 214(1): 121-127.
[43] orma A, Garcia H. Lewis acids: from conventional homogeneous to green homogeneous and heterogeneous catalysis[J]. Chemical Reviews, 2003, 103(11): 4307-4366.
[44] Busca G. Acid catalysts in industrial hydrocarbon chemistry[J]. Chemical Reviews, 2007, 107(11): 5366-5410.
[45] Davis R J. New perspectives on basic zeolites as catalysts and catalyst supports[J]. Journal of Catalysis, 2003, 216(1): 396-405.
Progress of Friedel-Crafts alkylation reaction in catalyst system of ethylene oligomerization
WANG Jun1, HOU Shuang1, SONG Lei2, WANG Sihan2, LI Cuiqin1
(1Provincial Key Laboratory of Oil & Gas Chemical Technology, School of Chemistry & Chemical Engineering, Northeast Petroleum University, Daqing 163318, Heilongjiang, China;2Daqing Petrochemical Research Center, CNPC, Daqing 163318, Heilongjiang, China)
Using transition metal complexes to catalyse ethylene oligomerization is an important route for preparing-olefins. The partially catalytic systems have entered the stage of pilot and industrial production. However, the recent researches have suggested that the oligomerization products of some transition metal catalysts in toluene solvent may react with toluene directly as Friedel-Crafts alkylation reaction, which could open a new way for the production of alkylbenzene. This paper reviews the progress of Friedel-Crafts alkylation reaction in ethylene oligomerization in recent years. The influence of the structure of catalysts, catalytic system and process conditions on the alkylation reaction is described in detail. Meanwhile, it gives the Friedel-Crafts alkylation reaction process in ethylene oligomerization, which would be of great significance to design the catalysts that could catalyse ethylene oligomerization to make mixed alkylbenzenes.
catalysis;ethylene oligomerization; catalyst; Friedel-Crafts alkylation; alkylbenzene; reaction
2016-05-11.
LI Cuiqin, licuiqin78@163.com
10.11949/j.issn.0438-1157.20160644
O 643.32
A
0438—1157(2016)11—4541—11
王俊(1965—),男,博士,教授。
國(guó)家自然科學(xué)基金項(xiàng)目(21576048);中國(guó)石油科技創(chuàng)新基金研究項(xiàng)目(2014D-5006-0503)。
2016-05-11收到初稿,2016-07-26收到修改稿。
聯(lián)系人:李翠勤。
supported by the National Natural Science Foundation of China (21576048) and the PetroChina Innovation Foundation (2014D-5006- 0503).

